经皮微通道显微手术治疗腰椎间盘突出症的效果分析
2021-03-25潘红利范雁东丁崇学
潘红利 范雁东 丁崇学 罗 坤
腰椎间盘突出症是指腰椎间盘的移位和腰椎间盘髓核脱出、纤维环及终板复合体的局限性移位,可引起剧烈疼痛及运动障碍[1]。随着技术发展及微创外科概念的不断深入,腰椎间盘突出症的手术治疗方式逐渐多样化,经皮微通道显微镜下腰椎间盘摘除术较传统的开放性手术创伤更小、术后恢复更快[2]。2018年12月至2020年2月采用经皮微通道显微镜下行腰椎间盘摘除术治疗单节段腰椎间盘突出症16例,现报道如下。
1 资料与方法
1.1 一般资料 纳入标准:①有明显腰痛伴下肢疼痛、麻木或运动障碍;②影像学检查示单节段腰椎间盘突出且突出节段与临床症状、体征对应;③经3个月正规保守治疗症状无法缓解或反复发作,严重影响日常生活及工作。排除标准:①影像学检查示腰椎不稳及滑脱;②合并有腰椎间盘炎、腰椎间盘结核等感染性腰椎间盘病变;②影像学资料不完整,随访时间<6个月。
共纳入符合标准的腰椎间盘突出症16例,其中男11 例,女5 例;年龄45~81 岁,平均(58.94±10.38)岁;腰椎MRI示突出节段:L1~L2节段1例,L2~L3节段3例,L3~L4节段2例,L4~L5节段7例,L5~S1节段3 例。所有病人均有腰痛伴下肢疼痛,直腿抬高试验阳性,其中伴有下肢肌力减退7例、大小便功能障碍3例、相应下肢神经支配区域皮肤感觉异常5例。
1.2 手术方法 用5 ml 注射器穿刺,C 臂X 线下定位确定病变椎间隙,并于病变椎间隙正中旁开1.5~2.0 cm处做2.0~3.0 cm的切口。自切口处置入克氏针至椎板,并循克氏针逐步置入扩张套管,逐级钝性分离椎旁肌,置入大小合适的工作通道固定于手术操作台旁,取出所有扩张套管后再次定位。移入显微镜,钝性分离椎板及关节突关节上附着的软组织,运用超声骨刀切除椎板及棘突根部骨质,下关节突去除减压时不超过关节突的1/2,咬除椎管内黄韧带,充分显露椎管内硬脊膜及神经根,顺着神经根走行方向找到椎间孔,切除神经根后外侧方黄韧带,将同侧神经根向中线方向牵拉,暴露突出或脱出的髓核组织,在有神经剥离子保护的情况下摘除突出或脱出的髓核组织,清理椎间隙残余的髓核并处理上下终板,充分止血并冲洗术区,检查有无硬脊膜损伤及神经根损伤。
术后5 d 内适当给予小剂量糖皮质激素减轻脊髓水肿,个体化补液维持内环境稳定。术后1 个月内佩戴腰围外固定,3个月内避免剧烈活动、弯腰提重物。
1.3 观察指标 记录手术时间、术中失血量、切口长度。术前、术后7 d、术后6 个月采用视觉模拟量表(visual analogue scale,VAS)评分和Oswestry 功能障碍指数(Oswestry disability index,ODI)分析疼痛缓解及神经功能恢复情况。术后6个月根据改良MacNab标准评估恢复优良情况。
1.4 统计学方法 应用SPSS 23.0软件分析;计量资料以±s表示,用t检验;P<0.05为差异有统计学意义。
2 结果
手术时间85~140 min,平均(102.00±18.07)min;术中出血量20~60 ml,平均(43.75±11.03)ml。术后未出现切口感染、神经根损伤、硬脊膜损伤等并发症。15例术后7 d腰腿疼痛症状明显缓解;1缓解不明显,对症处理,术后13 d明显改善。16例术后6个月疼痛基本消失。7 例下肢肌力减退术后3 d 基本恢复;3例大小便功能障碍术后6个月2例基本恢复正常,1例改善但未恢复至正常;5例皮肤感觉减退6个月基本恢复正常。术后复查腰椎MRI示椎管内及椎间孔减压充分,脊髓和神经根受压解除(图1)。术后7 d、6 个月,VAS 评分、ODI 均明显降低(P<0.05,表1)。术后6 个月,根据改良MacNab 标准评定为优9 例、良5 例、可2 例;优良率为87.5%(14/16)。
3 讨论
腰椎间盘突出症是一种临床较为常见的疾病,导致腰椎间盘突出症的原因可能有遗传因素、长期的脊柱轴向负荷过重、细菌等微生物感染引起腰椎间盘的慢性炎症等,严重影响病人的日常生活及工作。大多数腰椎间盘突出症,保守治疗为一线的治疗方式,但并没有强有力的循证医学证据证明其疗效,因此,手术仍是目前治疗腰椎间盘突出症最有效的方式[1,3]。
近年来,经皮微通道技术已被用于腰椎椎管狭窄、椎管内肿瘤、胸椎黄韧带骨化等手术中[4,5]。经皮微通道显微镜下腰椎间盘摘除术经过不断发展及改良,现已较为成熟[6],但在手术操作过程中仍需注意以下几点,以降低并发症发生率:①术前准确评估引起病人症状的责任椎间盘,术中准确定位,以避免术后病人症状缓解不明显、二次手术;②手术体位为俯卧位,腹部悬空,以降低术中静脉压及减少出血量;③去除椎板时,尽可能保护关节突关节,以减少术后关节不稳定性的发生率,并尽可能保持黄韧带的完整,以降低硬脊膜被无意切开的风险;④咬除椎管内黄韧带显露硬脊膜及神经根时,尽可能保留硬膜外静脉,减少双极电凝的使用,以减少术后硬膜外的瘢痕;⑤摘除突出或脱出的髓核组织时,尽可能整块摘除,以避免剩余的碎片掉入到硬膜囊下,造成脊髓二次受压;⑥术中如出现硬膜囊损伤,较小的撕裂口可覆以适当大小的人工硬脑膜,术后卧床休息2~3 d,较大的撕裂口则需转开放手术以严密缝合硬膜囊,防治脑脊液漏。

表1 手术前后VAS评分及ODI比较
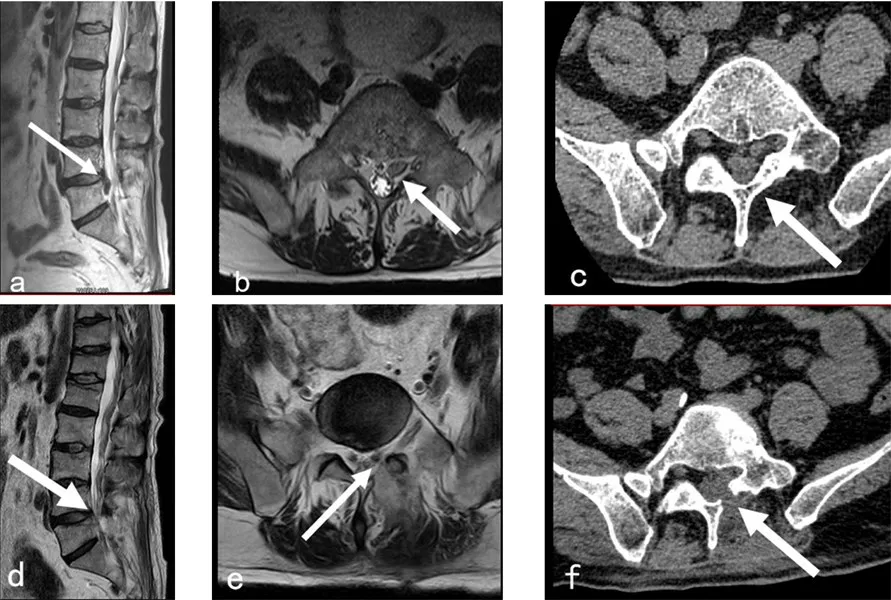
图1 L4~5椎间盘突出症经皮微通道显微手术前后影像学表现
本文16例术后腰腿疼痛症状明显缓解,肢体无力、大小便功能障碍、皮肤感觉减退等伴随症状均有不同程度的好转,其中1 例术后7 d 缓解不明显,考虑与术中神经根受牵拉时间过长有关,给予小剂量糖皮质激素结合中医理疗后好转,6个月随访期内,所有病人均未出现严重的术后并发症;术后7 d、6个月VAS评分及ODI较术前均明显下降。这说明经皮微通道显微技术在治疗腰椎间盘突出症上临床疗效显著。相关研究也表明经皮微通道显微镜下腰椎间盘摘除术相比于传统开放式椎间盘摘除术,具有创伤小、失血量少、术后并发症发生率低等优点[7,8]。本文16 例术后6 个月根据改良MacNab 标准评定的优良率为87.5%。这与文献[9]报道的307 例经皮内窥镜下经椎间孔椎间盘摘除的89.2%优良率无太大差别。同为微创手术,经皮椎间孔镜技术是在二维影像下操作的显微手术技术,学习曲线陡峭,需多次术中透视,在开展之初可能出现以下并发症:神经根损伤、硬膜囊损伤造成脑脊液漏、导丝断裂、椎间间隙感染、腰椎间盘突出复发、术中无法减压充分需转行开放手术等[10,11]。而经皮微通道技术在显微镜直视下操作可控性更强,术中可操作空间更大,对于神经根的减压更充分,降低了术后复发率,同时对椎旁肌肉及关节突关节损伤小,降低了对脊柱稳定性的影响;另外,在造成硬膜囊损伤可时有足够的操作空间进行及时修补、缝合,减少了脑脊液漏的发生率。
经皮微通道技术也存在一些问题:手术操作空间仍然有限,存在部分椎间盘组织残留、复发可能;术中定位对术者有一定经验积累要求,并需多次在C臂X线下定位,有一定辐射风险;术者需有一定显微手术操作基础,熟练掌握脊柱脊髓相关的局部解剖知识。
总之,经皮微通道技术治疗单节段腰椎间盘突出症,手术创伤小,失血量少,具有良好的临床疗效。
