两种促宫颈成熟方法用于宫颈电环切术后足月妊娠初产妇的临床观察
2021-03-24关艳杰荣艳霞王素颖
关艳杰,荣艳霞,王素颖
1.天津和平新世纪妇儿医院(天津 300040) 2.北京爱育华妇儿医院(北京 100176)
近年来随着宫颈癌筛查和诊断技术的普及,宫颈上皮内瘤变发病率逐年升高,且表现为低龄化趋势[1]。治疗方式有物理治疗、微波治疗、宫颈环形电切术(LEEP)、冷刀锥切治疗等,其中宫颈环形电切术因其操作简便,疗效满意而被广泛应用。宫颈环形电切术后的低龄育龄女性,在妊娠晚期因各种原因需要促宫颈成熟及引产时,临床治疗方式的选择给产科医生带来极大困扰,成为临床医生面临的棘手问题。宫颈成熟度是足月妊娠孕妇引产成功与否的关键[2]。宫颈环形电切术后的初产妇形成宫颈瘢痕,往往宫颈条件较差,最后常常以引产失败告终。在妊娠晚期促子宫颈成熟与引产指南(2014)[3]中提到两种促宫颈成熟方法:机械性方法(球囊、Foley尿管等)及前列腺素制剂(地诺前列酮栓、米索前列醇)。本文针对宫颈环形电切术后足月妊娠初产妇,拟采用两种不同方法进行临床干预并加以比较,探讨安全有效的宫颈电环切术后促宫颈成熟方法,现报道如下。
1 资料与方法
1.1一般资料选择2017年6月-2020年6月天津和平新世纪妇儿医院及北京爱育华妇儿医院住院需要引产的既往电环切术后的孕足月初产妇62例,纳入标准:①具备阴道分娩条件;②宫颈环形电切术手术资料齐全:明确手术切除深度<5 mm、手术至分娩时间<3年;③具备促宫颈成熟指征;④单胎妊娠、头位;⑤宫颈成熟评分(Bishop评分)<6分;⑥无相对及绝对剖宫产术指征。排除存在产前出血情况(胎盘早剥或前置胎盘);心、肝、肾等重要器官功能异常及阴道分泌物常规检查异常者。分为观察组和对照组,每组各31例,两组初孕妇均具备促宫颈成熟指征;两组初孕妇均具备促宫颈成熟指征;胎心监护反应型。观察组年龄24~36岁,平均(28±2.76)岁,孕周37~42周,平均(39.3±1.64)周,宫颈Bishop评分(2.67±0.41)分;对照组年龄24~37岁,平均(28±2.59)岁,孕周37~42周,平均(39.5±1.28)周,宫颈Bishop评分(2.59±0.63)分。两组初孕妇在年龄、孕周、宫颈Bishop评分等一般资料比较,差异无统计学意义(P>0.05),有可比性。
1.2方法两组初孕妇促宫颈成熟进入产程后严格按新产程标准(2014年)[4]观察及处理,并提供分娩镇痛。
1.2.1 观察组 采用地诺前列酮栓(英国CTS公司,进口药品注册号H20040368,批号MA19P02B)促宫颈成熟。孕妇排空膀胱呈截石位,消毒后将地诺前列酮栓横置于阴道后穹窿处。其后患者卧床30 min并行胎心监护。如无宫缩且胎心监护无异常时可随意活动。其后监护为胎心听诊1次/h,胎心监护,1次/2 h。若出现临产、胎膜自然破裂、子宫过度刺激、胎儿窘迫、前列腺素制剂的不良反应时立即取出;若无异常情况,24 h后取出地诺前列酮栓。无论何种指证取药,立即阴道检查进行宫颈Bishop评分。根据取药后宫颈Bishop评分,并结合其他情况采用催产素点滴引产或具备产科手术指征而行剖宫产终止妊娠。如静脉滴注催产素3 d仍未临产,则按“引产失败”手术指征行剖宫产终止妊娠。
1.2.2 对照组 采用COOK宫颈扩张球囊(美国CooK公司生产型号J-CRBS-184001,产品注册号20162662261,批号9842090,18号Fr导管,其一端为注水口,另一端为间段连接2个球囊,每个球囊最大容积80 mL)进行促宫颈成熟。孕妇排空膀胱呈截石位,消毒后经宫颈口置入COOK球囊,2个球囊均进入宫颈管内口上方,用注射器向子宫球囊内充盈0.9%氯化钠溶液20 mL。将COOK球囊整体向外缓慢牵拉,使子宫球囊紧贴宫颈内口,此时用注射器向阴道球囊内充盈0.9%氯化钠溶液20 mL,使阴道球囊紧贴宫颈外口。依次向2个球囊中注入0.9%氯化钠溶液20 mL至各球囊不超过80 mL,同时询问不适主诉,观察阴道出血情况。如出现临产、胎膜自然破裂、阴道异常出血、胎儿窘迫,则立即取出COOK球囊;如无任何异常情况,放置12 h后取出。无论何种指证取出COOK球囊,立即阴道检查进行宫颈Bishop评分,根据取出球囊后宫颈Bishop评分,并结合其他情况实施催产素静脉滴注引产或具备产科手术指征而行剖宫产终止妊娠。如静脉滴注催产素3 d仍未临产,则按“引产失败”手术指征行剖宫产终止妊娠。
1.3观察指标①观察并记录两组初产妇促宫颈成熟前后宫颈Bishop评分变化[5],评估促宫颈成熟效果,显效:宫颈Bishop评分提高>3分或临产;有效:宫颈Bishop评分提高2~3分,无效:宫颈Bishop评分提高<2分。②记录两组初产妇分娩方式(剖宫产,阴道助产和阴道分娩)。③记录两组初产妇促宫颈成熟时间(药械治疗开始时间至药械取出时间)、临产时间(药械治疗开始时间至临产时间)、第一产程时间(临产开始时间至宫颈口开全时间)、产后出血量(称重法)。④观察并记录两组母婴并发症:孕妇发生强直宫缩、发热、宫颈裂伤、胎儿窘迫情况;新生儿窒息发生情况。

2 结果
2.1宫颈Bishop评分及成熟度比较两组促宫颈成熟后宫颈Bishop评分较治疗前明显提高(P<0.05),两组间比较,差异无统计学意义(P>0.05),见表1。两组促宫颈成熟总有效率比较,差异无统计学意义(P>0.05),见表2。

表1 两组初产妇促宫颈成熟治疗前后宫颈Bishop评分比较分)
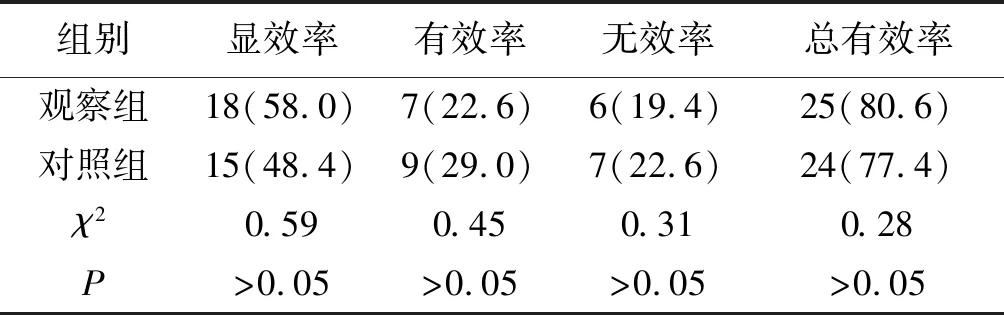
表2 两组初产妇促宫颈成熟度比较[n(%)]
2.2分娩情况比较观察组促宫颈成熟时间、临产时间、第一产程时间均明显短于对照组(P<0.05);两组产后出血量比较,差异无统计学意义(P>0.05),见表3。

表3 两组初产妇分娩情况比较
2.3分娩结局比较两组剖宫产率、阴道助产率比较,差异无统计学意义(P>0.05),见表4。

表4 两组初产妇分娩结局比较[n(%)]
2.4母婴并发症比较两组均无宫颈裂伤发生,观察组发生强直宫缩及胎儿窘迫高于对照组,发生发热低于对照组(P<0.05),见表5。

表5 两组初孕妇母婴并发症比较[n=31,n(%)]
3 讨论
子宫颈组织主要由大量的结缔组织和少量的平滑肌纤维、弹力纤维及血管组成。宫颈上皮内瘤变治疗中无论哪种手术方式,均会破坏子宫颈组织,形成瘢痕。冷刀子宫颈锥切手术切除宫颈组织后出血较多,愈合缓慢,瘢痕形成面积大,术后宫颈狭窄发生率明显升高,分娩时宫颈裂伤发生率也随之升高[6]。宫颈环形电切术通过超高频电波瞬间产生高热,切除少量宫颈浅表病变组织,同时止血。其手术时间短,创面整齐,切割精确,组织损伤小,出血少,坏死结痂脱落后组织再生愈合较快,形成瘢痕相对少且小[7],但因为仍然存在瘢痕,不同于正常宫颈组织,仍存在对生育期女性妊娠分娩方式的负面影响。产科医生在临床工作中遇到宫颈环形电切术后的孕妇,常常是视诊宫颈表面光滑,未见明显瘢痕组织,但触诊宫颈质硬,内口呈收缩“袖口”状,弹性差,且质地偏脆。临床上即使在孕前行宫颈环形电切术后孕足月自然临产后的孕妇,也常常会观察到第一产程时间尤其是潜伏期偏长的现象,一部分孕妇会因“宫颈坚韧”“产程异常”等行剖宫产术,一部分孕妇分娩时常常发生宫颈裂伤。宫颈电环切术后足月妊娠初产妇具有促宫颈成熟指征,选择哪一种促宫颈成熟方法更安全、更有效成为临床医生考虑的问题。
瘢痕形成是肉芽组织逐渐纤维化成胶原纤维结缔组织的过程。显微镜下早期瘢痕(一般创伤<3年)内可见含有肉芽组织、成纤维细胞、细胞间质、少量的血管。显微镜下晚期瘢痕(创伤>3年)呈大量平行或交错分布的胶原纤维束。两者比较抗拉力作用:早期瘢痕弱于晚期瘢痕,故暂时未引起组织明显挛缩;晚期瘢痕质坚而韧,缺乏弹性。地诺前列酮栓主要成分前列腺素E2主要局部作用于阴道内,在宫颈成熟生化和结构转变中起重要作用。该过程中局部胶原裂解酶及弹性胶原酶被激活,宫颈组织内胶原纤维及细胞外基质降解加速,黏多糖含量增加,使宫颈胶原纤维分离、断裂或消失,宫颈整体由坚硬变为柔软。较明显地使宫颈处肌肉纤维松弛,同时增强宫底处平滑肌收缩。增加子宫平滑肌细胞间缝隙连接结构数量,提高子宫体对缩宫药物的敏感性,协同发挥缩宫药物效果,诱发后继分娩完成[8]。但药品说明书中提到有文献报道用药过程中存在子宫收缩过强伴或不伴胎儿窘迫、子宫过度刺激、甚至子宫破裂风险。亦有孕妇出现胃肠道反应及发热等情况。这些情况可导致促宫颈成熟失败。COOK宫颈扩张球囊是通过机械性方法,对宫颈局部保持较大强度的持续性的扩张状态。这种内外较为平衡、温和、稳定、持续的张力对孕妇宫颈形成有效刺激,可以促进孕妇自身体内前列腺素的释放,引起宫颈条件改变,使宫颈接近自然成熟状态,诱发子宫收缩[9]。同时机械性压力可能会使宫颈环形电切术后形成的瘢痕发生微小断裂,失去原有坚硬结构,进而改变宫颈条件。其诱发宫缩作用不强,绝大多数需同时联合静点催产素引产才能进入临产状态[10]。相对于外源性途径给予前列腺素,通过机械性刺激自身产生内源性前列腺素数值难以测量,导致无法准确评估效果,故只能从临床上观察促宫颈成熟时间及第一产程时间来评判效果[11]。
在有效性方面:本研究观察到两种促宫颈成熟方法应用于宫颈环形电切术后足月妊娠初孕妇,均能够明显地、有效地促宫颈成熟。虽然在研究中地诺前列酮栓在宫颈条件改善及总有效率高于球囊,但两者经过统计学处理后并没有明显差异。地诺前列酮栓组促宫颈成熟时间、临产时间、第一产程时间均短于COOK球囊组,考虑为外源性途径给予前列腺素能够持久、缓慢地局部释放,而COOK球囊组最多放置12 h即取出,其作用持续性相对稍差,作用且较温和。在安全性方面:本研究观察到两组足月妊娠初孕妇分娩结局剖宫产率及阴道助产率经过统计学处理后并没有明显差异。地诺前列酮栓组初孕妇顺产例数稍多,考虑其改善宫颈条件作用更强,与有效性结果相互印证。但其助产例数较COOK球囊组稍多,考虑其可能出现子宫过度刺激及胎儿窘迫有关,与强直宫缩及胎儿窘迫统计结果相互印证。地诺前列酮栓用药会增加子宫过度收缩伴或不伴胎儿窘迫风险,如若经宫内复苏处理后强直宫缩缓解、胎心率恢复继续观察产程时,往往出现宫颈迅速扩张、第二产程胎儿再次出现胎儿窘迫情况,需阴道助产结束分娩。如若经宫内复苏处理后仍未能缓解,以“胎儿窘迫”行剖宫产结束分娩,同时亦会增加新生儿窒息风险。关于发热情况,COOK球囊组高于地诺前列酮栓组,考虑为COOK球囊在宫腔内放置时可能存在上行感染有关,但未做感染情况进一步观察及统计;地诺前列酮栓及分娩镇痛亦会出现使孕妇发热症状,但经过统计学处理后并没有明显差异。两种促宫颈成熟观察病例中均未出现宫颈裂伤,新生儿窒息情况、产后出血情况与正常阴道分娩时相当。在此研究过程中,有几点体会:在临床治疗前应仔细评估宫颈环形电切术手术治疗情况,手术实施的适应证、手术时长、术中切除组织面积或深度、术中出血情况、术后恢复情况及术后至妊娠分娩时间等;如若计划促宫颈成熟前宫颈Bishop评分过低,虽两种方法均可有效改善宫颈条件,但实际顺产率仍偏低;在严密监护下,经促宫颈成熟治疗后,宫颈环形电切术后孕足月的初孕妇仍存在阴道试产机会,应充分给予阴道试产。同时也应该看到本研究存在如下问题:虽然可以部分证实两种促宫颈成熟方法对宫颈环形电切术后初孕妇均有效,且较为安全,但样本例数偏少,且局限于宫颈环形电切术后3年内的初孕妇妊娠。关于宫颈环形电切术后的经产妇临床观察及宫颈环形电切术后大于3年内的临床观察还需要更多的临床样本数据。本研究临床观察数据较为简单,尤其是出现发热情况的孕妇没有进行后继感染指标的观察统计,应该补充更多的疗效评价指标及相关数据积累分析。
综上所述,对于宫颈环形电切术后(术后时间<3年)足月妊娠初孕妇,应用地诺前列酮栓及COOK球囊机械性促宫颈成熟均安全、有效。地诺前列酮栓促宫颈成熟时间更短,但强直宫缩及胎儿窘迫发生率稍高。在临床工作中,产科医生应将“母婴安全”放在首位,根据孕妇条件,综合评估后审慎地选择合理的促宫颈成熟方法,以期达到阴道分娩结局。
