基于网络药理学探讨潜阳封髓丹治疗慢性阻塞性肺疾病的潜在分子机制
2021-03-24于海洋陈云志刘怀全张旭飞
于海洋,陈云志,朱 星,刘怀全,赵 洁,张旭飞,李 文
贵州中医药大学(贵州 贵阳 550025)
慢性阻塞性肺病(COPD)是支气管、肺泡、肺泡间质等部位的呼吸系统慢性炎症性疾病,以咳嗽、咯痰、胸闷、气流受限为主要临床表现,且气流受限等症状会随病程的延长而呈现进行性加重的趋势,甚至会引发肺心病,严重影响患者的日常生活。目前,COPD已经成为一个严重的健康问题,流行病学调查显示[1],我国中青年人群的COPD患病率达13.7%。临床主要以控制性氧疗、口服支气管扩张剂、雾化吸入激素、注射抗炎药物等手段为主,虽在一定程度上缓解症状但预后欠佳。我国传统医学在治疗COPD的过程中取得了不错的效果,特别是在缓解临床症状、改善预后等方面尤为突出。
中医认为COPD应归属“肺胀”“喘症”“咳嗽”等范畴,其病理性质以本虚标实、上实下虚为主[2]。有统计表明[3]COPD患者有较大概率出现消瘦、潮热、咽喉不利、咳嗽、气喘、遗尿等症状。潜阳封髓丹出自许国祯所撰《御药院方》,由黄柏、砂仁、甘草组成。其中黄柏性味苦性寒,既可入心使心火不亢,使肺金无心火烦扰之忧,又可禀天冬寒水下滋肾水,有补虚泻实之妙。砂仁,味辛性温、无毒,入脾、肺、肾等经,主咳嗽胀满、温化寒痰、腹痛心疼、下气之功,其性温而不伤于热,行气而不伤于克,可健脾以祛痰之源。甘草健脾益气、祛痰润肺,又可调和诸药三药合力清上润下,祛痰行气恰中病机。清代火神派医家郑钦安十分推崇此方,认为此方可治一切咳嗽、喘促、面肿、喉痹、耳肿、目赤、鼻塞、遗尿等上实下虚之证。临床上,有医家将此方用于肺结核[4]、肺心病[5]等疾病,获得了较为理想的疗效。
网络药理学是近年来新兴的药物研究手段,兼顾了中药多成分多靶点等特点,可从分子水平上探究药物与疾病的相互作用,有利于整体而全面的认知药物的潜在作用机制。故本文拟基于网络药理学的角度寻找潜阳封髓丹治疗COPD的潜在靶点,为临床用药提供新的思路及方法。
1 材料与方法
1.1潜阳封髓丹活性成分及作用靶点的筛选通过中药系统药理学数据库与分析平台数据库TCMSP(http://tcmspw.com/)下载黄柏、砂仁、甘草的数据,并以类药性(DL)>0.18、口服生物利用度(OB)>30为条件筛选出三者的主要活性成分及药物靶点,并在 Uniprot数据库(http://www.uniprot.org/)中,对已获取的靶点进行标准化处理。
1.2COPD靶点的获取从TTD数据库(http://db.idrblab.net/ttd/)、DisGeNET数据库(http://www.disgenet.org/web/DisGeNET/menu/home)、MalaCards(https://www.malacards.org/)等数据库中查找COPD的疾病基因,合并后去除重复值。
1.3成分及靶点的网络构建将筛选后的数据导入Cytoscape 3.8.0构建药物—成分—疾病靶点网络图。
1.4蛋白质与蛋白质相互作用关系网络图(PPI)的构建将潜阳封髓丹与COPD的交集基因导入STRING数据库获取蛋白之间的结合度数据,并将数据导入Cytoscape 3.8.0实现可视化。
1.5、基因本体(GO)功能、京都基因与基因组百科全书(KEGG) 通路分析使用DAVID 6.8数据库对潜阳封髓丹治疗COPD的靶点进行GO、 KEGG分析,并设定物种为“Homo sapiens”[6]。借助R语言对两者的结果进行可视化处理。
1.6分子对接将药物成分中Degree值最高的化合物与PPI中Degree值最高的靶点导入PYMOL及AUTODOCK_VINA等软件进行对接,并以结合能的数值评估对接效果。分子对接过程中受体与配体的亲和力越好,则其结合能越低。本研究将结合能(affinity)≤-5.0 kcal/moL作为有效分子对接的筛选条件[7]。
2 结果
2.1潜阳封髓丹化学成分筛选及靶点收集结果在TCMSP数据库中按照筛选条件获得114个潜阳封髓丹的化学成分。并利用Cytoscape 3.8.0软件绘制化学成分-靶点网络图(图1)。图中包括961条边和225个节点,其中225个节点由114个化学成分(浅绿色三角形)和111个靶点(淡蓝色六边形)组成。

图1 化学成分-靶点网络图
2.2潜阳封髓丹化学成分治疗COPD的靶点网络
通过DisGeNET、TTD、Malacard数据库共获取1 494个COPD相关靶点。利用R语言得到48个潜阳封髓丹化学成分治疗COPD的相关靶点(图2)。

图2 共同靶点韦恩图
2.3成分及靶点的网络构建使用Cytoscape 3.8.0软件进一步构建潜阳补髓丹化学成分-COPD-靶点网络图(图3)。涉及141个节点和619条边,141个节点由91个化学成分(绿色三角形)、48个靶点(紫色圆形)、1个疾病(黄色四边形)和1个方名组成(粉色四边形)。通过Network Analysis功能模块对网络图进行分析,各个节点的拓扑参数,见表1。
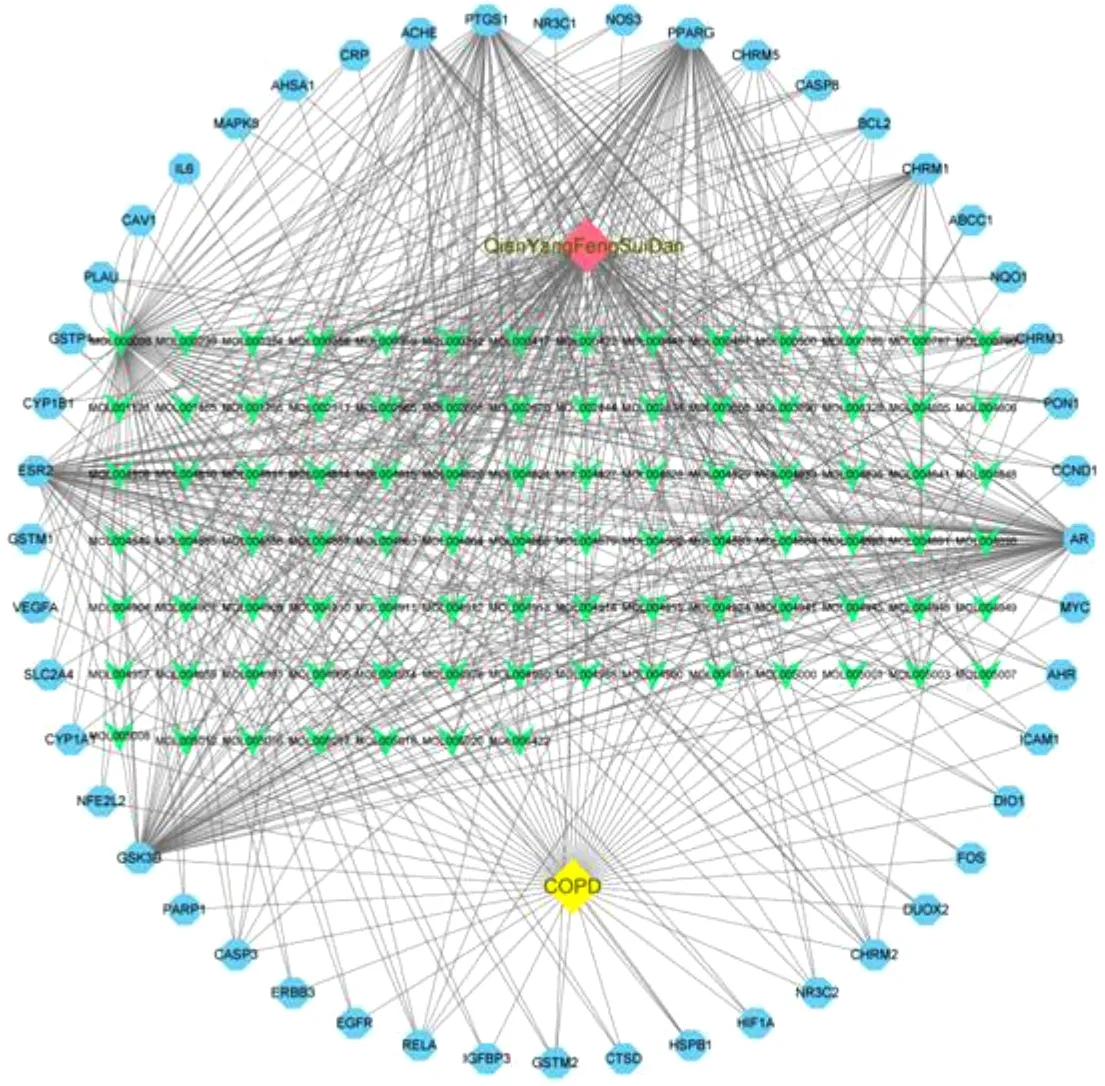
图3 药物成分-COPD-靶点网络图
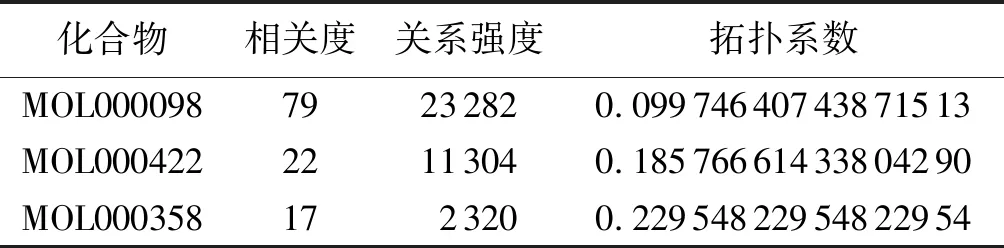
表1 活性化合物-COPD-靶点网络中Degree值较高的核心化合物
2.4PPI构建结果在String数据库中获得潜阳补髓丹治疗COPD的PPI网络,并利用Cytoscape 3.8.0软件进一步可视化(图4)。PPI网络图包含68个靶点和618条边,靶点越大和颜色越绿表示相应靶点的Degree值越高,PPI网络的拓扑参数,见表2。

图4 PPI网络图
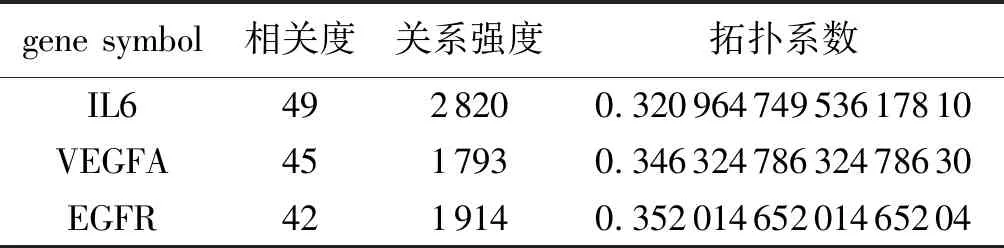
表2 PPI核心靶点及拓扑参数
2.5生物学功能和通路分析结果通过DAVID数据库对潜阳封髓丹治疗COPD的相关靶点进行GO功能和KEGG分析。GO功能分析结果发现48个靶点涉及413个富集结果(P<0.05),主要涉及细胞凋亡的调控、细胞增殖调控、氮化合物代谢过程的调控、乙酰胆碱、类固醇激素受体活性。KEGG分析结果发现48个靶点参与15条信号通路过程(P<0.05),主要涉及erbb信号通路、toll样受体信号通路、 MAPK信号通路、 p53信号通路等。本研究按照Count值大小筛选排名前15位的GO功能柱状图和KEGG信号通路图展示,见图5,图6。
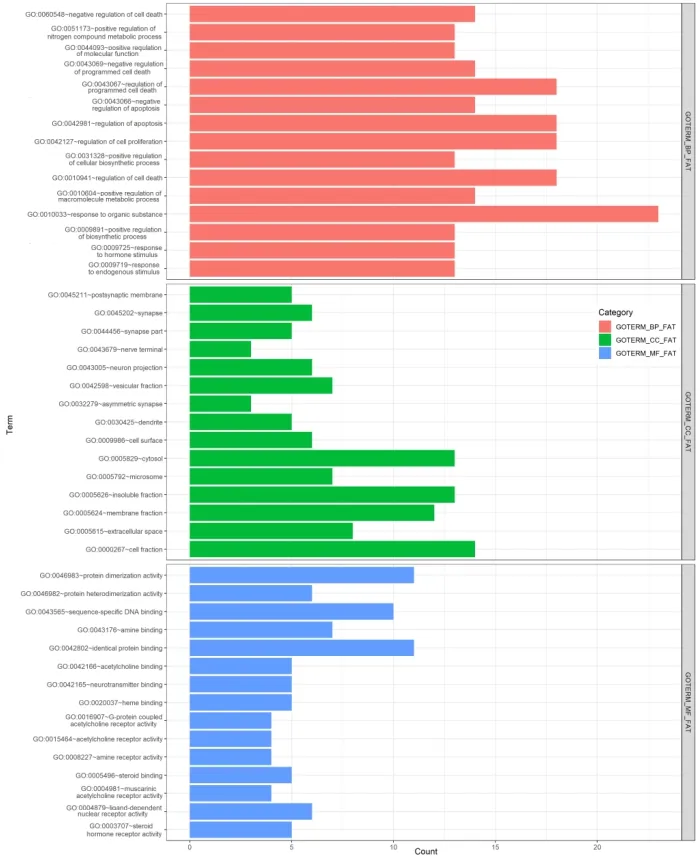
图5 GO功能分析图
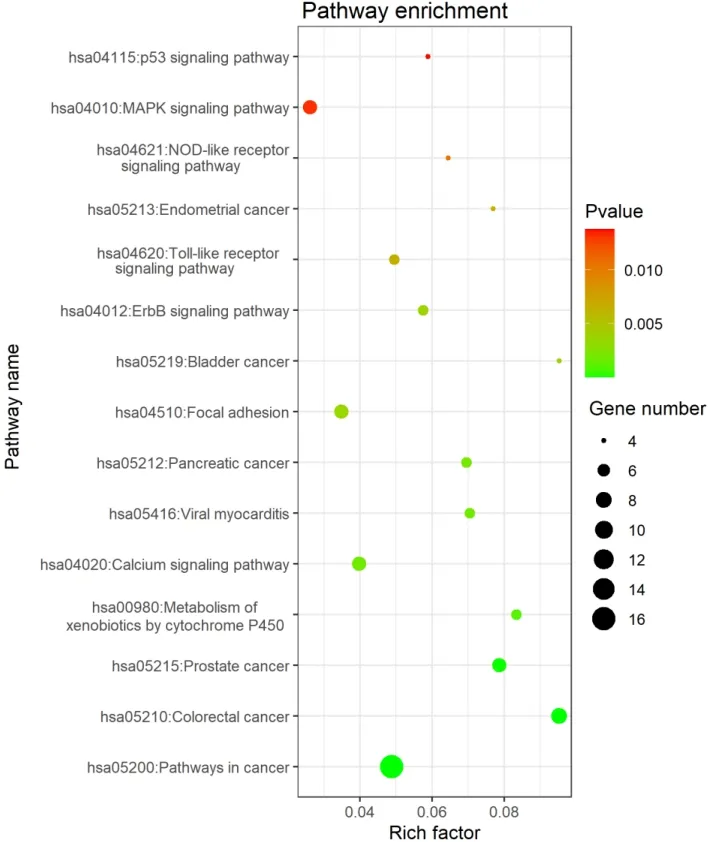
图6 KEGG分析图
2.6分子对接从RCSB PDB数据库(http://www.rcsb.org/)与TCMSP数据库中获取IL-6与槲皮素的分子结构,并进行对接(图7)。对接后发现两者的结合能为-21.338 kcal/moL,提示潜阳封髓丹中的活性化合成分与COPD的核心靶点之间有良好的结合能力。

图7 分子对接图
3 讨论
龚廷贤在《寿世保元》中记载:“热生于心,痰生于火。火者痰之根,静则伏于脾土动则发于肺金,乃心火克制肺金或寒邪停留肺,寒化为热,必生痰喘,咳逆上气肺胀”。肺胀是多种慢性肺系疾病久治不愈而成,久病必虚,故临床须在解决痰浊、气滞等因素时还应兼顾补虚。潜阳封髓丹由黄柏、砂仁、甘草组成,可从肺脾肾三脏同时施治,有祛痰行气、清热滋阴之功。
现代研究表明[8]COPD的发展受多种因素影响,尤其是炎症、氧化应激反应的增强会加重患者的气道高反应、气道重塑等临床表现。白细胞介素-6(IL-6)是多功能促炎因子,有凝聚胶原蛋白,促进气道纤维结缔组织形成及平滑肌增生,抑制细胞外基质分解,刺激成纤维细胞增殖等作用[9]。肿瘤坏死因子-α(TNF-α)可破坏患者小气道和肺组织正常结构与功能。转化生长因子β1(TGF-β1)可通过调控α-平滑肌肌动蛋白(α-SMA)抑制多种细胞增殖并诱导上皮细胞凋亡,同时又可以诱导间质样细胞增殖和向肌成纤维细胞分化,进而促进组织纤维化形成[10]。在COPD的炎症过程中,血管内皮生长因子促进缺氧诱导因子(HIF-1)表达进而诱导血管生成[11]。同时超氧化物歧化酶(SOD)、活性氧(ROS)、丙二醛(MDA)、一氧化氮(NO)等氧化因素之间的失衡也是加重COPD进展的另一重要因素[12]。
药物-化合物-靶点网络模型展示了潜阳封髓丹多成分多靶点的特点,经进一步分析发现Degree值>10的化合物主要有:槲皮素、山柰酚、2-甲基-7-甲氧基异黄酮、甘草查尔酮、甘草查尔酮G、β-谷甾醇、豆甾醇。研究表明[13]槲皮素在50 mg/kg剂量下对COPD大鼠模型无明显毒性,并可以降低IL-6、TGF-β1、α-SMA和TNF-α等的表达,对大鼠肺泡细胞凋亡,肺组织炎症和纤维化损伤有明显的缓解作用。查尔酮与甲氧基异黄酮均为黄酮类化合物,具有抗炎、抗菌、抗氧化、抗肿瘤等多种药理作用[14-15]。山柰酚是具有抗氧化、抗凋亡作用的黄酮类化合物,MDA含量及凋亡率均明显减少,总抗氧化能力(T-AOC)含量明显增加,减轻机体的氧化应激损伤[16]。β-谷甾醇能明显抑制肺中恶性细胞的生长,同时可将细胞周期进展停滞于G2/M期,并引起细胞凋亡性死亡,进而维护正常的细胞周期[17-18]。
结果显示ESR1、IL-6作为COPD患者的炎症标志物在急性发作期间异常增高[19]。VEGFA、EGFR与气道黏液高分泌有关,黏液高分泌会导致气道阻力增加、肺功能下降,促进细菌在气道内繁殖,同时也影响正常的清除功能,形成恶性循环。原癌基因 (myc)及CCND1在COPD患者成纤维细胞增殖中呈过度表达,这可能是患者气道重塑的作用机制之一[20-21]。PPARG基因为过氧化物酶体增生激活受体γ(PPARγ)的编码基因,正常情况下PPAR γ在支气管上皮细胞、肺泡上皮细胞、支气管黏膜下层、成纤维细胞中常呈低表达趋势,若其高表达则表现出胶原沉积、 肺纤维化明显等现象[22]。Rel A对NF-κB通路的活性进行调节,因其修饰方式不同会造成不同的结果,故还有待进一步研究。
对生物功能及KEGG信号通路进行富集分析,发现潜阳封髓丹可能通过erbb信号通路、toll受体信号通路、 MAPK信号通路、 p53信号通路干预COPD患者的进展。有文献表明[23]erbb通路的高表达会促进人类呼吸道上皮细胞分泌黏液。toll受体通路的激活可加重患者的炎症损伤[24]。MAPK通路可通过促进炎症反应及肺动脉高压的形成推动COPD的发展[25]。肺泡上皮细胞凋亡与p53蛋白表达增加是COPD发病过程中较为常见的现象,肺组织p53蛋白表达与肺泡上皮细胞凋亡呈正相关,使用p53抑制剂后可明显观察到p53蛋白表达与肺泡上皮细胞凋亡减少[26]。
综上所述,潜阳封髓丹具有多成分、多靶点等特点,可从多种途径改善COPD的炎症、氧化应激反应,抑制气道重塑,清除气道内高分泌黏液,减轻患者的临床症状。网络药理学是基于大数据进行系统性、整体性的药物分析,其本质与中医理论中的“整体观念”有异曲同工之妙,不仅可以用来寻找药物作用于疾病的潜在靶点,还可评估传统药物创新用法的可行性。因潜阳封髓丹可缓解COPD所造成的肺心病,且COPD患者临床中也易出现虚阳上越之症,故潜阳封髓丹有改善COPD患者临床症状的潜力。本研究用网络药理学验证发现,潜阳封髓丹可通过抑制炎症反应、氧化应激损伤、气道内黏液异常分泌、肺动脉高压的形成等途径改善COPD患者的预后。后续,课题组将结合分子生物学、生物信息学设计系统严谨的临床及动物实验,进一步明确潜阳封髓丹在治疗COPD中的作用机制。
