重症急性胰腺炎多重耐药病原菌感染的危险因素及预测模型的建立
2021-03-21黄荣胡可伟
黄荣,胡可伟
急性胰腺炎是临床常见的胆道炎症性疾病,包括轻型和重型2种,重症急性胰腺炎(severe acute pancreatitis,SAP)占15%~25%,主要表现为胰腺实质和胰周组织坏死,总体死亡率高达30%~70%[1]。SAP主要经历2个阶段,即早期炎症期(发病后2周)和晚期阶段(2周后)。脓毒症并发症是晚期死亡的主要原因[2]。
早期胃肠减压、足量广谱敏感抗生素治疗是保证临床疗效的关键,但是抗生素的持续和滥用导致耐药菌株尤其是多重耐药(multidrug resistance,MDR)病原体感染的发病率不断攀升,临床敏感抗生素可选性不断下降,同时患者死亡风险大大增加[3]。并且,MDR感染对导致重症监护病房(ICU)住院时间延长和医疗负担加重。MDR感染是目前临床处理十分棘手的一类疾病,在药敏试验的基础上通常会选择多黏菌素和替加环素,但是替加环素对细菌的最小抑菌浓度值却逐渐升高,降低了替加环素的敏感度[4]。因此,更好的预防和治疗MDR感染是临床面临的严峻挑战,努力选择SAP患者MDR感染发生的病原菌分布特征和主要危险因素具有十分重要的临床意义。
目前关于SAP患者MDR感染的相关报道较少,不同的临床干预方式如微创手术或开腹手术对SAP临床疗效及预后将产生不同结果,同时对病原菌感染以及MDR的发生也产生重要影响[5]。早期开放性胰腺坏死切除可增加患者的手术创伤,但微创手术显著降低了成本,缩短了住院时间,改善了SAP预后[6]。因此,本研究探讨SAP患者MDR感染的病原菌分布和主要危险因素,并建立定量列线图预测模型,以期指导临床应用。
1 对象与方法
1.1 研究对象
回顾性选取2018年9月至2020年9月张家港市第五人民医院和苏州大学附属第二医院收治的SAP患者232例,收集临床资料包括性别、年龄、病因、菌血症、死亡率、真菌感染、ICU住院、全身性疾病(胆囊炎、病毒性肝炎、肝硬化、高血压、糖尿病、肺炎、慢性阻塞性肺疾病、哮喘、慢性肾脏疾病)、侵入性治疗(胰管引流、胰腺切除术)、营养支持方式、住院时间、应用抗生素方式、首次使用碳青霉烯类以及抗生素疗程。根据多重耐药病原菌检测结果,分为MDR组(n=101)和非MDR组(n=131)。
纳入标准:①年龄>18岁;②初次发病,SAP诊断标准基于2012年亚特兰大分类法[7];③根据指南推荐进行临床治疗;④取得完整的细菌培养和药敏试验结果;⑤患者签署知情同意书,临床资料完整。排除标准:①合并肝胆肿瘤、胰腺癌、胃溃疡、炎症性肠病、结直肠肿瘤;②严重心肺肾脏器功能障碍、自身免疫性疾病、营养代谢性疾病;③妊娠、哺乳期女性;④近期大手术、外伤、输血。本研究通过张家港市第五人民医院伦理委员会批准(2018-A10),所有患者均知情同意并签署知情同意书。
1.2 SAP的治疗方法
所有患者入院积极完善相关检查,评估病情严重程度,根据指南[7]推荐进行综合药物和手术治疗。具体包括持续胃肠减压、营养支持、胃肠抑素微量泵持续应用、镇痛、灌肠、维持水和电解质稳定等,必要时候进行胰管持续引流、胰腺开腹或者微创手术进行部分或全部切除术等。
1.3 MDR病原菌检测
所有患者均采用静脉注射抗生素预防或治疗。病原菌的分离为从血液、细针抽吸、首次经皮穿刺引流或术中液体中获得细菌培养标本。使用compact-MeriWood系统进行抗菌药物敏感度测试,Mo或K-B法,根据临床和实验室标准研究所的建议进行诊断。MDR病原菌定义为至少1种药物在3个或3个以上的抗菌类别中获得性不敏感,纳入MDR组,其余纳入非MDR组。MDR[8]包括广泛耐药性(除2种或2种以下的抗菌药物,对至少1种药物不敏感)和泛耐药(对所有药物均不敏感)抗菌类别。耐甲氧西林金黄色葡萄球菌、耐万古霉素肠球菌、耐碳青霉烯类肠杆菌、耐多药鲍曼不动杆菌、耐多药铜绿假单胞菌为医疗相关感染病原菌,易产生多重耐药性。
1.4 统计学处理

2 结果
2.1 一般资料的比较
SAP的MDR发生率为43.5%(101/232)。MDR组菌血症和死亡率高于非MDR组,抗生素疗程和住院时间延长,全身性疾病、开腹手术和首次使用碳青霉烯类比例升高(P<0.05),见表1。

表1 两组一般临床资料比较
2.2 病原菌类型分布
232例患者共分离菌株325株,每例平均(1.4±0.3)株。革兰氏阳性菌97株(29.8%),以肠球菌属居多;革兰氏阴性菌195株(60.0%),以鲍曼不动杆菌、肺炎克雷伯菌和肠球菌属居多;真菌33株(10.2%)。MDR组多重耐药感染患者共分离菌株162株,革兰氏阳性菌56株和革兰氏阴性菌106株,见表2。
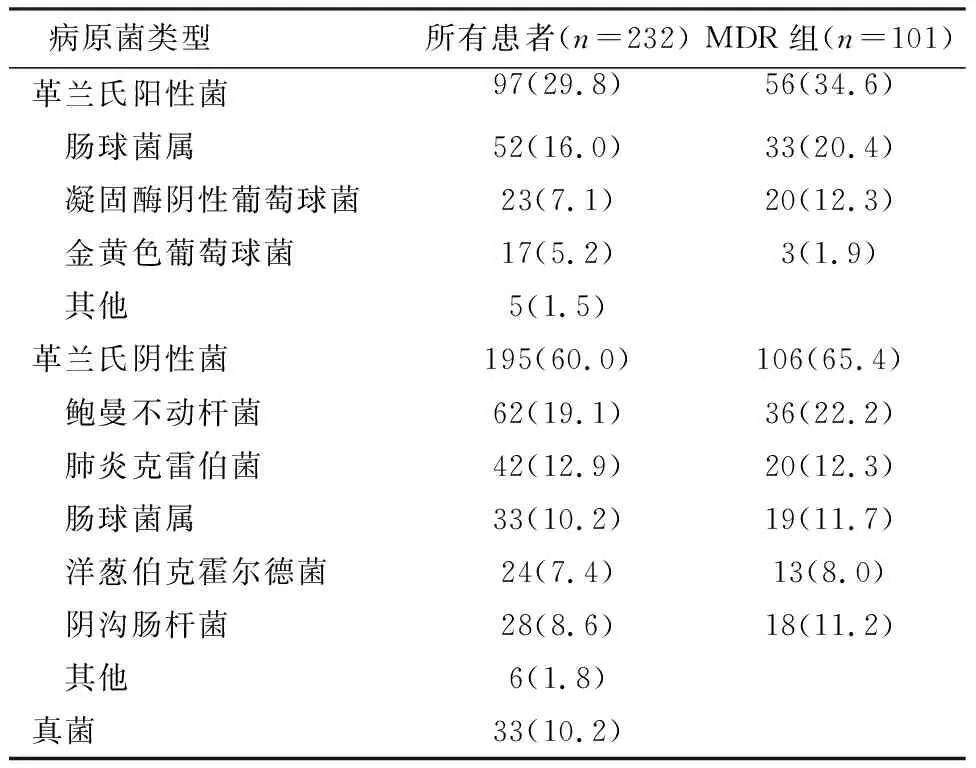
表2 所有患者和MDR组患者的病原菌类型分布 [n(%)]
2.3 MDR的主要危险因素分析
Logistic回归分析显示,全身性疾病、开腹手术和首次使用碳青霉烯类是MDR的主要危险因素(P<0.05),见表3。
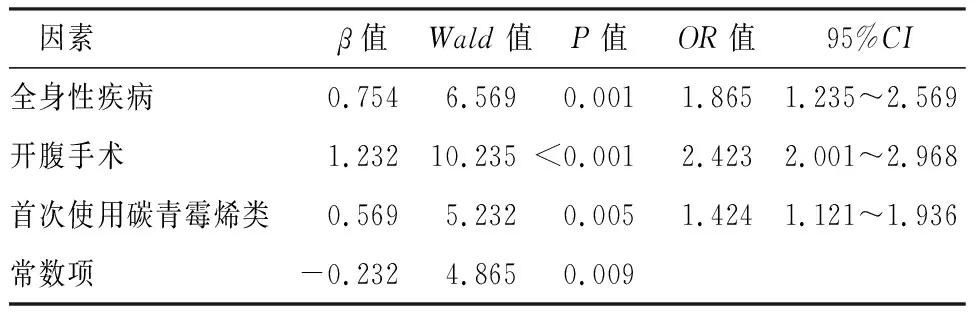
表3 MDR的主要危险因素分析
2.4 列线图模型的建立
根据筛选主要危险因素的权重进行定量赋值,建立列线图预测模型。见图1。模型的使用方法:每个变量对应列线图相应变量轴上相应点,以该点做变量轴的垂直线对应至上方评分标尺,得到该变量得分,通过对各变量得分求和得总分,以总分对应在MDR风险轴上的点,即为相对应的MDR风险。例如:某患者术前评估全身性疾病得分为1,对应50分;选择开腹手术对应60分;术后首次使用碳青霉烯类抗生素对应得分30分;相加总分为140分,对应MDR风险为0.9,提示术后发生MDR的风险极高。
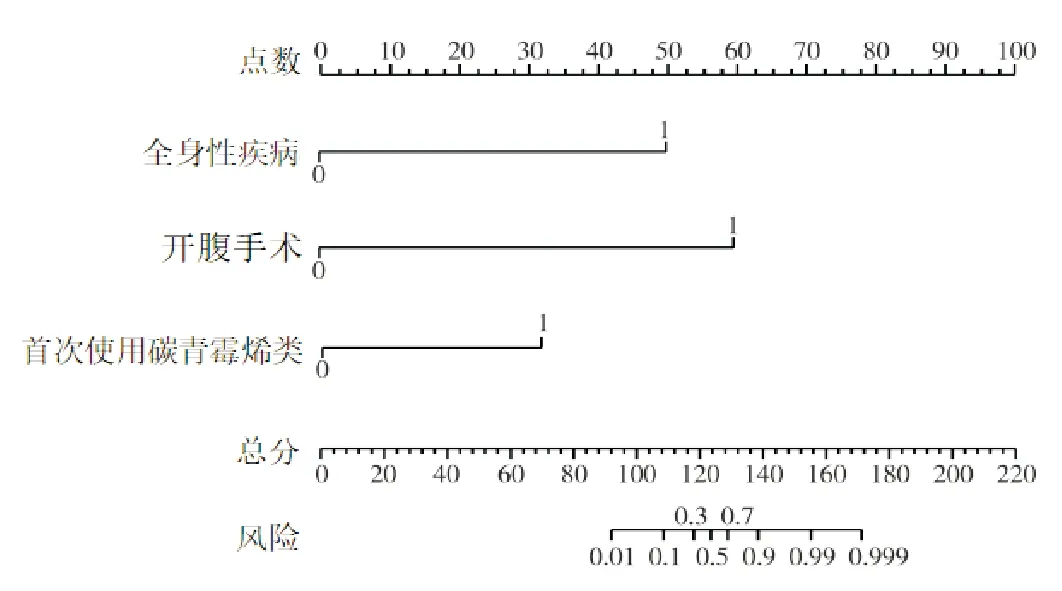
图1 MDR的列线图预测模型

2.5 列线图模型的预测效能
ROC曲线分析显示,列线图模型预测本研究MDR的AUC为0.868,(95%CI0.812~0.936,P<0.001),敏感度为80.5%,特异度为69.9%,见图2。

图2 列线图模型预测MDR的ROC曲线
3 讨论
既往研究报道,ICU入院、侵入性手术、高龄、全身性疾病、早期使用广谱抗生素是肝硬化、血液透析相关性肺炎及MDR病原体定植或感染的重要危险因素[9]。同时,初发诊断及进展性SAP患者的MDR细菌感染发生率较高,死亡率极高,预后极差[10]。
本研究结果显示,SAP的MDR发生率为43.5%(101/232),MDR组菌血症和死亡率高于非MDR组,抗生素疗程和住院时间延长,全身性疾病、开腹手术和首次使用碳青霉烯类比例升高(P<0.05)。胆石症是我国最常见胆道系统疾病MDR发生的致病因素,高脂饮食、缺乏运动、暴饮暴食、基础肝胆疾病是高脂血症性胰腺炎的主要诱因[11]。MDR易发生菌血症甚至脓毒血症,是死亡增加的主要原因。
232例患者共分离菌株325株,平均每例(1.4±0.3)株,革兰氏阳性菌株占29.8%,以肠球菌属居多,革兰氏阴性菌株占60.0%,以鲍曼不动杆菌、肺炎克雷伯菌和肠球菌属居多。MDR组病原菌中革兰氏阴性菌也明显高于革兰氏阳性菌,革兰氏阴性菌株是SAP及MDR发生的主要菌群。培养的肠球菌对万古霉素普遍敏感,鲍曼不动杆菌是引起MDR发病的主要革兰氏阴性菌株,而不合理应用抗生素是导致鲍曼不动杆菌耐药发生的重要原因,碳青霉烯类、第三代头孢菌素类和氟喹诺酮类药物是鲍曼不动杆菌获得性MDR的独立危险因素[12]。第三代头孢菌素和氟喹诺酮类药物静脉注射用于预防或治疗细菌感染,尽管抗生素预防不推荐用于预防MDR的发生及感染性并发症[13]。碳青霉烯类药物是胰腺坏死患者的一线治疗方法。此外,常规治疗包括机械通气和鼻胃管使用,也可能导致鲍曼不动杆菌感染[14]。MDR病原体可能是由于不受限制的使用抗生素引起,足量抗生素包括最佳剂量的治疗,抗生素的剂量和持续时间不当会导致MDR病原体产生[15]。
此外,SAP还可以影响抗生素的药代动力学。SAP患者血浆万古霉素的最低浓度显著降低,考虑是SAP相关的炎症反应综合征影响了万古霉素的分布和排泄[16]。建议采用更高剂量的治疗方案以提高MDR的疗效。首次使用碳青霉烯类是在未出现细菌培养结果之前,根据临床经验采用的抗生素方案,正是这种抗生素方案,可能导致细菌首次治疗未彻底治疗,进而导致细菌感染扩散,是多重耐药病原菌感染阳性的重要原因。
本研究结果显示,全身性疾病、开腹手术和首次使用碳青霉烯类是MDR的主要危险因素(P<0.05)。全身性疾病主要包括胆囊炎、病毒性肝炎、肝硬化、高血压、糖尿病、肺炎、慢性阻塞性肺疾病、哮喘、慢性肾脏疾病,可降低对抗生素的代谢效能,抑制抗生素对细菌的杀菌和抑菌能力,同时机体免疫抵抗力减弱,也是细菌感染扩散和MDR发生的不利因素[17]。开腹手术可能扰乱了正常消化道功能,导致菌群移位,进而出现定植菌扩散、真菌继发感染和脓毒血症等[18]。同时,开放性坏死切除术增大了腹腔脏器与外界的暴露机会,术后并发症尤其是切口和内脏器官感染的风险大大增加[19]。对采取经皮穿刺置管引流术治疗的患者需要预防性应用抗生素,也导致首次使用碳青霉烯类抗生素的机会增多,破坏了机体微生态平衡,产生MDR病原体[20-21]。剖腹引流、腹腔引流等治疗措施增加了多种医源性器械的应用,也可能增加MDR病原体的发病率[22-23]。多学科团队管理能够更好的把握抗生素的应用时机、最佳药物剂量及评估正确的治疗方案,对降低MDR的发生以及改善SAP临床预后具有较好的价值[24-25]。
本研究最后根据筛选的主要危险因素建立了定量列线图模型,具有较好的拟合效果。并且ROC分析显示,列线图模型预测MDR的效能为0.868(P<0.05)。列线图是一种可视化的logistic模型展示,是一种概率模型,提示纳入该模型中高危因素出现的几率,并对结果产生的重要影响,而不要求模型中所有高危因素同时发生。通过定量预测模型能够更好地指导临床早期识别MDR高危人群,进而采取恰当的抗生素管理策略以降低耐药菌的产生。
本研究存在一定局限性:本研究结果基于单中心回顾性研究,病例选择存在偏倚;总样本量有限,细菌检测技术可能影响菌群鉴定;列线图模型仅纳入定性资料,无定量资料,稳定性有待验证。
综上所述,SAP有较高的MDR发生率,以革兰氏阴性菌分布为主,主要有鲍曼不动杆菌、肺炎克雷伯菌和肠球菌属。MDR的菌血症和死亡率较高,抗生素疗程和住院时间延长。全身性疾病、开腹手术和首次使用碳青霉烯类是MDR的主要危险因素,定量列线图预测模型有较高的诊断效能,值得推广应用。
