气相色谱法测定大豆油脂肪酸组成不确定度的评定
2021-03-17李萍
李 萍
(广东文理职业学院,广东湛江 524400)
在我国,大豆油、棕榈油、菜籽油占据了植物油市场的绝大部分份额[1-2]。大豆油富含油酸、亚油酸、亚麻酸等不饱和脂肪酸,油酸17.0%~30.0%,亚油酸48.0%~59.0%,亚麻酸4.2%~11.0%[3],油酸作为植物油中最常见的不饱和脂肪酸,具有降低胆固醇、预防动脉硬化的功能特性,并已引起越来越多人的关注,而亚油酸、亚麻酸是人体必需脂肪酸,其无法被人体自身合成,必须从饮食中摄取,是人体维持正常生命活动所必需的[4]。总之,作为食用油,大豆油有着非常高的营养价值,而大豆油的市场价在所有植物油中有着不可比拟的价格优势,如此高的性价比也是大豆油在植物油市场不可被替代的原因之一。作为大豆油的特征指标,脂肪酸组成检验的准确性具有重要的生产及营养指导意义,目前关于脂肪酸组成检测的不确定度评定很少有报道,试验参考GB 5009.168—2016 《食品安全国家标准食品中脂肪酸的测定》[5]测定植物油的脂肪酸组成,并对测定结果的不确定度进行分析合成。
1 材料和方法
1.1 主要仪器和材料
日本岛津气相色谱仪: GC-2010Plus, 带AOC-20i 自动进样器,配置FID 检测器。
脂肪酸甲酯标准品:40 组分,纯度大于99%,异辛烷(色谱纯);氢氧化钾(分析纯);甲醇(分析纯);一水合硫酸氢钠(分析纯);一水合硫酸氢钠(分析纯);无水硫酸钠(分析纯,使用前650 ℃灼烧4 h,降温后存于干燥器中),一级大豆油。
氢氧化钾甲醇溶液约2 mol/L。将13.1 g 氢氧化钾溶于100 mL 无水甲醇中,可轻微加热,加入无水硫酸钠干燥、过滤,即得澄清溶液。
脂肪酸甲酯标准品(40 组分)溶液,将标准品瓶子打开,用异辛烷清洗瓶子内壁并全部转移至10 mL棕色容量瓶中,于4 ℃下避光保存6 个月内稳定,质量浓度为2.5 mg/mL。
1.2 色谱条件
色谱柱:RT-2560 100 m×0.25 mm×0.2 μm;进样量1 μL,气化室温度250 ℃,氮气流速1.0 mL/min,分流比50∶1;柱温箱:升序升温起始温度170 ℃,保留时间40 min,以2.0 ℃/min 升至220 ℃,保留时间25 min;检测器温度280 ℃,尾吹(氮气)流速 14.0 mL/min,氢气流速 40 mL/min,空气流速400 mL/min。
1.3 样品前处理
称取60.0 mg 试样于5 mL 具磨口玻璃塞试管中,加入4 mL 异辛烷溶解试样,加浓度为2 mol/L 氢氧化钾甲醇溶液200 μL,盖上玻璃塞猛烈振摇30 s 后静置至澄清透明,向溶液中加入约1 g 硫酸氢钠猛烈振摇,中和氢氧化钾,待盐沉淀后,将含有甲酯的上层溶液倒入10 mL 刻度玻璃试管中,得到的异辛烷溶液中甲酯含量约为15 mg/mL,取上清液按照1.2色谱条件进行气相色谱分析[5]。
2 结果与分析
脂肪酸组成使用面积归一化法,即假定试样的所有组分都显示在色谱图上,因此各峰的面积总和即代表100%的组分(完全洗脱),其数学模型为:
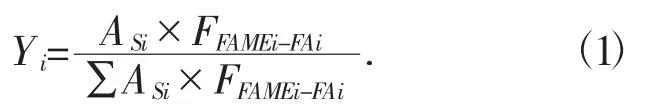
式中:Yi——试样中某个脂肪酸占总脂肪酸的百分比,%;
ASi——试样测定液中各脂肪酸甲酯的峰面积;
FFAMEi-FAi——脂肪酸甲酯i 转化成脂肪酸的系数;
∑A——试样测定液中各脂肪酸甲酯的峰面积的总和。
3 测量不确定度的来源
不确定度的测定主要来源于样品前处理引入的不确定度、重复测定引入的不确定度和气相色谱仪引入的不确定度。
4 不确定度分量的评定
样品前处理引入的不确定度包括称量样品引入的不确定度,移取异辛烷、氢氧化钾甲醇溶液引入的不确定度。
4.1 称量样品引入的不确定度
准确称取植物油 60 mg, 所用天平为万分之一,天平检定证书给出在0~50 g 称量范围的扩展不确定度为0.2 mg,标准不确定度= 0.2 mg/Ki=0.1 mg(按置信概率0.95,Ki 值取2),相对标准不确定度u(m)/m=0.1/60=0.001 667。
4.2 移取异辛烷、氢氧化钾甲醇溶液引入的不确定度
(1)单道移液器的不确定度。移取4 mL 异辛烷使用量程5 mL 移液器,其校准证书给出的扩展不确定度为 0.1 μL,标准不确定度 0.1 μL/Ki=0.05 μL(按置信概率0.95,Ki 值取2),相对标准不确定度为 0.5×0.000 1 mL/4 mL=0.000 012 5。
移取200 μL 氢氧化钾甲醇溶液使用量程200 μL移液器,其校准证书给出的扩展不确定度为0.1 μL,标准不确定度0.1 μL/Ki=0.05 μL(按置信概率0.95,Ki 值取 2),相对标准不确定度为 0.05 μL/200 μL=0.000 25。
(2)温度偏差导致的不确定度。视实验室温度的偏差为3 ℃,异辛烷的膨胀系数相同为1.2×10-3,其标准不确定度:相对标准不确定度:0.008 314/4=0.002 078。
视氢氧化钾甲醇溶液的膨胀系数与甲醇的膨胀系数相同为1.24×10-3,其标准不确定度:200×相对标准不确定度:0.429 5/200=0.002 148。
(3)待测液体积的相对标准不确定度。合成上述不确定度分量,移取异辛烷引入的标准不确定度:相对标准不确定度:u(V1)/V1=0.008 314/4=0.002 078;移取氢氧化钾甲醇溶液引入的标准不确定度:u(V2)=相对标准不确定度u(V2)/V2=0.432 4/200=0.002 162。
4.3 重复测定引入的不确定度
同一样品(试验选取一级大豆油作为检测对象)进行8 次重复性试验,标准不确定度依据公式(2)进行计算。
重复测定试验结果及对应标准不确定度见表1。
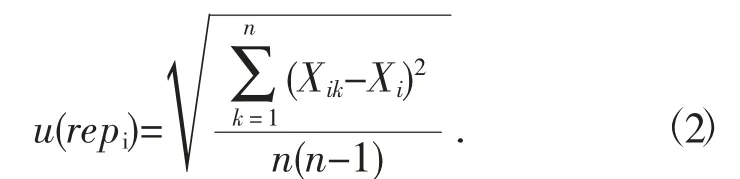
4.4 气相色谱仪引入的不确定度
气相色谱仪的不确定度来源主要有进样室、柱温箱、检测器引入的不确定度等,依据校准证书,将仪器的定量重复性2.6%作为气相色谱仪的主要不确定度,依据JJF1059.1—2012[6]对重复性的要求,所引入的标准不确定度为:0.026/2.83=0.009 187。
4.5 标准不确定度分量分析
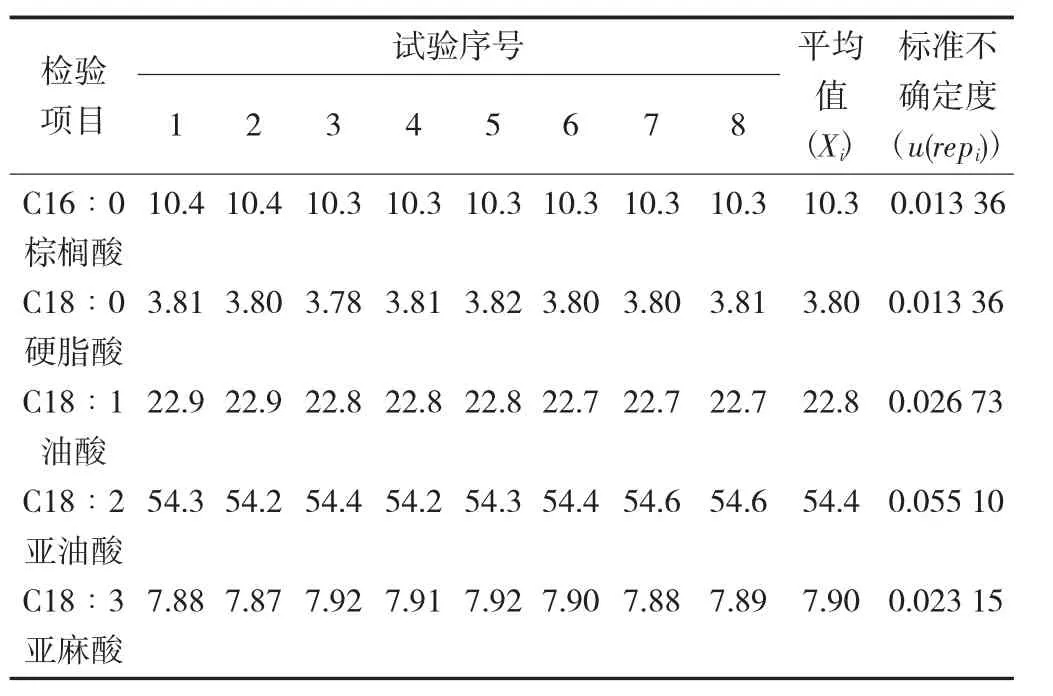
表1 重复测定试验结果及对应标准不确定度
标准不确定度分量见表2。

表2 标准不确定度分量
脂肪酸组成的结果是依据面积归一化进行计算的,由脂肪酸组成的数学模型可看出,称样量、异辛烷体积、氢氧化钾甲醇溶液体积不参与计算,三者引入的不确定度对脂肪酸组成结果的贡献很小,可忽略。试验仅考虑测量重复性及气相色谱重复性引入的不确定度分量。
5 测量结果的合成标准不确定度
脂肪酸组成的合成标准不确定度依据公式(3)进行计算。取置信水平为95%,包含因子K=2,则扩展不确定度依据公式(4)进行计算。


合成标准不确定度及扩展不确定度结果见表3。
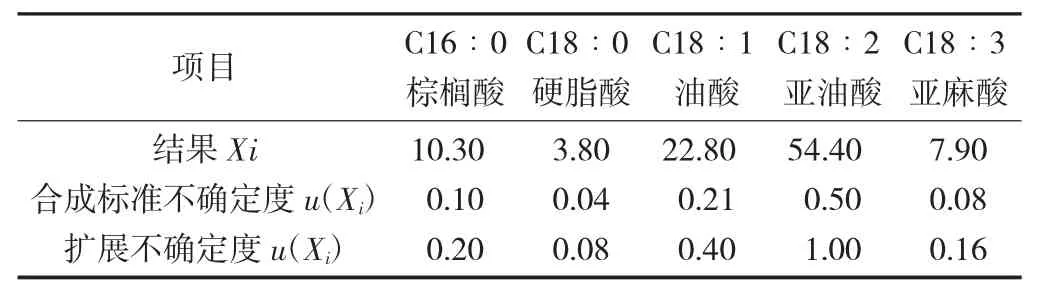
表3 合成标准不确定度及扩展不确定度结果
6 测量不确定度报告
大豆油中棕榈酸C16∶0 的含量为10.3%±0.2%,硬脂酸C18∶0 的含量为3.80%±0.08%,油酸C18∶1的含量为22.8%±0.4%,亚油酸C18∶2 的含量为54.4%±1.0%,亚麻酸C18∶3 的含量为7.90%±0.16%。
7 结论
从试验对植物油脂脂肪酸组成不确定度的评定过程中可以看出,气相色谱仪定量重复性、测定重复性是脂肪酸组成不确定度的主要来源,其中气相色谱仪定量重复性引入的不确定度最大。在日常工作检测过程中,应关注气相色谱仪的使用状态及维护,避免因气相色谱的不当使用而放大检测结果的偏差。
