天然植物人参中糖醛酸含量测定方法的建立
2021-03-15朱明月仝文科杜红娜苑军辉张延华孔素叶
朱明月,仝文科,杜红娜#, 苑军辉,张延华,杨 景,孔素叶,陆 安
( 1.中农翎翔河北生物科技有限公司 050699;2.行唐县动物卫生监督所 050699;3.行唐县畜牧工作总站 050699;4.行唐县畜牧局动物疫病预防控制中心 050699;5.石家庄燕科生物科技有限公司 050200)
作为“东北三宝”之一的人参,在中国药用历史悠久。 人参中含有多种有效成分,但对人参的研究,多集中于人参皂苷。 近年来,关于人参多糖的报道越来越多,现代研究发现,人参多糖具有增强机体免疫力[1-6]和通过提高免疫力辅助抗肿瘤的作用[4-10],显示多糖对人参药用价值的发挥亦起着重要作用。研究表明,人参多糖中的酸性多糖, 即含有糖醛酸结构单元的多糖生物活性较高[11]。 目前,药典“人参”饮片项下只有人参皂苷含量的测定方法,但未见人参中糖醛酸含量测定方法研究的报道。 因此,本试验拟建立一种准确可靠的人参中糖醛酸含量测定方法, 为人参饮片中人参多糖的质量控制提供可借鉴的分析方法。
1 仪器与材料
1.1 仪器
UV2550 型紫外-可见分光光度计( 日本岛津)
AUW120D 型电子天平(日本SHIMADZU 公司)
1.2 药物与试剂
D-半乳糖醛酸对照品 (中国食品药品检定研究院, 批号:111646-200301,供含量测定用),四硼酸钠(美国Sigma 公司),间羟联苯(美国Sigma 公司),咔唑(北京化学试剂公司), 其他试剂均为分析纯。
1.3 药材
人参药材购于安国药材市场, 经本公司质控部鉴别符合《中华人民共和国药典》2015 版(Ⅰ部)有关项下规定[12]。
2 方法与结果
2.1 供试品溶液的制备
取人参细粉0.25g,置圆底烧瓶中,加80%乙醇150mL,加热回流1h,趁热滤过,残渣用80%热乙醇洗涤3 次,每次10mL,洗涤液弃去。将残渣及滤纸置烧瓶中,加水100mL,加热回流1h,滤过。残渣再加水100mL,加热回流1h,趁热滤过。残渣及烧瓶用热水洗涤4 次,每次10mL,合并滤液及洗涤液,放冷,转移至250mL 量瓶中,加水至刻度,摇匀,滤纸过滤,取续滤液,即可。
2.2 对照品溶液的制备
称取D-半乳糖醛酸对照品10.08mg, 置100mL 量瓶中,加水溶解并稀释至刻度,摇匀,即得。
2.3 显色剂的配制
2.3.1 四硼酸钠-硫酸溶液的制备
称取四硼酸钠4.78g,置1000mL 量瓶中,加硫酸超声(功率250W,频率40kHz)使溶解,并稀释至刻度,摇匀,即得(0.0125 mol/L 四硼酸钠-硫酸溶液)。
2.3.2 间羟联苯溶液的制备
称取间羟联苯0.15g,置100mL 量瓶中,加0.5%的氢氧化钠溶液超声(功率250W,频率40kHz)使溶解,并稀释至刻度,摇匀,即得(0.15% 间羟联苯溶液)。
2.4 显色条件考察
2.4.1 最大吸收波长的选择
精密量取四硼酸钠-硫酸溶液6mL,置具塞试管中,于冰水浴中分别加入0.4mL 纯化水,摇匀,于冰水浴中,加入D-半乳糖醛酸对照品溶液0.6mL,摇匀,置沸水浴中加热12min,取出,置冰水浴中放冷至室温,加入间羟联苯溶液80μL,摇匀,室温放置40 min,以1mL 纯化水同上操作制得空白溶液调零,以紫外可见分光光度计,在400~700 nm 进行光谱扫描,结果显示,525nm 波长处吸光度值最大,因此,确定检测波长为525nm。
2.4.2 四硼酸钠-硫酸溶液用量考察
精密量取四硼酸钠-硫酸溶液3mL、4mL、5mL、6mL、7mL、8mL,分别置具塞试管中,于冰水浴中分别加入0.4mL 纯化水,摇匀,各加入D-半乳糖醛酸对照品溶液0.6mL,摇匀,其余操作同2.4.1 项,测定吸光度。结果显示:随着四硼酸钠-硫酸溶液用量的增加,D-半乳糖醛酸对照品溶液吸光度值先升高然后降低,其中以四硼酸钠-硫酸溶液用量为6mL 的吸光度值最大。 因此,确定四硼酸钠-硫酸溶液最佳用量为6mL。
2.4.3 沸水浴时间考察
精密量取四硼酸钠-硫酸溶液6mL,平行七份,分别置具塞试管中,于冰水浴中分别加入0.4mL 纯化水,摇匀,各加入D-半乳糖醛酸对照品溶液0.6mL,摇匀,置沸水浴中分别加热4min、6min、8min、10min、12min、14min、16min,其余操作同2.4.1 项,测定吸光度。 结果显示:沸水浴时间不同时,对照品溶液吸光度基本没有差异,说明沸水浴时间为4min 时,已反应完全。
2.4.4 间羟联苯用量考察
精密量取四硼酸钠-硫酸溶液6mL,平行十份,分别置具塞试管中,于冰水浴中分别加入0.4mL 纯化水,摇匀,各加入D-半乳糖醛酸对照品溶液0.6mL,摇匀,置沸水浴中加热4min,取出,置冰水浴中放冷至室温,再分别加入间羟联苯溶液30μL、40μL、50μL、60μL、70μL、80μL、90μL、100μL,摇匀,其余操作同2.4.1项,测定吸光度。 结果显示:随着间羟联苯用量的增加,对照品溶液吸光度值先增大后减小,其中以间羟联苯用量为80μL 的吸光度值最大,因此,确定间羟联苯最佳用量为80μL。
2.4.5 显色时间(室温放置时间)考察
精密量取四硼酸钠-硫酸溶液6mL,置具塞试管中,于冰水浴中加入0.5mL 纯化水,摇匀,加入D-半乳糖醛酸对照品溶液0.5mL,摇匀,置沸水浴中加热4min,取出,置冰水浴中放冷至室温,加入间羟联苯溶液80μL,摇匀,同法制备相应空白溶液,以紫外可见分光光度计,每隔5min 测定一次525nm 波长处的吸光度,连续测定60min。 结果显示:显色时间不同时,对照品溶液吸光度的RSD 值为0.30%,吸光度基本没有差异,说明显色5min即可。
2.5 供试品溶液制备方法考察
2.5.1 供试品溶液制备方法比较
为了考察人参皂苷对糖醛酸含量测定是否存在干扰,对80%乙醇醇提皂苷后再水提糖醛酸和直接水提糖醛酸的方法进行比较,光谱扫描图见图1。

图1 不同提取方法光谱扫描图
显色后颜色比较:醇提皂苷后再水提糖醛酸,供试品溶液显色后为砖红色;直接水提糖醛酸,供试品溶液颜色为咖啡色,两种供试品溶液制备方法显色后颜色不一致。 最大吸收波长比较:醇提皂苷后再水提糖醛酸,最大吸收波长为525nm,与对照品最大吸收波长一致,直接水提糖醛酸,最大吸收波长为508nm,与对照品最大吸收波长525nm 不一致。综上所述,若直接水提进行显色,则药材中人参皂苷对糖醛酸含量测定存在干扰。 因此,需醇提皂苷排除干扰后再水提糖醛酸进行检测。
2.5.2 醇提次数比较
对80%乙醇醇提皂苷的次数(1 次、2 次、3 次)进行了比较,结果显示:醇提次数不同时,供试品溶液显色后颜色一致,均为砖红色,且最大吸收波长均在525nm 附近,且糖醛酸含量差异较小,说明提取1 次,人参皂苷已提取完全,因此确定80%乙醇醇提次数为1 次。
2.5.3 溶剂用量考察
对糖醛酸提取溶剂 (水) 用量—50mL、100mL、150mL、200mL 进行了考察,结果显示:随着溶剂用量的增加,糖醛酸含量增高,但溶剂用量为100mL、150mL 和200mL 时,糖醛酸含量差异较小,因此,确定溶剂用量为100mL。
2.5.4 水提次数考察
对糖醛酸水提次数进行了考察,结果显示:随着水提次数的增加,糖醛酸含量增高,但水提2 次和3 次,糖醛酸含量差异较小,说明提取2 次,糖醛酸已提取完完全。 因此,确定水提次数为2 次。
2.6 标准曲线的制备
精密量取四硼酸钠-硫酸溶液6mL,置具塞试管中,平行六份, 于冰水浴中分别加入D-半乳糖醛酸对照品溶液0.1mL、0.2mL、0.3mL、0.4mL、0.5mL、0.6mL,以纯化水补足1.0mL,摇匀,置沸水浴中加热4min,取出,置冰水浴中放冷至室温,再分别加入间羟联苯溶液80μL,摇匀,室温放置5min,同法制备空白溶液,以紫外可见分光光度计,分别测定525nm 处的吸光度,并制备标准曲线,结果见图2。
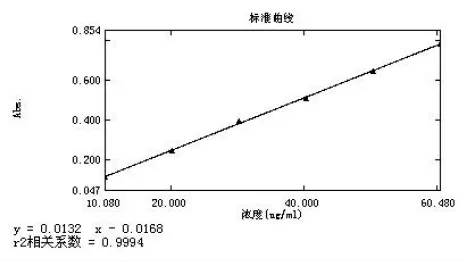
图2 标准曲线
上述结果显示:以D-半乳糖醛酸浓度为横坐标(x),吸光度为纵坐标(y) 作标准曲线,方程为y=0.0132x-0.0168(r=0.9997),说明D-半乳糖醛酸溶液对照品溶液在10.08μg/mL~60.48μg/mL 范围内线性关系良好。
2.7 方法学考察
2.7.1 重复性考察
按取样量0.8∶1.0∶1.2 的比例分别称取样品,各平行三份,精密称定,按已确定的方法制备供试品溶液,并吸光度,计算糖醛酸含量。 九份样品测定结果RSD 值为2.26%, 该方法重复性良好。

表1 回收率考察结果
2.7.2 精密度考察
取对照品溶液及重复性考察项下的供试品溶液, 以间羟联苯法显色, 对对照品溶液和供试品溶液连续测定6 次525nm 处吸光度, 计算RSD 值。 对照品和供试品溶液RSD 值分别为0.08%和0.00%,该方法精密度良好。
2.7.3 稳定性考察
取对照品溶液及重复性考察项下的供试品溶液, 以间羟联苯法显色, 每隔30min 测定一次525nm 处的吸光度, 连续测定3h,计算RSD 值。 对照品和供试品溶液RSD 值分别为0.77%和2.15%,表明供试品溶液在3h 内显色稳定。
2.7.4 回收率考察
按取样量0.25g 的1/2 即0.125g 称取本品,精密称定,平行9 份,取已知浓度的的D-半乳糖醛酸对照品溶液,按照0.8∶1.0∶1.2 的比例分别加入样品溶液中,各平行三份,按确定的样品处理方法制备供试品溶液,以间羟联苯法测定糖醛酸含量,计算回收率及回收率的RSD 值。 结果见表1。
上述结果显示: 九份供试品溶液中,D-半乳糖醛酸回收率介于95%~105%之间, 回收率均值为100.49%,RSD 值为2.63%,该方法回收率良好。
2.8 人参多糖中糖醛酸的含量测定
精密称取人参细粉0.25 g,按照“2.1”项下供试品溶液制备方法和“2.4”项下显色条件显色,测定吸光度,计算供试品溶液中糖醛酸含量。结果人参中糖醛酸含量为3.99%,RSD 为1.23%(n=3)。
3 讨论
文献显示,糖醛酸含量测定方法分为“咔唑法”和“间羟联苯法”两种,咔唑法收载于《国家中成药汇编》中“人参多糖注射液”项下;间羟联苯法见于文献[13],该文献报道咔唑法在测定人参酸性多糖中糖醛酸含量时, 因中性糖与硫酸咔唑络合形成棕色衍生物,从而对糖醛酸含量测定存在干扰。 笔者对咔唑法和间羟联苯法进行了比较,试验结果显示:采用间羟联苯法测定时,对照品溶液和供试品溶液最大吸收波长均为525nm, 且供试品溶液和对照品溶液均为紫红色;采用咔唑法测定时,对照品溶液最大吸收波长在525nm,而供试品溶液最大吸收波长在539nm,两者最大吸收波长不一致,对照品溶液为紫红色,而供试品溶液为咖啡色;且咔唑法和间羟联苯法相比,供试品溶液的吸光度咔唑法比间羟联苯法高0.286,说明咔唑法测定糖醛酸含量时,确实对测定结果的影响,同时验证间羟联苯法的可行性。 因此,确定人参饮片中糖醛酸含量测定方法为间羟联苯法。
供试品溶液制备方法考察过程中, 考虑到人参中含有皂苷和多糖两类成分,因此,笔者对皂苷是否对糖醛酸含量测定存在干扰进行了考察,结果发现,皂苷类成分存在时,间羟联苯法显色后,供试品溶液的颜色和最大吸收波长均存在差异,说明皂苷类成分的存在,对糖醛酸含量测定确实存在干扰。 因此,供试品溶液制备方法中确定先醇提除去人参皂苷,然后再水提多糖,以保证含量测定方法的准确度。
经多次试验验证,间羟联苯法测定人参饮片中糖醛酸含量,重复性好,准确度高,适用于人参饮片中糖醛酸含量的测定。 该方法可为药典 “人参” 饮片项下人参酸性多糖质量控制提供参考,以便更好地控制人参饮片质量。
