Fenton 和类Fenton 技术处理水中盐酸四环素试验研究
2021-03-13宋成智张娇李依杨阳阳韩岗华
宋成智, 张娇, 李依, 杨阳阳, 韩岗华
(青岛农业大学 资源与环境学院 青岛市农村环境工程研究中心, 山东 青岛 266109)
抗生素污染问题已经成为世界范围内普遍存在的环境问题, 作为抗生素的生产和使用大国, 我国的抗生素污染及治理问题也引起广泛重视[1-2]。 盐酸四环素作为一种广谱抗生素, 主要应用于人和动物传染病的治疗, 在废水中也很常见[3-4], 在地表水、 地下水、 海水、 生活饮用水中也广泛存在[5-8],已被美国环境保护署和欧洲联盟列为新兴污染物。
Fenton 法对有机物的处理效果好、 操作简单、投资较低, 广泛应用于水中有机物的去除[9-10], 对盐酸四环素有较好的去除效果[11]。 然而Fenton 反应存在最佳pH 值范围较窄(pH 值为2.5 ~3.5)、 H2O2利用率不高[12]、 铁离子易于沉淀等缺点[13], 因此一系 列 类Fenton 反 应 技 术 引 起 了 广 泛 关 注[14-17]。 类Fenton 反应是Fe3+、 含铁矿物以及其他一些过渡金属如Co、 Cd、 Cu、 Ag、 Mn、 Ni 等可以加速或替代Fe2+, 从而对H2O2起催化作用的一类反应的总称[13]。乙二胺四乙酸(EDTA)作为络合剂可以防止铁离子沉淀, 使Fenton 技术pH 值适用范围更广, 也被应用于水和废水处理中[18-19]。 目前, 大多数Fenton 及类Fenton 技术处理有机物的报道相对独立, 研究对象、 研究方法、 反应条件、 处理效果等均基于不同的条件, 针对常用的铁基催化剂均相Fenton 技术处理盐酸四环素的对比研究尚未见报道。
本试验选用材料易得、 价格便宜、 实际应用可行的4 种均相Fenton、 类Fenton 技术(EDTA-Fe3+、Fe3+、 Fe6+类Fenton 技术), 对比研究其对盐酸四环素的去除效果。 考察pH 值、 反应时间等参数对盐酸四环素去除效果的影响, 对均相Fenton 技术在水处理领域的应用具有重要意义。
1 材料与方法
1.1 试验药剂
盐酸四环素(简称TC, 纯度为98%)、 三氯化铁、 硫化亚铁、 高铁酸钾(纯度为90%)、 30%H2O2、乙二胺四乙酸(简称EDTA)、 硫酸(纯度为98%)、氢氧化钠(纯度为96%), 药剂均为分析纯。
1.2 试验用水
试验用水采用自配原水, 均现用现配, 称取0.2 g 纯度为98%的TC 置于2 L 容量瓶内, 用纯水稀释至标线, 混匀。 水质指标如表1 所示。
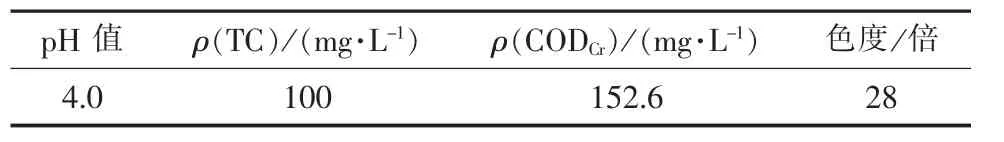
表1 TC 原水水质指标Tab. 1 TC raw water quality indexes
1.3 试验方法
取500 mL 水样于1 000 mL 烧杯中, 用NaOH和H2SO4调节pH 值, 加入Fenton 或EDTA-Fe3+、Fe3+、 Fe6+类Fenton 试剂, 在磁力搅拌器上以150 r/min 快速搅拌, 不同时间间隔取样, 检测TC 浓度。 考察pH 值、 反应时间、 H2O2投加量、 H2O2与铁离子的物质的量比及其投加量对试验结果的影响, 得到最佳试验条件。 在最佳试验条件下, 分析出水CODCr浓度及色度, 并对水样进行紫外全波长扫描, 对比分析原水经Fenton 及类Fenton 氧化处理后出水各项指标的变化。
1.4 分析方法
样品经过0.22 μm 滤膜过滤后测定各项参数。TC 浓度采用紫外-可见分光光度计于360 nm 下定量测定, pH 值采用pH 计测定, 色度采用稀释倍数法, CODCr采用重铬酸钾氧化法, H2O2浓度采用高锰酸钾滴定法标定[11]。
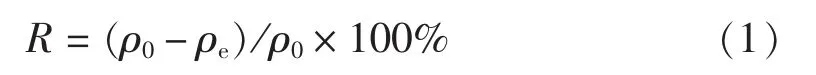
式中: R 为TC 去除率, %; ρ0为原水中TC 质量浓度, mg/L; ρe为处理后出水TC 质量浓度, mg/L。
2 结果与讨论
2.1 pH 值与反应时间对处理效果的影响
pH 值是影响Fenton 反应的重要参数[17]。 Fenton、EDTA-Fe3+、 Fe3+、 Fe6+类Fenton 等4 个反应体系均设置pH 值为3、 4、 5、 7 等水平, 反应时间为120 min, H2O2投加量为1 mmol/L, H2O2与铁离子的物质的量比为10 ∶1, EDTA-Fe3+类Fenton 体系中EDTA 与Fe3+的物质的量比为1 ∶1, 试验开始后每隔10 min 取样1 次, 考察pH 值与反应时间对TC去除率的影响, 结果如图1 所示。
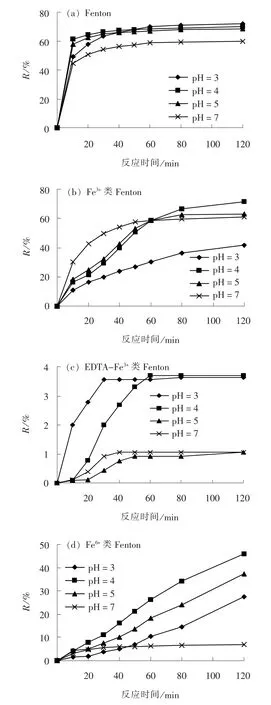
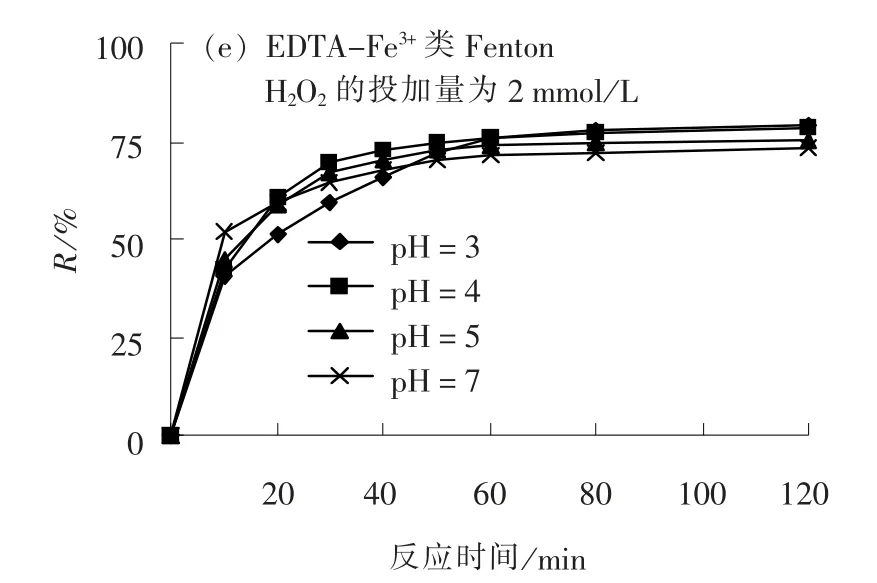
图1 pH 值对TC 去除效果的影响Fig. 1 Effect of pH value on TC removal
由图1 可以看出, TC 在4 种反应体系中的降解过程有明显差异。 从降解效果来看, 效果最好的是Fenton 反应, 其次是Fe3+类Fenton 反应。 Fenton反应中自由基以·OH 为主, Fe3+类Fenton 反应中产生HO2·, HO2·氧化能力低于·OH[20], 因此处理效果略差。 EDTA-Fe3+类Fenton 反应对TC 的去除效果最差, 仅为0.9%~3.6%。 由此可见, 投加EDTA 后对Fe3+的催化作用产生了抑制。 李春娟等[18]研究表明EDTA 促进Fe3+的溶解, 强化了Fe3+对H2O2的催化分解反应, 加速了有机物的降解。 这与本试验结论正好相反, 经过对比研究发现, 本试验中H2O2投加量比文献[18]中的要低很多, 猜测是因为其投加量过低造成本次反应的去除率不高, 当提高H2O2投加量为2 mmol/L 时, TC 去除率有明显增加(见图1(e))。 分析认为在H2O2浓度较低时, 对Fe3+的需求较少, EDTA 的促进作用不明显, 反而作为有机物的EDTA 有可能会与TC 竞争较少的·OH,从而降低了TC 的去除率。 Fe6+类Fenton 体系中TC的去除率在8%~50%之间。 文献[21]表明高铁酸钾与水反应会生成氢氧化钾与氧气, 导致出水pH 值上升, 而且高铁酸钾的氧化能力和稳定性受pH 值的影响很大, 其在酸性条件下的氧化性要远远高于中性和碱性条件。
不同反应体系中pH 值对TC 去除效果的影响也存在明显的差异。 由图1(a)可知, Fenton 反应前40 min, pH 值为4 时, TC 的去除率最高, pH值为7 时处理效果最差。 当pH 值过低, Fe3+不能够顺利地被还原成Fe2+, 造成·OH 的链反应受阻;pH 值过高, 一方面会造成铁离子以氢氧化物的形式沉淀从而使催化作用降低, 另一方面会抑制·OH的生成[22]。 在反应40 min 后, 当pH 值为3 ~5 时,TC 的去除效果差异不大。
由图1(b)可知, Fe3+类Fenton 体系中pH 值对反应效果影响更大, 当pH 值为3 时, TC 去除率最低, pH 值为中性时, 前50 min 内TC 去除效果最好, 在50 min 后pH 值为4 时反应效果最好, 略高于Fenton 反应。 由图1(c)、 (e)可知, EDTAFe3+类Fenton 反应受pH 值的影响较小。
反应时间对不同体系中TC 的去除效果影响也有较大差异。 由图1 可知, Fenton 反应速度最快,10 min 内基本完成反应, 20 min 后去除效果基本稳定; EDTA-Fe3+体系20 min 基本完成反应, 60 min后保持稳定; pH 值对Fe3+类Fenton 体系反应速度影响较大, 中性条件下, 反应速率较快, 60 min 后基本稳定; Fe6+类Fenton 体系在120 min 内, TC去除率一直保持上升的趋势, 反应达到平衡所需时间较长。
因此, 经综合考虑, 试验最佳pH 值为4, 反应时间为60 min。
2.2 H2O2 与铁离子物质的量比对处理效果的影响
调节进水pH 值为4, 反应时间为60 min, H2O2的投加量为1 mmol/L, 改变不同反应体系中铁离子投加量, 使H2O2与铁离子物质的量比为5 ∶1 ~15 ∶1, 考察其比值对TC 去除率的影响, 结果如图2所示。
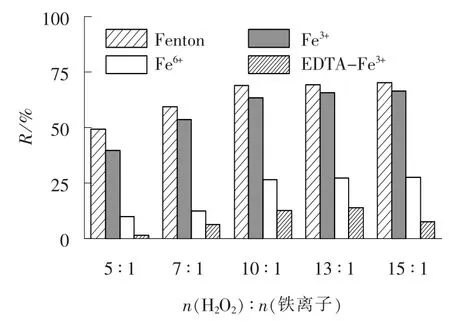
图2 H2O2 与铁离子物质的量比对TC 去除效果的影响Fig. 2 Effect of mass ratio of H2O2 to Fe on TC removal
由图2 可以看出, 虽然4 种反应中TC 的去除效果存在明显的差异, 但其去除率均随着两者物质的量比的增加而增加, 当H2O2与铁离子物质的量之比超过10 ∶1 后, 去除率增加的幅度较小。 从处理效果和经济角度考虑, H2O2与铁离子最佳物质的量比为10 ∶1。 此时, Fenton 反应中TC 的去除率为68.9%, Fe3+类Fenton 反应中TC 的去除率为63.5%,Fe6+类Fenton 反应中TC 的去除率为26.7%。
EDTA-Fe3+类Fenton 反 应 中, H2O2与 铁 离子物质的量比对TC 去除率影响的趋势与其他3 个反应存在一定的差异, 当两者物质的量比为13 ∶1 时,TC 的去除效果最好, 最大去除率为14.1%; 当两者的物质的量比为10 ∶1 时, TC 的去除率略微降低。这进一步说明, EDTA-Fe3+类Fenton 反应需要比其他3 种反应更高的H2O2投加量。
因此, 经综合考虑, 最佳H2O2与铁离子物质的量比为10 ∶1。
2.3 试剂投加量对处理效果的影响
进水pH 值为4, H2O2与铁离子物质的量为10 ∶1, 反应为60 min 的条件下, 考察H2O2投加量对TC去除率的影响, 结果如图3 所示。
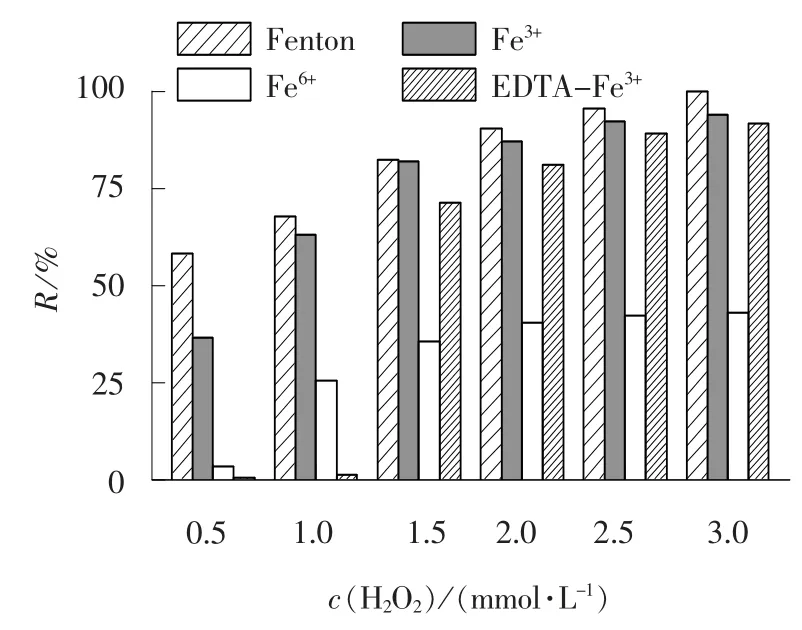
图3 H2O2 投加量对TC 去除效果的影响Fig. 3 Effect of H2O2 dosage on TC removal
由图3 可以看出, TC 的去除率均随着H2O2投加量的增加而增加, 去除率大小依次为Fenton >Fe3+>EDTA-Fe3+>Fe6+, 该结果与图1 有所不同。Fenton 试剂在H2O2投加量为2.0 mmol/L 时, TC 去除率已达到90.4%, 当H2O2投加量为2.5 mmol/L 时TC 的去除率更达到95.6%, 此后增加投加量对处理效果的影响不大, 因此Fenton 试剂反应中H2O2最佳投加量为2.5 mmol/L。 Fe3+类Fenton 反应在H2O2投加量为2.5 mmol/L 时, 对TC 的去除率已达到92.3%, 去除率也基本保持稳定。
对于EDTA-Fe3+类Fenton 试剂, 当H2O2投加量低于1 mmol/L 时, TC 的去除率非常低, 甚至低于Fe6+类Fenton 试剂; 当H2O2投加量达到1.5 mmol/L时, TC 的去除率迅速增加; 当H2O2投加量为2.5 mmol/L 时, TC 的去除率为89.3%; 当H2O2投加量为3.0 mmol/L 时, TC 的去除率为91.9%。 试验结果表明H2O2投加量是影响EDTA-Fe3+类Fenton 试剂去除效果的重要因素之一, 且EDTA-Fe3+类Fenton反应中TC 的去除率仍低于Fenton 和Fe3+类Fenton反应。 这与文献[18]的研究成果存在差异, 分析原因可能是本试验在酸性条件下完成, EDTA 对Fe3+类Fenton 试剂的促进作用没有发挥出来。
对于Fe6+类Fenton 反应, 在H2O2投加量为2.0 mmol/L 时, TC 的去除率为40.4%, 此后增加其投加量对去除率的影响不大。 同样也可以看出,Fenton 与其他2 种类Fenton 相比, Fe6+类Fenton 试剂的去除效果不理想。
因此, 综合考虑, 最佳的H2O2投加量为2.5 mmol/L。
2.4 对出水CODCr 浓度的影响
在进水pH 值为4, H2O2投加量为2.5 mmol/L,H2O2与铁离子物质的量比为10 ∶1, 反应时间为60 min 的条件下, 分别对原水以及Fenton、 3 种类Fenton 法处理后出水CODCr浓度进行检测, 结果如图4 所示。
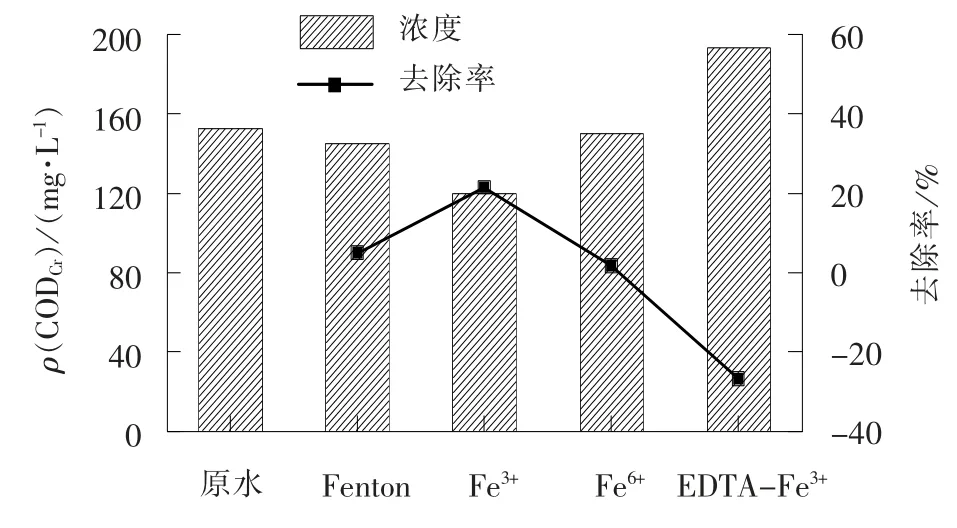
图4 不同处理方法对出水CODCr 浓度的影响Fig. 4 Influence of different treatment processes on effluent CODCr concentration
由图4 可见, 本试验中Fenton 法和类Fenton 法对CODCr的去除效果均较差, 经Fe3+类Fenton 法处理后CODCr的去除率最高, 但仅为21.4%; Fe6+类Fenton 法对CODCr去除率仅为1.6%; EDTA-Fe3+类Fenton 处理后出水CODCr浓度高于进水, 分析其原因可能是EDTA 为有机物, 增加了废水中有机物负荷。 因此, 单从CODCr去除角度来看, EDTA-Fe3+类Fenton 不适合用于废水处理。 由此可见, 试验采用的Fenton 试剂和类Fenton 试剂并不能使TC 完全矿化, 在试验最佳条件下有机物矿化率较低, 这可能是因为TC 为四环结构, 结构十分稳定[21]。
2.5 对出水色度的影响
在上述最佳试验条件下, 考察不同处理方法对出水色度的影响, 结果如图5 所示。
由图5 可见, 废水经Fenton 法和类Fenton 法处理后, 色度均有明显的增加, 由原来的28 倍,增加到68 ~72 倍。 4 种方法处理后出水色度差异性并不明显, 其中EDTA-Fe3+类Fenton 法的出水色度略低于其他处理方法, 这与EDTA 对Fe3+络合作用有关。
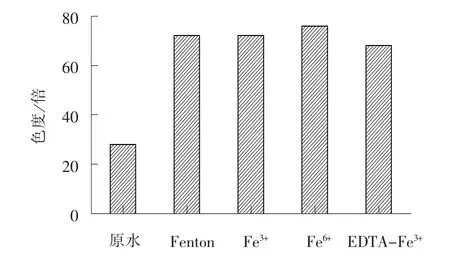
图5 不同处理方法对出水色度的影响Fig. 5 Influence of different treatment processes on effluent chroma
由此可见, 在实际应用中, 采用Fenton 法、 类Fenton 法处理TC 废水, 其出水需进一步脱色处理,出水色度升高是该方法的一个明显缺点。 在EDTAFe3+类Fenton 体系中, EDTA-Fe3+具有强烈的络合作用, 虽然出水色度略低于其他几种试剂, 但其后续脱色的难度较大。
2.6 紫外全波长扫描结果分析
本研究对选定条件下出水进行了紫外-可见光谱(200 ~800 nm)波长进行了扫描, 结果如图6 所示。
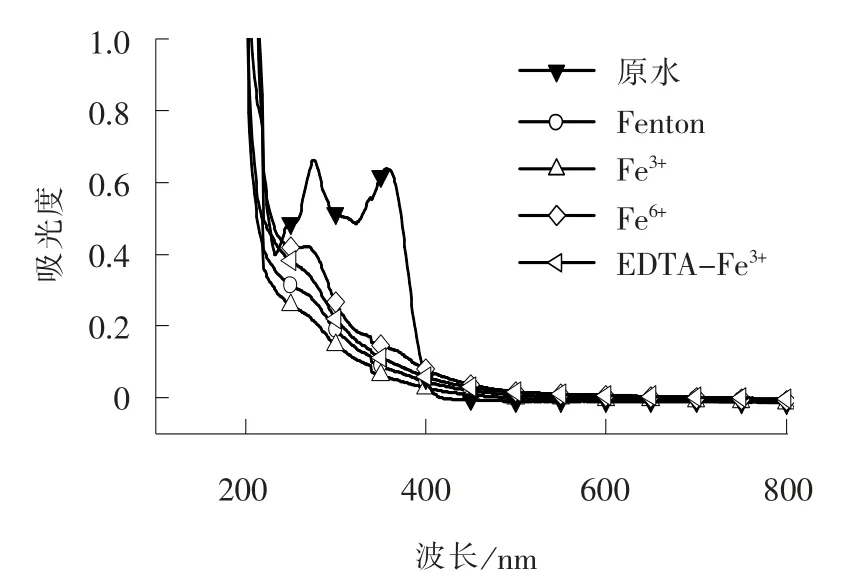
图6 进出水紫外全波长扫描结果Fig. 6 UV full wave scanning results of influent and effluent water
TC 具有多个共轭结构, 因此在紫外可见波段都有特征吸收[11]。 从图6 可以看出, TC 原水在275、360 nm 左右有2 个很明显的吸收带, 这2 个吸收带分别对应着TC 上4 个不同的环结构[21]。 TC 的吸收峰在经过Fenton 法、 类Fenton 法处理后急速降低,在360 nm 波长处吸收峰已完全消失, 在275 nm 波长处存在较低吸收峰。 这说明TC 被迅速降解, 共轭结构被迅速破坏, 已经分解成极其微小的分子碎片, 共轭结构被破坏的部位可能发生在TC 最为脆弱的不饱和双键部位[11]。 Fe3+类Fenton 法处理后的吸收峰最低, Fe6+类Fenton 处理后吸收峰最高, 结合图4, 进一步说明Fe3+类Fenton 处理后TC 的矿化程度最高, Fe6+类Fenton 处理效果最差。 经EDTAFe3+类Fenton 法处理后的峰高要低于Fe6+类Fenton法, 表明EDTA-Fe3+类Fenton 法对TC 的处理效果好于Fe6+类Fenton 法, 出水CODCr中有一部分来源于EDTA 本身。
3 结论
(1) 在H2O2投加量为1 mmol/L, H2O2与铁离子的物质的量比为10 ∶1, EDTA-Fe3+类Fenton 体系中EDTA 与Fe3+的物质的量比为1 ∶1 的条件下,Fenton 反应在pH 值为3、 4、 5 时对TC 的去除效果均较好, pH 值为7 时处理效果较差; Fe3+类Fenton法在pH 值为3 时处理效果较差, pH 值为4 ~7 之间差异不大; Fe6+类Fenton 法在pH 值为4 时的处理效果最好; EDTA-Fe3+类Fenton 法适用的pH 值范围较宽。
(2) 在pH 值为4, 反应时间为60 min, H2O2的投加量为1 mmol/L 的条件下, H2O2与铁离子的物质的量比对Fenton 法、 类Fenton 法的处理效果有较大影响。 Fenton 法、 Fe3+、 Fe6+类Fenton 法中H2O2与铁离子的物质的量比为10 ∶1 时处理效果最佳;EDTA-Fe3+类Fenton 法中H2O2与铁离子的物质的量比为13 ∶1 时处理效果最佳。
(3) 在pH 值为4, 反应时间为60 min, H2O2与铁离子的物质的量比为10 ∶1 的条件下, Fenton、Fe3+、 EDTA-Fe3+类Fenton 法中H2O2的最佳投加量为2.5 mmol/L, Fe6+类Fenton 法中H2O2的最佳投加量为2.0 mmol/L。 其中EDTA-Fe3+类Fenton 法受H2O2投加量影响较大, 低投加量时处理效果较差。
(4) 从实际应用角度分析, 高铁酸盐不适合直接作为类Fenton 试剂处理TC 废水; Fenton 法在pH值为3 ~5 时处理效果最好; Fe3+类Fenton 法的处理效果较Fenton 法差, 但由于Fe3+较为经济, 也是类Fenton 试剂的一个很好选择, 且其对TC 的矿化率较高; EDTA-Fe3+类Fenton 法虽然pH 值范围较广, 但所需的H2O2投加量较高, 而且EDTA 作为有机物, 会增加进水的有机物负荷, 导致CODCr去除效果不佳, 同时其对Fe3+的络合作用将给后续脱色处理带来困难。 总体上看, Fenton 法、 类Fenton法处理后出水色度均较高, 后续需进行脱色处理。
