碳纳米管的功能化修饰及其药物负载的研究进展
2021-03-12田胜池昊顾晨露李秀童珊珊徐希明
田胜,池昊,顾晨露,李秀,童珊珊,徐希明
(江苏大学药学院,江苏 镇江 212013)
碳纳米管是由日本科学家饭岛澄男博士在研究富勒烯过程中发现的一种奇特碳结构[1],因其独特的结构和物理化学性质,迅速成为生物医药领域的研究热点。碳纳米管是由石墨烯片同轴卷曲而成的新型纳米碳材料,按照石墨烯片层数不同,可分为单壁碳纳米管(single-walled carbon nanotubes,SWCNTs)和多壁碳纳米管(multi-walled carbon nanotubes,MWCNTs)。
单壁碳纳米管是由一个单一的圆柱形石墨烯层组成,两端覆盖着一个半球形的碳网络,柱体的闭合是由于生长过程中包含了五边形和七边形的C-C结构,如图1A所示。而多壁碳纳米层与层之间无序排列,层间距为(0.34±0.01) nm[2],直径为2~25 nm,长度为0.1~50.0 μm,内部结构如图1B。MWCNTs的外径一般大于2.5 nm,而SWCNTs的外径在0.6~2.4 nm之间。平面内sp2杂化的刚性s-键长为1.42 Å,具有极高的杨氏模量,而平面外p键则具有较弱的范德华层间粘合力。MWCNTs的不同壳体通过范德华力相互作用(在没有结构缺陷的情况下),而SWCNTs形成管束,其中管间耦合也是由范德华力相互作用决定的。这些结构中强sp2键合和弱范德华力的不同程度的相互作用,是纳米管异常多样的力学行为的根源。MWCNTs结构与富勒烯相似,管壁主要是由sp2杂化的六边形碳原子网格围成,每个碳原子与相邻的三个碳原子键合。但这种同轴卷曲会导致纳米材料的量子限域效应和σ-π再杂化,π轨道离域后偏向管壁外侧,而C原子上的其他三个σ轨道偏离平面,使其比石墨具有更高的机械强度,独特的光学力学和催化性质,较大的比表面积以及良好的生物化学活性[3]。
目前商品化多壁碳纳米管已经广泛运用在众多应用领域,如电子学、光学、生物医学等。MWCNTs由于其强大的比表面和相互之间的范德华作用,长径比过大,经常会团聚从而形成致密的网络,且碳纳米管表面缺少亲水的官能团,分散性和生物相容性较差,使得其在生物和生物医学领域的应用受到了各种限制。
碳纳米管表面可修饰不同功能的基团,使其与大量活性位点相结合,提供堆叠功能,增加其分散性和生物相容性,成为医药领域的研究热点[4-5]。首先,由于存在较大的长径比,碳纳米管之间存在很强的范德华力,极易产生缠绕团聚,局部区域有凸凹现象,石墨烯结构中的六边形相连过程中易出现五边形和七边形。当MWCNTs端口处出现七边形时,其表面会凹陷,拓扑缺陷会改变碳纳米管的sp2杂化结构,导致电子能带的改变进一步造成结构的改变,所以MWCNTs管端和侧面易于被氧化和表面修饰(图1)[6]。其次,碳纳米管是由单一的碳原子通过sp3和sp2杂化组成,化学活性低,结构稳定,很难与聚合物基体发生化学反应,所以需要对碳纳米管进行有效的表面修饰,改善其分散性能,从而发现其潜在作用,拓宽其应用范围[7-8]。
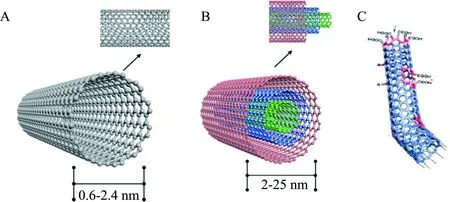
A:单壁碳纳米管;B:多壁碳纳米管;C:表面缺陷结构
功能化的过程也有助于将治疗分子或配体与碳纳米管的表面或末端结合,增强其对靶细胞的活性,本文主要从碳纳米管的多种表面修饰及功能化方法方面,探究其在药物负载中的应用。
1 碳纳米管的表面修饰
1.1 共价修饰
利用化学方法,将各种分子基团共价接枝到材料表面是一种重要的修饰手段。如图2所示,用不同氧化剂处理后,碳纳米管表面可能会引入不同的官能团,包括醇类、羧酸类、醛类、酮类和雌激素类的含氧官能团。修饰的方法包括酸化反应、1,3-偶极环加成反应、亲电加成反应以及电化学反应等[9]。

图2 碳纳米管共价修饰后表面含氧基团可能存在的结构[10]
根据修饰物的不同,目前研究的共价修饰的MWCNTs的反应条件及目的用途如表1所示。

表1 对MWCNTs共价修饰方法
共价修饰对碳纳米管的功能化改性具有重要的作用,一般情况下共价修饰会在碳纳米管端口或侧链上引入—OH或—COOH等含氧基团,同时也会使碳纳米管产生破损或断裂。碳纳米管破损(或断裂)一方面使其细化,另一方面增多了碳纳米管中不饱和键(π键)的碳原子数目,增强了碳纳米管自身反应活性。
碳纳米管还可以通过不同的方法引入其他基团,运用到药物载体中。如图3所示,碳纳米管上的羧基可与其他表面活性分子结合,或直接与短肽、蛋白质、抗肿瘤药(如甲氨蝶呤) 或靶向分子(如叶酸) 的氨基生成酰胺键连接。碳纳米管载药系统具有靶向作用,简单的羧基化MWCNTs改善了生物相容性及分散性,而经叶酸[22]或透明质酸[23]等靶向因子后续修饰后可具有主动靶向作用。孟艾等[22]制备了大内径多壁碳纳米管靶向抗肿瘤药物缓释系统,通过聚乙二醇的氨基与靶向分子叶酸的羧基发生酰胺反应,在碳管表面接枝叶酸,利用受体在肿瘤细胞表面高表达的特点,使载体系统具有肿瘤靶向性。

图3 SWCNTs功能化结构图[24]
1.2 非共价修饰
非共价修饰保留了碳纳米管结构的完整性,不会对碳纳米管的固有特性产生较大影响。碳纳米管具有非常大的比表面积和较强的吸附活性,表面有高度离域的、稳定的大π键,非共价化学改性主要是通过π-π堆积、范德华力、疏水力等弱相互作用力实现,其独特的优点是简便易操作且反应条件温和,在分散碳管的同时不破坏碳管本身的电子网络结构。非共价修饰主要有三大类,用来包裹MWCNTs的分子通常包括亲水性聚合物、表面活性剂和生物分子三大类,分散过程主要通过超声波、离心和过滤,方法快速而简单。
表面活性剂的疏水基团能与碳纳米管的疏水表面相互作用,而另一端亲水基团伸向水相溶液中,使碳纳米管表面具备高浓度的亲水基团,增强碳纳米管亲水性,从而提高碳纳米管在水中的分散性能,对其起到增溶等效果。表面活性剂能够渗透质膜,并且具有自身的毒性。因此,表面活性剂与生物系统相互作用的影响可能限制稳定的碳纳米管复合物在生物医学中的应用。
聚合物被广泛用作药物输送的分子载体,在碳纳米管的增溶过程中,其成为表面活性剂良好替代品。分散机理基于聚合物缠绕在碳纳米管周围,聚合物的空间排斥作用可提高碳纳米管分散性。非离子和阳离子共聚物,如聚乙烯吡咯烷可用于改善分散性,为聚合物碳纳米管的药物载体系统提供帮助[25]。
DNA、核酸、蛋白质等生物分子通过非共价键吸附或缠绕在碳纳米管表面的方式,能增加碳纳米管的生物相容性。其中,碳纳米管通过疏水相互作用或电荷转移相互作用与蛋白质结合,主要与蛋白质中氨基酸残端相互作用。
2 基于碳纳米管表面修饰的药物负载
碳纳米管具有较大的长径比和比表面积,使其能够吸附各种治疗分子或与之结合。通过适当的功能化,碳纳米管可以纳米载体等形式用于抗癌药物、基因和蛋白质的转运方面,现已成为新的研究热点[26]。见表2。
2.1 碳纳米管荷载化学药物
通过对碳纳米管的结构进行分析,碳纳米管层与层之间易成为陷阱中心而捕获各种缺陷,因而其管壁上通常布满小洞样的缺陷,这些缺陷在碳管载药时可作为药物进出的通道,可通过连接修饰基团实现药物的缓释或控释。部分药物分子可以利用碳纳米管结构,直接被包于碳纳米管腔内或吸附在其碳管内或碳束间,还可以利用共轭作用与功能化的碳纳米管外壁结合形成复合物运输至细胞内部。

表2 碳纳米管作为药物载体研究
载体系统充分利用碳纳米管纳米材料的性能优势,克服抗肿瘤药物在血液中分散性差、体内代谢清除快、穿透细胞屏障能力差等缺点,从而提高肿瘤患者化疗效果并最大程度减小化疗副反应,减轻患者痛苦。图4为Khorsand等[34]利用GGA/PBE泛函和DZP基函数,并结合范德华密度泛函计算青霉胺药物在扶手椅和锯齿形单壁碳纳米管中的包封情况。结果表明,包裹在碳纳米管空腔内的药物呈弱结合,与扶手椅型单壁碳纳米管相比,锯齿形单壁碳纳米管更有利于药物的渗入。
碳纳米管具有中空结构、高强度韧性及良好的化学和热力学稳定性等特点,尤其具有纳米尺度的圆柱形孔洞。因此,碳纳米管可以利用管体空腔容纳药物分子,而且可在载送过程中保护药物分子免受破坏。碳纳米管作为药物传送系统的运输载体可以避免光敏感性药物暴露在载体表面而造成的药物失活。
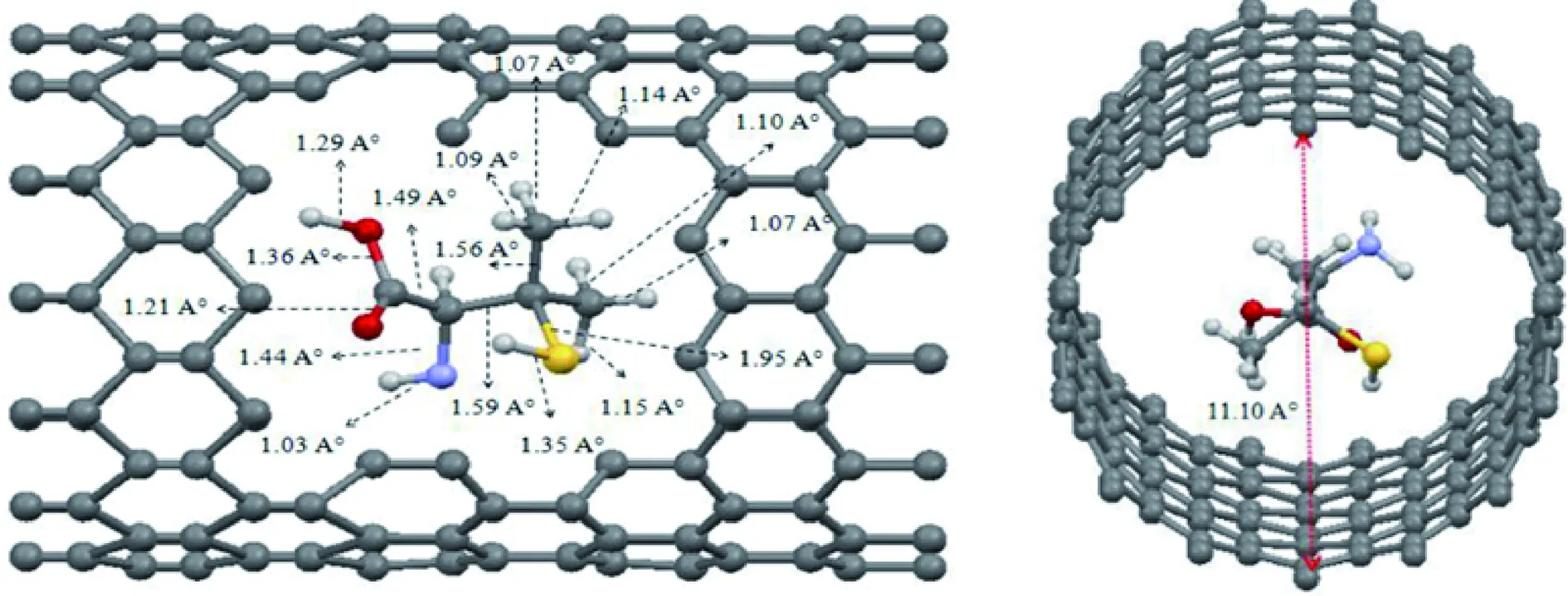
图4 青霉胺药物包裹在碳纳米管官腔内[34]
性能优异的抗肿瘤载药系统除须具有较高的载药率及合理的药物释放模式外,还应具有肿瘤细胞靶向性,碳纳米管多应用于抗肿瘤药物的载体。共价修饰或非共价修饰后的碳纳米管均可利用π-π键同时连接药物分子和靶向活性基团,形成一个高效的靶向药物递送系统,将一些抗肿瘤药物如阿霉素类、顺铂等包封后,增加载药量,并且其载体具有缓释效果,可显著地降低毒副作用以及提高治疗效率[35]。
2.2 碳纳米管荷载大分子药物
蛋白质等大分子能自发吸附在羧基化碳纳米管的侧壁上,从而形成蛋白质—CNT共轭物。蛋白质的传递由羧基化碳纳米管的阴、阳离子所介导,碳纳米管可以实现多肽和蛋白质在生物体内的转运,并在低毒的基础上保留并促进其原本所具有的生物活性。由于受氨基酸硫原子孤对电子以及甲基氢原子的H-π作用影响,碳纳米管与含硫氨基酸侧链在不同电荷状态下结构呈现不同的变化。
此外,电荷对碳纳米管与芳香环氨基酸侧链的结合有着很好的调控作用,随着MWCNTs复合物表面电荷的增多而结合增强。Li等[36]通过实验研究聚赖氨酸修饰的AFM针尖与羧化碳纳米管在不同pH值下的黏附性能,结果证明随着pH值的降低和氧化时间的延长,聚赖氨酸与碳纳米管之间的黏附力增加。见图5。

图5 在不同pH值下,聚赖氨酸与羧化碳纳米管之间相互作用示意图[36]
重要的是,碳纳米管与芳香环氨基酸侧链作用时,进行分子轨道分析后发现电荷都聚集在碳纳米管表面。这种电子积累说明在蛋白质修饰过的碳纳米管电极中,电荷可以通过π-π通道从蛋白质转移到碳纳米管。
分子模拟方法广泛应用在碳纳米材料的生物医学领域的研究中,可从原子水平上揭示各种物质分子在碳纳米管表面的物理行为。如图6所示,蛋白质吸附能力随着碳材料的表面曲率减小而增加。蛋白质在碳纳米结构上的相互作用和吸附程度主要取决于这些纳米材料的表面曲率。研究人员利用基于经验力场的计算机模拟,使用分子动力学模拟计算两亲性全长淀粉样β(Ab)肽与SWCNTs凹表面、石墨烯平面、SWCNTs凸表面的结合自由能,发现内(凹)表面对具有代表性的两亲性肽的吸附最为强烈和有效,其次是平面和外(凸)表面。

A:SWCNTs凹表面;B:石墨烯;C:SWCNTs
类似的研究包括通过对SWCNTs与药物代谢细胞色素P450酶CYP3A4的相互作用[38]进行详细计算,研究证明单壁碳纳米管与CYP3A4之间可直接相互作用(图7)。因此,可利用碳纳米管特性将蛋白质有效递送至细胞中,保护其免受酶的水解。因此,碳纳米管可以携带蛋白质类药物通过细胞内吞作用进入到细胞内。
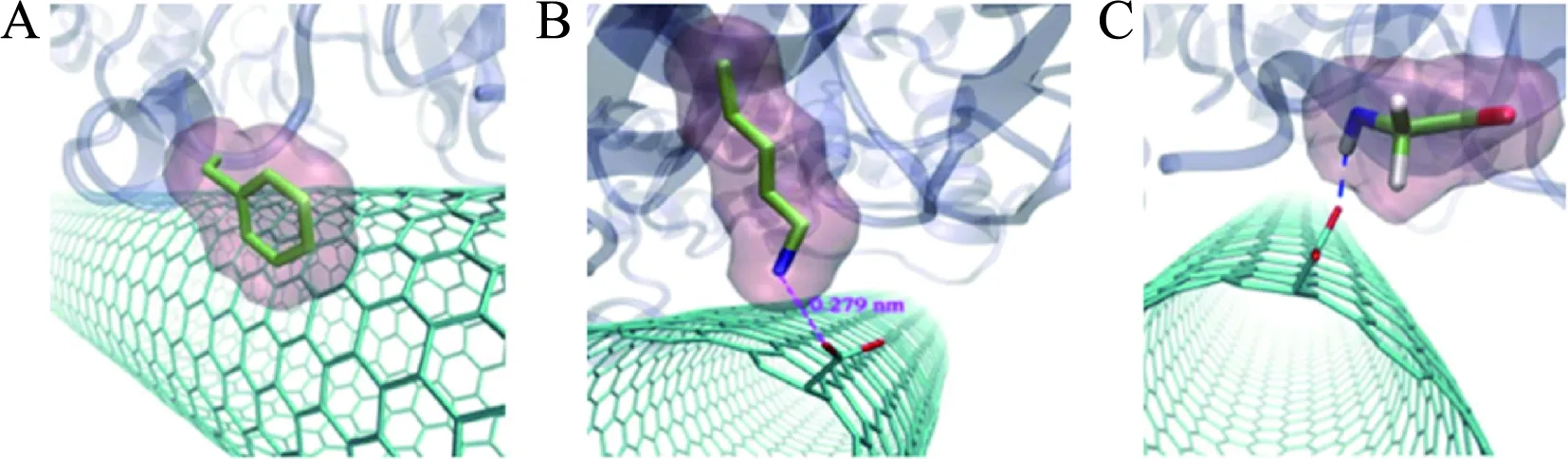
A:π-π堆积相互作用;B:盐桥相互作用;C:氢键相互作用
2.3 磁性碳纳米管的物理化学靶向作用
不同于生物靶向活性分子,磁性靶向物质需要在外加磁场的作用下发挥靶向作用,即以放置于肿瘤部位的磁场为引导,促使载药系统向该部位聚集。
超顺磁性纳米粒Fe3O4可以沉积至氧化的碳纳米管表面,形成超顺磁性碳纳米管粒子,即碳纳米管-Fe3O4纳米复合物。碳纳米管负载在刚性基质表面,同时进行亲水改性是解决其分散性差、易团聚的有效途径。将碳纳米管与Fe3O4磁性纳米粒子复合,制得的磁性碳纳米管具有分散性好、比表面积大、吸附性能好、易于实现液固分离等优点。如图8所示,在外加磁场的作用下,碳纳米管-Fe3O4纳米复合物发生定向聚集。同理,携带抗肿瘤药物的磁性碳纳米管在外加磁场的作用下,可在磁场区域靶向聚集并选择性地杀死肿瘤细胞[39-40]。
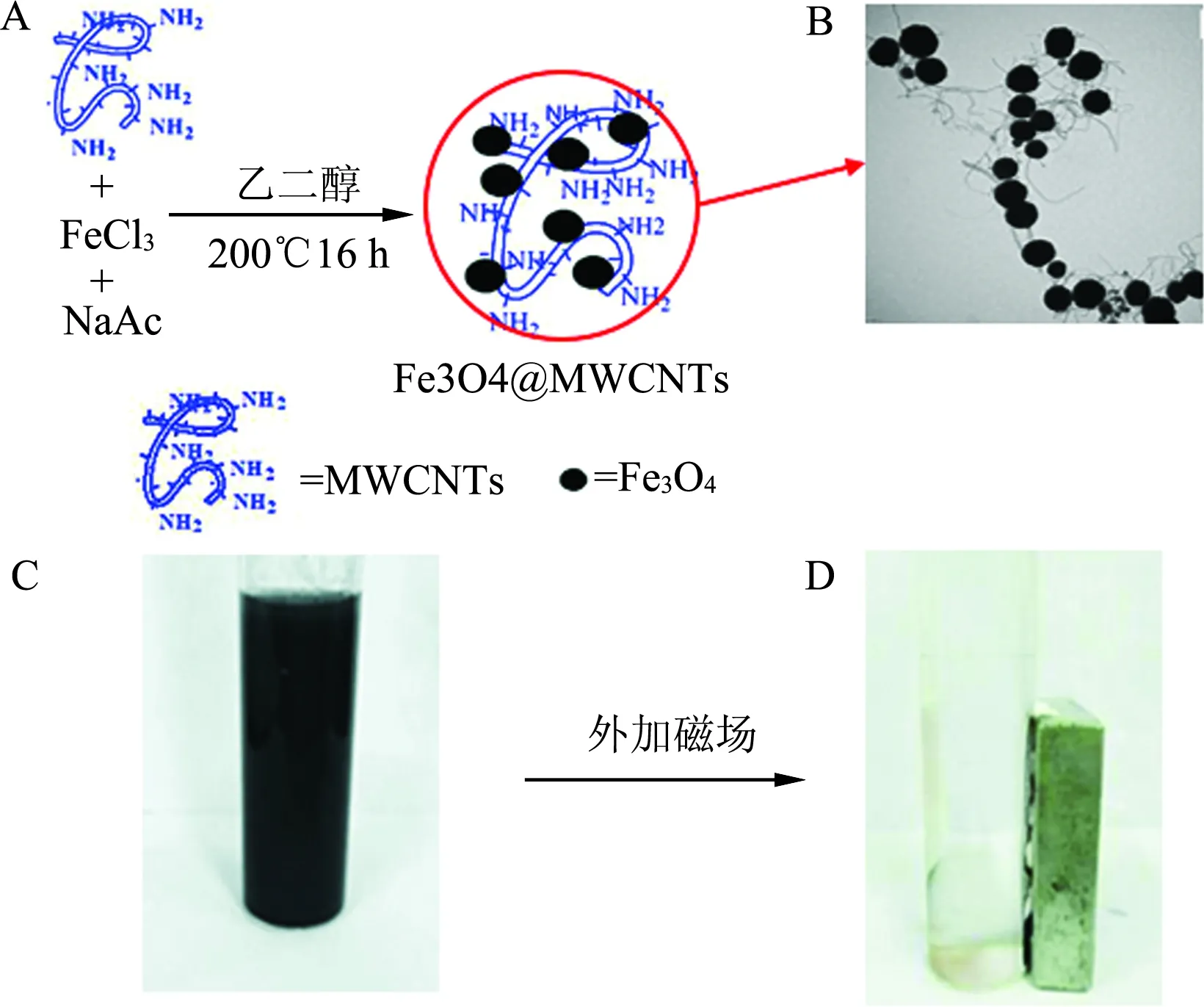
A:制备原理;B:表征;C:未加磁场;D:加磁场后
3 小结
基于碳纳米管的自身特性,碳纳米管纳米材料代表了一类新的药物载体,可与具有治疗活性的分子或蛋白质大分子进行共价和非共价功能化结合进行治疗。发展碳纳米管潜在应用的同时,碳纳米管的安全性是不可忽视的问题。目前,碳纳米管的临床应用前景仍存在一定的缺陷。在药学领域,对碳纳米管细胞毒性研究是对其安全性研究的重点,此方面工作自1991年国内外相关论文约2 800篇。2017年,世界卫生组织国际癌症研究机构将碳纳米管、多壁碳纳米管MWCNT-7归纳入2B类致癌物清单中,说明碳纳米管在人体内的安全问题仍未完全得到解决。碳纳米管的分散性、碳纳米的长度以及团聚情况是其经细胞摄取的关键,未经任何基团修饰的碳纳米管由于高度疏水性,在细胞培养过程中与细胞发生相互作用,与蛋白质、核酸等物质聚合,产生一定细胞毒性。碳纳米管毒性的大小不仅会随孵育时间、浓度分散程度、细胞种类的变化而变化,也与其粒径、表面积、制备方法、修饰基团等相关。因此选择合适的修饰方法对碳纳米管进行修饰,提高碳纳米管的分散性和生物相容性对其在新型给药系统中的应用有着重要作用。
以碳纳米管作为药物载体,所选择的药物必须具有特殊结构,能与碳纳米管的官能团相结合,或是药物的结构能够与相应的中间连接物反应,通过中间连接物的特殊官能团与碳纳米管结合。目前虽已证实多种方法可实现碳纳米管的修饰,但对其修饰方法、界面结构、产品特性等知识尚不完善,仍需进一步探讨最佳的碳纳米管表面修饰位点和饱和度。
值得注意的是,碳纳米管在波长808 nm处有热敏效应且具有良好的导电性能,在肿瘤热疗领域也有一定的应用。通过控释系统控制碳纳米管和药物在肿瘤部位释放,在连续的近红外光照射下,碳纳米管的特性可将光能迅速转化成热能,使肿瘤细胞因局部过热而死亡,说明该研究能适用于肿瘤热疗法。
目前研究人员正在不断探索碳纳米管在药物传递方面的潜力,充分了解其相容性的局限性,将有助于碳纳米管纳米材料载药系统的合理设计。功能化碳纳米管用于药物输送的主要目的是增加其在水介质中的溶解度,且功能化碳纳米管在生理系统中与原始碳纳米管相比更具生物相容性。
