杂原子掺杂碳材料用于氧还原反应催化剂的研究*
2021-03-08魏家崴强富强王焕磊
魏家崴,李 平,强富强,王焕磊
(中国海洋大学 材料科学与工程学院,山东 青岛 266100)
0 引 言
煤、石油、天然气等化石燃料的开采与消耗引起了能源枯竭和环境污染等问题,迫使我们需要发展效率高、环境友好的新型能源技术。燃料电池[1]和空气电池[2]是拥有高比容量和高能量密度的环保型便携器件,拥有很高的研究价值和广阔的应用市场。然而,阴极动力学缓慢的氧还原反应(ORR)极大地限制了电池的总反应速度,也因此影响了电池性能的进一步提升,所以提高电池效率的一个方法是改善阴极的氧还原反应,即在阴极材料中添加氧还原反应催化剂[3-5]。
目前市面上的氧还原反应催化剂为Pt/C贵金属[6],催化能力高但也面临着许多问题,比如储量稀少带来的高价格以及循环稳定性差和耐甲醇等燃料的毒副作用能力不佳等[7-9]。碳基材料催化剂被认为是最有希望的贵金属替代物,碳基材料不仅拥有低廉的成本,也有优异的导电能力、良好的化学稳定性和较大的比表面积等,易于氧还原反应中氧的吸脱附和电子的传输[10-11]。对碳材料进一步掺杂以提高碳材料的催化能力、稳定性等是近年来研究的热点[12]。如图1所示,杂原子掺杂无金属碳材料用于ORR反应催化剂的研究逐年增加,因此本文简要讨论了氧还原反应的机理并总结了用于氧还原反应催化剂的杂原子掺杂碳材料,给出了用于掺杂的杂原子的类型以及掺杂提高催化性能的可能原因,最后,展望了碳基氧还原催化剂的发展方向。

图1 近几年关于无金属杂原子掺杂碳材料ORR催化剂发表论文数量
1 氧还原反应相关理论
氧还原反应一般发生于固、液、气三相界面上,可分为分为4e-转移和2e-转移。2e-转移会产生大量的过氧化物,过氧化物的强氧化作用会破坏电池的隔膜而降低电池的寿命,所以对于电池反应的氧还原过程而言,4e-转移是理想的还原过程。
1.1 氧还原反应过程
1.1.1 在碱性条件下的4e-转移
直接4e-转移,氧与水、电子生成氢氧根的过程:
O2+2H2O+4e-→4OH-,E0=0.401 V
或分两步进行:
1.1.2 在碱性条件下的2e-转移
第一步与4e-转移两步方式的第一步相同:
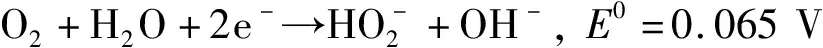
第二步为分解反应,不再获取电子:
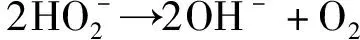
1.1.3 在酸性条件下的4e-转移
直接4e-转移,氧与质子、电子生成水的过程:
O2+4H++4e-→2H2O,E0=1.229 V
或分两步进行,生成中间产物过氧化氢:
O2+2H++2e-→2H2O2,E0=0.670 V
H2O2+2H++2e-→2H2O,E0=1.277 V
1.1.4 在酸性条件下的2e-转移
第一步与4e-转移两步方式的第一步相同:
O2+2H++2e-→2H2O2,E0=0.670 V
第二步为分解反应,不再获取电子:
2H2O2→2H2O+O2
1.2 氧吸附模型
对于氧还原过程还存在许多争议,为多数研究者所接纳的一种理论为氧在催化剂表面的还原方式与它的吸附方式有关,氧在催化剂表面的吸附模型分为三种,侧基式、桥基式和端基式[13]。
侧基式是氧分子中心的σ键与催化剂相作用,这种吸附方式可以使O—O键减弱,有利于使氧分子进行直接4e-转移过程;桥基式是氧的两个原子同时吸附在催化剂的表面,可以使两个氧原子同时得到活化,从而也有利于4e-转移过程;而端基式吸附则不同,端基式为氧分子中的一个与催化剂接触,从而只有一个氧原子得到活化,一般这种吸附方式为2e-转移过程。
在实际的氧还原过程中存在的反应十分复杂,在还原过程中可能存在着多个反应同时进行的现象,而且对于不同的催化剂也会存在不同的反应过程,甚至对于同种催化剂,在不同的酸碱溶液中也拥有不同的催化能力,分别进行4e-转移和2e-转移过程。
杂原子进入碳基体之后,会因为自身和碳基体之间的性质差异如电负性、原子半径等而引起碳基体的性质发生改变,如提高碳材料的电导率,改善材料对氧的吸附及还原产物的脱附能力等,而对于某些杂原子如氮原子,掺杂后形成的吡啶N和石墨N公认对氧还原反应有催化活性,可以提高碳材料的催化性能。

2 杂原子掺杂碳材料
碳材料本身在碱性条件下就拥有一定的氧还原催化能力,这可能与碳材料的边缘缺陷有关[14-15],但是它只在碱性条件下有活性且催化能力有限,杂原子掺杂碳材料就是将N、P、S、B等元素掺杂进碳材料从而进一步提高碳材料的催化能力、极限电流密度、循环稳定性、耐毒副能力等。可作为碳载体的材料有石墨烯[16]、碳纳米管[17]、MOF材料[18]和一些生物质材料[19-20]及其衍生物[21]等。
关于杂原子掺杂提高催化性能的理论还存有争议,但让大多数学者所接受的观点是催化能力的提高与杂原子和碳基体间的化学性质差异有关,杂原子和碳原子之间存在电负性、原子尺寸、键长键角等方面的差异,将其掺杂入碳原子后会引起周围原子电子密度和自旋等方面性质的改变,且会在碳基体中形成更多的缺陷[22],这可能是催化的活性位点。
2.1 N单原子掺杂碳材料
值得注意的是,N原子是在氧还原催化剂的制备中最常用的,也是最有效果的杂原子,这可能与N原子独特的电负性和原子半径等因素有关,N掺杂进入碳基体以后形成的吡啶N和石墨N常常被认为是氧还原反应的活性位点[23-24],所以大多数用于氧还原反应催化剂的碳材料都会选择N原子掺杂或者N与其他原子的共掺杂。
N掺杂碳材料可以通过多种方式制备,比如通过将含氮的碳前体或者均匀混合的氮源和碳源热解,或者以化学气相沉积(CVD)的方法将氮原子整合进碳体系中,制备过程中常用双氰胺[23]、尿素[25]、三聚氰胺[26]、氨气铵盐[27-28]、丙烯腈[29]等作为额外的N源。戴黎明[30]等人首先报道了利用高温下热解酞菁铁的方法制备了垂直排列的氮掺杂碳纳米管(VA-NCNT),用于碱性条件下的氧还原催化剂,并通过电化学氧化的方法去除了催化剂中的铁原子。通过与不掺杂N的碳纳米管(NA-CCNT)和Pt/C催化剂的对照结果表明,VA-NCNT的催化能力与Pt/C接近且远远超过了NA-CCNT,且VA-NCNT的扩散受限电流密度超过了Pt/C,这表明了N掺杂确实可以提高碳材料的催化性能且拥有比Pt/C催化剂更优良的性能。值得一提的是,VA-NCNT和Pt/C都是4e-转移而NA-CCNT是2e-转移,由此提出了氧在催化剂表面的吸附模型(如图2所示):碳基体中的吡啶型N原子拥有较高的电负性,会使相邻碳原子拥有更多正电荷,使氧在催化剂表面的吸附由端吸附变为侧吸附,从而使两个氧原子都得到活化而进行4e-转移过程。戴黎明[31]等人进一步用CVD的方法将含氮反应气体混合物(NH3:CH4:H2:Ar)沉积到镍薄膜上,再用盐酸蚀刻镍得到了氮掺杂石墨烯薄膜。XPS显示,N-石墨烯相较于石墨烯拥有更强的O 1s峰,表明N-石墨烯有对氧更强的吸附能力。研究表明N-石墨烯表现出与VA-NCNT相同的一步4e-转移途径,极限电流密度是Pt/C的3倍;耐交叉和毒性好,计时电流曲线显示加入氢气、葡萄糖甲醇和CO后电流密度基本不变,而Pt/C电极电流下降明显;循环稳定性好,在200 000次循环后没有明显的电流下降。
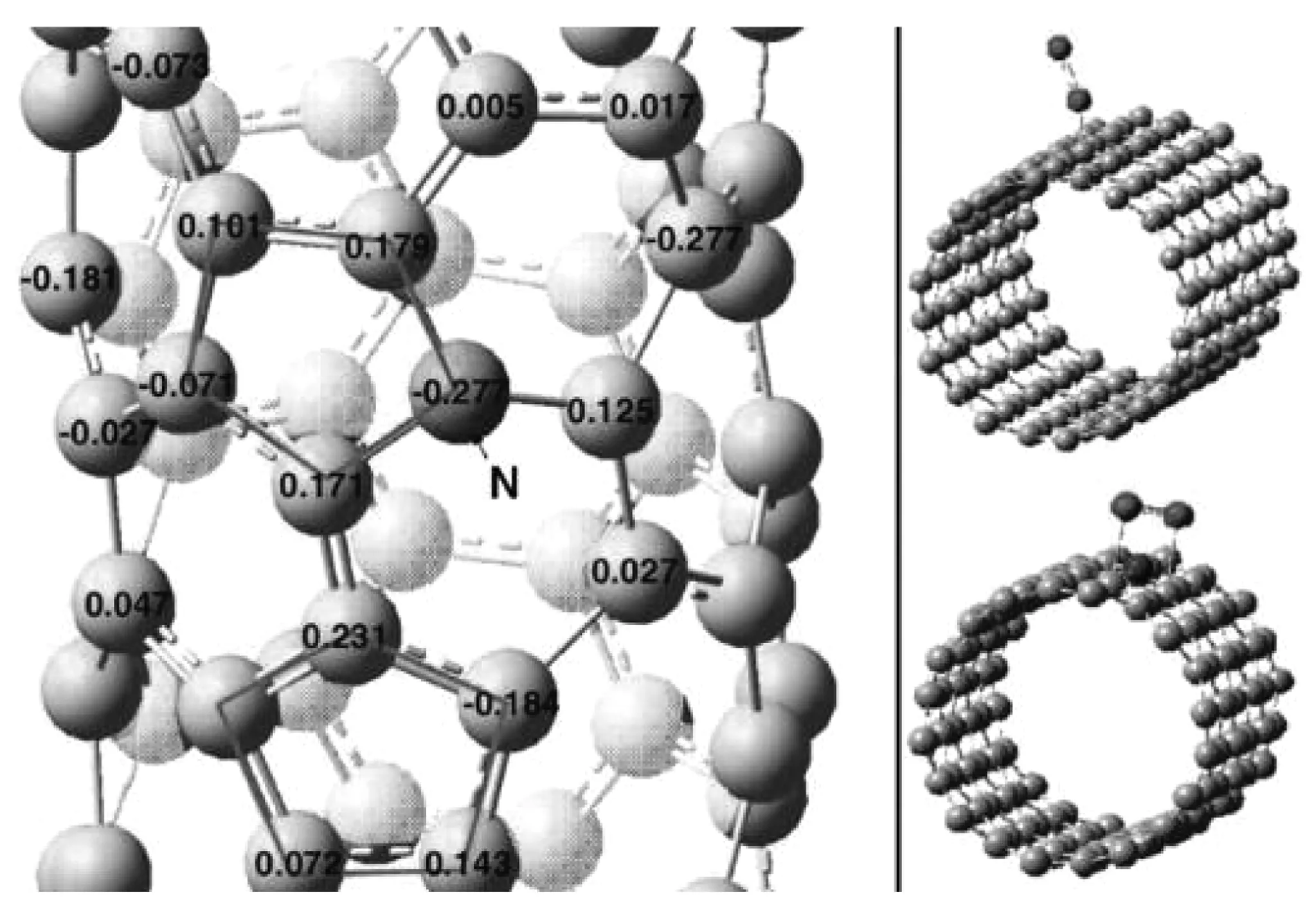
图2 VA-NCNT上氧的吸附模型[30]
N掺杂碳材料的催化性能引起了人们的关注,众多科研工作者通过不同途径制备N掺杂碳催化剂并对其进行研究。Zhen Huan Sheng[32]通过将氧化石墨烯(GO)与三聚氰胺研磨混合并在氩气气氛下碳化的方法制备了氮掺杂石墨烯(NGs)(图3(a))。电化学表征显示,NGs在碱性条件下拥有良好的氧还原催化活性,与垂直排列的氮掺杂碳纳米管类似。通过控制三聚氰胺用量和碳化温度的方法实现了NGs中N元素含量的调节,在GO与三聚氰胺质量比为0.2、碳化温度为700 ℃时N原子掺杂量可达10.1%(原子分数)。但是NGs的催化活性不受N元素含量的影响,主要可能与吡啶N的含量有关,表明提高吡啶N的含量可以进一步提高催化性能。Wen Yang[33]等以纳米SiO2为模板,通过将核酸碱基溶解在有机离子液体(Emim-dca)中形成的凝胶碳化,制备了表面积高达1 500 m2/g的介孔氮掺杂碳材料,材料中的氮含量达12%(质量分数),拥有接近Pt/C催化剂的活性。Daguo Gu[23]等以柠檬酸和双氰胺分别作为碳源和氮源,双氰胺缩合得到的中间体g-C3N4起到了作为热分解模板和原位氮源的作用,在1 000 ℃下碳化制备了N掺杂类石墨烯层状碳纳米片NC,如图3(b)所示。与市售Pt/C催化剂相比,双氰胺/柠檬酸质量比为6时制备的NC片的半波电位(E1/2)相差66~68 mV,具有较好的长期稳定性和良好的抗甲醇交叉性能。Jing Liu[25]将廉价炭黑BP与尿素研磨混合并在Ar气氛下于950 ℃下热解1.5 h得到了氮掺杂样品BPN。通过实验和量子化学计算的方法揭示了不同含N位对氧还原的催化活性顺序为吡啶N>吡咯N>石墨N>氧化N>C;Dheeraj Kumar Singh[34]将管状埃洛石粘土和盐酸多巴胺溶于TRIS buffe缓冲液中,生成了聚多巴胺涂层的纳米粘土,将其在800 ℃下于Ar气氛下热解,得到了N掺杂碳,简称为NDC-800,如图3(c);Yi Wang[35]以间苯二酚、甲醛和碳酸铵聚合并热解的方法制备了大比表面积的N掺杂分级多孔碳(LNHPC),制备示意图如图3(d),并且通过LNHPC和氨水于180 ℃下水热处理增加了材料中的N掺杂含量从而提高了材料的催化性能。Hengcong Tao[36]报道了一种制备N掺碳的无碳化方法,即在5 ℃的低温下将氧化石墨烯在氨水溶液中超声处理以实现氮的掺杂,控制超声时间和浴温实现了N掺杂水平的有效调节。
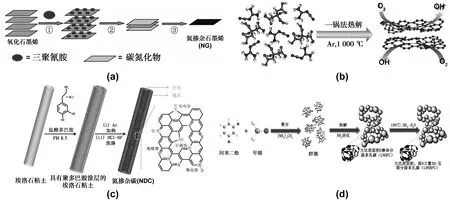
图3 (a)三聚氰胺在GO层中掺氮过程[32];(b)N掺杂类石墨烯层状碳纳米片的制备[23];(c)管状N掺杂碳材料的制备[34];(d)大比表面积的N掺杂分级多孔碳制备示意图[35]
2.2 双原子掺杂碳材料
2.2.1 N,P共掺杂碳材料
磷是氮族的一种元素,具有与氮相似的化学性质,由此人们探索了P掺杂对碳材料氧还原性能的影响。可以作为P源的物质有三苯基膦[37](TPP)、植酸[38]、磷酸[39]和六氯环三磷腈[40]等。N、P的共掺杂可以增加碳材料中缺陷的密度,减少氧还原反应中过氧化物的产生,提高在酸性溶液下的催化性能,氧还原活性的提高可能是由于自旋密度或电子转移的不对称性增强所致。
N、P共掺杂和石墨烯边缘效应是催化活性的关键,Jintao Zhang[38]通过用三聚氰胺、植酸(PA)和氧化石墨烯(GO)的协同组装并热解的方法将N和P整合进了石墨烯基体中(如图4(a)所示)。所制备的电极电子转移数为3.7,展现出与Pt/C相当的性能。将制备的三维多孔N,P-共掺杂石墨碳网络作为空气阴极组装了锌空电池,其峰值功率密度为310 W/g,在90 h内无电位下降,具有优异的耐用性。Jintao Zhang[41]等人随后又将苯胺在植酸水溶液中聚合形成凝胶,在1 000 ℃下热解制备了N、P共掺杂介孔泡沫碳(NPMC,如图4(b)),NPMC-1000的比表面积(1 663 m2/g)与NPMC-900相比增加了一倍以上,这很可能是由于聚苯胺气凝胶碳化产生挥发性物质,形成了一个分级多孔结构。NPMC-1000对氧还原有良好的电催化性能,LSV图显示起始电势(Eonset)为0.94 V,E1/2为0.85 V,如图4(c)所示。以此制备的一次性电池的开路电位为1.48 V,比容量为735 mAh/g,双电极充电电池在2 mA/cm2下可稳定循环180次,组装的锌空电池示意图如图4(d)所示。文中提到热解温度十分重要,高的热解温度可以得到高的石墨化程度,较高的导电性和较大的比表面积,因此具有更好的电催化活性(NPMC-1000优于NPMC-900)。但是温度过高(比如1 100 ℃)可能导致掺杂剂分解从而使性能下降。
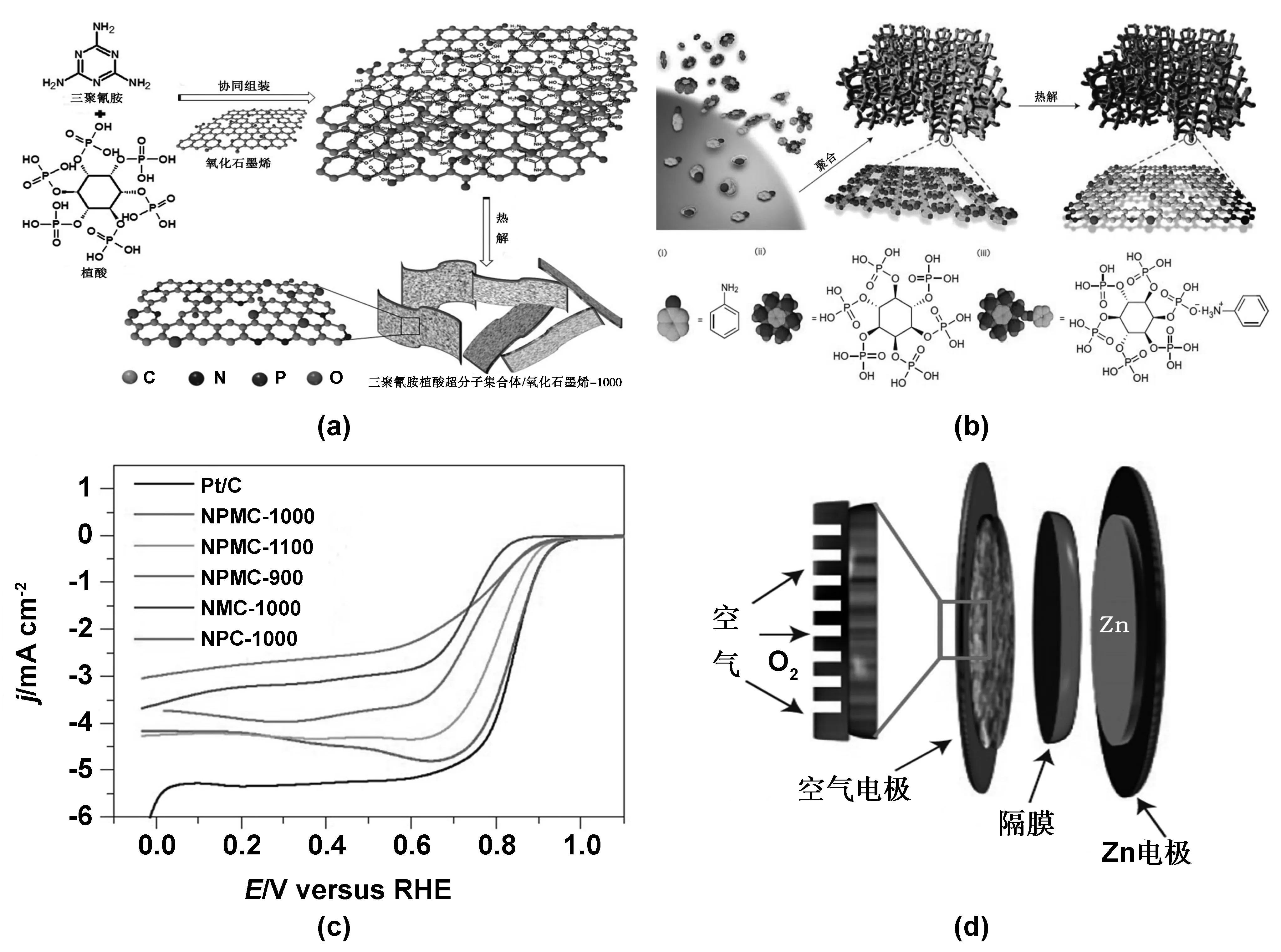
图4 (a)MPSA/GO-1000协同组装热解制备工艺[38];(b)NPMC泡沫制备工艺示意图[41];(c)不同温度下碳化的碳材料的LSV曲线[41];(d)组装的锌空电池示意图[41]
N、P共掺杂碳材料的优秀催化能力引起了众多科研工作者的关注。Rong Li[42]以热解氧化石墨烯、聚苯胺(PANi)和植酸组成的聚合物凝胶的方式制备了具有分层多孔三明治状结构N,P-GCNS纳米片,如图5(a)所示。多元素掺杂纳米碳由于协同作用导致反应物的活性中心增多,可以表现出比单元素掺杂纳米碳更好的催化活性。大的活性比表面积和有序的孔结构可以保证反应物分子的可接近性和快速的传质过程,集成的石墨烯纳米片可以促进氧化还原过程中的电荷转移。
Jianbing Zhu[43]等以三聚氰胺-二苯基膦酸配合物晶体(MDPCC)为原料,在高温下热解合成了N,P共掺杂催化剂(NPC-X-T,X为N/P比,T为碳化温度,如图5(b)),并且通过ZnCl2活化形成了多孔结构(命名为NPC-X-T-Zn,图5(c)),提高了催化剂的比表面积以提高催化剂的催化性能。Zhengping Zhang[45]通过吡咯和植酸之间的聚合反应、以聚苯乙烯球为模板并采用直接热解法制备了N,P-共掺杂介孔炭(N,P-MC)。N,P-MC具有优异的氧还原活性,显著的电化学稳定性和优异的甲醇耐受性,与工业Pt/C催化剂相当甚至更好,这与N,P-MC具有介孔结构和大量的N、P共掺杂形成的活性位点有关。Maryam Borghei[44]用椰子壳粉于磷酸中浸渍碳化、尿素溶液中浸渍碳化实现N和P的掺杂,制备示意图如图5(d),生物衍生的电活性炭与Pt/C催化剂标准材料相比,表现出了可媲美的电催化活性,对甲醇交叉效应的耐受性,以及在碱性介质中进行氧还原反应的长期耐久性。Lianwen Zhu[46]通过将爆米花放置在管式炉的中心部分,并将管式炉一端的针阀关闭,另一端的针阀保持打开状态下直接热解制备N,P共掺杂碳,在碱性电解液中的锌空气电池具有1.44 V的开路电压和36.6 mW/cm2的峰值功率密度和良好的稳定性,这是由于爆米花中蛋白质与磷酸盐中的含氮和含磷基团与石墨基质缩合形成N-C和P-C键,而热解副产物(如H2O和CO2)可以刻蚀无序的碳结构区域,形成层次孔隙和边缘碳。

图5 (a)N,P-GCNS催化剂的制备工艺和结构示意图[42];(b)NPC-X-T电催化剂的合成示意图[43];(c)NPC-4-1100-Zn的SEM图像[43];(d)由椰子壳合成N, P掺杂多孔碳的原理图[44]
2.2.2 N,S共掺杂碳材料
S比P多一个电子,硫因其取代碳原子的能力和与氮掺杂剂的强协同效应而备受关注,硫原子引起的结构缺陷有利于电荷位错和氧的吸附,另一方面,硫原子的两个孤对电子也有助于掺杂碳与分子氧的相互作用。通常用于硫源的物质有硫粉[47]、硫脲[48]、二苯硫醚[49]和其他含硫物质[50-51]。合理设计的形貌和多孔结构有利于获得更高的氧还原性能,有望提供更好的电解液渗透性和更快的电子传输和质量传输。
Xiaobao Li[47]以聚丙烯腈和硫为前驱体、改性SiO2纳米球为模板,采用热解法制备了氮硫掺杂的空心炭碗(CB-3S),制备方法如图6(a)所示,这是因为去除二氧化硅模板时形成的碳壳破裂而产生碳碗,碳碗的SEM图如图6(b)。CB-3S具有较高的氧还原反应性能,其E1/2与Pt/C催化剂在碱性介质中的E1/2相当; CB-3S还表现出卓越的耐甲醇性和稳定性,以及对四电子路径的高选择性。结合表征结果,认为CB-3S性能优异的主要原因有:(1)活性组分含量高,包括石墨/吡啶N组分和-C-S-C-型S,它们被认为可以改变表面电荷分布并产生缺陷和活性位点;(2)高比表面积(1 146 m2/g),可以提供更多暴露的活性位点;(3)碗状形貌,使碳壳的内表面更容易接触电解质和氧气。
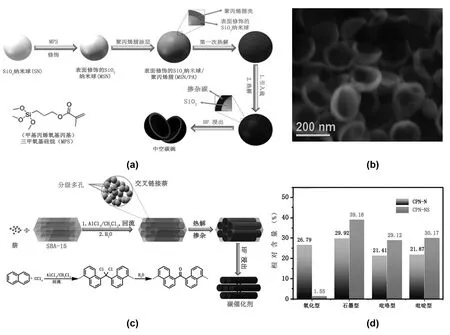
图6 (a)N,S掺杂中空碳碗制备方案示意图[47];(b)中空碳碗的SEM图像[47];(c)CPN-NS催化剂的制备示意图[52];(d)CPN-NS和CPN-N中不同种类的N含量[52]
Chenghang You[52]以SBA-15为模板、通过萘的福瑞德-克拉夫兹反应形成碳基体,再通过其与硫粉研磨并在NH3中热解以实现N、S的掺杂,如图6c,催化剂命名为CPN-NS。S的引入使催化剂的微孔体积增大,说明S的加入有利于微孔的形成,这应归因于S的掺杂和碳晶格的分解,而且S的加入有助于维持N的含量和调节N的组成,从图6d来看,CPN-NS与CPN-N相比形成了更多含量的吡啶N和石墨N,这有利于提高反应的活性。CPN-NS具有较高的氧还原性能,其半波电位(E1/2)为0.868 V,比商用Pt/C催化剂(E1/2=0.838 V)更高。
Mingbo Wu[53]通过三聚氰胺和三硫氰酸(简称MT)聚合在石油焦(PC)衍生石墨烯纳米片上原位形成的超分子聚合物,不仅可以作为掺杂杂原子的来源,而且可以防止石墨烯纳米片的聚集,从而形成多孔结构的N,S双掺杂碳材料N,S-PGN。N,S-PGN具有较高的比表面积和较大的孔体积,这是因为MT聚合物阻止了石墨烯结构的坍塌,使超薄石墨烯层形成了介孔网络,并且MT分解原位释放的气体可以产生更多的孔隙和随机的边缘位置。高比表面积、大体积和丰富的拓扑缺陷可以促进电解液的进入和反应物的扩散,也可以为氧还原提供额外的活性位点。
大多数掺杂杂原子通常来自碳源之外的掺杂剂,这给控制催化剂结构和组成的均匀性带来了困难。在这方面,含有杂原子的有机材料是制备掺杂碳材料的较佳来源。Jinhui Tong[54]以甲基橙(Fe(III))配合物为原料,经高温裂解,除去酸中的金属元素,制备了氮硫双自掺杂的介孔和微孔石墨碳催化剂。该催化剂在酸性和碱性介质中均表现出较高的电催化活性、长期稳定性和对甲醇的耐受性。炭化过程中Fe物种的存在有助于增加催化活性N-C位点,如吡啶N和吡咯N物种,从而更有效地促进氧还原活性。铁还可以增加制备的碳的石墨相,从而改善碳骨架的导电性。热解温度和酸处理对控制材料的比表面积和催化活性具有重要作用,酸腐蚀不稳定的铁物种,可大大提高催化剂的催化性能、耐甲醇性和长期稳定性。角蛋白[55]的主要半胱氨酸骨架成分,不仅含有丰富的S和N原子,而且呈现出由大量扁平重叠的鳞片构成的平行螺旋结构,在碳化过程中,由于扁平重叠单元之间的弱相互作用,这种层状结构可以保留下来,形成片状碳。Jiawei Zhu[56]以角蛋白为碳、氮、硫元素的前驱体,通过碱活化和氨活化巧妙地产生了固有缺陷,设计和制备了一种富缺陷的N/S双掺杂类干酪状多孔碳纳米材料CF-K-A。高含量的活性N和S掺杂,在碳基体中含有丰富的本征缺陷,可以有效地提高周围碳原子的电荷密度,减小HOMO-LUMO能隙,从而加速间隙间的电子转移和氧还原反应中间产物的形成,改变其对吸附质的化学反应性,电化学测试表明,该材料具有与工业Pt/C催化剂相当的氧还原活性(E1/2=0.835 V),并具有优异的耐用性和耐碱性。
2.2.3 N,B共掺杂碳材料
B(x=2.04)的电负性低于C(x=2.55),而N(x=3.04)的电负性高于C,B、N共掺杂产生附加的电子受体和电子给体态,可以通过掺杂体与周围碳原子之间的协同电子转移相互作用来调节能带隙和电荷密度,从而为氧还原提供了潜在的更活跃的位点。在N掺杂的碳物种中,氧还原反应增强是由于氮从碳的最高占据分子轨道(HOMO)吸引电子,在具有高自旋密度的相邻碳上诱导部分正电荷并随后降低了O2的吸附能,硼离子可以增强氧的化学吸附,这是由于π-共轭碳体系中空位2pz硼轨道上的电子积聚,从而促进电子转移到吸附的氧并削弱O-O键。N和B共掺碳催化剂的性能似乎取决于合成方法、掺杂程度以及催化剂中B和N官能团的分布,由于B和N对邻近的碳产生相反的电子效应,来自N的额外电子和B的空位轨道之间发生中和效应,从而不利于O2的化学吸附和随后的还原。通常以硼酸[57]或硼酸的衍生物[58-59]作为掺杂B的来源。
Hassina Tabassum[60]通过硼酸、尿素和聚乙二醇(PEG)在水溶液中混合,然后在900 ℃下于Ar气氛中热解制备了BCN,并且指出PEG的分子量对产物的形貌有着深刻的影响。高分子量的PEG(例如PEG-8000)衍生的产物是具有B-N键的2D BCN皱褶纳米片,而低分子量的PEG产物中可以观察到具有B-C和N-C键的理想的一维管状结构,如图7(a)所示,管状结构的碳框架中存在的B-C和N-C键可以通过提高电子自旋密度,产生比B-N键更合适的电子态,从而具有良好的氧还原性能,所制备的N、B掺杂管状碳材料对氢电极的E1/2为0.82 V,可与Pt/C(0.84 V)相媲美, BCN纳米管的SEM图像如图7(b)所示。
Ruopeng Zhao[61]提出了一种利用NaCl辅助热解法制备高B,N掺杂量超薄碳纳米片结构(BN/C)的方法,制备过程见图7(c)。NaCl晶体在801℃开始熔化,作为模板来支撑和分散前驱体;H3BO3和C2H10N6在分解过程中通过层间空隙产生CO、CO2和NH3等气体来造孔。所制备的BN/C催化剂活性高于氮或者硼单掺杂的碳材料,在碱性介质中E1/2=0.8 V,与工业Pt/C催化剂相当,具有较好的长期稳定性和较好的甲醇交叉耐受性,BN/C催化剂的LSV曲线和稳定性测试图如图7d、e。这种优异的性能是由于BN/C的结构和组成特点,包括大的比表面积(1 085 m2/g)、层次多孔结构、B,N共掺杂的协同效应和高含量的氧还原活性物。
Li Qin[62]以氮掺杂的多孔石墨烯(N-PG)为基体,使用硝酸氧化石墨烯并采用硼酸直接退火法合成了B,N-PG-O-15催化剂。B,N-PG-O-15的Eonset和E1/2分别为0.99 V和0.86 V,具有高的电子转移数(n=3.84~3.95)和低的H2O2产率(H2O2%<9),与工业Pt/C(n=3.87~3.92,H2O2%<7)相当接近。B,N-PG-O-15具有优异的耐久性,10000 s后电流衰减缓慢,约为5.4%,而商用Pt/C的损耗为19.6%。加入甲醇后,Pt/C催化剂的电流密度明显降低,而B,N-PG-O-15催化剂的电流密度几乎不变。Mingli Zhang[63]以近似的方法,将N/GO在55 ℃超声条件下分散在硼酸水溶液中,所得NB/GO复合材料在700 ℃的N2气氛中退火1 h,得到了NB/GO-55-700催化剂。NB/GO样品显示出较好的氧还原电催化活性,氧还原的催化活性的提高被认为是由于在团簇型量子的基础上降低了HOMO-LUMO。较小的HOMO-LUMO间隙意味着向高水平LUMO中添加电子或从低水平HOMO中移除电子更容易,有利于氧还原的进行。
Tao Sun[64]以乙基纤维素和高沸点4-(1-萘基)苯硼酸为原料,采用廉价的锌基模板剂,在NH3气氛中热解制备了B,N-碳催化剂,这种碳材料具有丰富的碳缺陷。典型的多级孔分布有利于反应物在电催化反应过程中的扩散,也有利于生成更多暴露于电解液中的活性位点。在碱性介质中,B,N-碳材料表现出较高的氧还原活性,Eonset达到0.98 V,E1/2为0.84 V,与Pt/C仅相差17 mV。5 000次循环后B,N-碳的Eonset降低了大约10 mV,表明具有良好的氧还原稳定性。
2.3 3种及以上杂原子共掺杂碳材料
杂原子掺杂的碳材料在氧还原催化剂领域优异的性能引起了众多科研工作者的关注,因此人们纷纷探索其他的杂原子掺杂对碳材料氧还原性能的影响,这其中除了前文中提到的N、P、S、B原子外,还有F[65]和Cl[66]等,多杂原子掺杂碳材料[67-68]开始被众多研究者所探索,学者们选用不同的元素组合掺杂于碳材料中以进一步探索碳掺杂材料的氧还原过程。
Lei Wang[65]以聚丙烯腈(PAN)和四氟硼酸铵为原料,通过静电纺丝法和随后的热处理合成了氮、氟、硼三元掺杂碳纤维(TD-CFs),并应用于锌空气电池;YaNan Zhu[68]以g-C3N4为形貌模板,六氯环磷酰胺、磺酰二苯酚和三乙胺分别为P、S、N源制备了N,P,S共掺杂超薄碳纳米片,用于碱性介质中氧还原反应的电化学催化剂;Mingguang Wu[69]通过NaPF6和聚丙烯腈(PAN)的静电纺丝和后续热处理的方法合成了N,F,P三元掺杂的大孔碳纤维(NFPC),由于其大的比表面积、多孔结构和N,F,P的协同效应,表现出良好的催化活性;Xiangjun Zheng[70]以尿素作为氮源和模板,溴化四苯基膦(C6H5)4PBr和氯化三苯砜(C6H5)3SCl作为P和S源,采用一锅法合成了N,P,S掺杂石墨烯(NPS-G),催化剂的高活性和良好的稳定性可归因于以下因素:(1)石墨烯中N、P和S掺杂引起的高活性中心增加;(2)促进了氧物种在NPS-G上的化学吸附;(3)降低了固有电阻和电荷转移电阻。
3 结 语
总之,碳材料合理的杂原子掺杂可以提高材料的氧还原催化性能,包括较大的半波电势、起始电势和极限电流密度,良好的循环稳定性以及较强的耐毒副能力等。
杂原子掺杂碳材料催化能力的提高与杂原子和碳基体间的性质差异有关,具体可以表现为:(1)杂原子和碳原子之间存在电负性、原子尺寸、键长键角等方面的差异,将其掺杂入碳基体后会引起周围原子电子密度和自旋等方面性质的改变,在碳基体中形成更多的缺陷,这可作为催化的活性位点从而具有对氧还原反应的催化能力;(2)通过控制材料的形貌提高其电化学比表面积,使更多的催化位点得以暴露,从而提高催化剂的催化性能;(3)通过合理的杂原子掺杂提高碳材料对氧分子的吸附能力和氧还原反应产物的脱附能力,改善材料的传输电子和传质的能力,从而提高材料的电化学催化性能。
当然,杂原子掺杂碳材料还存在许多问题,比如:(1)催化位点作用于氧的催化机理还不是很清晰;(2)催化剂的性能还需进一步提高以满足实际应用的需要。随着科学技术的不段发展与进步,通过众多科研工作者对其不懈的研究与探索,以及更先进的测试技术和更精确的计算方法的应用,杂原子掺杂碳材料的氧还原催化能力将越来越高且其催化机理也会越来越清晰,杂原子掺杂氧还原催化剂也会在电池的发展中发挥出不可磨灭的作用。
