复方生地合剂对MRL/lpr狼疮小鼠TLR-NF-κB信号通路的调节作用❋
2021-03-06陈薇薇肖小莉阿古达木
陈薇薇,肖小莉,阿古达木,苏 励,苏 晓△,徐 俊
(1. 上海中医药大学附属市中医医院风湿科,上海 200071; 2. 上海中医药大学附属龙华医院风湿科,上海 200032)
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种多系统广泛累及的自身免疫性疾病,其发病机理为异常的免疫应答引发T、B细胞过度活化、自身抗体生成、炎症因子释放,最终损伤脏器组织[1-4]。目前西医在急性活动期治疗上发挥了积极作用,然而激素与细胞毒药物的长期应用带来的毒副作用却是新难题。中医药辨治SLE依托经典理论,在临床中不断实践、不断优化,与西医药齐头并进,在控制疾病、撤减激素方面取得实效,彰显效佳毒小优势。上海市名中医沈丕安教授从事SLE诊疗30余年,以阴虚立论确定了“养阴滋肾、清热通络”治疗大法,研制自制制剂复方生地合剂治疗活动型SLE。经研究发现具有免疫抑制效应,且能减少糖皮质激素的用量,提高生存质量[5-7]。
SLE发病机制复杂,国内外多项研究发现如Toll样受体(toll like receptors,TLRs)通过识别病原相关分子模式,经过一系列信号传导分子激活核因子-κB(nuclear factor κB,NF-κB),使T和B淋巴细胞异常活化并产生多种细胞因子,参与SLE的发病过程[8]。本研究在临床取效的前提下,采用由美国Jackson实验室Murphy和Roths等于1978年成功建立最为经典的SLE动物模型——MRL/lpr狼疮小鼠模型,探讨复方生地合剂干预免疫应答上游TLR-MyD88-NF-κB 信号通路的调节作用。本实验已通过上海中医药大学附属市中医医院实验动物伦理委员会审查。
1 材料与方法
1.1 动物及分组
采用随机数字表法将30只12周龄雌性SPF MRL/lpr狼疮小鼠分为中药组、西药组和模型组各10只,体质量35.8~40.6 g。正常组采用12周龄雌性SPF级C57BL/6鼠10只。实验动物均由上海斯莱克实验动物有限责任公司供应,许可证号SCXK(沪)2017-0005,饲养于上海市中医医院无特异病原体(SPF)级动物房,5只一笼,温度保持在20~25 ℃,湿度保持在40%~70%。
1.2 主要试剂与仪器
M-TNF-alpha HS(杭州联科生物技术股份有限公司);M-IFN-α(上海江莱生物科技有限公司);PrimeScriptTM RT reagent Kit,SYBR® Premix Ex TaqTMII(TAKARA公司);TRIzol Reagent(Ambion公司);Anti-NF-κB p65 antibody,Anti-MyD88 antibody,Anti-TLR7 antibody,Anti-beta Actin antibody(英国abcam公司);酶标仪(Thermo Multiskan MK3);荧光定量PCR仪(罗氏,LightCycler®96);电泳仪(北京六一厂);转膜仪(北京六一厂)。
1.3 给药
模型组和空白组给予生理盐水灌胃,中药组给予复方生地合剂灌胃,西药组给予强的松悬液灌胃。根据《人与动物间体表面积折算的等效剂量比值表》折算成小鼠药物剂量[9]。复方生地合剂(本院中药制剂室制),由生地黄、生石膏、忍冬藤组成,给药剂量为18.495 ml/(kg·d),给药浓度为2.8 g/ml(从预实验低、中、高剂量浓度1.4 g/ml、2.8 g/ml、5.5 g/ml筛选而得的最佳有效浓度)。强的松为12.33 mg/(kg·d)。强的松片(上海上药信谊药厂有限公司,产品批号018180403)10 mg,溶于8.1 ml纯净水中配制出1.23 mg/ml浓度的泼尼松悬液,当天配置当天使用。灌胃量为0.1 ml/10 g,每天1次,连续给药8周。
1.4 取材与指标检测
1.4.1 取血 取小鼠眼眶血入EP管,室温静置2 h,3000rpm离心20 m收集上清,-80 ℃冰箱保存备用。
1.4.2 取脾 将断颈处死的小鼠酒精消毒后转移至超净工作台,打开腹腔在腹腔左侧胃后方暴露脾脏,用镊子轻轻取出脾脏,分成3份装入1.5mlEP管中,放入-80 ℃低温冰箱冻存。
1.4.3 酶联免疫方法检测外周血小鼠抗双链dsDNA 抗体、IFN-α和TNF-α水平的表达 取适量血清按照试剂盒说明书进行操作。
1.4.4 定量聚合酶链反应测定脾组织TLR7/9,髓样分化因子88(myeloid differentiation primary-response gene 88,MyD88),NF-κB的基因表达 取冻存的各组小鼠脾组织匀浆,提取总RNA。逆转录合成cDNA,以甘油醛-3-磷酸脱氢酶(GAPDH)为内参,进行基因实时荧光定量PCR检测。运用Primer Premier 5结合 Dnastar分析软件及网上BLAST分析,设计并由华大基因合成引物。引物序列如下:GAPDH-F:AGGTCGGTGTGAACGGATTTG,GAPDH-R:TGTAGACCATGTAGTTGAGGTCA,产物大小123 bp;TLR7-F:AGATGCTTTGCAATTGCGCT,TLR7-R:ACCAGACAAACCACACAGCA,产物大小158 bp;TLR9-F3:CCTGGTTCCAAGGTCTGGTC,TLR9-R3:AGGCGGGTTAGGTTCTGAAAG,产物大小103 bp;MyD88-F:TGTTCTTGAACCCTCGGACG,MyD88-R:TTCCAGCTCTCGGATCTCCA,产物大小92 bp;NF-κB1-F:TCCGCTATGTGTGTGAAGGC,NF-κB1-R:TTGCAAATTTTGACCTGTGGGT,产物大小94 bp。PCR 反应体系20 μL。PCR程序为95 ℃预变性30 s,PCR反应 95 ℃,5s,60 ℃,34 s,40~45循环,溶解阶段95 ℃,15 s,60 ℃,60 s,95 ℃,15 s。上机扩增检测,利用2-ΔΔCt法计算相对表达量。
1.4.5 蛋白质印迹分析法测定脾组织TLR7、MyD88、NF-κB的蛋白表达 按蛋白抽提试剂盒程序提取并行蛋白定量和变性后分离电泳,PVDF 转膜,一抗孵育,4 ℃孵育过夜。二抗37 ℃孵育1 h。加入显色底物,用Image lab显影,采用Image J软件对图像进行灰度值分析。用目标蛋白的灰度值和对应内参蛋白β-catin的灰度值比值作为样本中目标蛋白的相对表达量,并将此作为参数对目标蛋白进行半定量分析。
1.5 统计学方法
2 结果
2.1 一般情况
模型组毛发脱落、皮肤血管炎、浅表淋巴结肿大较其余3组明显。中药组8只、西药组9只、模型组7只和空白组10只小鼠存活至实验终点。中药组死亡2只,分别于治疗第2、3周死亡;西药组死亡1只,于治疗第5周死亡。模型组3只,分别于治疗第1、7、8周死亡,空白组无死亡。死亡小鼠死亡前1周均有体质量下降、活动力下降现象,毛发脱落、皮肤血管炎、浅表淋巴结肿大症状明显,解剖发现其颈部、腹腔淋巴结肿大,未发现有气管异物等。
在脾脏组织取材时因个别小鼠脾脏组织过小,空白组和中药组各8个,西药组9个,模型组7个样本完成检测。检测过程中个别脾脏组织的条带不显影,每组7个样本完成检测。
2.2 外周血dsDNA抗体水平
表1示,MRL/lpr小鼠外周血清dsDNA抗体、TNF-α和IFN-α平均异常升高(P<0.01,P<0.01,P<0.05),复方生地合剂可以减低MRL/lpr小鼠外周血清的dsDNA抗体、TNF-α和IFN-α水平均水平(P<0.05)。
表1 各组小鼠外周血dsDNA抗体及TNF-α和IFN-α水平比较
2.3 脾脏组织TLR-MyD88-NF-κB通路相关基因表达
表2示,MRL/lpr小鼠外周血清的TLR7mRNA、TLR9mRNA、MyD88mRNA和NF-κBmRNA水平均异常升高(P<0.01),复方生地合剂可以下调MRL/lpr小鼠脾脏组织的TLR7mRNA、TLR9mRNA、MyD88mRNA和NF-κBmRNA表达(P<0.05)。
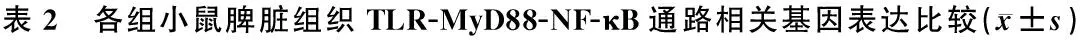
2.4 脾脏组织TLR-MyD88-NF-κB通路相关蛋白表达

图1 各组TLR7蛋白表达

图2 各组MyD88蛋白表达

图3 各组NF-κB p65蛋白表达
表3 各组小鼠脾脏组织TLR-MyD88-NF-κB通路相关蛋白表达比较
表3示,MRL/lpr小鼠脾脏组织的TLR7、MyD88和NF-κB蛋白表达异常上调(P<0.01),复方生地合剂可以下调MRL/lpr小鼠脾脏组织TLR7、MyD88和NF-κB的蛋白表达(P<0.01)。
3 讨论
MRL/lpr小鼠是由C57BL/6 J、AKR/J、LG/J和C3H/HeDi四类品系小鼠交配到第12代时产生[10-11],是自发性SLE的常用动物模型,其表现与人类SLE症状相似,可观察到明显的全身性淋巴结肿大,dsDNA抗体、Sm抗体等各种抗体也在2~3月龄时随日龄而上升[10]。dsDNA抗体作为SLE特异性抗体,在MRL/lpr狼疮鼠中阳性率达90%以上[12]。本研究发现,复方生地合剂与强的松都能降低MRL/lpr狼疮鼠外周血中dsDNA抗体水平,即能进一步抑制抗原抗体复合物形成和补体激活,减少炎症和组织损伤。
研究发现[13],感染会增加SLE的发病率和死亡率,而TLRs在机体感染病原体后发起的免疫应答中起决定性作用,并通过内源性配体参与诱导的急性和慢性炎症过程。TLR识别病原体成分后,经信号传导途径激活转录因子NF-κB,进而活化T和B淋巴细胞,调节与免疫有关的基因表达,分泌各种细胞因子参与SLE的发病[14-15]。TLRs的激活导致免疫细胞的活化产生许多细胞因子,直接参与SLE发病。业已证实,TLR多态性与SLE易感性增加有关。TLR7和TLR9通过对自身核酸以及相关免疫复合物的识别,在SLE发病机制中尤为重要[16-23]。由免疫复合物激活TLR7、TLR9,继而导致TNF-α和IFN-α的表达[24-25]。
本研究在TNF-α和IFN-α的结果表明,MRL/lpr小鼠外周血的TNF-α和IFN-α水平异常升高,支持TNF-α和IFN-α参与SLE的观点。中药组的TNF-α和IFN-α水平低于模型组,提示复方生地合剂可以降低MRL/lpr小鼠外周血TNF-α和IFN-α水平。鉴于TNF-α和IFN-α是TLR信号通路上的重要炎性因子,推测复方生地合剂可能通过清热解毒凉血作用减少TLR的激活,而降低免疫应答下游细胞因子TNF-α和IFN-α水平,展现了中医药“损其有余”的治疗理念。
本研究在TLR-MyD88-NF-κB通路相关基因和蛋白表达方面的结果提示,复方生地合剂可以下调MRL/lpr小鼠脾脏组织TLR7(TLR9)、MyD88和NF-κB的mRNA和蛋白表达,即具有抑制TLR-MyD88-NF-κB通路信号传导作用,天然免疫的启动和获得性免疫的发生发展随之减少或减轻。
综合免疫上游TLR-MyD88-NF-κB通路信号与免疫下游TNF-α和IFN-α的抑制结果,分析复方生地合剂作用机理可能从免疫应答上游环节抑制或减少抗原与免疫细胞表面的TLR7、TLR9结合,减少抗原递呈和通路依赖的MyD88,避免NF-κB和后续减少T、B细胞活化,免疫应答下游的炎症因子和自身抗体随之减少,进而减轻脏器组织损伤。
上海市名中医沈丕安教授将SLE辨为热瘀毒滞积,先天真阴不足,邪毒肾损,肾阴亏损,阴虚内热,据此制定治疗原则以养阴清热、凉血通络为主,研制了自制制剂复方生地合剂治疗SLE。复方生地合剂由生地黄、生石膏、忍冬藤组成。以生地黄为君药,滋补肾阴、清热凉血,现代药理报道,生地黄具有抑制免疫作用,其有效成分为甾醇类,且具有抗炎作用[26];生石膏清热泻火,加强生地的清热凉血作用,解气分血分之热,为臣药;忍冬藤清热解毒通络,药性善于走窜,作为使药助生地、生石膏驱卫气营血之热,凉脏腑经脉之血,解表里之毒,通四肢关节之络通达全身、疏经通络。现代药理报道,忍冬藤含有木樨草素有显著抗炎活性和抗菌作用[26]。生地黄、生石膏和忍冬藤相须相使,共奏养阴清热、凉血通络之效。全方紧凑而力专,滋阴而不留邪,清热而不伤正,凉血而不留瘀。复方生地合剂可能通过养阴清热凉血解毒作用,减少或减轻感染,TLR对病原体成分的识别相应减少,截断一系列免疫级联反应,保护机体免受免疫炎性损伤与破坏,发挥抑制免疫和抗炎作用。
