床旁即时肺部超声结合压力-容积曲线设定PEEP对ARDS 肺复张的临床评价
2021-03-05罗前程曲凯丽郭东风
罗前程, 刘 瑞, 曲凯丽, 许 磊, 冯 刚, 郭东风
(1.上海市浦东新区公利医院急诊医学科,上海 200135; 2.上海市浦东新区公利医院重症医学科,上海 200135;3.上海市浦东新区公利医院内分泌科,上海 200135; 4.宁夏医科大学上海市浦东新区公利医院研究生培养基地,上海 200135)
“肺开放策略”是机械通气治疗急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)中的主要方案[1],常规采用以低潮气量结合呼气末正压(positive end-expiratory pressure,PEEP)[2]促使塌陷肺泡复张、增加肺容积、改善肺顺应性和调节通气/血流比例,达到有效的肺复张,进而改善患者氧合功能。研究[3]表明,ARDS 的肺复张是一个持续的过程,受气道内压力变化影响较大以及存在呼吸机相关性肺损伤(ventilator induced lung injury,VILI)等原因[4],对于选择合适的PEEP 仍是ARDS 治疗中的关键点和难点。个体化的PEEP 设置有助于减少不适当的高PEEP引起的肺损伤[5]。因此,在ARDS 病情动态变化中,能够及时、准确、安全、动态地进行肺部检查评估是临床治疗迫切需要的。
传统的肺复张评估指导方法存在搬动、转运患者及辐射等不足,如放射性影像检查,临床难以广泛实施;压力-容积(pressure-volume,P-V)曲线法与患者既往肺容积情况影响较大,缺乏标准的测定方法以及需要患者处于深度镇静、肌松状态,使用受到限制[6]。近年来,肺部超声(lung ultrasound,LUS)以其无创、便捷、安全、动态评估等优势,在ARDS 的诊疗中受到关注[7-8]。Bouhemad 等[9]在研究LUS 与肺CT 有相关性的基础上建立的超声再气化评分(ultrasound re-aeration score,US-RAS)能够有效监测PEEP 对塌陷肺泡的开放作用。但LUS 检查有赖于医师对肺部超声形态的判断和评估,带有一定的主观性,以及对肺泡的过度膨胀不敏感和在肥胖人群使用受限等因素,使得超声不能作为唯一的工具去代替传统的评估手段。
因此,本研究把能够在患者床边即时开展的P-V 曲线描记和LUS 检查相结合,研究在P-V曲线评估ARDS 肺内压力状态,利用LUS 可视化、可重复、可定量[9-10]等特点,个体化指导ARDS机械通气患者的PEEP 设定及评价肺复张效果,探索更合理的床边即时肺部超声(point-of-care lung ultrasound,POC-LUS)指导下的肺复张PEEP滴定方案。
1 资料与方法
1.1 研究对象
依据ARDS 柏林诊断标准[11],选取2017 年10月至2019 年3 月上海市浦东新区公利医院急诊监护病房(EICU)和重症医学科(ICU)收治的行有创机械通气、年龄≥18 岁确诊的ARDS 患者,并结合该标准中氧合指数[动脉血氧分压(PaO2)/动脉血二氧化碳分压(PaCO2)]情况,将病情分为轻度(200 mmHg <PaO2/ FiO2≤300 mmHg,且PEEP≥5 cmH2O)、中度(100 mmHg<PaO2/FiO2≤200 mmHg,且PEEP≥5 cmH2O)或重度(PaO2/FiO2≤100 mmHg,且PEEP≥5 cmH2O)。同时排除存在以下情况者:颅内高压、合并气胸或纵隔气肿、严重低氧血症(PaO2/FiO2<50 mmHg)、血流动力学不稳定、胸部外伤、胸部畸形或手术史、妊娠等。本研究共纳入30 例患者,根据所采用的肺复张评价方法,随机等分为POC-LUS 组(n=15)和最大氧合法(maximum oxygenation,Max-Oxy)组(n=15)。本研究经上海市浦东新区公利医院伦理委员会批准并在研究中获得受试者家属知情同意。
入组对象均接受常规镇静[咪达唑仑0.05~0.1 mg·(kg·h)-1]、镇痛[芬太尼0.7~1.5 μg·(kg·h)-1],根据病情需要将镇静深度维持在Ramsay评分4~5 分。在气管插管下,使用Marquet Servo-i呼吸机(德国西门子公司),遵循肺保护性通气策略(潮气量6 mL·kg-1,气道峰压<40 cmH2O,1 cm H2O=0.098 kPa)进行机械通气。使用Philips MP40多功能监护仪(荷兰皇家飞利浦公司)常规监测心率(HR)、指脉氧饱和度、无创血压等。使用BD PresetTM采血针(美国碧迪公司)采集股动脉或桡动脉血样进行动脉血气(arterial blood gas,ABG)分析(ABL90,丹麦雷度米特公司)。
1.2 P-V 曲线描记
使用Marquet Servo-i 呼吸机自动测量描记P-V 曲线,先加强患者镇静深度(Ramsay 达到6分),并临时加用神经肌肉阻滞剂[顺苯磺酸阿曲库铵0.03~0.3 mg·(kg·h)-1],镇静、肌松满意后开始测量。采用恒速低流量法,呼吸机设置为容量控制通气,潮气量6 mL·kg-1,氧浓度100%,呼吸频率10 次/min,调节吸呼比,使呼吸机的动态P-V 曲线的呼气支和吸气支连接闭合,得到P-V曲线。
1.3 LUS 和US-RAS
使用Philips Sonos 4500 超声诊断仪及1.0~5.0 MHz 弧形探头(美国飞利浦公司)进行超声检查。LUS 检査方法[12]:患者先取仰卧位,定位于双侧锁骨中线第2、5 肋间及腋中线相同水平两个肋间的肺部超声影像;再由助手协助抬高患者一侧身体,抬离床面约60°,便于超声探头检查该侧肩胛线相应第2、5 肋间隙肺野,同理检查另一侧后胸部肺野。如上,共对胸部12 个区域在呼气末进行超声检查,保持超声探头中心垂直于检查部位胸壁,沿纵向和横向扫查,局部区域内避开骨性遮挡,观察每个肺区有无积液、实变及间质的改变。超声影像分为4 类[9,13],(1)正常通气(N):表现为平滑的A 线或者少于2 条孤立的B 线;(2)肺部通气轻度减少(B1):可见多条边界清楚、规律分布且间距7 mm 以上或不规律分布的B 线;(3)肺部通气严重减少(B2):弥漫分布且间距3 mm 以内的连续融合B 线;(4)肺实变征象:肝样回声伴动态支气管充气征。
US-RAS 分为4 个等级,在不同时点动态观察上述12 个区域的肺超声影像变化,根据变化情况进行评分(表1)[9]。本研究中的LUS 检查,固定由一名经过急危重病超声培训并能熟练床边超声操作的医师进行。

表1 US-RAS 计算方法
1.4 最佳PEEP 滴定
POC-LUS 组在肺复张开始前,PEEP 为0 时(ZEEP),采集当时ABG、肺超声及各监测指标作为基线情况;该组根据P-V 曲线呼气支最大曲率点(point of maximum curvature,PMC)确定初始PEEP[14-15]。Max-Oxy 组初始PEEP 设置依据P-V曲线的吸气支低位拐点(lower inflection point,LIP)基础上增加2 cmH2O[16]。两组呼吸机其余设置相同,均在压力控制模式下,施行PEEP 递增法进行肺复张,气道峰压上限为40 cmH2O。根据初始PEEP,调整压力控制水平,使潮气量维持在6 mL·kg-1,将FiO2均设置为80%,以保持两组在相同氧供条件下进行比较。后续各次ABG 及LUS 检查均在调整PEEP 参数10 min 后进行。以PaO2/FiO2为复张后氧合改善指标进行两组比较。
POC-LUS 组:从初始PEEP 设定后开始,在第15 min、1 h、2 h、6 h、12 h、24 h、36 h 及48 h 分别行POC-LUS、ABG 检查,记录监护仪、呼吸机相关参数。若各时间点记录的US-RAS 较前环比增加20%,则考虑有可能肺过度膨胀,存在VILI风险,将该时间点的PEEP 降低2 cmH2O;若该时间点记录的US-RAS 较前环比增加未超过10%,则考虑有可能肺复张不全,将该时间点的PEEP增加2 cmH2O;若介于10%~20%,则维持当前PEEP 值,此时的PEEP 即为最佳维持PEEP。
Max-Oxy 组:检测时间点及所记录指标同上组,从本组初始PEEP 开始,以PaO2+PaCO2值作为肺复张评估依据[17],若PaO2+PaCO2<380 mmHg,提示有肺泡重新塌陷,肺复张不全,将PEEP 增加2 cmH2O;若≥400 mmHg,则达到完全复张,保持当前PEEP,待下一时间点复测,调节PEEP 至维持肺泡复张的最低水平,此时的PEEP 即为最佳维持PEEP。
1.5 观察指标
1.5.1 首要观察指标 (1)US-RAS;(2)循环指标:HR、收缩压(SBP)及平均动脉压(MAP);(3)呼吸力学指标:呼吸机自动监测并提供的PEEP、气道峰压(Ppeak)、平均气道压(Pmean)、动态顺应性(Cdyn);(4)肺换气指标:由ABG 提供的血pH、PaO2、PaCO2计算PaO2+PaCO2及PaO2/FiO2;(5)入组时病情严重程度评分:急性生理学与慢性健康状况评分系统Ⅱ(APACHE Ⅱ),Murray 急性肺损伤评分。
1.5.2 次要观察指标 (1)气胸;(2)纵隔气肿;(3)SBP 较前下降30%及以上;(4)其他不良事件。
1.6 统计学方法
数据采用SPSS 23.0 软件进行统计学分析。计量资料以均数±标准差(±s)表示,组间比较采用t 检验;计数资料组间比较采用卡方检验;使用Pearson 积差相关系数分析US-RAS 与氧合指数的相关性。P≤0.05 为差异有统计学意义。
2 结果
2.1 一般资料
两组研究对象在基本情况及病情严重程度方面的差异均无统计学意义(P 均>0.05),具有可比性。见表2。导致ARDS 的主要病因分为肺内及肺外两类,肺内因素包括社区获得性肺炎、支气管肺炎、肺挫裂伤;肺外因素包括脓毒症、休克、非胸部多发伤(车祸、高处坠落)、胰腺炎、淹溺。
2.2 初始PEEP 设置及最佳PEEP 滴定
POC-LUS 组和Max-Oxy 组中各患者P-V曲线获得的初始PEEP 值(11.2±0.9 cmH2O vs.8.4±1.8 cmH2O)比较差异具有统计学意义(P<0.0001)。依照两组的US-RAS 和PaO2+PaCO2变化情况对应调整PEEP 后发现,POC-LUS 组患者在第6 h 的PaO2/FiO2较前一时段升高(t=8.731,P<0.0001),此时PEEP 为(14.7±1.9)cmH2O,此后氧合逐渐好转。而Max-Oxy 组的PaO2/FiO2在6 h环比差异无统计学意义(t=1.652,P= 0.1096),在第12 h 环比增加差异有统计学意义(t=2.989,P=0.0058),此时对应PEEP 值为(13.5±1.3)cmH2O,此后氧合逐渐改善。以此确定两组的最佳PEEP值,两者比较差异无统计学意义(t=2.019,P=0.0532)。见表3。
2.3 两组肺复张效果的比较
POC-LUS 组患者在入组第6 h 滴定得到最佳PEEP,较Max-Oxy 组早发现6 h,两组在最佳PEEP 状态下的肺复张效果比较显示,POC-LUS组与Max-Oxy 组的PaO2/FiO2(P<0.001)、Cdyn(P均<0.05)差异均有统计学意义,pH、PaCO2、HR、MAP、Ppeak、Pmean和Murray 评分差异均无统计学意义(P 均>0.05)。见表3、图1。
2.4 US-RAS 与氧合指数变化趋势及相关性分析
在施行肺复张及PEEP 滴定过程中发现,POC-LUS 组的US-RAS 在各时间点总体呈下降趋势,除第48 h 外,环比各时点数值变化均有统计学意义(P 均<0.05),而该组PaO2/FiO2逐渐升高,除在第2 h 升高较前时间段差异无统计学意义外,其余时段氧合指数改变差异均有统计学意义(P 均<0.05)。POC-LUS 组的US-RAS 分值与PaO2/FiO2呈负相关(r=-0.8725,R2=0.7613,P=0.0047)。见图2。

表2 两组患者基线情况比较
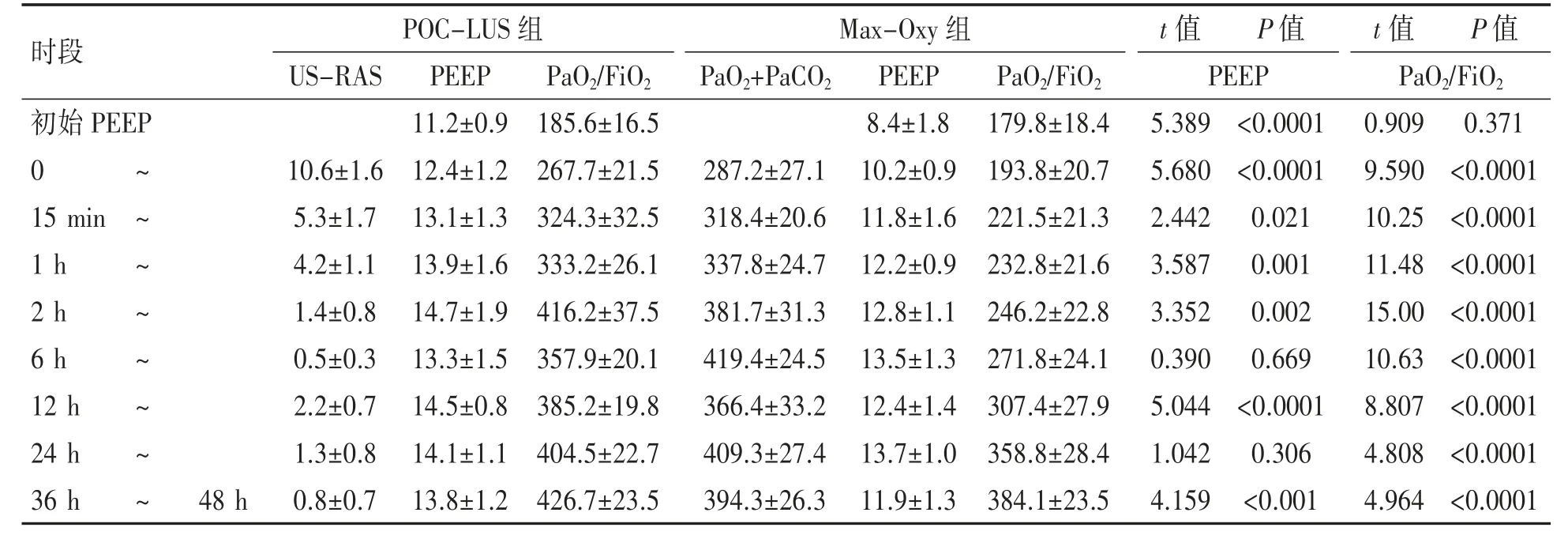
表3 两组PEEP 滴定过程比较
2.5 不良事件
在滴定PEEP 过程中,未发生明显心血管不良事件、气胸等并发症,无死亡发生。
3 讨论
PEEP 是ARDS 的机械通气治疗的一项维持肺复张状态的重要参数。ARDS 患者的病因、病变范围、严重程度存在很大的差异,不同的肺对于PEEP 的反应也各不相同[4]。对于可复张性差的肺,使用较高的PEEP 可导致正常通气区域过度膨胀,造成更为严重的VILI;而对肺可复张性较好的患者使用较低水平的PEEP 又会使复张肺泡再次塌陷,同样也可能会加重肺的损伤[18]。因此,在ARDS 机械通气时,推荐使用能防止肺泡塌陷的最低PEEP 水平[19]。
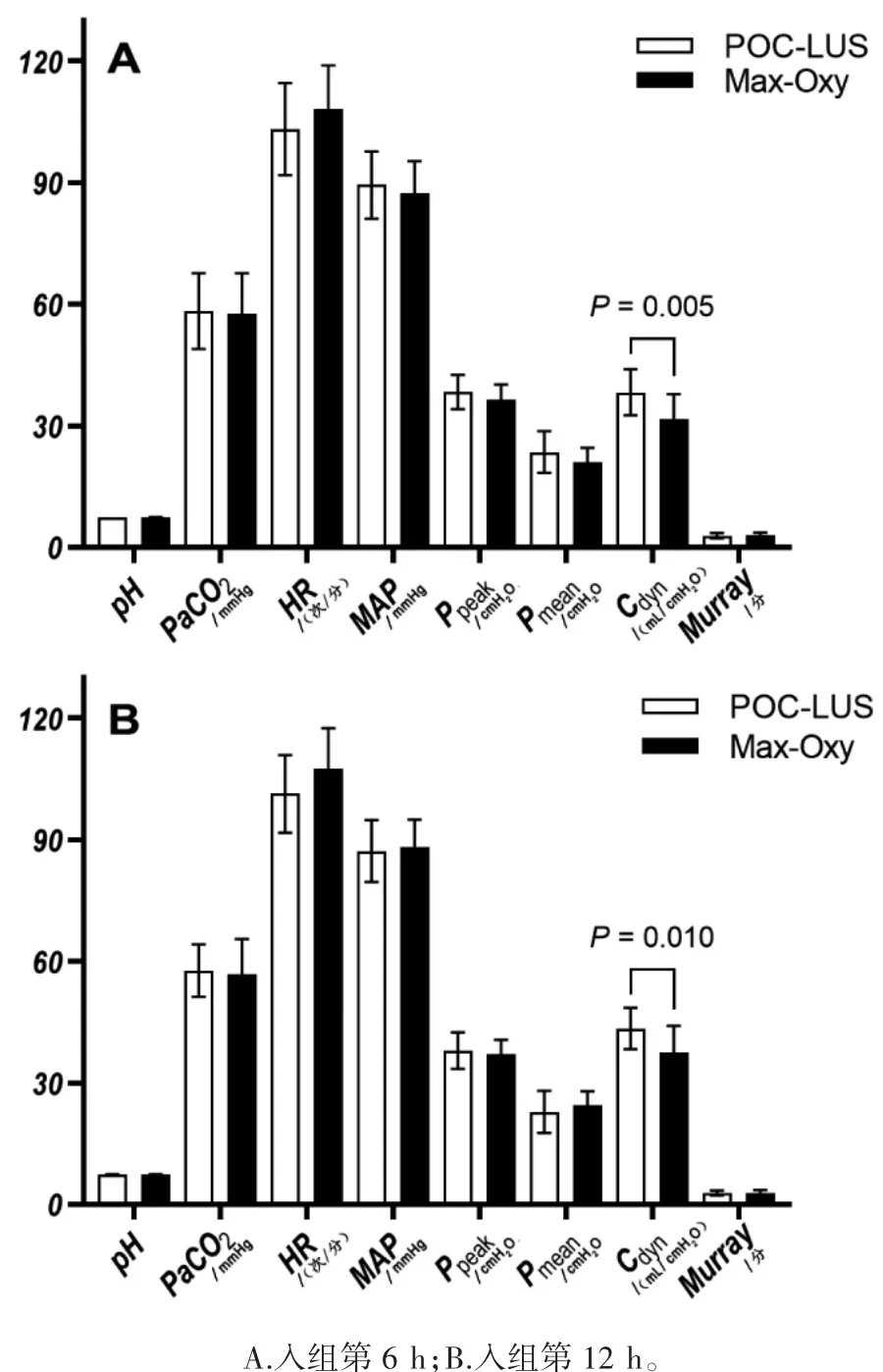
图1 两组在最佳PEEP 状态下的肺复张效果比较
P-V 曲线在临床中常用来指导PEEP 的设置[20],以往以P-V 曲线的LIP+2 cmH2O 作为PEEP依据[16,20]。但Albaiceta 等[3]利用CT 研究肺P-V曲线中肺的复张情况时发现,当呼吸道压力大于LIP 时肺复张开始发生,并持续到压力大于高位拐点(upper inflection point,UIP)仍存在肺膨胀;而从UIP 一直降至呼气支PMC 时,没有观察到复张后再塌陷的发生,当压力低于PMC 时复张后再塌陷开始出现,并沿着呼气支曲线持续进行,提示PMC 与复张后再塌陷的发生相关性更强。因此本研究以PMC 作为POC-LUS 组初始PEEP的依据,以LIP 作为对照组设置,发现PMC 值较LIP 值设置的PEEP 相对更高,能够在机械通气一开始获得较好的氧合改善。当两组各自达到最佳PEEP 时,各组氧合状况均能改善,但两组的最佳PEEP 差异无统计学意义,提示两组的评价标准均能够对肺复张起到指导作用,但POC-LUS 组在PMC 基础上能够较早地达到良好的肺复张状态。目前临床使用的呼吸机大多可以进行动态P-V 曲线的自动描记,在将患者镇静、肌松后,尽量降低胸廓阻力及自主呼吸干扰后,能够得到准静态P-V 曲线[21],这在临床上具有操作性,便于开展,同样具有临床指导意义。

图2 POC-LUS 组在肺复张过程中US-RAS 与氧合指数变化趋势及相关性分析
LUS 检查是基于肺脏含气量的多少所造成的超声“伪差”来作出疾病诊断[22],同时它还能早期发现与肺部含水量相关的肺间质肺泡综合征[23-24]。因此,LUS 可用于评估ARDS 肺复张过程中肺通气水平的动态变化,对肺复张过程进行实时评价和指导。Bouhemad 等[9]使用肺部超声对30例ARDS 患者肺可复张性进行了评估,结果显示再通气评分与氧合的改善密切相关。本研究中发现,动态评估US-RAS 的变化,实时指导PEEP的设置,US-RAS 分值的降低与氧合的改善具有负相关性,并能够可视化观察肺复张对肺的局部区域造成的影响,而且POC-LUS 组的氧合改善状况较对照组差异也具有统计学意义。因此,POCLUS 可以作为ARDS 肺复张有意义的评价体系。
同时,不足之处也要充分总结。首先,本研究仅关注了ARDS 机械通气的前48 h,虽然这一阶段在肺复张治疗中是关键时间,但肺部病理、生理改变会持续超过这一时间,对后续肺复张的效果仍需要进一步观察评估。其次,为了利于组间比较,将两组的呼吸机吸入氧浓度值均固定为80%,这在一定程度上可能会影响PEEP 的调节,因为持续的高氧浓度可能会掩盖一部分患者最佳PEEP 的发现。最后,LUS 评估了双肺12 个区域,但仍并不能涵盖全肺的状况,临床开展中可结合实际情况着重观察局部肺野。
综上所述,对有创机械通气的ARDS 患者在床边进行个体化的P-V 曲线描记,并依照患者的实际情况设定初始PEEP,这能够最大程度上避免经验性取值而造成的误差。再联合床边肺部超声检测,实时、动态、定量地评估肺膨胀情况,调节PEEP 的设置,相比较传统依赖动脉血气分析的方法,可以较快地滴定得到最佳PEEP 值。本研究可作为传统PEEP 调节方法的有益补充,为临床提供参考,值得进一步深入研究。
