康莱特注射液联合阿帕替尼治疗晚期胃癌的临床研究
2021-03-05刘登湘王娜何莉莉郭军孙雅薇朱晓燕郭治靳毅
刘登湘,王娜,何莉莉,郭军,孙雅薇,朱晓燕,郭治,靳毅
(邢台市人民医院肿瘤内科,河北 邢台 054031)
中国胃癌的发病率居世界前五,患者占全球总例数的42%,已成为危害国民健康的主要疾病[1-3]。早期胃癌症状不明显,前来就诊的患者以晚期胃癌为主。阿帕替尼作为治疗晚期胃癌的靶向药物,其疗效与剂量及不良反应呈相关性,标准剂量(850 mg/d)下患者通常会面临不同程度的并发症的困扰;而500 mg/d的剂量虽然并发症风险明显下降,但疗效会降低[4-6]。因此,晚期胃癌患者急需寻找新的治疗方案来获得更高的治疗效益。康莱特注射液是中国首个自主研发的具有完全自主知识产权的植物抗肿瘤注射剂,是临床应用较为理想的双相广谱抗肿瘤药物[7]。本研究旨在康莱特注射液联合阿帕替尼治疗晚期胃癌的疗效及安全性。
1 资料与方法
1.1 一般资料
将2017年6月至2018年9月邢台市人民医院收治的90例晚期胃癌患者,按照愿意接受治疗的方式分为两组。其中,试验组45例,男性27例,女性18例;TNM分期:Ⅲ期17例、Ⅳ期28例;年龄40~76岁(53.94±6.23)岁。对照组45例,男性26例,女性19例;TNM分期:Ⅲ期20例、Ⅳ期25例;年龄39~75岁(52.32±7.68)岁。两组一般资料比较,差异无统计学意义(P>0.05)。
1.2 纳入标准和排除标准
纳入标准:(1)经组织病理学检测确诊为Ⅲ~Ⅳ期胃癌;(2)经医院伦理委员会审批,患者对本研究知情同意;(3)生存期>3个月。排除标准:(1)合并其他恶性肿瘤;(2)合并出血倾向;(3)合并传染性疾病;(4)合并肝、肾等主要脏器功能障碍;(5)中途退出研究者。
1.3 治疗方法
对照组:口服阿帕替尼(江苏恒瑞医药股份有限公司),500 mg/次,1次/d,21 d为1个疗程,持续口服两个疗程。试验组:在对照组基础上静脉输注200 mL康莱特注射液(浙江康莱特药业有限公司),1次/d,21 d为1个疗程,共计两个疗程。
1.4 评价标准
(1)两组患者临床疗效。化疗前、化疗结束2周,按照RECIST评价[8]疗效,完全缓解(CR):可见病变消失,扫描无异常,持续至少4周;部分缓解(PR):肿瘤最大直径(LDs)和最大垂直直径(LPDs)之积缩小≥50%;疾病稳定(SD):肿瘤LDs与LPDs之积缩小<50%或增大<25%;疾病进展(PD):一个或多个病灶的LDs与LPDs增加≥25%。客观缓解率(ORR)=(CR+PR)/总人数×100%。(2)两组炎症因子水平对比。采集化疗前后患者静脉血5 mL分离血清,利用ELISA检测血清IL-2、TNF-α、INF-γ浓度。(3)两组毒副反应发生情况。根据毒性通用标准,将高血压、手足综合征、蛋白尿、肝肾功能异常和消化道出血分为0~Ⅳ级.(4)两组远期疗效及预后情况比较。比较两组随访1年期间无进展生存期(PFS)、1年生存期(OS)时间,统计其1年生存率。(5)两组生存质量改善状况比较。采用Karnofsky评分评价,满分100分,得分高表示健康状况好,其中改善:化疗后评分增加>10分;稳定:评分增加或减少10分内;下降:化疗后评分减少>10分,生活质量改善率=(改善+稳定)/总人数×100%。
1.5 统计学分析
2 结果
2.1 两组患者近期疗效比较
化疗结束后,两组患者ORR比较,差异无统计学意义(P>0.05)。见表1。
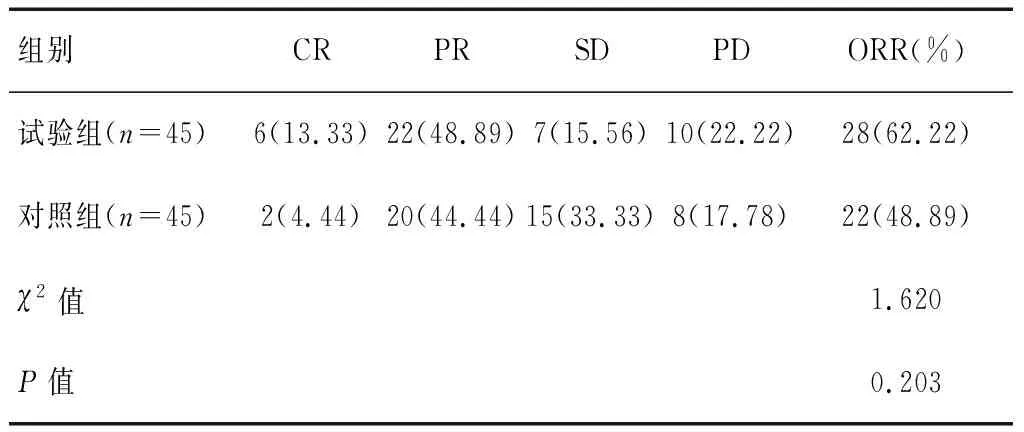
表1 两组患者近期疗效比较[n(%)]
2.2 两组患者血清IL-2、TNF-α、INF-γ水平对比
化疗后,两组患者血清炎症因子水平均高于治疗前;试验组血清IL-2、TNF-α、INF-γ水平低于对照组(P<0.05)。见表2。
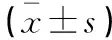
表2 两组IL-2、TNF-α、INF-γ水平对比
2.3 两组患者毒副反应发生情况
化疗后,试验组患者0~Ⅳ级贫血、肝功能异常的毒副反应发生率低于对照组(P<0.05)。见表3。
2.4 两组患者远期疗效及预后情况比较
两组患者随访1年,试验组、对照组PFS分别为(8.18±1.32)个月、(7.95±1.41)个月,试验组、对照组OS分别为(11.32±0.52)个月、(10.84±0.64)个月。两组PFS、OS比较差异无统计学意义(t=0.799、1.440,P=0.427、0.153);试验组1年生存率高于对照组,差异无统计学意义(46.67%vs.37.78%,χ2=0.729,P=0.393)。见图1。

表3 两组毒副反应发生情况[n(%)]
2.5 两组患者生存质量改善状况比较
化疗结束后,试验组患者生活质量改善率为高于对照组(86.67%vs.66.67%,P<0.05)。
3 讨论
目前,临床针对晚期胃癌患者的治疗手段比较单一,化疗方案基本贯穿整个治疗过程;其中的一、二线化疗药物疗效确切,但由于个体差异、耐药、化疗毒副作用等因素的存在,部分晚期胃癌患者经化疗治疗后收效甚微,甚至出现生活质量下降的情况。因此,探索更为有效的抗肿瘤药物及联合治疗方案势在必行。
阿帕替尼在中国获批适应症为晚期胃癌三线治疗,其通过抑制新生血管来延缓肿瘤的进展[9-10]。蔡红许等[11]研究指出,阿帕替尼联合紫杉醇、替吉奥对晚期胃癌患者的疗效确切,但常规剂量的阿帕替尼会给患者机体带来较多毒副反应。康莱特注射液是一种从药用植物薏苡仁中提取、研制而成,有益气养阴、消症散结之功效,安全性极高[12]。有研究[13-14]显示,康莱特注射液通过抑制肿瘤细胞增殖、调节肿瘤相关酶的表达、抑制新生血管生成等方式发挥抗肿瘤效用,在胃癌、肺癌等恶性肿瘤患者的治疗中均取得了较好的治疗效果。
本研究中,试验组ORR略高于对照组,差异无统计学意义,表明联合治疗进展期胃癌的近期疗效与单独使用阿帕替尼相似,推测是因为本研究中纳入的Ⅳ期病例较多有一定关联。化疗会在一定程度损害免疫系统功能。本研究试验组血清炎症因子水平低于对照组,说明康莱特注射液有保护胃癌患者免疫功能的作用,推测与康莱特注射液中的纯薏苡的镇痛、抗炎、增强机体免疫力有关。本研究中,试验组贫血、肝功能异常的0~Ⅳ级发生率低于对照组,试验组生活质量改善率高于对照组,与沈刚等[12]研究结果相似。提示大部分患者对于化疗剂量是可以耐受的,联合康莱特注射液可以在一定程度上减小化疗毒副反应、提高患者的生活质量。本研究两组PFS、OS、1年生存率比较,差异无统计学意义,可能与本研究纳入晚期患者较多,整体生存期较短有关。
综上所述,与阿帕替尼单药化疗相比,联合康莱特注射液可降低晚期胃癌患者的化疗毒副反应及炎症因子水平,提高生活质量。但由于本研究随访时间较短,有待扩大样本容量及随访时间,进一步讨论康莱特注射液对晚期胃癌患者远期预后的疗效。
