干扰素α-2b联合抗HPV蛋白敷料治疗宫颈HPV感染的临床效果
2021-03-03冯文丽
冯文丽
宫颈癌在妇科恶性肿瘤中十分常见,且目前其发病人群日趋年轻化,而(高危型)人乳头瘤病毒(HPV)感染是导致宫颈癌前病变并最终诱发宫颈癌的重要因素[1]。相关统计资料显示,全世界范围内宫颈HPV感染率在15%左右,10%HPV感染患者的感染情况会长期持续存在,这也是最主要的引发宫颈癌的原因之一[2]。现阶段,临床治疗HPV感染最普遍的方案是局部用药,而治疗HPV的药物众多且用法不一,所产生的治疗效果也存在着较大差异[3]。因此,十分有必要探索更为规范、科学、高效的用药方案,本研究选取50例宫颈HPV感染患者,观察予以干扰素α-2b联合抗HPV蛋白敷料治疗的效果,明确该治疗方案的有效性,报道如下。
1 资料与方法
1.1 一般资料
纳入2018年1月-2020年2月本院收治的50例宫颈HPV感染患者。纳入标准:(1)经阴道镜检、液基细胞学检查(TCT)均确诊为HPV感染;(2)年龄>20岁且有性生活史;(3)HPVDNA检查结果呈阳性。排除标准:(1)伴急性生殖道炎症;(2)伴精神障碍;(3)伴心肝肾等重要器官疾病;(4)有宫颈手术史;(5)存在血液系统疾病;(6)妊娠期或哺乳期;(7)入组前有物理药物治疗史。以随机数字表法分为对照组和研究组,各25例。对照组24~49岁,平均(35.72±2.28)岁;孕次0~5次,平均(2.31±0.52)次;产次0~3次,平均(0.84±0.36)次。研究组26~47岁,平均(35.35±2.53)岁;孕次0~5次,平均(2.42±0.69)次;产次0~3次,平均(0.91±0.27)次。两组基线资料对比差异无统计学意义(P>0.05),有可比性。患者知情同意本研究,本研究获医院伦理委员会批准。
1.2 方法
对照组单纯予以干扰素α-2b(厂商:上海华新生物高技术有限公司;批准文号:国药准字S20050075;规格:80万IU/粒)治疗,睡前在阴道后穹隆置入本品1粒,连续10 d。研究组联合应用干扰素α-2b及抗HPV生物蛋白敷料(厂商:山西锦波生物医药股份有限公司;批准文号:晋械注准20152640040)治疗,用法为月经干净后3 d,睡前阴道后穹隆置入抗HPV生物蛋白敷料1支,连续10 d为1个疗程,间隔3 d同部位置入干扰素α-2b 1粒,连续10 d。
1.3 观察指标
随访3个月后比较两组下列指标:(1)HPV转阴时间、HPV-DNA负荷量,采集阴道残端或宫颈管标本检测HPVDNA,阳性标准为负荷量≥1.0 pg/ml[4]。(2)治疗前后C反应蛋白(CRP)指标,采用免疫透射比浊法进行检测。(3)宫颈液基细胞学指标,采用TBS分类标准[5]。包括未见上皮内病变或恶性细胞(NILM)、低度鳞状上皮内病变(LSIL)、意义不明的非典型鳞状细胞(ASCUS)3类,收集阴道残端或宫颈管标本通过TCT技术进行检测。
1.4 统计学处理
本研究数据采用SPSS 22.0统计学软件进行分析和处理,计量资料以(±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组HPV转阴时间、HPV-DNA负荷量、CRP水平比较
研究组HPV转阴时间显著早于对照组;治疗后,HPVDNA负荷量、CRP水平显著低于对照组(P<0.05),见表1。
表1 两组HPV转阴时间、HPV-DNA负荷量、CRP水平比较 (±s)
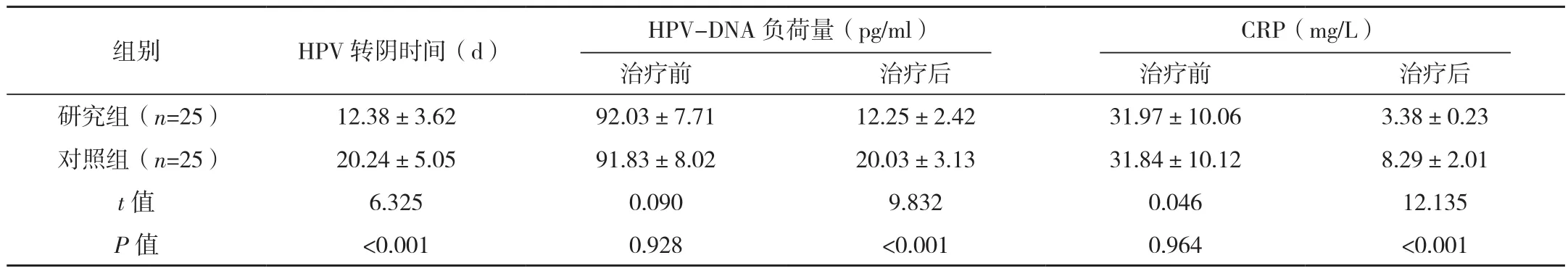
表1 两组HPV转阴时间、HPV-DNA负荷量、CRP水平比较 (±s)
治疗前 治疗后 治疗前 治疗后研究组(n=25) 12.38±3.62 92.03±7.71 12.25±2.42 31.97±10.06 3.38±0.23对照组(n=25) 20.24±5.05 91.83±8.02 20.03±3.13 31.84±10.12 8.29±2.01 t值 6.325 0.090 9.832 0.046 12.135 P值 <0.001 0.928 <0.001 0.964 <0.001组别 HPV转阴时间(d) HPV-DNA负荷量(pg/ml)CRP(mg/L)
2.2 两组治疗前后宫颈液基细胞学指标比较
治疗后,研究组NILM阳性率显著高于对照组,ASCUS阳性率显著低于对照组,差异均有统计学意义(P<0.05);两组LSIL阳性率比较差异无统计学意义(P>0.05),见表2。

表2 两组治疗前后宫颈液基细胞学指标比较 例(%)
3 讨论
宫颈HPV感染是诱发宫颈病变十分危险的因素,如果诊疗不及时而导致病情持续进展,细胞转化为恶性表型的概率会有所升高,有大概率会诱发宫颈癌[6]。因此,临床治疗宫颈HPV感染需尽早,目前治疗方案包括手术治疗、药物治疗及组合治疗方案,但手术治疗易对生殖系统造成损伤,因此,不建议作为首选治疗方案。随着临床治疗技术的不断成熟,现阶段药物联合治疗方案愈加被广泛应用,本院联合应用干扰素α-2b及抗HPV蛋白敷料治疗宫颈HPV感染获得了较为理想的治疗效果。
研究结果显示,研究组HPV转阴时间显著早于对照组,HPV-DNA负荷量、CRP水平显著低于对照组(P<0.05),与伍天慧等[7]的研究报告十分接近,提示联合应用干扰素α-2b及抗HPV蛋白敷料治疗宫颈HPV感染,可更为有效地降低HPVDNA负荷量及CRP水平,加快HPV转阴;另外,治疗后,研究组NILM阳性率显著高于对照组,ASCUS阳性率显著低于对照组(P<0.05),与肖鸣盛等[8]的研究结果基本一致,提示该治疗方案可有效改善宫颈液基细胞学指标。相关研究指出,若患者机体免疫功能正常,四分之三左右的HPV感染会通过自身免疫应答而自行消除[9-10]。由此可见,HPV持续感染与机体免疫功能低下密切相关,因此,在开展抗病毒治疗的同时,应格外重视调节患者免疫功能。干扰素α-2b可对病毒的繁殖、生长加以有效控制,促进肿瘤坏死因子及白介素-2、CRP等炎性因子消除,增强宿主细胞免疫应答功能,实现抗病毒、免疫调节的作用,最终将HPV有效清除[11]。抗HPV生物蛋白敷料经实验室试验证实可杀灭HPV病毒,并经由物理调节机制阻断基底细胞与HPV的结合途径[12]。茶多酚、JB蛋白、卡波姆是该药物最主要的三种活性成分,其中茶多酚能够促使局部免疫力提升;JB蛋白则以其正负电荷作用机制破坏HPV蛋白构象而加速HPV失活;卡波姆作用机制在于包裹失活HPV并将其排除,进一步修复创面,三种活性成分的作用机制相辅相成[13]。因此,抗HPV生物蛋白敷料能够发挥出灭活病毒、提高局部免疫、愈合损伤创面的综合作用,全方位控制感染,有效改善炎症因子水平,加速HPV转阴。联合应用上述两种药物,可发挥疗效协同作用,进一步优化治疗效果。
综上所述,治疗宫颈HPV感染期间采用干扰素α-2b及抗HPV蛋白敷料联合用药方案,疗效显著,具有推广价值。
