多层螺旋CT在胃癌术前分期中的应用进展
2021-03-03马江磊陈华亮杨德君蔡清萍
马江磊,陈华亮,杨德君,蔡清萍
(1.海军军医大学 基础医学院,上海 200433;2.海军军医大学长征医院 胃肠外科,上海 200003)
目前,胃癌仍然是人类生命健康的重要威胁,是世界范围内的第五常见癌症和第三大癌症致死原因[1]。根据肿瘤侵犯的程度(T)、有无区域淋巴结转移(N)及远处转移(M)可对胃癌进行TNM分期。TNM分期被认为是判断各种肿瘤预后的主要参考指标[2]。与其他肿瘤类似,TNM分期系统是胃癌分期的金标准。对胃癌的治疗采用分期治疗的原则,病灶较小且局限于黏膜下的早期胃癌可以通过内镜治疗,即内镜下黏膜切除或内镜黏膜下剥脱;对于进展期可切除/潜在可切除胃癌,首选治疗方式依然是根治性切除手术,结合围手术期化疗和术后辅助化疗;对于不可切除的晚期转移性胃癌而言,考虑进行转化化疗后行根治性手术或姑息性治疗,部分出现并发症的晚期胃癌患者还考虑姑息性手术治疗。因此,准确的胃癌术前分期对拟定治疗方案和评估预后等具有重要的意义[3]。目前对胃癌的术前分期诊断以内镜和影像学手段为主,而影像学检查中又以多层螺旋CT(multi-slice spiral CT,MSCT)应用最为广泛。近年来,随着MSCT扫描技术的进步以及各种后处理功能软件的开发,其在胃癌术前分期中发挥的作用越来越重要。本文主要针对胃癌TNM分期的演变和MSCT对胃癌TNM分期评估的进展进行综述,以期为胃癌术前分期的评估方式的选择与应用提供借鉴。
1 胃癌TNM分期系统的沿革与现状
近几十年来,业界提出了多种胃癌分期方法,其中大多数方法经临床实践验证发现存在明显不足而被淘汰。目前,国际上有三家胃癌分期的权威机构,即美国癌症联合委员会(American Joint Committee on Cancer,AJCC)、国际抗癌联盟(Union for International Cancer Control,UICC)和日本肿瘤协会(Japanese Gastric Cancer Association,JGCA)。由AJCC/UICC颁布的TNM分期系统已经得到全球公认。
肿瘤TNM分期的概念首先由Pierre Denoix提出,之后UICC成立临床肿瘤分期委员会对TNM分期系统进行完善,并在1966年首次制定出胃癌TNM分期法(未参照手术和病理检查结果)。1969年,AJCC组建胃癌特别工作组,明确指出分期需按照手术和病理检查结果制定。上世纪70年代末,JGCA对胃癌进行了分期,将胃周淋巴结分为3站16组。
1975年,为统一胃癌分期标准,三家代表召开了联合会议,但最终因各执己见而未探讨出统一结果。1984年,三方代表召开第二次联合会议,经过商议,最终诞生了一个统一的分期系统。在1985年的日内瓦国际会议上,UICC正式颁布了胃癌TNM分期法(第4版)[4-5]。
但是,在临床应用中,研究发现此分期方法存在很多缺点,例如淋巴结的位置只能在手术中由外科医生来判断,病理科医生很难在标本经福尔马林固定后进行诊断[6]。因此,UICC于1997年出版了第5版TNM分期,第5版胃癌TNM分期的主要改进之处在于N分期,其不再以转移淋巴结的解剖部位与肿瘤边缘的距离是否>3 cm为判断标准,而是以转移淋巴结的数目作为N分期的标准[7]。
为进一步完善胃癌TNM分期系统,UICC于2002年制订了第6版TNM分期,该版将T2期又细分为T2a和T2b。Yoo等[8]的研究结果表明,第6版分期中的各亚期与预后结果的匹配度比第5版好。但是第6版TNM分期法依然存在不足,比如清扫送检的淋巴结数目如果<15枚,无论其范围都认为是Nx,即无法评估淋巴结分期,难以对这类患者的预后进行客观评价。
随后,第7版胃癌TNM分期系统于2009年出版并于2010年实施。第7版TNM分期将旧版的N1期(1~6个淋巴结转移)拆分为N1(1~2个淋巴结转移)和N2(3~6个淋巴结转移),将旧版的N2(7~15个淋巴结转移)重新定义为N3a,旧版的N3(>15个淋巴结转移)定义为N3b,但是最终却未将N3a和N3b纳入任何阶段组[9]。见表1。在临床应用过程中,其不足之处逐渐显现,使得该分期系统已经不能满足临床诊疗需要。在此之后,国际胃癌协会(International Gastric Cancer Association,IGCA)提出了一种新的胃癌分期系统,该系统与第7版分期系统共享相同的TNM分期,但在最终分期中引入N3a和N3b。Shu等[10]的研究表明,IGCA分期系统比第7版胃癌TNM分期系统对Ⅲ期胃癌患者的生存分层更为准确。
因此,在AJCC、UICC和IGCA的共同努力下,通过胃癌大数据分析,于2016年底出版了第8版胃癌TNM分期系统。最新版的胃癌TNM分期系统将N3期细分成N3a期和N3b期,并将其归入TNM分期系统,使得分期更加精确,更能反映胃癌患者真实的预后情况。见表2。另外,第8版胃癌TNM分期系统还新增了胃癌临床TNM(cTNM)分期标准和新辅助治疗后TNM(ypTNM)分期标准[11]。
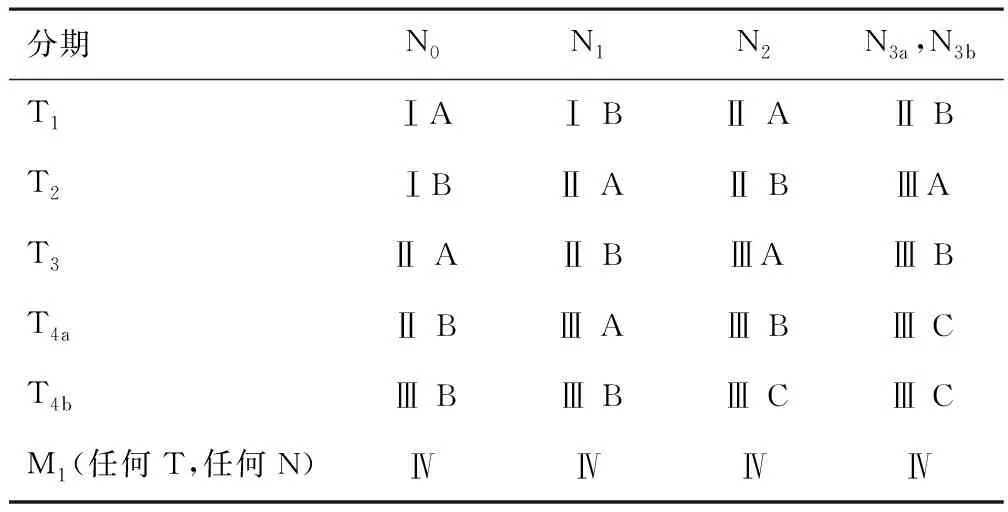
表1 第7版胃癌TNM分期
2 胃癌TNM分期的优势与不足
TNM分期作为胃癌分期的金标准,术前进行准确的分期判定可以指导临床医生拟定更合理的治疗方案以及对治疗方案的疗效进行更科学的评估,还有助于准确地评估患者预后。第8版TNM分期将N分期的N3a和N3b两个亚组纳入了最终的分期中,使其更能反映患者的真实预后[11]。但最近国外有文献报道,与第7版TNM分期系统相比,第8版TNM分期系统并没有带来显著的预后改善。在临床分期患者中,第7版和第8版的ⅢC期和Ⅳ期之间存在显著重叠。当然,此结果还需以后在临床实践中进一步验证[12]。另外,新的TNM分期系统增加的cTNM分期和ypTNM分期,对于为不同患者提供更准确的分期从而进行治疗前评价和初始治疗的决策具有重要意义[13]。
但是,新版胃癌TNM分期也有不足,建立系统时的数据84.8%来自日本和韩国,由于地域、人种等方面的差异,使得不少学者对于新版胃癌TNM分期系统是否在全球范围内适用产生了质疑。针对此问题,有研究使用美国癌症数据库对主要使用亚洲数据创建的分期系统是否适用于美国人群进行了评估,结果显示第8版胃癌TNM系统对美国人群仍然适用[14]。
3 MSCT对于胃癌T分期的诊断
在TNM分期系统中,T分期表示肿瘤浸润胃壁的深度,胃癌是否出现浆膜侵犯作为MSCT的诊断重点,将直接影响到胃癌切除手术成功率和术后5年生存率,准确的T分期可为手术治疗提供十分重要的依据。有研究表明,MSCT对胃癌术前T分期的总诊断准确率为91%[15]。但是经大量研究表明,MSCT判定胃癌T2、T3、T4期的准确率较高,而对于临床上意义重大的T1期,即早期胃癌,MSCT判定的准确率却不尽如人意。Feng等[16]的研究显示,MSCT判定胃癌T1、T2、T3和T4期的准确率分别为20.8%、36.4%、89.5%和86.7%。曾广正等[17]和Marta等[18]的研究结果也与上述相符合。究其原因,MSCT判定胃癌T1分期准确性较低的原因可能是早期胃癌表现多样,有隆起型、表浅型和溃疡型等,同时由于胃的蠕动,导致MSCT对于一些微小病灶容易漏诊,尤其当早期胃癌呈表浅型和溃疡型时更易遗漏。目前针对MSCT判定胃癌T1分期准确率不高的问题,有文献报道,采用MSCT与胃镜相结合,可提高对T1期的诊断准确率。因为胃镜是直视下检查,对于微小的黏膜中断破坏也能十分清晰地观察到,不易遗漏微小病变。另外,胃镜还可对病变局部进行组织活检,明确病变性质。这些都是胃镜相对于MSCT的优势。但是胃镜无法观察到黏膜下以及浆膜外的病变,亦无法观察病变与相邻器官的关系,而这些恰好是MSCT的优势,所以MSCT与胃镜结合可以大大提高胃癌T分期的诊断准确率。Kristina等[19]通过比较不同MSCT扫描方法对胃癌T1期诊断准确率的结果发现,使用20 g·L-1的泛影葡胺水溶液作为胃对比剂,MSCT对于T1的诊断准确率为90.1%,而使用水作为胃对比影剂,诊断准确率仅为83.8%。最近有文献报道,使用飞利浦64排增强CT扫描对于胃癌T1分期的准确率达到了97.11%,相比之前文献报道的数据有了显著提高。有研究建议使用飞利浦64排螺旋CT术前进行胃癌T分期时,应该密切观察病变范围的强化深度、胃周脂肪间隙的改变、浆膜面的光整程度等[20]。
此外,有研究通过探索MSCT的胃黏膜成像技术并研究其在早期胃癌诊断中的应用价值,现已获得了一定的成果。吴惠强等[21]研究表明,MSCT扫描效果较好的胃黏膜成像技术方案为:进行上腹部CT增强扫描患者,扫描前10 min常规山莨菪碱10 mg注射并进行清水充胃,用80 mL的350 g·L-1碘海醇以3 mL·s-1的注药速度注射后应用MSCT扫描,扫描方案:动脉期中期(25 s)、对比剂剂量80 mL、对比剂注射速度3 mL·s-1扫描。此方案与胃镜检查组的结果相比较,相符病例数和准确率均比胃镜有统计学优势。此项研究成果提高了MSCT对早期胃癌诊断的准确率,预期在早期胃癌诊断方面将具有重要的临床应用价值。
4 MSCT对于胃癌N分期的诊断
N分期表示区域淋巴结的转移情况,淋巴结转移是胃癌主要的转移途径,胃癌的术前评估、治疗方案的确定以及预后评估均需要准确的局部淋巴结转移情况作为参考依据[22]。以往关于N分期有两种不同的分期方法,一种是JGCA的胃癌日本分期法,该分期系统根据转移淋巴结的位置进行分期;另一种是AJCC/UICC颁布的TNM分期系统,该分期系统强调转移淋巴结的数目而不考虑转移淋巴结所处的解剖位置。AJCC/UICC分期系统的淋巴结转移情况可以较好地评价预后,日本分期法因其淋巴结分类复杂且淋巴结跳跃性转移的现象存在而不能很好地评价预后。目前新的日本胃癌N分期已经不再以转移淋巴结所处的部位进行分期,而是以转移数目进行分期,日本分期已与国际分期全面接轨[23]。
因此,准确地判定转移淋巴结的数目尤为重要。以往MSCT通常根据淋巴结的直径来判断有无淋巴结转移,故而存在一定局限性。有文献报道,在经手术切除的结节中,转移性淋巴结直径<5 mm的占5.1%,5~9 mm的占21.7%,10~14 mm的占23%,≥14 mm的占82.6%,随着淋巴结直径的增大,发生转移的可能性越大,但较小直径的淋巴结并不能排除转移可能。因此,仅依靠淋巴结的直径来判断转移情况是不够准确的[24]。针对此问题,目前大多数研究采用淋巴结的直径结合增强扫描时的强化程度(相对高密度或周围高密度中心低密度)来进行综合判断,以提高诊断准确率。Jiang等[25]研究表明,应用这些综合诊断标准,术前MSCT对胃癌患者N分期的诊断在准确性方面上具有良好的效果。其结果表明,总N分期的准确率为86.3%,N0、N1、N2、N3分期的准确率分别为83.5%、89.0%、83.5%和89.0%。与以往的研究相比,该研究显示MSCT对N分期的诊断准确率有所提高。目前对于判定淋巴结转移情况尚无统一标准,且上述研究的病例数较少,所以研究结果还需要以后的多中心随机对照研究加以证实。
此外,影响诊断淋巴结转移准确性的因素还包括淋巴结的形态、位置以及胃周脂肪含量的高低。由于炎症反应性增生的淋巴结经MSCT扫描易被误判为转移性淋巴结;MSCT对于所处空间较小、位于胃癌病灶或在肝十二指肠韧带周围的淋巴结检出率较低;当胃周围脂肪含量减少使得胃与周围器官的间隙减小甚至消失也可影响MSCT对淋巴结的观察。对于这些问题,Bai等[26]研究表明,血清肿瘤标志物CA-724和CA199可以作为MSCT扫描的辅助手段,并在胃癌淋巴结转移的联合诊断中显示出良好的敏感性(89.3%)。这可为临床医生判定胃癌患者术前的淋巴结转移情况提供一条重要思路。另外,这些问题还有望通过PET/MRI来解决,Liu等[27]研究表明,淋巴结可以通过弥散加权成像和T2饱和脂肪序列来识别,因此PET/MRI可以检出更多的淋巴结,也可以从中检出更多的转移性淋巴结。此外,PET/CT显像可从分子代谢水平上显示肿瘤原发灶和转移灶,故有可能准确地检测出这些微转移灶,从而对N分期进行准确的判定。虽然MSCT对于胃癌N分期的判定存在上述的不足,但是大量研究结果表明,MSCT对于胃癌N分期判定的准确率在71.59%~89.60%[17,22,28-32],说明MSCT检查对于评估胃癌的术前N分期具有较高的价值。
5 MSCT对于胃癌M分期的诊断
M分期表示胃肿瘤细胞的远处转移,肝是胃癌转移的最常见器官,其次为肺和腹膜腔。MSCT对于胃癌M分期的诊断有着不可替代的重要地位,因为传统的胃镜和消化道钡餐造影检查均无法观察到胃腔外的侵犯情况及远处器官有无转移。林秉淞[28]研究表明,超声内镜和MSCT判定胃癌M分期的准确率分别为65.82%和79.75%,可以看出MSCT在判断胃癌M分期中的准确性较超声内镜为高。大量研究结果显示,MSCT诊断M分期的准确率在81.00%~97.14%,相比于MSCT诊断N分期的准确率而言,其对于M分期评估的准确性较高[17,22,32,33,35]。有文献报道,在美国,术前行MSCT扫描主要用于判定是否存在远处器官的转移,即M1期,而不是常规用于判定T和N分期[36]。以上结果均表明MSCT对于胃癌M分期的判定具有极高的价值。
但是,MSCT判断胃癌M分期依然存在局限性,其难点在于对微小转移灶和腹膜上的转移灶的判断,因为在CT图像上难以准确鉴别,需要增强扫描调整强化程度。此外,MSCT对于诊断胃癌腹膜转移的M1期的准确率较低,可能与网膜或腹膜转移主要为小结节容易漏诊有关。对于胃癌腹膜转移灶较小难以诊出的问题,鲁福文等[37]建议对于确实未发现病灶,但出现中至大量顽固性腹水,排除门脉高压等因素后应考虑胃癌腹膜种植转移的可能。
6 后处理在胃癌分期中的作用
MSCT对胃癌进行术前分期诊断所采用的后处理技术主要包括仿真内镜、多平面重建技术(multi-planar reconstruction,MPR)、最大密度投影(maximal intensity projection,MIP)。其仿真内镜图像可以清晰显示出肿瘤在腔内的大小、形态及表面情况,立体直观地看到病灶及其与胃腔及周围组织结构的空间位置关系[38]。另外,仿真内镜在胃腔内无“盲点”,可以提供比传统内镜检查更广阔的视野[39]。MPR技术可获得任意角度多层面清晰图像,可进一步明确胃壁增厚程度、病灶胃腔内隆起及胃周围血管的状况,显示信息更为丰富。对于进展期胃癌根治术,清扫沿着胃周围血管分布的第2站淋巴结,较D1清扫患者的预后更佳。王杰夫等[40]的研究表明,MPR可清晰地显示胃周血管的解剖位置和变异情况,为胃癌根治术相关淋巴结的清扫提供指引,减少术中出血及术后并发症的发生。此外,MSCT结合MPR能较为准确发现腹腔内的远处转移情况,包括肝转移、腹腔种植转移、网膜转移等,为晚期胃癌M分期的判定提供了可靠的依据[41]。MIP是通过容积组织或物体中每个象素的最大强度值进行投影,因为其反映的是组织密度间的差异,所以对比度很高,能够显示胃内血管次级分支,可以比较清晰地显示胃的肿瘤血供[42]。
综上所述,MSCT已成为目前胃癌术前分期最为常用的诊断方法之一,可以观察原发灶及周围组织的情况,同时也可以准确了解淋巴结及远处组织器官的转移情况,在胃癌TNM分期中具有较高的应用价值。随着MSCT和后处理技术的进一步发展,MSCT对胃癌的术前诊断将会更加准确,对于合理治疗方案的制定以及预后评估都具有重要的指导意义。
