帕金森病患者嗅觉减退的临床特点及影响因素分析
2021-02-28汤海燕谈鹰冯颖张冰王庄
汤海燕 谈鹰 冯颖 张冰 王庄
帕金森病(Parkinson's disease,PD)是最常见的运动障碍性疾病,也是第二大神经系统退行性疾病[1],其主要病理改变为基底核黑质多巴胺能神经元缺失。PD 临床症状分为运动症状和非运动症状,前者表现为静止性震颤、肌强直、行动迟缓和姿势步态异常;后者包括嗅觉障碍、便秘、焦虑抑郁、睡眠障碍、认知功能障碍等[2]。根据Braak 分期,PD 病理改变最初出现在嗅球和胃肠神经丛,由此,PD 患者的嗅觉障碍、便秘等非运动症状往往在运动症状出现前即已发生,此期称为PD 的运动前期[3]。然而目前对于运动前期各生物标志物之间以及临床期非运动症状之间的关系研究甚少。近年来,国内外均有研究证实血尿酸[4]、载脂蛋白A1(apolipoprotein A1,ApoA1)[5]及总谷胱甘肽[6]与PD 发病和临床特征相关,PD 患者上述血清生化指标较正常健康人群水平低,但关于PD 嗅觉障碍与上述生化指标间关系的研究目前尚缺乏。因此,本研究旨在分析PD 嗅觉减退与其他非运动症状以及与血尿酸、ApoA1、总谷胱甘肽的相关性,并探究PD 患者嗅觉减退的影响因素。
1 对象和方法
1.1 对象 回顾性分析2019 年2 月至2020 年5 月在湖州市中心医院神经内科门诊及住院的PD 患者84例,其中男35 例,女49 例;年龄43~84(68.86±9.08)岁;病程5 个月~13 年,平均3(1,6)年。所有PD 患者均符合2015 年国际运动障碍协会诊断标准[7],明确为原发性PD。排除标准:(1)继发性帕金森综合征、帕金森叠加综合征;(2)合并存在其余神经系统变性疾病和神经精神疾病;(3)滥用药物史、鼻腔或鼻窦有严重疾病或手术史、3 周内发生过呼吸系统感染等导致嗅觉减退的病史;(4)近3 个月内有使用苯海索、苯二氮卓类等可能导致认知障碍的药物史;(5)伴恶性肿瘤、胃肠疾病、肝肾功能不全、痛风及其他严重躯体疾病;(6)近3 个月内有使用影响血脂、尿酸的药物史。本研究经医院医学伦理委员会审批通过。
1.2 方法
1.2.1 临床资料收集 收集患者年龄、性别、文化程度、病程、抗PD 药物使用情况及左旋多巴每日等效剂量(levodopa-equivalent daily dose,LEDD)。
1.2.2 尿酸、ApoA1、总谷胱甘肽检测 所有患者均于就诊当日或次日清晨空腹抽取肘静脉血5 ml,放置于EDTA 抗凝剂试管中,通过离心得到血清,采用美国雅培全自动生化分析仪(C16000)检测尿酸、ApoA1,同步采用液相色谱质谱联用仪(API4500MD,美国AB SCIEX公司)检测血清总谷胱甘肽。
1.2.3 运动症状评估 所有患者均在“关”期采用统一PD 评定量表第Ⅲ部分(unified Parkinson's disease rating scale-Ⅲ,UPDRS-Ⅲ)评分评估PD 患者运动功能[8];采用Hoehn-Yahr(H-Y)分期评价病情程度,将H-Y 分期1~2.5 级定义为早期,H-Y 分期3~5 级定义为中晚期[9-10]。
1.2.4 非运动症状评估 (1)采用T&T 嗅觉计(日本第一药业株式会社)判断嗅觉检知阈值和认知阈值以评估PD 患者嗅觉功能有无减退,将所有PD 患者分为PD 伴嗅觉减退组和PD 不伴嗅觉减退组。(2)患者主诉提供有无便秘症状。(3)通过快速眼动期睡眠行为障碍筛查问卷(rapid eye movement sleep behavior disorder screening questionnaire,RBDSQ)评估患者是否存在快速眼动期睡眠行为障碍(rapid eye movement sleep behavior disorder,RBD):评分≥6 分判断存在RBD[11]。(4)通过病史询问及汉密尔顿抑郁量表(Hamilton depression scale,HAMD)-17 项版本、汉密尔顿焦虑量表(Hamilton anxiety scale,HAMA)-14 项版本、痴呆简易筛查量表(mini-mental state examination,MMSE)分别评估患者有无抑郁、焦虑、认知障碍:HAMD<8 分为无抑郁症状,≥8 分有抑郁症状;HAMA<7 分为无焦虑,≥7 分存在焦虑;MMSE 根据文化程度文盲<17 分、小学文化程度评分<21 分、中学及以上文化程度评分<24 分认为存在认知障碍[12]。
1.3 统计学处理 采用SPSS 20.0 统计软件。符合正态分布的计量资料以表示,组间比较采用两独立样本t检验;不符合正态分布的计量资料以M(P25,P75)表示,组间比较采用Mann-Whitney U 检验。计数资料组间比较采用χ2检验。采用Spearman 等级相关分析PD 患者嗅觉减退与其他非运动症状及血清生化指标的相关性。采用二分类logistic 回归分析PD 患者嗅觉减退的影响因素。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者临床特征和运动症状比较 84 例PD 患者中,PD 伴嗅觉减退组44 例,PD 不伴嗅觉减退组40 例。两组患者性别、年龄、病程、LEDD、H-Y 分期及UPDRS-Ⅲ评分比较差异均无统计学意义(均P >0.05),见表1。
2.2 两组患者非运动症状及血清生化指标比较 PD伴嗅觉减退组患者便秘、RBD、焦虑和认知障碍发生率均高于PD 不伴嗅觉减退组,血清总谷胱甘肽水平低于PD 不伴嗅觉减退组,差异均有统计学意义(均P<0.05);但两组患者抑郁发生率、血清尿酸和ApoA1 水平比较差异均无统计学意义(均P >0.05),见表2。

表1 两组患者临床特征和运动症状比较
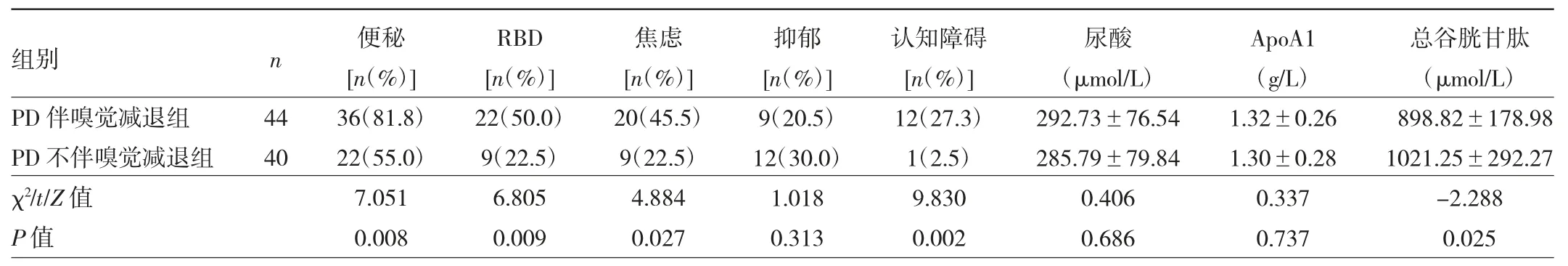
表2 两组患者非运动症状及血清生化指标比较
2.3 PD 患者嗅觉减退与非运动症状及血清总谷胱甘肽水平的相关性分析 Spearman 等级相关分析显示,PD 患者嗅觉减退与便秘、RBD、焦虑、认知障碍发生率均呈正相关(r=0.290、0.285、0.241、0.342,均P<0.05),但与血清总谷胱甘肽水平无相关性(r=0.194,P >0.05)。
2.4 PD 患者嗅觉减退的影响因素分析 将上述Spearman 等级相关分析有统计学意义的便秘、RBD、焦虑及认知障碍作为自变量,以有无嗅觉减退作为因变量,作二分类logistic 回归分析,结果显示认知障碍是PD 患者嗅觉减退的影响因素(P<0.05),见表3。

表3 PD 患者嗅觉减退的影响因素分析
3 讨论
本研究发现PD 伴嗅觉减退与不伴嗅觉减退患者病程比较差异无统计学意义,与王瑞丹等[13]的研究结果一致。这一结果说明PD 嗅觉障碍的发生率并未随着病程的延长而升高,且PD 的嗅觉症状并非依赖于运动症状而产生。运动症状的产生是因为黑质多巴胺能的丢失,嗅觉减退则是由于路易小体沉积于嗅球、前嗅核、嗅束以及梨形皮层[14]。
本研究发现PD 伴嗅觉减退患者便秘发生率更高,符合PD 早期病理改变累及的部位。本研究发现PD 伴嗅觉减退患者更易出现RBD,与王瑞丹等[13]的研究结果一致。PD 患者Braak 分期发展到Ⅱ期时路易小体累及脑干的中缝核即可出现睡眠症状。Miyamoto 等[15]研究显示原发性RBD 患者嗅觉功能的损害可能与中脑边缘系统通路受损有关。边缘系统参与嗅觉形成,与内嗅皮质和嗅球有密切的联系,故而可解释嗅觉障碍与RBD 之间的关系。同样,情感障碍也是PD 患者整个病程中常见的非运动症状,因边缘系统的参与,嗅觉减退与情感障碍的关联即可解释。本研究发现PD 伴嗅觉减退患者更易发生焦虑,而两组患者抑郁发生率比较差异无统计学意义;但二分类logistic 回归分析并未发现焦虑是PD嗅觉障碍的影响因素。本研究发现PD 伴嗅觉减退患者更易发生认知障碍,且二分类logistic 回归分析证实认知障碍是PD 患者嗅觉障碍的影响因素。Lee 等[16]研究发现PD 伴嗅觉减退患者认知相关灰质萎缩,以梨状皮层、眶额皮质等嗅觉皮层更明显,该解剖结构提示两者存在密切联系。Bohnen 等[14]发现PD 患者嗅觉识别能力与前脑胆碱能通路完整性有关,特别是边缘皮层胆碱能神经失支配与嗅觉受损相关,故从神经生化机制上可解释嗅觉与认知的相关性。张威等[17]曾总结嗅觉障碍可作为PD 患者痴呆的危险因素,可见PD 嗅觉障碍与认知障碍有相辅相成的关系。
尿酸一直被认为在神经元中发挥抗氧化应激作用,是PD 患者的神经保护剂。Qiang 等[18]研究显示血浆ApoA1 水平与多巴胺转运蛋白(DAT)再摄取程度相关,ApoA1 水平越低,DAT 缺乏越严重,预示ApoA1 水平同样能导致PD 易感。然而本研究却未发现PD 伴嗅觉减退和不伴嗅觉减退患者间尿酸及ApoA1 的差异,与Lee等[19]的结论相一致。谷胱甘肽作为人体内一项重要的抗氧化指标,亦参与了PD 的氧化应激代谢。韦慧君等[20]发现PD 患者血谷胱甘肽水平较正常人低,合并认知障碍的患者更低。本研究发现PD 伴嗅觉减退患者血总谷胱甘肽水平较不伴嗅觉减退患者低,这一发现刷新了对于谷胱甘肽作为氧化应激保护剂的认识。PD 的嗅觉障碍存在小胶质细胞活性增加、炎性介质的释放、局部细胞凋亡等病理机制。谷胱甘肽作为重要的氧化应激指标,极大可能参与其中。目前亦有研究支持前驱期PD 存在的氧化应激与嗅觉损害相关[21]。
综上所述,本研究发现PD 伴嗅觉减退患者更易出现便秘、RBD、焦虑、认知障碍,且认知障碍为嗅觉减退发生的独立影响因素。血谷胱甘肽在PD 嗅觉减退患者中呈现低水平,提示该氧化应激指标参与PD 嗅觉障碍的形成。上述结论为今后PD 非运动症状的干预和治疗提供了依据。但本研究尚存在一些不足之处:(1)样本量偏小,以至于嗅觉减退与其余非运动症状之间的关系与其他学者的研究略有差异;(2)未将认知障碍、焦虑、抑郁等指标做等级分析,故嗅觉减退与各指标严重程度的相关性未获悉。未来将进一步扩大样本量,探索PD 不同运动亚型非运动症状之间及与生化指标间的关系。
