鼻敏颗粒的临床前药效学研究
2021-02-22程媛唐熠谭亿民李涓
程媛,唐熠,谭亿民,李涓
过敏性鼻炎又称变态反应性鼻炎,以阵发性反复发作性的鼻痒、鼻塞、喷嚏、流清水样鼻涕为主症[1],属中医学“鼻鼽”范畴[2-3]。目前过敏性鼻炎的发病率不断增高,在我国患病率为4%~38%[4],儿童和青少年的发病率更高[5],其易反复发作,影响患者正常的学习、工作和生活。目前,西药治疗过敏性鼻炎的药物主要有抗组胺药、减充血剂、肥大细胞稳定剂、白三烯受体拮抗剂、鼻内糖皮质激素等[6],但存在疗效有限或使用不当不良反应大的风险[6-7],因此,开发治疗过敏性鼻炎的制剂应用前景广阔。鼻敏颗粒是我院老中医有效验方,组方为黄芪、地肤子、地龙、鹅不食草、细辛,临床应用数十年,已有多例临床病例的收集[8],疗效确切,并已完成制剂工艺的研发[9]。鼻敏颗粒具有益气固表、温阳通窍、摄涕止嚏的功效,既可祛邪外出,又可消除局部症状,有进一步研究开发制成院内制剂,广泛应用于临床的价值。本文通过鼻敏颗粒的临床前药效学和安全性评价等相关研究,对整个制剂安全性、有效性进行科学评价,为院内制剂的开发奠定基础,也为医院制剂的发展提供思路。
1 材料与方法
1.1 材料 (1)实验动物:昆明种小鼠,体质量18~22 g,SPF级动物,由成都中医药大学实验动物中心提供,许可证号:SCXK(川)2014-11。豚鼠,体质量220~260 g,普通级动物,由四川省实验动物专委会养殖场提供,许可证号:SCXK(川)2013-14。灭菌全价鼠料由成都中医药大学实验动物中心提供,全价豚鼠料由四川省实验动物专委会养殖场提供。(2)试药试剂:鼻敏颗粒浸膏,3.69 g生药/g膏,由成都中医药大学附属医院药剂科提供,实验前用蒸馏水稀释至相应浓度。吲哚美辛肠溶片由重庆科瑞制药有限责任公司生产,批号641002。二甲苯,批号2015060501;甲苯二异氰酸酯(TDI),批号2016090603;橄榄油,批号2015080101,均由成都市科龙化工试剂厂生产。(3)仪器设备:打孔器、光镜、Mias2000图像分析系统。
1.2 实验方法
1.2.1 鼻敏颗粒的急性毒性实验:KM小鼠40只,体质量18~22 g,雌雄各半,随机分为给药组和对照组,每组20只,雌雄各10只。禁食16 h后,采用最大给药量法,给药组灌胃给予鼻敏颗粒药液(2.15 g生药/ml)0.4 ml/10 g,每天1次。对照组同法灌胃等体积蒸馏水。观察给药后14 d内小鼠出现的毒性反应与死亡情况,并于给药后第7、14天称取小鼠体质量。给药第14天,处死小鼠,解剖,肉眼观察主要脏器。
1.2.2 鼻敏颗粒的抗炎作用:KM小鼠60只,体质量18~22 g,雄性,随机分为5组,分别为模型组、鼻敏颗粒高、中、低剂量组、吲哚美辛组。鼻敏颗粒高、中、低剂量组给药剂量依次是20.2、10.1、5.05 g生药/kg(分别相当于临床拟用剂量的28、14、7倍)。吲哚美辛组给药剂量为10 mg/kg。各组小鼠每天以20 ml/kg灌胃给予相应的药物1次,连续给药3 d。模型对照组同法给予等体积饮用水。第3天给药30 min后,每只小鼠左耳廓内外侧滴涂20 μl二甲苯致炎,右耳不涂。20 min后处死小鼠,用直径7 mm的打孔器分别于左、右耳相同部位打下耳片,十万分之一电子分析天平称重,以左、右耳片重量差值表示肿胀度。计算各组耳肿胀度和肿胀抑制率。肿胀抑制率(%)=(模型组平均肿胀度-给药组平均肿胀度)÷模型组平均肿胀度×100%。
1.2.3 鼻敏颗粒对过敏性鼻炎动物模型的治疗作用:豚鼠一批,体质量220~260 g,随机抽取10只作为空白组,剩余的豚鼠用10%TDI橄榄油溶液经微量加样器滴鼻进行造模。方法如下:豚鼠每侧鼻孔滴入10%TDI橄榄油溶液5 μl,每天1次,连续7 d激发。末次激发后即刻至30 min,通过行为学评分判断模型是否成功。评分标准:轻度搔鼻1~2次、喷嚏1~3个、流涕至鼻孔各记1分;搔鼻多次、喷嚏4~10个、流涕超出前鼻孔各记2分;剧烈搔鼻、喷嚏11个以上、涕流满面各记3分。各症状记分叠加,总分超过5分为造模成功。选取造模成功的豚鼠50只,随机分为5组,每组10只,分别为模型组、鼻敏颗粒高、中、低剂量组、氯雷他定组。鼻敏颗粒高、中、低剂量组给药剂量依次是14.4、7.2、3.6 g生药/kg(分别约相当于临床拟用剂量的20、10、5倍)。氯雷他定组给药剂量是1 mg/kg;各给药组豚鼠每天以10 ml/kg灌胃给予相应的药物1次,连续给药7 d;模型组给予等体积蒸馏水。同时继续滴鼻10%TDI橄榄油溶液10 μl/只,隔天1次,维持致敏状态。空白组动物同法滴鼻给予橄榄油。末次给药后1 h后,给药组和模型组用10%TDI橄榄油溶液滴鼻激发动物,空白组用橄榄油滴鼻,记录30 min内行为学评分。处死动物,剥离鼻周围皮肤,沿鼻中线切开,剪下鼻中隔黏膜,用FAA液固定。石蜡包埋,切片4 μm,HE染色,光镜下观察鼻黏膜被覆上皮细胞表面炎性渗出物分级,其中,-:无炎性渗出物或每张切片炎性渗出物的总面积低于1/4视野,+:每张切片炎性渗出物的总面积高于1/4视野、但低于1/2视野,++:每张切片炎性渗出物的总面积高于1/2视野、但低于3/4视野,+++:每张切片炎性渗出物的总面积高于3/4视野。Mias2000图像分析系统半定量计数炎细胞面积。

2 结 果
2.1 鼻敏颗粒的急性毒性实验 给药后小鼠活动减少,约1 h后动物基本恢复正常。至给药后14 d,动物行为、活动、饮水、排便均未见异常,无死亡。给药组小鼠给药后7 d和14 d的体质量和体质量增长值与对照组比较无显著性差异(P>0.05)。给药第14天,处死小鼠,解剖,肉眼观察主要脏器,心、肝、脾、肺、肾等主要脏器未见异常。说明鼻敏颗粒灌胃给予小鼠的最大给药量为86 g生药/kg,约为临床拟用剂量(0.72 g生药/kg)的119倍,未见明显毒性反应。见表1。
2.2 鼻敏颗粒的抗炎作用 高剂量组、吲哚美辛组肿胀度与模型组相比有显著性差异(P<0.05),高剂量组肿胀度抑制率为29.4%。见表2。
2.3 鼻敏颗粒对过敏性鼻炎动物模型的治疗作用 鼻敏颗粒各剂量组及氯雷他定组行为学评分与模型组相比有显著性差异(P<0.05)。见表3。病理切片光镜下观察鼻黏膜被覆上皮细胞表面炎性渗出物结果见表4。鼻敏颗粒各剂量组及氯雷他定组炎细胞浸润面积与模型组相比有显著性差异(P<0.05)。见表5。

表1 鼻敏颗粒急性毒性实验对小鼠体质量的影响

表2 鼻敏颗粒对二甲苯致小鼠耳肿胀度的影响

表3 治疗前后动物行为学评分分)

表4 鼻敏颗粒对豚鼠过敏性鼻炎模型鼻黏膜被覆上皮表面渗出物的比较
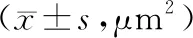
表5 鼻敏颗粒对豚鼠过敏性鼻炎模型鼻黏膜被覆上皮酸性白细胞的影响比较
3 讨 论
本研究根据《四川省医疗机构制剂研究技术指南》[10](试行版)的要求,参照国家药监局颁布的《中药、天然药物急性毒性研究技术指导原则》《中药新药研究指南(药学、药理学、毒理学)》,对鼻敏颗粒进行临床前安全性评价和主要药效学实验。在急性毒性实验中,观察小鼠在24 h内一次性给予鼻敏颗粒后14 d内产生的毒性反应及死亡情况。在药效学评价中,选用过敏性鼻炎及经典的炎症动物模型,全面评价鼻敏颗粒的对过敏性鼻炎的治疗作用,为临床研究提供依据。研究表明,鼻敏颗粒毒性低,药效显著,有明显的抗炎和治疗过敏性鼻炎的作用,其缓解过敏性鼻炎症状的原因与降低鼻黏膜渗出物和减少炎性细胞产生有关。本研究中表4显示,空白组豚鼠鼻黏膜被覆上皮表面无炎性渗出物、上皮细胞无变性、坏死及炎细胞浸润,基底膜清楚。模型组黏膜被覆上皮表面出现多少不等的炎性渗出物,多数动物被覆上皮表面炎性渗出物数量多。渗出物由大量酸性粒细胞构成,并有中性粒细胞及纤维素。被覆上皮细胞有不同程度的变性、坏死及酸性、中性粒细胞浸润,基底膜完整,黏膜固有层可见充血、水肿、酸性粒细胞、中性粒细胞浸润。各给药组豚鼠被覆上皮表面炎性渗出物不同程度减少,被覆上皮细胞变性、坏死及酸性、中性粒细胞浸润不同程度减轻,黏膜固有膜内充血、水肿、酸性、中性粒细胞浸润也不同程度减轻。说明鼻敏颗粒缓解过敏性鼻炎的症状,治疗过敏性鼻炎的原因与降低鼻黏膜渗出物和减少炎性细胞产生有关。但鼻敏颗粒通过何种信号转导通路发挥减少渗出物和炎细胞的产生尚不明确,因此在今后的研究中,应进一步深入探索其发挥作用的分子机制。
综上所述,鼻敏颗粒开发成院内制剂前景良好,本研究的临床前安全性评价及药效学实验为今后鼻敏颗粒申请临床试验及申报院内制剂打下了基础。
