运动干预在食管癌同步放化疗病人中的应用
2021-02-07李晓珊张艳萍郑雅芬
李晓珊,张艳萍,张 宏,郑雅芬
福建省肿瘤医院(福建医科大学附属肿瘤医院),福建 350014
食管癌是我国的高发恶性肿瘤,2015年新发病例约24.57万例,死亡病例约18.81万例[1]。由于我国经济条件有限,胃镜尚未广泛普查,加上食管癌起病隐袭,大部分病人初诊时已失去手术机会。同步放化疗成为无法手术切除食管癌的标准治疗方案[2],但也出现骨髓抑制、胃肠道反应、放射性肺炎、疲乏等症状[3]。癌因性疲乏(cancer-related fatigue)是肿瘤病人最常见、感受最痛苦的症状之一,美国国家综合癌症网络(National Comprehensive Cancer Network,NCCN)将癌因性疲乏定义为是与癌症或者癌症治疗有关的一种痛苦的、持续的、主观上躯体、情感或认知的疲惫感,与近期的活动不成比例[4]。先前研究表明运动干预可减轻乳腺癌化疗病人癌因性疲乏程度[5]。本研究探讨运动干预在不可手术切除的食管癌同步放化疗病人中的作用,现报道如下。
1 资料与方法
1.1 一般资料
选取2018年1月—2019年9月于福建省肿瘤医院就诊的食管癌病人。纳入标准:①病理明确为食管癌;②无法行根治性手术切除行同步放化疗;③卡式功能评分≥70分;④病人能独立完成调查问卷表;⑤病人知情同意,随访可靠。排除标准:①有心、肝、肺等严重基础疾病;②存在意识清、精神障碍;③因腰椎间盘突出等原因导致运动受限;④无法配合该项研究。剔除标准:①由于各种原因导致无法完成既定的放化疗计划;②病人不愿配合,中途退出;③病人治疗过程中死亡。根据纳入及排除标准,共有120例病人纳入研究,按照数字随机法分成运动组和对照组,各60例。根据剔除标准,7例病人化疗1次后拒绝继续化疗;4例病人失联;3例病人依从性差,中途拒绝运动干预。最终106例食管癌病人完成研究,其中运动组52例,对照组54例。两组病人的年龄、性别、文化程度及体质指数比较,差异无统计学意义(P>0.05),具有可比性,详见表1。本研究通过我院伦理委员会审批(批号:YKT2017-01-03)。
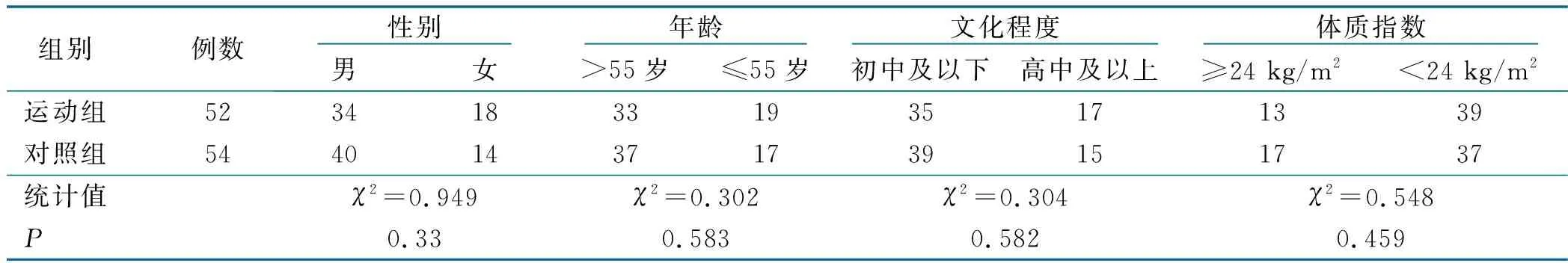
表1 两组病人一般资料比较 单位:例
1.2 干预措施
1.2.1 对照组
给予常规的护理。①治疗前:向病人及家属宣教,包括放化疗的目的、大致流程及不良反应,嘱病人定期复查血常规、生化全套。解答病人及家属的疑问,争取病人及家属的理解和配合。②心理指导:肿瘤病人常伴有焦虑、抑郁等不良情绪,评估病人心理状态,对有心理问题的病人予以心理疏导,必要时请心理医生协助诊治。③饮食处理:化疗时少量多餐、细嚼慢咽,多摄入高热量、高蛋白、低脂易消化食物,避免坚硬、辛辣刺激的食物。④放化疗毒副作用处理:出现放射性食管炎时,黏膜炎性反应为Ⅰ度以软食为主,Ⅱ度或Ⅲ度以进食半流质或流质饮食,食物温度在35~40 ℃,进食后口服100 mL温生理盐水。疼痛病人用利多卡因+地塞米松缓慢入咽以减轻水肿。⑤骨髓抑制:予以对应的药物处理,加强口腔护理,保持皮肤完整。
1.2.2 运动组
在常规护理基础上予以运动干预。运动措施包括:①发放宣传单,向病人讲解运动的益处、方式及注意事项。②运动时病人佩戴运动手环、手机,手机APP具有同步手环信息,可收集、分享运动步数及心率。病人每周将手机APP上的运动步数、心率截图后分享医护人员,使医护人员能对病人的活动量进行实时、动态监控及指导。③根据2018年美国运动医学会(American College of Sports Medicine,ACSM)制定的“运动处方”[6]。有氧运动措施:根据病人的体制、病情、个体运动偏好定制个性化的运动方案。运动强度为中度强度,运动时心率达到最大心率的55%~70%(最大心率=220-年龄);运动形式包括快走、慢跑、上下楼梯等。运动时间为每次30 min,每周3次或4次。④抗阻运动措施:使用弹力带进行针对性的抗阻运动,针对大肌群(即胸部、肩部、上肢、腹部、臀部和下肢)进行训练。每次动作维持10 s,每个动作重复10次,组间休息2~3 min。依据病人体能逐渐增加病人训练的强度。运动时间为每次30 min,每周3次或4次。有氧运动和抗阻运动均在化疗前1 d开始,总的干预时间为8周。
1.3 评价指标
1.3.1 癌因性疲乏
采用Piper修正疲乏量表(Revised Piper Fatigue Scale,PFS-R)对病人癌因性疲乏进行评估,该量表由行为、情感、躯体及认知4个维度组成,共22个条目。各条目的得分范围为在0~10分。总量表及各维度得分为所含条目总分值和除以条目数,总分为0~10分,得分越高,疲乏程度越大[7]。
1.3.2 生活质量
采用第4版癌症病人生命质量测定量表共性模块(Functional Assessment of Cancer Therapy-Generic Scale,FACT-G)对病人的生活质量进行评价,包括生理状况(7条)、社会/家庭状况(7条)、情绪状态(6条)、功能状况(7条)4个维度,27个条目。各条目得分相加(逆向条目则反向计分),得分越高表明其生活质量越好[8]。
1.4 统计学方法

2 结果
2.1 癌因性疲乏(见表2)
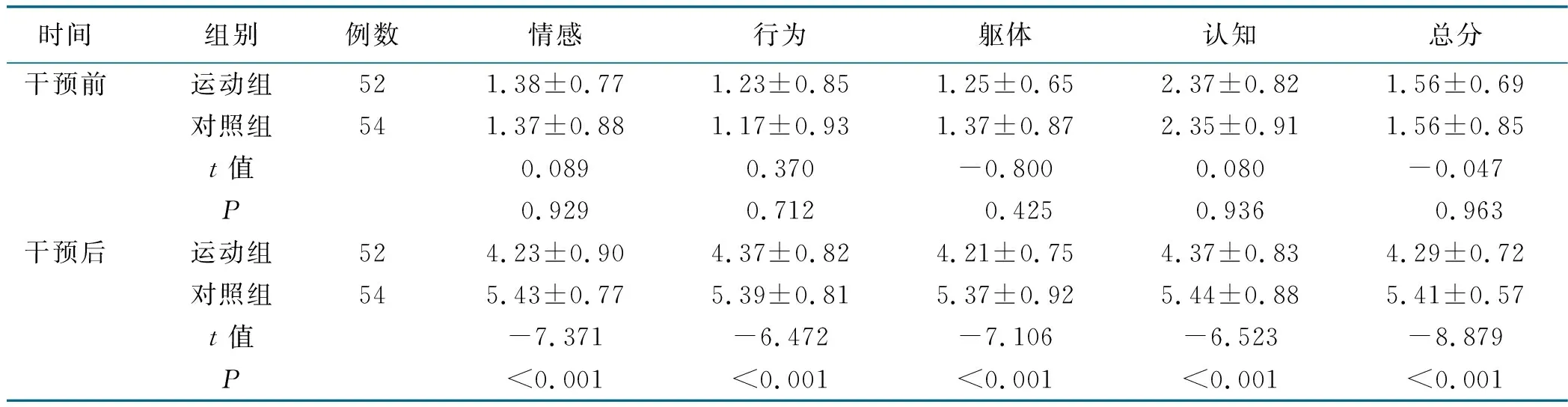
表2 两组病人干预前后PFS-R得分比较 单位:分
2.2 生活质量(见表3)

表3 两组病人干预前后FACT-G得分比较 单位:分
3 讨论
我国是食管癌好发国家,每年新发的病例占全世界50%左右。根治性手术是食管癌治疗的首选方式,然而80%的食管癌病人初诊时无法行手术治疗[9]。当前放疗技术迅速发展,包括三维适形放疗、调强放疗及图像引导技术的广泛应用,使肿瘤的局部控制率明显提升。化疗不仅可增强放射野内肿瘤的局部控制,还可抑制全身微小肿瘤病灶。同步放化疗可提高食管癌的临床疗效,延长病人的生存期[10]。但61%~100%的癌症病人在放化疗期间有不同程度的疲乏,25%病人即使在放化疗结束后癌因性疲乏仍持续数年,并导致难以重返工作,严重影响病人的生活质量。癌因性疲乏在癌症病人中普遍存在,尤其是化疗病人。原因可能为:一方面,恶性肿瘤给病人造成巨大心理恐慌和压力,病人进而出现情绪低落、睡眠障碍及疲乏症状。另一方面.肿瘤的慢性消耗对体能造成伤害;化疗在杀伤肿瘤细胞的同时,也对人体产生一系列的毒副作用,如食欲减退、恶心、呕吐、骨髓抑制,进而加重疲乏。过去临床医生最开始建议癌症病人应注意休息并且尽量避免运动,然而长时间的休息和睡眠并不能缓解癌因性疲乏,反而加重其程度,增强病人的不适感。越来越多的人将运动应用到临床癌症护理中。本研究有氧运动方式为快走、慢跑、上下楼梯,安全有效、经济方便,室内外均可进行,适合各个年龄段病人。选用弹力带进行抗阻运动,弹力带具有易于携带,对场地要求低,可随时随地进行训练的特点。目前,尚未有明确的药物改善癌因性疲乏症状,美国肿瘤护理学会推荐运动锻炼是改善癌因性疲乏的有效措施。本研究表明中等强度的有氧运动结合抗阻运动可以缓解癌因性疲乏,保持病人身体机能及改善病人的精神状态,与国外的研究结果[11-12]一致。考虑原因主要为:①运动后全身血液循环加速,促进新陈代谢,肌肉的能量及供氧得到改善,肌肉及体能得到增强。②癌症病人常伴随抑郁、焦虑等不良情绪,表现为兴趣索然、无精打采、脑力及体力不足及不愿活动等,运动可以显著减轻癌症病人的抑郁症状[12]。③内啡肽也被称之为“快感荷尔蒙”或者“年轻荷尔蒙”,运动可刺激垂体腺分泌β-内啡肽,在其激发下,人的身心处于轻松愉悦的状态中,增强机体对刺激的耐受力。④运动时机体神经系统产生微电刺激,调节大脑神经递质和应激激素的分泌,可缓解肌肉紧张和病人精神抑郁[13]。当前医疗服务模式从传统生物医学模式(以疾病为中心),逐步向“以病人为中心”的新模式转变,病人不仅要求肿瘤的控制,更是需要躯体、心理和社会适应方面的完好状态。本研究中,运动可提高食管癌同步放化疗病人的生活质量。运动增强病人的免疫功能,改善病人焦虑、抑郁、失眠等症状,提高病人的支持感、归属感及自我效能,进而对生活保持更加乐观的心态。
4 小结
综上所述,对食管癌同步放化疗病人进行为期8周的运动干预可以减轻病人癌因性疲乏,提高病人生活质量。
