儿茶素与咖啡碱络合物的晶体学研究
2021-02-06董燕茹曹妍彦卢佳纯梅思凡河润陈萍
董燕茹,曹妍彦,卢佳纯,梅思凡,河润,陈萍
儿茶素与咖啡碱络合物的晶体学研究
董燕茹,曹妍彦,卢佳纯,梅思凡,河润,陈萍*
浙江大学茶叶研究所,浙江 杭州 310058
通过高效液相色谱分析发现儿茶素和咖啡碱占绿茶乳酪总质量的88%以上。以乳酪中含量最高的两种酯型儿茶素和对应的非酯型儿茶素与咖啡碱络合建立绿茶乳酪简化体系CATs-CAF,发现4种儿茶素在沉淀中的分布比例为EC∶ECG∶EGC∶EGCG≈1∶2∶1∶2。选用ECG和EC分别与咖啡碱络合制备单晶,扫描电镜观察络合前后晶体的显微形貌,X-射线单晶衍射分析立体化学结构。结果表明,两种络合物晶体均为针状,通过分子间氢键和面对面π-π堆积作用形成。其中,EC可与相邻EC、CAF分子形成O-H...O型氢键,通过A环和CAF的六元环发生π-π堆积,形成1∶1络合物;而ECG可与相邻ECG、CAF分子形成O-H...O型氢键以及O-H...N型氢键,并且所有芳香环均能与CAF发生π-π堆积,形成2∶4络合物,每个ECG的A环、B环可分别与相邻两个ECG的B环、A环共用CAF的六元环,而ECG的D环和CAF的六元环则通过两种排列方式在a轴上延伸。
茶乳酪;络合机理;扫描电镜;X-射线单晶衍射
茶汤在冷却后变浑浊的现象被称为“冷后浑”,其中的悬浮或沉淀物质被称为“茶乳酪”。1944年,Bradfield等首先提出了茶乳酪与茶汤品质之间的关系,引起了广泛关注[1]。目前关于茶乳酪的研究主要包括沉淀的物质组成、沉淀形成的影响因素和少量机理研究。
茶乳酪由咖啡碱、茶多酚、蛋白质、多糖、含氮化合物、类黄酮以及矿物质等物质组成[2-8],不同的化学组分参与沉淀形成的能力和贡献度有所不同,而咖啡碱和茶多酚对茶乳酪的形成贡献最大[9]。Roberts[2]首次分析了红茶乳酪的主要化学组成为茶黄素、茶红素和咖啡碱,而Penders等[10-11]的研究也表明咖啡碱和儿茶素及其氧化物对红茶茶汤的茶乳酪形成具有重要作用。Yin等[4]研究表明,绿茶乳酪中儿茶素类占总质量的12.80%~42.50%,主要为表没食子儿茶素(EGC)、表没食子儿茶素没食子酸酯(EGCG)、表儿茶素(EC)和表儿茶素没食子酸酯(ECG)。Xu等[5]基于咖啡碱与酯型儿茶素的含量,对茶汤沉淀量进行了公式预测。
茶乳酪的形成受诸多因素影响,包括茶树品种[12]、原料嫩度[5]、原料发酵程度[9]、加工[13]与提取工艺[14-15]等。不同茶类的生化基质差异较大[16],冲泡后茶汤沉淀的形成量、化学组分以及粒径大小等也有所不同[9]。绿茶乳酪的粒径明显比红茶乳酪大,且两者的化学组成完全不同[17],其形成机理可能也有所差别。对红茶乳酪的研究显示,咖啡碱可通过氢键和π-π堆积相互作用与茶黄素形成2∶1络合物[18],蛋白中的氨基酸分子也可通过氢键和疏水作用力与多酚类物质络合[19]。
然而,目前关于绿茶乳酪形成机理的研究相对较少,尤其缺乏微观层面的立体化学结构解析。X射线衍射分析技术是现代物质微观结构无损分析、鉴定和研究的基本手段,也是目前研究原子在三维空间分布的最精确手段。其中X射线单晶衍射技术对于物质微观结构新理论的构建具有独特优越性,在材料学、物理学、化学、生物学等领域应用广泛[20],但在茶叶领域中的应用鲜有报道,可能会对探明绿茶乳酪形成机制有所帮助。
因此,本研究通过高效液相色谱结合扫描电镜和X射线单晶衍射手段,构建绿茶乳酪的简化体系,对绿茶乳酪中儿茶素类物质和咖啡碱的络合机理进行深入探究,为绿茶乳酪的形成机制研究提供参考依据。
1 材料与方法
1.1 试验材料与试剂
绿茶(惠明茶),购自浙江六江源绿色食品有限公司。
儿茶素标准品:儿茶素(C)、EC、没食子儿茶素(GC)、EGC、儿茶素没食子酸酯(CG)、ECG、没食子儿茶素没食子酸酯(GCG)、EGCG;生物碱标准品:咖啡碱(CAF)、可可碱(TB)、茶碱(TP);没食子酸(GA),均购自上海源叶生物科技有限公司(HPLC≥98%)。Bradford蛋白浓度测定试剂盒,购自碧云天生物技术有限公司。本试验所用到的甲醇、甲酸、乙腈、乙酸均为色谱级,购自德国Sigma-Aldrich公司。
1.2 主要仪器设备
Prominence LC-20A型高效液相色谱仪(日本Shimadzu公司/日本岛津公司),Synergy UV水过滤系统(法国默克公司),SIGMA-3K15型离心机(德国西格玛公司),Agilent5 TC-C18分离柱(美国安捷伦科技有限公司),HWS28恒温水浴锅(上海一恒科学仪器有限公司),LE104E型电子天平(梅特勒-托利多仪器上海有限公司),SU8010高分辨冷场发射扫描电子显微镜(日本日立公司),APEXII型X射线晶体分析仪(德国布鲁克AXS有限公司),Synergy H1全功能酶标仪(美国伯腾仪器有限公司),CHRIST冻干机(德国格马有限责任公司)。
1.3 样品处理
称取25 g绿茶茶样于500 mL锥形瓶中,加入300 mL沸水,移入沸水浴中浸提30 min,浸提完毕趁热减压过滤,冷却后以9 600 r·min-1离心25 min,分离上清液定容至300 mL,于4℃冰箱中冷藏诱导沉淀,2 d后离心(9 600 r·min-1,4℃,25 min)分离得到茶乳酪,作为待测样品。
1.4 绿茶乳酪物质组成的测定
总质量测定:将绿茶乳酪样品于–40℃下真空冷冻干燥后称重。
蛋白质质量的测定:建立蛋白标准曲线,用考马斯亮蓝G-250比色法[21],测定绿茶乳酪中蛋白质的质量。
没食子酸、儿茶素以及生物碱的测定:采用高效液相色谱(HPLC)检测法对GA、8种儿茶素、3种生物碱进行测定,用12种物质的标准品进行外标法定量。检测条件:Agilent TC-C18色谱柱(4.6 mm×250 mm,5 μm);流动相A为乙腈∶乙酸∶水=6∶1∶193,流动相B为乙腈∶乙酸∶水=60∶1∶139。45 min梯度洗脱,B相初始浓度20%,35 min上升至65%,而后降至20%;流速1 mL·min-1;检测波长280 nm;柱温设置25℃;进样量10 μL。
1.5 绿茶乳酪简化体系(CATs-CAF)的建立
将4种儿茶素单体(EC、ECG、EGC、EGCG各0.10 mmol)混合物(CATs)和咖啡碱(0.40 mmol)在100℃下溶于2 mL超纯水中,室温下静置48 h,分离得到上清液和粘性沉淀物。粘性沉淀物溶解于甲醇溶剂中,使用HPLC检测法(同1.4章节)分别测定体系中上清液和沉淀的物质组成及含量。
1.6 络合物晶体的制备
选用一对酯型和非酯型儿茶素(ECG和EC),分别与CAF以1∶1的摩尔比溶于超纯水中,100℃水浴30 min后,室温下静置缓慢结晶,得到ECG-CAF和EC-CAF络合物晶体。
1.7 络合物晶体的扫描电镜观察
取适量制备好的络合物晶体以及EC、ECG和CAF单体,分别在25℃下真空干燥12 h。取真空干燥后的样品,均匀涂抹在双面碳导电胶带上,将涂好的样品放置于HITACHI MC1000离子喷镀仪进行离子喷镀,喷镀完成后用扫描电镜(SU8010)观察形貌。仪器参数设置:加速电压ETH=3 kV,分辨率1.0 nm/15 kV,工作距离WD=9 mm,冷场发射型检测器,探测器Signal A=SE2,分析级SDD探头分辨率Mn K=129 eV。
1.8 络合物晶体的结构测定
选取大小合适的络合物晶体,在Bruker APEX-II CCD衍射仪上进行衍射实验:EC-CAF用Ga K射线(=1.341 39 nm),扫描方式,在2.98°≤≤55.00°的范围内收集独立衍射点;ECG-CAF用Cu K射线(=1.541 78 nm),扫描方式,在3.50°≤≤72.20°的范围内收集独立衍射点。EC-CAF采用的权重方案分别为=[2(o2)+(0.083 9)2]-1和=(o2+2c2)/3,ECG-CAF采用的权重方案分别为=[2(o2)+(0.137 3)2+1.558 2]-1和=(o2+2c2)/3。络合物的晶体学参数列于表1。
1.9 数据分析
所有试验数据以平均值表示,3次重复,统计分析采用GraphPad Prism 8软件处理,采用多重检验进行分析,<0.05表示有统计学意义。利用Mercury和Diamond软件分析晶体结构和作用力。
2 结果与分析
2.1 绿茶乳酪的物质组成
本研究中,25.0 g绿茶茶样冲泡的茶汤通过低温诱导沉淀后得到绿茶乳酪总质量为0.284 0 g。用Bradford比色法测得绿茶乳酪中蛋白质的质量为0.031 7 g,占绿茶乳酪样品总质量的11.16%;用HPLC检测法得到8种主要儿茶素总量和咖啡碱的质量分别为0.194 8 mg和0.055 7 mg,在绿茶乳酪中的占比为68.59%和19.61%(图1-A)。发现儿茶素类和咖啡碱占绿茶乳酪总质量的88%以上,是绿茶冷后浑的主要成分。比较绿茶乳酪中主要儿茶素的含量,发现酯型儿茶素的含量更高,其中EGCG和ECG占儿茶素总质量的3/4以上(图1-B)。
2.2 绿茶乳酪简化体系的组成
选取绿茶乳酪中具有代表性的酯型和非酯型儿茶素,与咖啡碱建立简化体系CATs-CAF,研究体系中上清液和沉淀的物质分布及含量,结果如表2所示。在参与反应的咖啡碱足量情况下,4种等摩尔比儿茶素(EC、ECG、EGC、EGCG)在沉淀中的分配比例约为1∶2∶1∶2。可以看出,简单儿茶素与酯型儿茶素的分配比例约为1∶2,而结构相近的儿茶素络合参与度大致相同。

表1 晶体学数据和结构参数
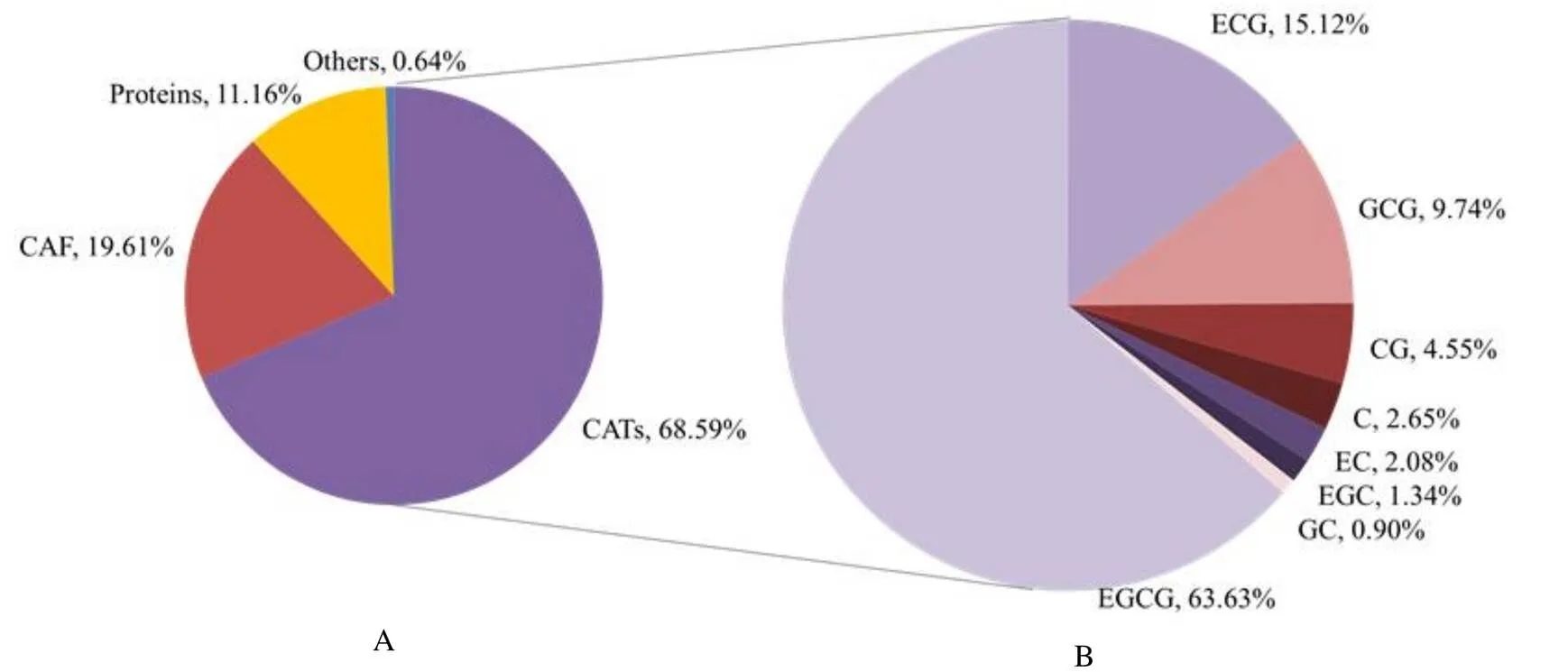
图1 绿茶乳酪中各物质含量
2.3 络合物晶体的扫描电镜结构
分别在放大500倍和5 000倍下观察晶体的显微形貌及颗粒大小,发现晶体呈不规则分布。CAF晶体呈针状且表面光滑,颗粒大小不均(直径0.5~10 μm)。EC晶体呈无定形块状且表面粗糙,ECG晶体呈针状且表面光滑。EC和ECG分别与CAF络合形成的晶体(EC-CAF、ECG-CAF)均为针状且表面光滑(图2)。
2.4 络合物晶体的立体化学结构
通过X射线晶体学手段,进一步研究络合物晶体的立体化学结构。
试验结果表明,EC和CAF以1∶1络合,结晶于单斜晶系2空间群,形成针状晶体EC-CAF。单个晶粒尺寸为0.1 mm×0.008 mm×0.006 mm,其晶胞尺寸为a=27.241 3(6) Å,b=6.665 8(2) Å,c=17.340 7(4) Å。1个晶胞包含4个EC-CAF络合单元,每个络合单元中,EC的A环和CAF的六元环面对面(图3)。
进一步分析分子之间的作用力,发现络合物结构通过氢键和π-π堆积相互作用维持(图4)。EC可与相邻的EC和CAF形成O-H...O型氢键;通过EC分子中A环与CAF的六元环之间形成的面对面π-π堆积相互作用,络合单元在与b轴相同的方向上平行堆叠。每个EC分子平均结合1个CAF分子,因此EC-CAF的络合比例为1∶1。
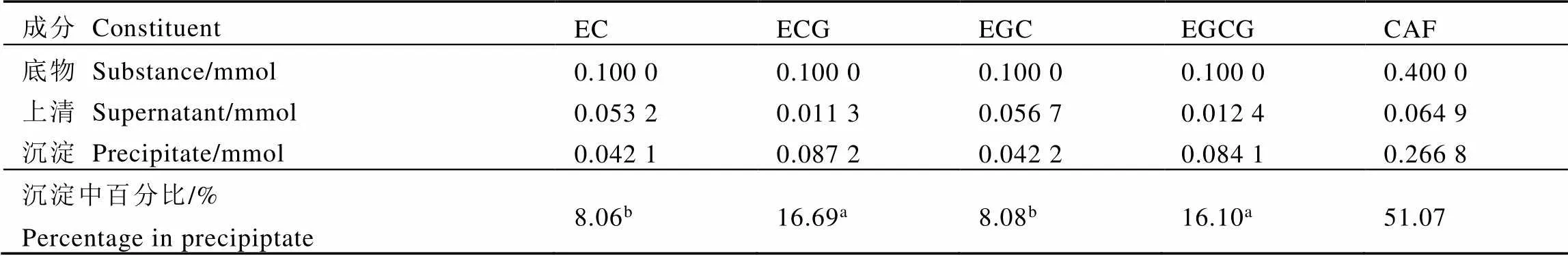
表2 CATs-CAF中上清液和沉淀的物质分布及含量
注:表中数据为3个重复平均值,同一行标注字母不同者差异显著(<0.05)
Note: Each value was the mean of three replicates. Different letters within a column indicate a significantly different (<0.05)

图2 扫描电镜(SEM)下的晶体形貌
ECG和CAF以2∶4络合,结晶于单斜晶系P21空间群,形成针状晶体ECG-CAF。单个晶粒尺寸为0.28 mm×0.19 mm×0.14 mm,其晶胞尺寸为a=13.980 7(7) Å,b=8.978 3(4) Å和c=31.836 4(16) Å。一个晶胞包含两个不完全对称的ECG-CAF络合单元Ⅰ和Ⅱ,以及12个作为晶体溶剂的水分子,每个络合单元中,ECG的D环和CAF的六元环交替出现,但Ⅰ中存在明显错位(图5)。ECG的D环与CAF的六元环沿a轴方向依次排列(图6);ECG的A环和B环分别与CAF的六元环相对,沿c轴方向延伸(图7-B)。
进一步分析分子之间的作用力,发现络合物结构通过氢键和π-π堆积相互作用维持(图8)。ECG可与相邻的ECG和CAF形成O-H...O型及O-H...N型氢键;ECG的A环,B环和D环均与相邻CAF的六元环产生面对面π-π堆积相互作用。
在a轴方向上,D环和CAF存在左右交错和上下交叠两种排列方式,这两种排列方式沿c轴依次出现,每个ECG的D环平均可与1个CAF的六元环配对(图6)。

注:A:EC-CAF晶胞;B:EC-CAF层结构

注:虚线表示氢键,双箭头表示面对面的π-π堆积相互作用
3 讨论
关于绿茶乳酪的化学组成,大量研究表明茶多酚和咖啡碱是绿茶乳酪的重要组分[4-5,8-9],其中茶多酚占绿茶乳酪总质量的78.66%,儿茶素类是多酚参与乳酪形成的主体成分[4],咖啡碱和儿茶素(尤其是酯型儿茶素)是决定绿茶乳酪形成的关键化学组分[5,8]。本研究中,儿茶素和咖啡碱为绿茶乳酪的主要组成物质,占乳酪总质量的88%以上,是绿茶“冷后浑”形成的关键化学成分,其中,酯型儿茶素更容易参与绿茶乳酪的形成,与前人的研究结果一致。而绿茶乳酪简化体系CATs-CAF试验则进一步表明,简单儿茶素与对应结构的酯型儿茶素在乳酪沉淀中的分配比例约为1∶2,说明不同儿茶素的结构差异可能对茶乳酪的形成有较大影响。

注:A:ECG-CAF晶胞;B:晶胞a轴方向俯视图
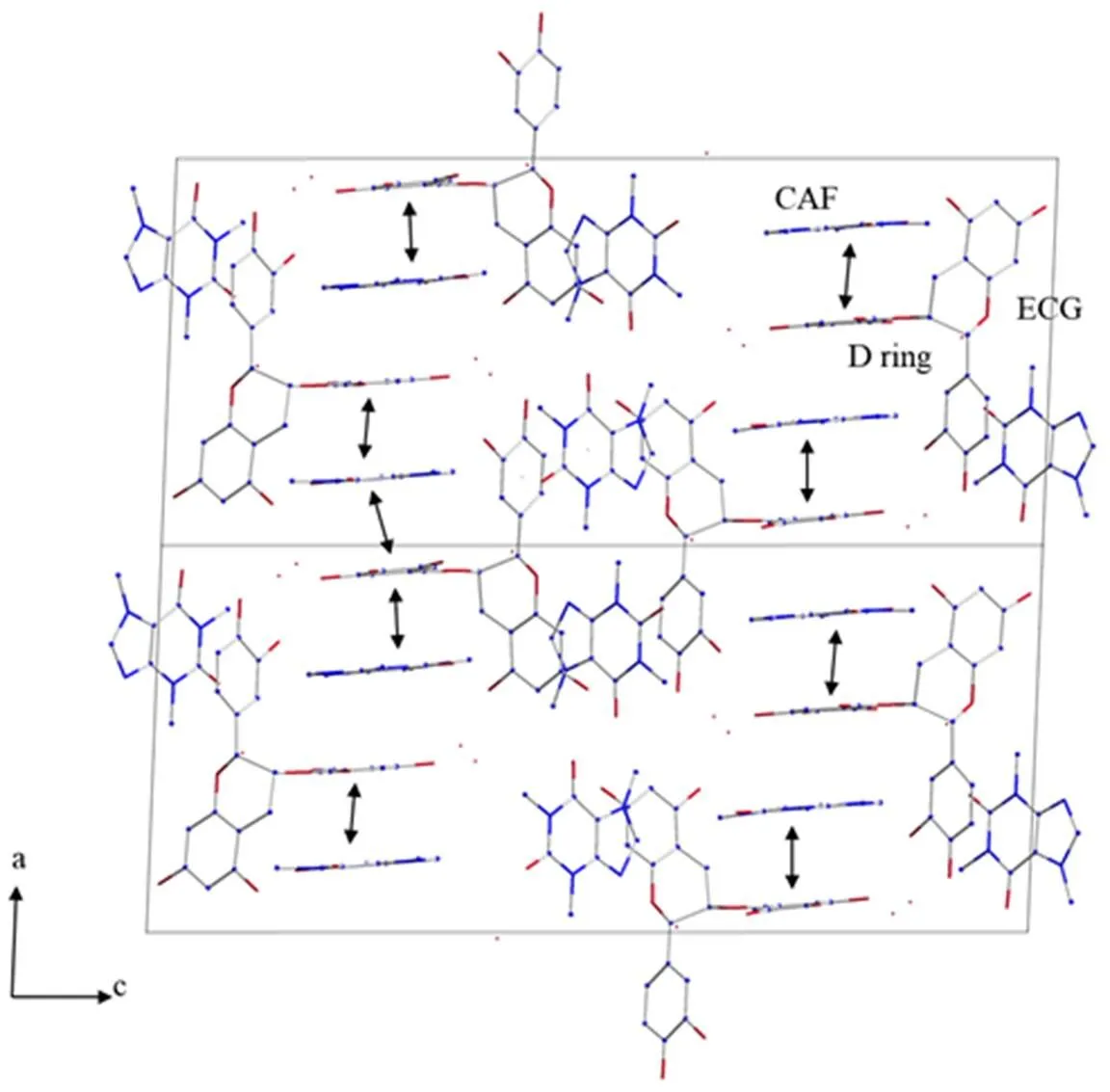
注:双箭头表示面对面的π-π堆积相互作用

注:A:ECG和CAF之间的π-π堆积相互作用;B:BC平面俯视图

注:虚线表示氢键,双箭头表示面对面的π-π堆积相互作用
本试验中,儿茶素与咖啡碱络合形成白色针状单晶EC-CAF和ECG-CAF。结合X-射线单晶衍射手段对晶体的立体化学结构进行解析,发现EC-CAF,ECG-CAF均通过分子间氢键和面对面π-π堆积作用络合,但非酯型儿茶素EC和酯型儿茶素ECG与CAF的作用部位有所差异:EC可与相邻的EC、CAF分子形成O-H...O型氢键,面对面π-π堆积作用仅发生在EC的A环与CAF的六元环之间,形成1∶1络合物EC-CAF;而ECG可与相邻的ECG、CAF分子形成O-H...O以及O-H...N型氢键,且ECG的所有芳香环都能与CAF的六元环互作,形成2∶4络合物ECG-CAF,这与Sato等[22]的研究结果相似。
此外,我们还发现ECG的D环和CAF的六元环在a轴方向上并非简单的依次排列,而是存在左右交错和上下交叠两种排列方式,这两种排列方式沿c轴交替出现;ECG的A环、B环分别与相邻ECG的B环和另一个ECG的A环在BC平面共用不同CAF的六元环;平均每个ECG的D环可与1个CAF配对,A环或B环分别络合1/2个CAF,即1个ECG分子能结合2个CAF分子,再根据其最小重复单元得出ECG-CAF的络合比例为2∶4。
本研究分析了绿茶乳酪简化体系CATs-CAF的宏观分配比例及微观结构特性。发现EC和ECG均与CAF形成氢键和面对面π-π堆积作用,并可以在一定方向上堆叠晶胞;EC-CAF和ECG-CAF的络合比例分别为1∶1和2∶4,这与CATs-CAF中EC∶ECG≈1∶2的结果相对应,进一步揭示了ECG相对于EC更容易和咖啡碱进行络合的机理,为探明绿茶冷后浑的形成机制提供一定的理论基础。
[1] 阎守和, 金盾. 茶多酚-生物碱的聚沉与转溶[J]. 北京大学学报(自然科学版), 1982(2): 55-61. Yan S H, Jin D. Tea polyphenol-alkaloids coagulation and dissolution [J]. Journal of Peking University (Natural Science Edition), 1982(2): 55-61.
[2] Roberts E A H. Phenolic substances of manufactured tea. Ⅹ. creaming down of tea liquors [J]. Journal of the Science of Food and Agriculture, 1963, 14(10): 700-705.
[3] Smith R F. Studies on formation and composition of cream in tea infusions [J]. Journal of the Science of Food and Agriculture, 1968, 19(9): 530-534.
[4] Yin J F, Xu Y Q, Yuan H B, et al. Cream formation and main chemical components of green tea infusions processed from different parts of new shoots [J]. Food Chemistry, 2009, 114(2): 665-670.
[5] Xu Y Q, Chen S Q, Shen D Y, et al. Effects of chemical components on the amount of green tea cream [J]. Agricultural Sciences in China, 2011, 10(6): 969-974.
[6] Xu Y Q, Chen G S, Du Q Z, et al. Sediments in concentrated green tea during low-temperature storage [J]. Food Chemistry, 2014, 149: 137-143.
[7] Lin X R, Gao X, Chen Z Z, et al. Spontaneously assembled nano-aggregates in clear green tea infusions fromand[J]. Journal of Agricultural and Food Chemistry, 2017, 65(18): 3757-3766.
[8] Chen X Q, Du Y, Wu L, et al. Effects of tea-polysaccharide conjugates and metal ions on precipitate formation by epigallocatechin gallate and caffeine, the key components of green tea infusion [J]. Journal of Agricultural and Food Chemistry, 2019, 67(13): 3744-3751.
[9] Liang Y R, Lu J L, Zhang L Y. Comparative study of cream in infusions of black tea and green tea [(L.) O. Kuntze] [J]. International Journal of Food Science and Technology, 2002, 37(6): 627-634.
[10] Penders M, Scollard D, Needham D, et al. Some molecular and colloidal aspects of tea cream formation [J]. Food Hydrocolloids, 1998, 12(4): 443-450.
[11] Penders M, Jones D P, Needham D, et al. Mechanistic study of equilibrium and kinetic behaviour of tea cream formation [J]. Food Hydrocolloids, 1998, 12(1): 9-15.
[12] 张凌云. 不同茶树品种绿茶饮料适制性研究[D]. 杭州: 浙江大学, 2004. Zhang L Y. Study on processing property of different tea cultivars for green tea drinks [D]. Hangzhou: Zhejiang University, 2004.
[13] 尹军峰, 林智, 谭俊峰, 等. 绿茶初制工艺对饮料加工特性的影响[J]. 茶叶科学, 2005, 25(3): 189-196. Yin J F, Lin Z, Tan J F, et al. Effect of raw material processing technology on processing characteristic of the green tea beverage [J]. Journal of Tea Science, 2005, 25(3): 189-196.
[14] Chao Y C, Chiang B H. Cream formation in a semifermented tea [J]. Journal of the Science of Food and Agriculture, 1999, 79(13): 1767-1774.
[15] Chandini S K, Rao L J, Subramanian R. Influence of extraction conditions on polyphenols content and cream constituents in black tea extracts [J]. International Journal of Food Science and Technology, 2011, 46(4): 879-886.
[16] 张燕忠,张凌云. 原料发酵程度及生化基质对茶饮料冷后浑稳定性的影响[J]. 茶叶科学, 2010, 30(s1): 533-543. Zhang Y Z, Zhang L Y. Effect of raw tea’s fermentation degree and biochemical substrates on tea cream stability of tea drink [J]. Journal of Tea Science, 2010, 30(s1): 533-543.
[17] Lin X R, Chen Z Z, Zhang Y Y, et al. Comparative characterisation of green tea and black tea cream: Physicochemical and Phytochemical Nature [J]. Food Chemistry, 2015, 173: 432-440.
[18] Charlton A J, Davis A L, Jones D P, et al. The self-association of the black tea polyphenol theaflavin and its complexation with caffeine [J]. Journal of the Chemical Society, 2000(2): 317-322.
[19] 陆建良. 茶汤蛋白对茶饮料冷后浑形成的影响[D]. 杭州: 浙江大学, 2008. Lu J L. Effects of proteins on haze formation of ready-to-drink tea [D]. Hangzhou: Zhejiang University, 2008.
[20] 解其云, 吴小山. X射线衍射进展简介[J]. 物理, 2012, 41(11): 727-735. Xie Q Y, Wu X S. The development of X-ray diffraction [J]. Physics, 2012, 41(11): 727-735.
[21] Bradford M M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding [J]. Analytical Biochemistry, 1972, 72: 248-254.
[22] Sato T, Kinoshita Y, Tsutsumi H, et al. Characterization of creaming precipitate of tea catechins and caffeine in aqueous solution [J]. Chemical and Pharmaceutical Bulletin, 2012, 60(9): 1182-1187.
Crystallographic Study on the Complex of Catechins and Caffeine
DONG Yanru, CAO Yanyan, LU Jiachun, MEI Sifan, HE Run, CHEN Ping*
Tea Research Institute, Zhejiang University, Hangzhou 310058, China
Through HPLC analysis, it was found that catechins and caffeine accounted for more than 88% of the total mass of green tea cream. The CATs-CAF, a simplified green tea cream system, was established by two ester catechins that with the highest content in green tea cream, and their corresponding non-ester catechins complexed with caffeine. The distribution ratio of 4 catechins in precipitate was that EC∶ECG∶EGC∶EGCG≈1∶2∶1∶2. Single crystals were prepared by complexing ECG and EC respectively with caffeine and observed under scanning electron microscopy to record their micro-morphology before and after complexation. Using X-ray single-crystal diffraction to analyze the stereochemical structure, the results show that two needle crystals were formed by intermolecular hydrogen bonding and face-to-face π-π stacking. EC formed O-H...O type hydrogen bonds with adjacent EC and CAF molecules, and π-π stacking occurred between the A ring of EC and the six-membered ring of CAF to form a 1∶1 complex of EC-CAF. While the ECG could form O-H...O and O-H...N type hydrogen bonds with adjacent ECG and CAF molecules, and the π-π stacking of ECG-CAF occurred among all aromatic rings to form a 2∶4 complex, in which the ring A and B of each ECG shared the six-membered ring of CAF separately with the ring B and A of the adjacent ECGs, while the D ring of ECG and the six-membered ring of CAF extended on the a axis in two arrangements.
tea cream, complexation mechanism, scanning electron microscope, X-ray single crystal diffraction
S571.1;O723+.6
A
1000-369X(2021)01-080-10
2020-05-06
2020-07-21
董燕茹,女,硕士研究生,主要从事制茶工程与品质鉴定研究,21716063@zju.edu.cn。*通信作者:pingchen@zju.edu.cn
(责任编辑:赵锋)
