硼高效掺杂LiNi0.5Co0.2Mn0.3O2正极材料及其性能提升机制
2021-01-30朱华威余海峰江仟仟杨兆峰江浩李春忠
朱华威,余海峰,江仟仟,杨兆峰,江浩,李春忠
(华东理工大学超细材料制备与应用教育部重点实验室,上海200237)
引 言
发展高性能锂离子电池是解决电动汽车“里程焦虑”问题的重要途径之一,而相比于目前市场常用的石墨负极,正极材料比容量较低,是限制锂离子电池能量密度提升的关键[1-2]。相比于磷酸铁锂、钴酸锂、锰酸锂等正极材料,层状三元正极LiNi0.5Co0.2Mn0.3O2(NCM)中Ni、Co、Mn 三种元素的协同作用使其兼具高比容量、长寿命和安全等优势,成为目前最受欢迎的正极材料之一[3]。近年来,为了进一步提升其能量密度,研究人员倾向于将NCM的工作电压拓宽至4.5 V[4-5]。然而,在高工作电位下更多锂离子从材料内部的脱出会加剧层状结构向电化学惰性的尖晶石甚至盐岩相转变,造成比电容量和电压平台的快速衰减[6]。与此同时,在充电过程中材料表面产生的Ni4+会加剧电极-电解液界面处的副反应,形成更厚的钝化层,从而影响电极材料的动力学行为[7-8]。因此,在提高NCM 正极材料工作电压的同时保持较长的循环寿命和良好的功率密度仍然是一个挑战。
表面包覆是改善层状正极材料电化学性能的有效策略之一[9-14]。然而,单一的表面包覆难以从根源上稳定材料的晶体结构。实验和理论计算表明杂原子掺杂(Ce,Mo,V,Ti 等)可以显著提高材料晶体结构稳定性[15-18]。例如,Wu 等[15]通过物理混合和一步锻烧将Ce3+引入LiNi0.8Co0.1Mn0.1O2中,煅烧过程中强氧化性的Ce4+可以有效减少Li/Ni 混排,同时引入的高键能Ce3+—O 键可以有效稳定层状晶体结构,因此该材料在循环100 圈后容量保持率提高至86.9%。值得注意地是,类似这种高键能异质元素的掺杂量通常非常有限,易吸附在表面或者自成核,从而限制了电化学性能的进一步提高[19-20]。因此,开发一种简单高效的异质元素掺杂策略对于改善高压NCM正极材料电化学性能非常有意义。
本文利用含硼前体在颗粒表面富集及后续高温煅烧过程中硼离子的扩散强化,制备了硼高效掺杂的NCM 正极材料(NCM-B)。基于正极材料表面含硼前体与本体材料之间巨大的B3+浓度差,通过高温煅烧过程强化B3+在NCM 正极材料中的体相扩散,实现了硼离子的梯度掺杂。高键能B—O 键的引入抑制了电化学过程中晶格氧析出;表面残余的Li2O-B2O3是锂离子导体,且可以稳固电极-电解液界面。因此,在3.0~4.5 V 电压区间,改性后NCM-B正极材料在10 C 的大电流密度下,比电容量提升了41.8 mA·h·g-1。1 C 下经过100 圈循环后比电容量是初始容量的90%,远高于未改性的正极材料(73%)。
1 实验部分
1.1 材料制备
首先,将5.0 g 的商用LiNi0.5Co0.2Mn0.3O2正极材料加入装有100 ml 去离子水的烧杯中,搅拌至溶液混合均匀,接着称取0.1 g 的硼酸慢慢加入,然后将烧杯放在80℃恒温热台上低速持续搅拌,直到溶液完全挥发。将所得到的混合物放入玛瑙研磨罐研磨均匀,并置于纯氧环境中煅烧,在500℃恒温6 h 后,继续升温到900℃保持4 h,其中升降温速率均为5℃·min-1。
1.2 材料表征
采用日本Rigaku 公司的X 射线衍射仪(D/max 2550 VB/PC 型)分析样品的晶体结构,日立公司的Gemini SEM 500场发射扫面电子显微镜和日本电子公司的JEOL-2100F 透射电子显微镜被用来表征样品形貌。将粉末样品压制成片状,采用辐射源为Al Kα,能量为2 keV 的Ar 等离子体对其进行不同深度刻蚀,测试光斑面积为400 μm,刻蚀区域为2.5 μm×2.5 μm,单次刻蚀时间为100 s,共刻蚀3 次。随后,采用X 射线光电子能谱(XPS: AXIS Ultra DLD)对样品的化学组成和化合价态进行分析。
1.3 电化学性能测试
将活性电极材料、导电碳黑(Super-P)和黏结剂聚偏氟乙烯(PVDF)按8∶1∶1 的质量比混合均匀,用N-甲基吡咯烷酮(NMP)制成浆料后均匀涂覆于铝箔上,120°C 真空干燥10 h 后将烘干的铝箔冲压成直径为12 mm 的圆形极片,活性材料的面负载量为1.5~2.0 mg·cm-2。采用直径为16 mm 的纯锂片为负极,1 mol·L-1的LiPF6(VEC∶VEMC=3∶7)为电解液,单电池电解液量为200 μl,隔膜选用直径为18 mm 的聚丙烯膜(Celgard 2400),在充满氩气的手套箱内(O2<0.00001%,H2O<0.00001%)组装成CR2016 型扣式电池。 采用LAND 电池测试系统(LANDCT2001C)对组装的扣式半电池进行恒电流充放电测试;采用电化学工作站(AUTOLAB PGSTAT302N)对电池进行循环伏安测试,电压区间选用3.0~4.5 V。

图1 NCM-B的制备示意图(a);NCM的SEM图(b)和TEM图[(c),(d)];B-coated NCM 的SEM图(e)和TEM图[(f),(g)];NCM-B的SEM图(h)和TEM图[(i),(j)];NCM-B的不同刻蚀深度的XPS总谱图(k),O 1s谱图(l)和B 1s谱图(m)Fig.1 Schematic illustration for the preparation of NCM-B(a);SEM(b),and TEM[(c),(d)]images of the NCM;SEM(e)and TEM[(f),(g)]images of the B-coated NCM;SEM(h)and TEM[(i),(j)]images of the NCM-B;XPS survey spectra(k),O 1s(l)and B 1s(m)XPS spectra of the NCM-B with different etching depth
2 结果与讨论
图1 显示了NCM-B 材料的制备与形貌结构。NCM-B 正极材料的制备过程如图1(a)所示。先将NCM 与硼酸在液相中均匀混合并干燥得到两者的混合物粉末,随后借助低温熔融过程辅助含硼化合物均匀沉积在NCM 正极材料表面,最后基于正极材料表面含硼前体与本体材料之间巨大的B3+浓度差,通过高温煅烧过程强化B3+在NCM 正极材料中的体相扩散,实现了硼离子梯度掺杂NCM-B 正极材料的制备。图1(b)、(e)、(h)分别是NCM,B-coated NCM和NCM-B 的扫描电镜图,对比发现改性过后NCMB 仍然保持颗粒紧密团聚形成的球形,说明改性并没有破坏材料的基础形貌。NCM,B-coated NCM 和NCM-B 正极材料的高倍TEM 图如图1(d)、(g)、(j)所示,可以明显观察到NCM 和NCM-B 材料内部具有完整的晶面间距为0.47 nm 的晶格条纹,这对应于NCM(003)晶面;B-coated NCM 材料内部具有完整的晶面间距为0.24 nm 的晶格条纹,这对应于NCM(101)晶面。此外,其良好的晶格条纹说明硼离子掺杂并没有破坏NCM 的晶体结构[21]。在500℃下得到的中间产物(B-coated NCM)的外表面可以观察到一层均匀的约10 nm 厚度的无定形包覆层,同时在NCM-B 正极材料外表面观察到一层均匀的2~3 nm厚度的无定形包覆层,推测对应于表面残留的Li2OB2O3化合物[22]。材料表面包覆层厚度的减少表明表面富集和扩散强化的策略可以实现高键能离子的高效掺杂。采用不同深度刻蚀的XPS 对材料表面和体相元素的价态以及含量进行分析,如图1(k)~(m)所示。通过O 1s精细谱和B 1s精细谱,可以明显看到材料表面的吸附氧和B 的含量远高于材料内部,进一步佐证材料表面存在Li2O-B2O3无定形包覆层。同时,随着刻蚀深度增加至20、40、70 nm,仍然可以明显观察到B 的特征峰,而且硼离子含量从5.32%(mol)逐渐降低至2.41%(mol),表明硼离子梯度掺杂在NCM 内部中。因此,通过TEM 和XPS 表征,证明了借助含硼前体在颗粒表面富集及后续高温煅烧强化扩散的策略,实现了硼梯度掺杂以及表面包覆锂离子导体(Li2O-B2O3)NCM的制备。
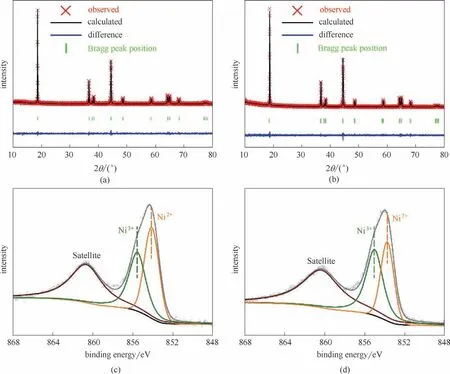
图2 NCM-B(a)和NCM(b)的XRD精修谱图;NCM-B(c)和NCM(d)的XPS Ni 2p3/2谱图Fig.2 XRD Rietveld refinement patterns of the NCM-B(a)and NCM(b);Ni 2p3/2 XPS patterns of the NCM-B(c)and NCM(d)
图2(a)、(b)为NCM-B 和NCM 正极材料 的XRD衍射精修谱图,两种样品均对应于典型的α-NaFeO2层状结构和R-3m空间群。同时,NCM 和NCM-B 正极材料的(003)/(104)峰的峰强度比值均大于1.2,而且明显出现了(006)/(102)和(108)/(110)这两对分裂峰,说明样品的阳离子混排程度低以及层状结构良好[23-25]。进一步采用XRD 精修精确分析材料物相特征及具体晶胞参数[26-27],如表1 所示(1 Å=0.1 nm)。NCM-B 正极材料的a 轴和c轴数值分别为2.8703 和14.2502 Å,均高于NCM 正极材料的晶胞参数(2.8670 和14.2289 Å)。这是因为B3+的离子半径很小(0.27 Å),在晶体中会占据氧离子四面体间隙位置,从而扩大晶胞体积[20]。此外,增加的c 轴间距能够增加Li+在层间的传输速率,从而提升充放电过程中的动力学。图2(c)、(d)为NCM-B 和NCM 正极材料的XPS Ni 2p3/2谱图。发现两个样品中的镍离子均包含二价和三价,而且NCM-B 中Ni2+的含量相比于NCM 有所增加,这主要是由于B3+的引入带来的电荷补偿作用[21]。综上所述,B3+的引入不仅未对材料晶体结构造成影响,还在一定程度上优化了材料的晶体结构,改善了锂离子传输速率。
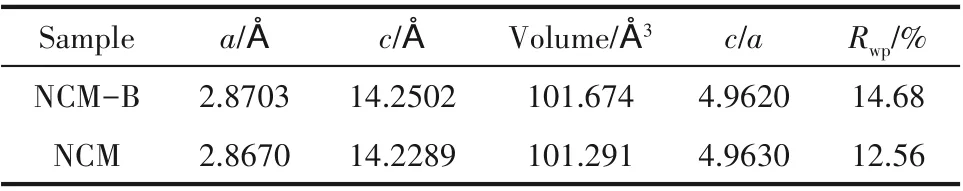
表1 根据XRD精修得到的NCM-B和NCM的晶格常数Table 1 Lattice constants of the NCM-B and NCM calculated from X-ray Rietveld refinement

图3 NCM-B和NCM的倍率(a)、循环性能(b)及其不同循环圈数的充放电曲线[(c),(d)]Fig.3 Rate capability(a),cycling stability(b)and the corresponding charge-discharge curves[(c),(d)]of the NCM-B and the NCM for 100 cycles
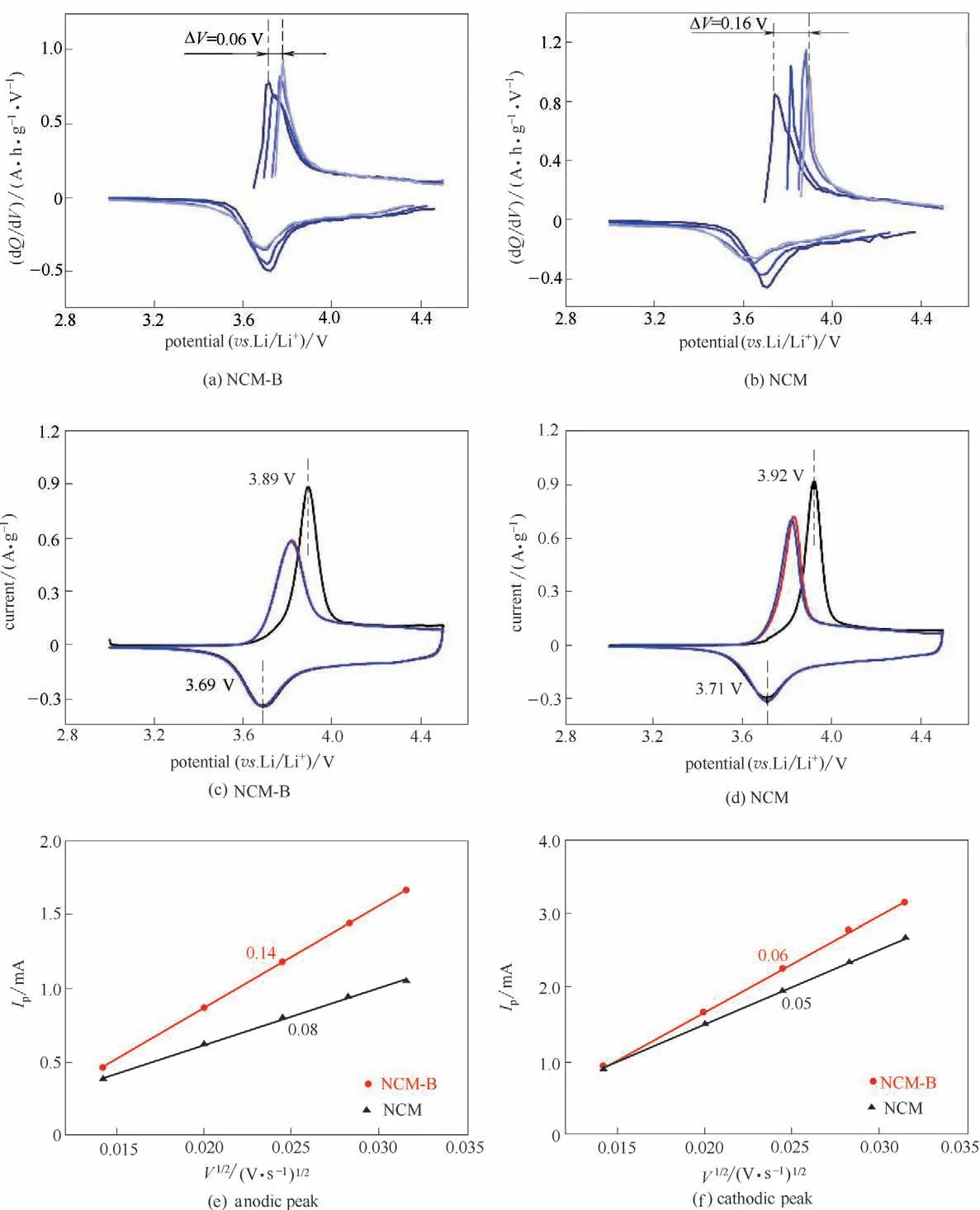
图4 NCM-B和NCM的dQ/dV曲线[(a),(b)]、前三圈循环伏安曲线[(c),(d)];NCM-B和NCM的峰电流和扫速平方根的线性关系图[(e),(f)]Fig.4 The calculated dQ/dV profiles[(a),(b)],the initial three CV curves at 0.2 mV·s-1[(c),(d)]of the NCM-B and the NCM;Linear relationship between the anodic/cathodic peak current(ip)and the square root of the scan rate(v1/2)of the NCM-B and the NCM[(e),(f)],respectively
利用扣式电池对NCM-B 和NCM 样品在3.0~4.5 V电压范围内的倍率和循环性能进行测试,如图3(a)、(b)所示。在0.2 C 小电流下,NCM-B 和NCM 展现了相同的放电比容量(194.7 mA·h·g-1),但是当电流密度逐渐增大,NCM-B的大电流放电能力明显优于NCM。特别是10 C 时,NCM-B 仍然能够保持120 mA·h·g-1的超高比容量,远高于未改性NCM(78.2 mA·h·g-1)。不仅如此,在1 C 下循环100圈后,NCM-B 的容量保持率可以达到90%,而反观NCM仅具有73%的初始容量。同时,NCM-B的首圈库仑效率略微提高,在后续循环过程中库仑效率均大于99.5%。图3(c)、(d)为NCM-B 和NCM 正极材料在1 C 下不同循环圈数的充放电曲线图。相较于NCM,NCM-B 的电压衰退和容量衰减程度得到了大幅度的缓解,表明B3+的引入能够有效稳定层状晶体结构从而增加NCM在长循环下的结构稳定性。
图4(a)、(b)是对第1、30、70 和100 圈的放电曲线进行微分得到的dQ/dV 关系图。每一组dQ/dV 曲线在约3.7 V 都有一对氧化还原峰,对应Ni2+/Ni4+的氧化还原反应。随着循环圈数的增加,由于材料表面副产物的积累,电极极化程度逐渐加重,伴随着氧化还原峰宽化和偏移。从图中看出,NCM-B的氧化还原峰向高电压偏移0.06 V,远低于NCM(0.16 V),表明NCM-B 的极化程度得到了缓解,这得益于B3+掺杂和Li2O-B2O3包覆层有效抑制了晶体结构的恶化和电极-电解液界面副反应。对两种材料进行CV 测试得到前三圈循环伏安曲线[图4(c)、(d)]。与dQ/dV曲线相似,CV曲线中出现在约3.7 V的一对氧化还原峰对应于Ni2+/Ni4+的氧化还原反应。首圈充放电曲线中,NCM-B 的阴极和阳极峰的电压差为0.2 V,略低于NCM(0.21 V),而且NCM-B 在后续的两圈中曲线重合性更高,说明其极化更小,可逆性更高,对应更优的倍率和循环性能。此外,进一步借助多倍率CV 对材料的锂离子传输动力学做了详细的分析,并根据多倍率CV 中锂离子扩散公式[式(1)]求得具体的锂离子扩散系数[28-29]。

式中,n 是电化学反应中的电子数量;A 是电极面积;D 是锂离子扩散系数;C0是正极材料首圈锂离子浓度;ν 是扫速。峰电流和扫速平方根的线性关系图[图4(e)、(f)]表明锂离子在材料内部的迁移是扩散控制的过程。经过计算,NCM-B 和NCM 正极材料在充电/放电过程的锂离子扩散速率分别为9.75×10-10cm2·s-1/1.79×10-10cm2·s-1和3.08×10-10cm2·s-1/1.35×10-10cm2·s-1,可以发现硼改性后材料的锂离子扩散速率不管在充电还是放电过程都有所提高。这表明引入的B3+能够优化晶体结构,增加c 轴间距从而加快Li+在材料内部的迁移;此外,表面包覆的Li2O-B2O3是锂离子导体,可以提高界面处锂离子传输速率。因此,体相和界面处锂离子迁移速率的协同提高最终有效改善了材料电化学反应动力学。

图5 NCM-B和NCM在1 C电流密度下循环100圈后的XRD谱图[(a),(b)]和SEM图[(c),(d)]Fig.5 XRD patterns[(a),(b)]and SEM images[(c),(d)]of the NCM-B and the NCM after 100 cycles at 1 C
为进一步研究改性对于材料稳定性的影响,对循环后的电极材料进行了表征。图5(a)、(b)展现了NCM-B 和NCM 在1 C 下循环100 圈后电极材料的XRD 谱图。由图可知,两个样品均保持与本体材料循环前相似的特征峰,此外XRD 谱图中还存在与集流体Al相关的衍射峰。但是,NCM 正极材料在循环后的XRD 衍射峰的峰强度下降程度更加明显(Al 衍射峰的峰强度更强),进一步比较图中黄色区域,可以发现NCM 的(108)/(110)衍射峰几乎没有分裂,而NCM-B 仍然具有明显的(108)/(110)衍射峰分裂,说明NCM-B 正极材料循环后仍然具有良好的层状结构,而NCM 电极材料遭受了严重的结构破坏[30]。这是由于引入的B3+具有较高的B—O 键能(809 kJ·mol-1)可以稳固其晶格氧框架,抑制氧原子析出,进而改善晶体结构稳定性[31]。同时,由循环后电极表面SEM[图5(c)、(d)]可知,循环后NCM-B 正极材料仍然保持良好的球形且平铺在集流体上,而NCM 电极材料在循环后二次颗粒出现了大量的裂纹甚至破碎。NCM-B 良好的形貌一方面得益于晶体结构稳定性的提高,另一方面源于Li2O-B2O3包覆层对于电极-电解液界面副反应的抑制。
图6是循环后的电极材料的XPS谱图。图6(a)、(c)展示了C 1s谱图,284.8 eV 位置处的C—C 键对应于super P 中的C,两侧的C—H 和C—F 键则与黏结剂PVDF 有关。另外,C—O 键(288.5 eV)以及C O键(289.3 eV)对应于电化学过程中电解液的分解产物,分别用绿色和黄色标出,这与O 1s 谱图[图6(b)、(d)]中534.3 和532.5 eV 位置处的C—O、C O 键相对应[32]。对比分析,可以发现NCM-B 电极中的C—O,C O 键的含量明显低于NCM 样品,说明NCM-B电极中的电解液产物更少,进一步证明电化学过程中活性材料表面的副反应明显减少[33-34]。与此同时,O 1s 谱图中529.8 eV 位置的特征峰对应于晶格中的氧[35]。显然,NCM-B 中晶格氧的含量也明显高于NCM,这是由于NCM 表面副反应的加重形成了过厚CEI膜[36],而NCM-B 由于Li2O-B2O3包覆层的保护,有效缓解了CEI的形成,提高了界面稳定性并降低了界面处离子/电子的传输势垒。
3 结 论
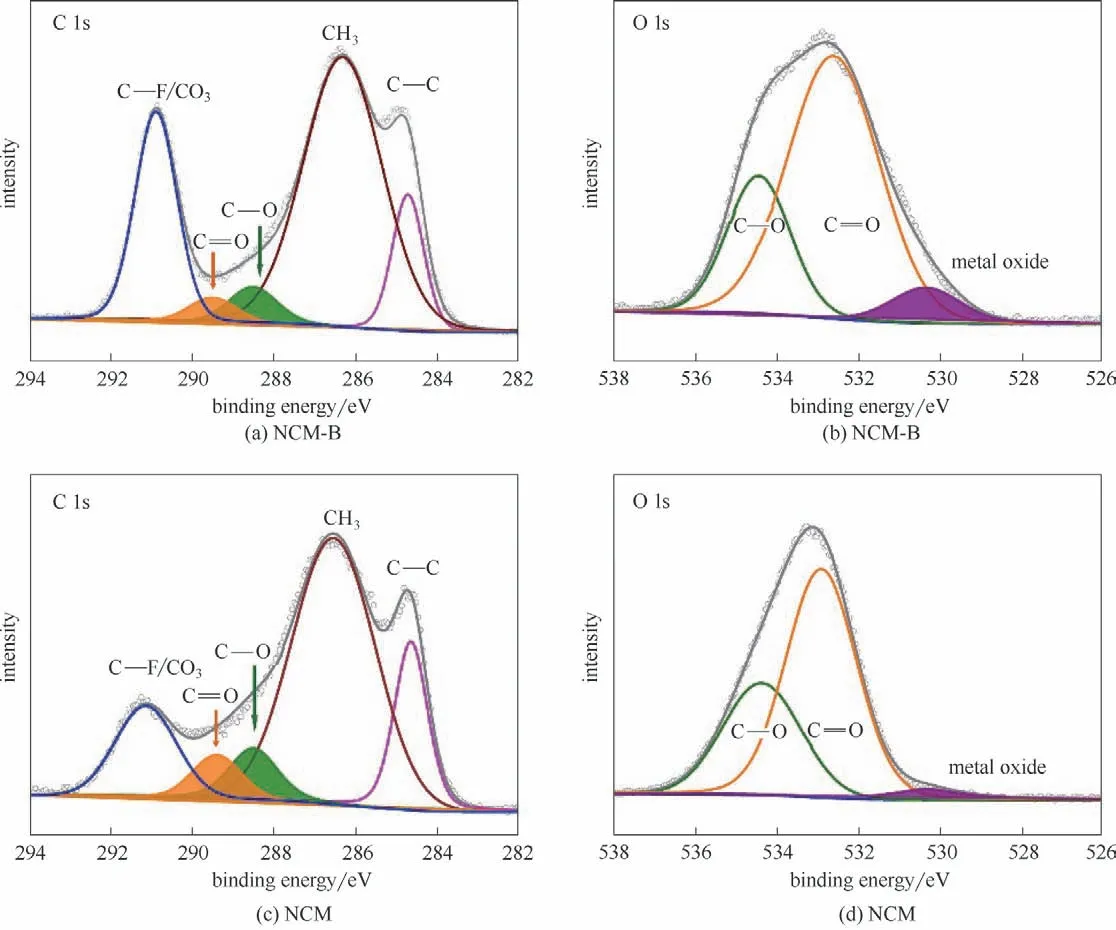
图6 NCM-B和NCM在1 C下循环100圈后的C 1s[(a),(c)]和O 1s XPS[(b),(d)]谱图Fig.6 XPS spectra of C 1s[(a),(c)]and O 1s[(b),(d)]regions for the NCM-B and the NCM after 100 cycles at 1 C
本文利用含硼前体在颗粒表面富集及后续高温煅烧强化B3+在NCM 正极材料中的体相扩散,成功制备了硼离子高效掺杂NCM 正极材料(NCM-B)。高键能的B—O 键(809 kJ·mol-1)可以有效稳固其晶格氧框架,抑制氧原子析出,进而改善晶体结构稳定性,有效缓解极化,提高材料的电化学循环性能;表面残余的Li2O-B2O3包覆层具有明显的物理屏障作用,可以有效缓解电解液的侵蚀,进而提高电极-电解液界面稳定性,同时其高的锂离子电导率可以加速界面处的离子传输,提高材料的大电流放电能力。因此,改性后的NCM-B 正极材料在3.0~4.5 V电压区间的可逆比电容量为193.7 mA·h·g-1,即使在10 C的大电流下仍具有高达120 mA·h·g-1的放电比容量。不仅如此,NCM-B 正极材料在1 C 下循环100 圈后仍具有初始容量的90%。这种优异的电化学性能表明所制备的NCM-B 材料有利于促进高电压LiNi0.5Co0.2Mn0.3O2三元正极材料的商业化应用。
