血清外泌体源性长链非编码RNA H19在骨肉瘤中的表达及其临床意义 *
2021-01-29杨彪魏新锁赵晓光李卓王瑶
杨彪,魏新锁,赵晓光,李卓,王瑶
(西安医学院第一附属医院a.骨科, b.检验科,西安 710077)
骨肉瘤(osteosarcoma)是儿童和青少年常见的骨原发性恶性肿瘤,主要侵犯长管状骨,恶性程度高,发展迅速,死亡率高,严重威胁着患者的健康和生命[1]。因此,研究骨肉瘤发生、发展的分子机制,寻找有效的早期诊断指标及治疗靶点具有重要的临床意义。
外泌体(exosome)是纳米级脂质包涵体,包裹转运多种物质,如环状RNA、长链非编码RNA(long non coding RNA,LncRNA)和信使RNA等[2],主要通过细胞间信号转导起作用[3]。外泌体可以在血液、唾液和乳汁等体液中被释放,不仅可以调节受体细胞的功能,还可以作为疾病诊断的生物学标志物[4]。近年来,有关外泌体来源的LncRNA在肿瘤中的功能得到广泛研究,外泌体LncRNA H19的生物学功能和分子机制也得到进一步的认识[5]。本研究旨在通过分析骨肉瘤患者血清外泌体中LncRNA H19的表达水平,为进一步探讨骨肉瘤的发生机理及相关靶向治疗提供依据。
1 资料与方法
1.1临床资料 收集2016年3月至2019年10月于西安医学院第一附属医院骨科及肿瘤科诊治的骨肉瘤患者46例作为病例组,男性29例,女性17例,年龄13~32岁。纳入标准:(1)所有研究对象均经骨科及肿瘤科专家联合确诊;(2)无放、化疗等抗癌治疗史。排除标准:(1)合并其他肿瘤者;(2)有心脏病、器官衰竭、精神障碍、高血压、糖尿病、创伤性疾病和免疫疾病的患者;(3)合并其他心、肾、肝脏功能不全者。收集同期就诊的50例无骨肿瘤病史的体检健康者作为健康人对照组,男性30例,女性20例,年龄为15~28岁。本研究经西安医学院第一附属医院医学伦理委员会审核批准(No.XYFYEC2016022),各研究对象均知情同意。
1.2主要试剂与仪器 外泌体RNA 提取试剂盒、QuantiNova SYBR Green PCR试剂盒(德国Qiagen公司),逆转录试剂盒及qRT-PCR实时荧光定量试剂盒(北京诺博莱德公司),PCR引物(苏州金唯智公司),基质金属蛋白酶9(MMP-9)、血管内皮生长因子(VEGF)、胰岛素样生长因子2(IGF-2) ELISA检测试剂盒(武汉默沙克生物科技公司)。CFX96实时荧光定量PCR仪(美国Bio-Rad公司),NanoDrop ND-1000UV微量紫外分光光度计(美国Thermo公司),Multiskan FC型酶联仪(上海赛默飞世尔仪器公司),NICOMP 380粒径分析仪(美国PSS公司)。
1.3方法
1.3.1标本采集 采集各研究对象的空腹静脉血4 mL(骨肉瘤患者于手术前采集,体检健康者于体检时采集),置于含分离胶的促凝采血管中,2 h内4 ℃、3 000×g离心10 min,4 h内完成MMP-9、VEGF、IGF-2的ELISA法检测,剩余血清加入至无RNase的Ep管中,置于-80 ℃保存。
1.3.2血浆外泌体RNA的提取及其效率评价 按照exoRNeasy试剂盒说明书提取外泌体。简化步骤如下:样品于4 ℃、10 000×g离心2次,每次30 min,取上清液转移至新Ep管中,加入0.5倍体积的PBS稀释,再加入0.05倍体积蛋白酶K溶液,37 ℃温育15 min;而后加入0.3倍总体积的外泌体分离试剂,4 ℃温育2 h,10 000×g离心20 min,取沉淀即为外泌体。提取外泌体采用2种方法评价:(1)经4 mL PBS重悬,置于NICOMP380粒径分析仪进行粒径分析;(2)通过检测外泌体常见的特异性标志蛋白——白细胞分化抗原63(cluster of differentiation 63,CD63)和CD81作为外泌体纯度的指标。步骤:提取的外泌体用100 μL PBS复匀,加入20 μL荧光直标抗体CD63或CD81温育,以不染色为空白对照,流式细胞仪检测并统计分离的外泌体阳性百分比,用以判断外泌体的纯度。
1.3.3逆转录反应 按照逆转录试剂盒说明书将RNA逆转录为cDNA,cDNA样本用DEPC溶液稀释10倍,置于-20 ℃保存。
1.3.4实时荧光定量PCR 根据GenBank中的LncRNA H19及β-actin的基因序列号(分别为NM_001293171.2、NM_001101.3),用 Primer Premier 5.0软件设计引物,并由苏州金唯智公司合成。LncRNA H19上游引物序列:5′-TGCTGCACTTTACAACCACG-3′,下游引物序列:5′-ATGGTGTCTTTGATGTTGGGC-3′,退火温度60 ℃,产物片段大小为182 bp;β-actin上游引物序列:5′-TCCTCTCCCAAGTCCACACA-3′,下游引物序列:5′-GCACGAAGGCTCATCATTCA-3′,退火温度60 ℃,产物片段大小为129 bp。PCR总反应体系为25 μL,包括:10 μmol/L上、下游引物各1.0 μL,SYBR Rremix Ex TaqⅡ(2×)12.5 μL,cDNA 2.0 μL,ddH2O 8.5 μL。循环参数:95 ℃ 30 s,95 ℃ 5 s,60 ℃ 30 s,共45个循环;72 ℃时采集荧光信号,使用7500 System Software-SDS 2.2软件进行熔解曲线分析,检测PCR产物的特异性。每孔均设3个复孔,以β-actin作为内参基因,采用2-△△Ct法计算LncRNA H19的表达水平,公式:△Ct=Ct目的基因-Ct内参照。
1.3.5ELISA法测定血清MMP-9、VEGF、IGF-2水平 采用双抗体夹心ELISA法,按试剂盒说明书操作,使用Multiskan FC型酶联仪在450 nm波长处读取吸光度(A)值,采用标准曲线法计算各标本浓度。血清MMP-9、VEGF、IGF-2的参考范围分别为:MMP-9≤1 137.65 pg/mL、VEGF≤293.62 pg/mL、IGF-2≤0.76 pg/mL。
1.4统计学分析 采用 SPSS 22.0 统计软件进行分析。数据为非正态分布,以中位数(四分位数)[M(P25,P75)]表示,组间比较采用Mann-WhitneyU检验。采用ROC曲线评价LncRNA H19对骨肉瘤的筛查价值。以P<0.05为差异具有统计学意义。
2 结果
2.1血清外泌体提取效率的评价 提取的外泌体经NICOMP 380粒径分析仪分析,证实分布粒径在20~200 nm范围内的样品占8%以上,与外泌体的粒径分布相吻合,其平均粒径及主峰均在外泌体粒径范围内,粒子的分布系数在0.07~0.8之间,表明体系分数适中,检测置信度高。各血清外泌体提取物经荧光染色后均呈阳性,CD63和CD81的阳性率均在70%以上,证实所提取物为外泌体。
2.2血清外泌体LncRNA H19水平与骨肉瘤患者临床病理参数关系 将血清外泌体LncRNA H19的表达水平与骨肉瘤患者性别、年龄、居住地、发病部位、AJCC分期及是否远处转移进行分析,结果发现血清外泌体LncRNA H19的表达水平与肿瘤分期及是否远处转移相关(P均<0.01),而与患者性别、年龄、居住地及发病部位均无显著关系(P均>0.05),见表1。
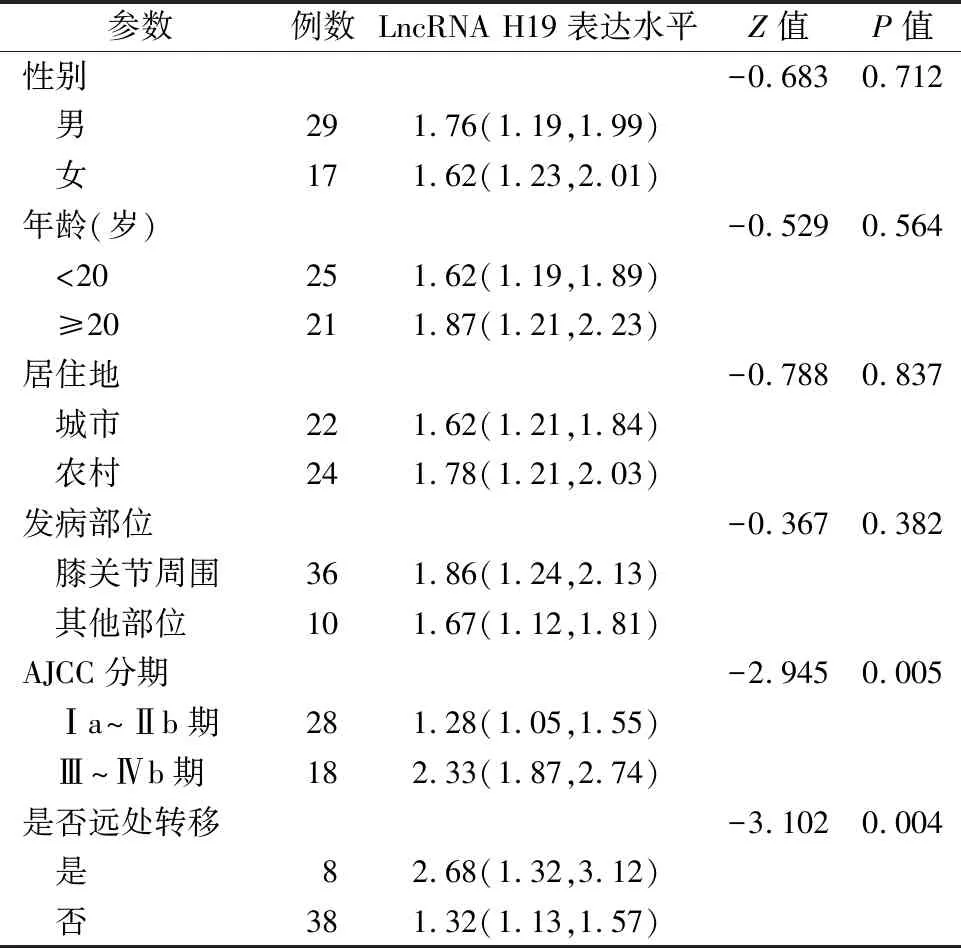
表1 血清外泌体LncRNA H19表达水平与骨肉瘤患者临床病理参数的关系
2.3外泌体LncRNA H19和血清MMP-9、VEGF、IGF-2检测结果 骨肉瘤组患者外泌体LncRNA H19和血清MMP-9、VEGF、IGF-2的表达水平均显著高于健康人对照组,差异有统计学意义(P均<0.01),见表2。

表2 各组血清外泌体LncRNA H19和血清MMP-9、VEGF、IGF-2含量检测结果
2.4外泌体LncRNA H19、血清MMP-9、VEGF、IGF-2检测对骨肉瘤的筛查价值 以骨肉瘤组为疾病组,以健康人对照组为对照组,绘制ROC曲线评估各项指标筛查骨肉瘤的筛查效能,结果表明LncRNA H19的ROC曲线下面积(AUCROC)为0.881(95%CI:0.835~0.947),当cut-off值为0.395时,其筛查骨肉瘤的敏感性为87.2%,特异性为75.6%;外泌体LncRNA H19、血清MMP-9、VEGF、IGF-2联合检测的AUCROC为0.932(95%CI:0.886~0.978),敏感性为92.5%,特异性为86.2%,均高于3项指标的单独筛查价值,见表3、图1。

图1 外泌体LncRNA H19、血清MMP-9、VEGF、IGF-2筛查骨肉瘤的ROC曲线

表3 各项指标筛查骨肉瘤的效能评价
3 讨论
近年来,LncRNA被报道参与了骨肉瘤的发生过程。有证据表明,LncRNA H19不仅参与骨肉瘤的发生,而且在细胞迁移和肿瘤侵袭的过程中发挥重要的作用[5]。Luo等[6]发现LncRNA H19在肿瘤组织中的表达水平明显高于邻近的癌旁组织,且LncRNA H19阳性细胞比例较高的患者具有更高的癌症转移风险。Li等[7]通过研究发现,LncRNA H19可以海绵样吸附于miR-200,从而抑制miR-200的抑制作用,最终促进骨肉瘤的发展及转移。此外,亦有研究表明,LncRNA H19的表达水平与骨肉瘤细胞转移距离及侵袭能力呈正相关[8]。有学者发现LncRNA H19通过诱导NF-κB通路,并激活PI3K/AKT信号通路,调控VEGF等因子的表达,从而导致骨肉瘤的迁移和入侵[9]。另有研究证实,LncRNA H19通过竞争性结合miR-200,上调ZEB1和ZEB2,进而诱导骨肉瘤细胞的侵袭,从而促进转移[7]。本研究结果显示,血清外泌体中LncRNA H19在骨肉瘤中的表达水平与患者的性别、年龄、居住地及发病部位均无显著相关(P均>0.05),而与骨肉瘤患者的临床分期及是否发生远处转移显著相关(P<0.01),这提示LncRNA H19可能成为筛查骨肉瘤的生物学标志物。
Yang等[10]研究表明,Yes相关蛋白1(Yes-associated protein 1, Yap1)过表达促进了Runx2和骨钙素的表达,而Runx2是成骨细胞分化的关键转录因子。另有研究证实,Runx2调控了MMP-9和VEGF的表达,原因可能与肿瘤转移过程有关[11]。IGF2和LncRNA H19在大多数正常人体组织中均有印迹,但在肿瘤中印迹往往缺失。IGF2和/或LncRNA H19印迹缺失常发生在癌症中,并可能参与肿瘤恶性转化。本研究采取与骨肉瘤发生相关的MMP-9、VEGF、IGF-2因子作为研究对象,通过检测其在骨肉瘤患者及健康人对照组中的表达,并比较LncRNA H19在骨肉瘤筛查中的作用,结果表明,骨肉瘤组外泌体可稳定表达LncRNA H19,其表达水平显著高于健康人对照组(P均<0.01),且血清MMP-9、VEGF、IGF-2的敏感性和特异性也都高于健康人对照组(P均<0.01),这提示外泌体中LncRNA H19和血清MMP-9、VEGF、IGF-2、MMP-9均可作为骨肉瘤筛查的生物学指标;血清外泌体LncRNA H19的AUCROC为0.881,其筛查骨肉瘤的敏感性为87.2%,特异性为75.6%,均高于其余各单项组,表明血清外泌体 LncRNA H19具有更高的骨肉瘤的筛查价值。
综上所述,鉴于血清学的无创性特点,而MMP-9、VEGF、IGF-2等细胞因子受多种内外因素影响较大,因此,血清外泌体LncRNA H19更适用于大量人群的筛查。LncRNA H19在骨肉瘤筛查中更具明显的优势,有望成为骨肉瘤筛查、靶点个体化治疗及疗效监测的生物学标志物。
