喷雾干燥法制备石墨烯包覆富锂锰基材料Li1.22Mn0.52Ni0.26O2及其电化学性质
2021-01-19王继贤彭思侃南文争燕绍九戴圣龙
王继贤,彭思侃,南文争,陈 翔,王 晨,燕绍九,戴圣龙
(1中国航发北京航空材料研究院;2北京石墨烯技术研究院有限公司,北京100095)
近年来,电动汽车、智慧电网及便携电子设备等领域迅速发展,进一步提升锂离子电池的能量密度面临严峻技术挑战。当前以碳基材料为负极的锂离子电池体系中,正极材料的性能是制约锂离子电池能量密度的关键因素,开发高比能量锂离子电池正极材料迫在眉睫。富锂锰基正极材料具有高比容量(250 mA·h/g)、高工作电压、低成本和环境友好等优点,是极具潜力的下一代锂离子电池正极材料[1-5]。但是,较大的首次不可逆容量损失、较差的循环稳定性和倍率性能及电压降限制了其大规模应用[6-9]。表面包覆是提升正极材料性能的有效手段,在富锂锰基材料表面包覆Al2O3、TiO2及AlPO4能够改善电极/电解液界面反应,提升材料的循环稳定性[11-14]。但是,富锂锰基材料自身电导率较低,而表面包覆所采用的氧化物和磷酸盐虽然具有良好的结构稳定性,但其电导率往往较低,包覆后容易导致材料的倍率性能进一步恶化。具有特定结构的碳材料(包括碳纳米管、石墨烯和多孔碳等)能够协助电极材料在电极中构建高效导电网络,有效提升电池的倍率性能,并减缓电极/电解液界面副反应,提升电池的循环稳定性[15]。石墨烯作为一种纳米结构的二维碳材料,具有优异的电子导电性和化学稳定性,在高性能锂离子电池电极材料制备中有广阔的应用前景[16-17]。Jiang 等[18]通过机械搅拌法制备了富锂锰基正极/石墨烯复合材料,电化学分析表明,石墨烯加入后电极的极化得到明显缓解,倍率和循环性能得到明显提升。夏永姚等[19]先在富锂锰基材料表面包覆氧化石墨烯,之后在空气中350 ℃热处理提升氧化石墨烯的电导率,有效提升了富锂锰基材料的倍率性能。虽然文献中已有很多制备石墨烯包覆富锂锰基材料的报道,但是规模化制备石墨烯均匀包覆富锂锰基材料仍然存在以下技术难点亟待解决:①采用高电导率的石墨烯进行包覆,石墨烯在液相体系中需要长时间的超声分散,能耗较高且均匀性难以控制,在复合过程中极易出现石墨烯的团聚,进而大大降低包覆的均匀性;②如采用氧化石墨烯预先包覆加后续热处理的工艺,在高温烧结过程中氧化石墨烯容易还原富锂锰基材料中的高价过渡金属离子,导致结构转变和杂相的生成。
为了解决以上难题,本文首先以NMP 为液相介质,采用高压液相均质剥离法[20]制备了高稳定性、石墨烯片径为5~10 μm 的石墨烯浆料,之后将所制备的Li1.22Mn0.52Ni0.26O2均匀分散于上述溶液中,再经喷雾干燥法制备了石墨烯包覆Li1.22Mn0.52Ni0.26O2材料。包覆后材料的结构及电化学测试分析表明,本文实现了石墨烯对富锂锰基材料的均匀包覆,经过石墨烯包覆后,材料的循环和倍率性能均得到较大提升。该工艺流程简单易放大,有望应用于大规模制备石墨烯包覆富锂锰基材料。
1 实验材料及方法
1.1 石墨烯包覆富锂锰基材料的制备
实验所用的富锂锰基材料采用文献报道的碳酸盐共沉淀法合成[21],化学式为Li1.22Mn0.52Ni0.26O2,记为LNMO。取1 kg 富锂锰基材料和一定量石墨烯NMP分散液,分别按照石墨烯+LNMO材料在混合后悬浊液中总固含量为50%、55%、60%、65%和70%加入高速搅拌器中搅拌混合10 min 后,采用Brookfield DV-S黏度计分别测量各悬浊液的黏度。
图1(a)为所制备的石墨烯与LNMO混合悬浊液黏度随固含量变化,从图中可以看到,当固含量≤55%时,悬浊液的黏度<350 mPa·s,此时所形成的悬浊液中富锂锰基颗粒极易沉降,导致石墨烯与富锂锰基材料的分相,这将导致包覆后材料的均匀性大大降低。当固含量为70%时,悬浊液的黏度>1700 mPa·s,超过了喷雾干燥所用蠕动泵的输送黏度上限。图1(b)为固含量为65%的石墨烯与LNMO混合悬浊液的光学照片,可以看出,混合悬浊液流动性良好,且富锂锰基与石墨烯未出现沉降分层。因此,实验选取固含量65%的石墨烯与LNMO 混合悬浊液制备G-LNMO材料。
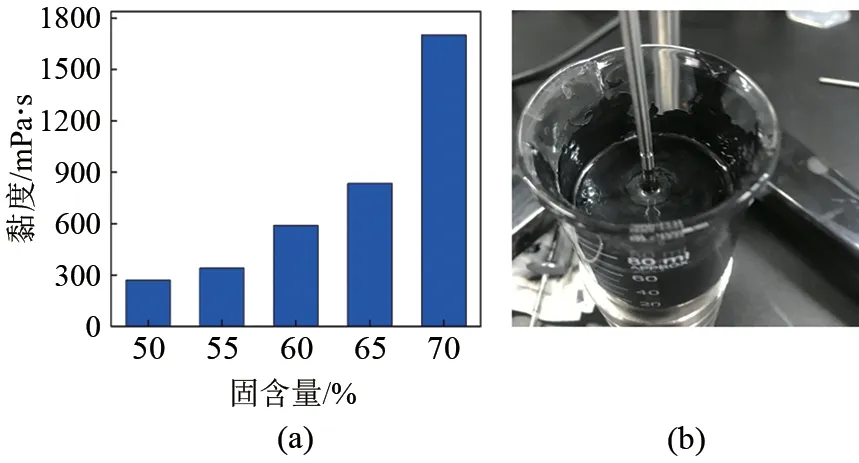
图1 (a)石墨烯+富锂锰基悬浊液黏度随固含量变化;(b)65%固含量混合悬浊液光学照片Fig.1 (a)viscosity of as-prepared suspensions as a function of solid content;(b)OM image of as-prepared suspension with 65%solid content
图2为喷雾干燥法制备G-LNMO材料的工艺路线。首先按照石墨烯+富锂锰基材料总固含量65%,石墨烯∶LNMO质量比为1∶100,依次向搅拌器中加入一定量的NMP溶剂、石墨烯NMP分散液和LNMO材料,并保持匀速搅拌,搅拌速率为300 r/min,搅拌10 min后,使用蠕动泵将混合悬浊液以500 mL/h的速度泵入离心式喷雾干燥器中,干燥器喷盘直径15 cm,喷盘转速设置为12000 r/min,料液喷口温度设置为215 ℃,干燥保护气氛为氮气,待喷雾干燥器的物料收集罐内粉末冷却到60 ℃以下,取出即得到G-LNMO材料。

图2 喷雾干燥法制备石墨烯包覆富锂锰基材料制备工艺Fig.2 Scheme of preparation of graphene coated Li1.22Mn0.52Ni0.26O2 oxide
1.2 材料物性表征
采用Bruker D8 Advance (with Cu-Kαradiation)研究材料的晶体结构;采用FEI Nova Nano SEM450 扫描电镜研究材料的微观形貌;采用EI Tecnai G2 F30 透射电镜分析材料的微观结构。
1.3 扣式电池电极制作及电池组装测试
扣式电池电极极片制备过程如下:
(1)对于LNMO材料,按照正极材料∶导电炭黑(Super P)∶黏结剂(PVDF)质量比为96∶2∶2 分别称取材料;对于G-LNMO,按照正极材料∶导电炭黑(Super P)∶黏结剂(PVDF)质量比为97∶1.04∶2分别称取材料。以NMP 为溶剂,磁力搅拌8 h 后,分别制备两种正极浆料。
(2)采用涂布机将正极浆料以200 μm 的厚度涂覆于铝箔上,100 ℃干燥4 h后,设置80 μm的间隙在双对辊碾压机上反复碾压4次,后转移至真空干燥箱于120 ℃干燥12 h 以完全去除NMP 及残余水分。
(3)将干燥后电极裁成直径为14 mm的圆片即制得工作电极。
扣式电池的组装过程如下:选取CR2032 电池模具,负极选取锂片,隔膜选取Celgard2500 聚丙烯隔膜,采用1 mol/L LiPF6(DMC+EC+DMC体积比1∶1∶1)为电解液,在充满干燥氩气的手套箱中完成扣式电池装配,控制手套箱内水、氧浓度低于1 ppm(1 ppm=10-6)。扣式电池在手套箱中封壳之后静置老化8 h 后,使用蓝电电池测试系统(LANDHE,武汉蓝电电子股份有限公司)对扣式电池进行充/放电测试,电压范围为2.0~4.8 V。使用电化学工作站(Zennium,德国Zahner 公司)对扣式电池进行电化学阻抗(EIS)测试,EIS测试的频率范围为10 mHz~100 kHz。
2 结果与分析
2.1 晶体结构分析
图3(a)、(b)分别为LNMO 及G-LNMO 材料的XRD 图谱。可以看出,石墨烯包覆后的样品和未包覆样品的XRD 衍射曲线基本一致,主要衍射峰均与层状α-NaFeO2结构相对应(空间群为R-3m),且006/012、018/110 两峰均分裂明显,显示出良好的二维层状结构有序度[22]。其中,XRD 图谱在2θ 角度为20°~25°区间内出现的超晶格峰,与过渡金属层中LiMn6的有序排列有关,是Li2MnO3结构的特征峰[9,23]。此外,G-LNMO 样品的XRD 谱图中未观察到石墨烯的衍射峰,这可能是由于石墨烯包覆量仅有1%。以上结果说明本实验所采用的包覆工艺未对LNMO 材料的结构造成影响,G-LNMO 材料仍然保持富锂锰基的晶体结构。

图3 (a)LNMO材料和(b)G-LNMO材料的XRD图谱Fig.3 XRD patterns of(a)pristine LNMO and(b)G-LNMO samples
2.2 形貌分析
图4(a)、(b)分别为实验所使用的LNMO材料及石墨烯的SEM图。从图4(a)中可以看出,LNMO材料为不规则形貌的二次颗粒,由一次颗粒团聚形成,一次颗粒粒径大约在500~1000 nm。从图4(b)中可以看出,实验所制备的石墨烯的片径约为4~5 μm。图4(c)为所制备G-LNMO 材料的SEM 图,图中可以看出,在G-LNMO 材料中,LNMO 颗粒保持了原有形貌,部分颗粒经过石墨烯包覆后发生团聚,石墨烯在G-LNMO 材料中没有发生明显团聚,均匀贴附于LNMO正极颗粒表面。图4(d)为GLNMO 材料的TEM 照片,可以清晰地看到,在LNMO颗粒表面包覆了薄层的石墨烯。以上结果显示,本文所采用的喷雾干燥工艺能够实现石墨烯对LNMO材料的均匀包覆,借助于石墨烯的高电导率和化学稳定性,这种包覆结构有望提升G-LNMO材料的电导率和电化学稳定性,进而提高材料的循环和倍率性能。

图4 (a)LNMO材料的SEM照片;(b)石墨烯的TEM照片;(c)G-LNMO材料的SEM照片(黄色箭头处为石墨烯)和(d)G-LNMO材料的TEM照片Fig.4 (a)SEM image of LNMO;(b)TEM image of graphene nanosheets;(c)SEM image of G-LNMO;(d)TEM image of G-LNMO
2.3 电化学性能表征
图5(a)为LNMO 和G-LNMO 材料电池在0.5 C(100 mA/g)倍率下的循环性能曲线。从图中可以看出,LNMO材料首次放电容量为146.2 mA·h/g,100次充放电循环后容量为103.4 mA·h/g,容量保持率约为71%;而G-LNMO材料首次放电容量为159.8 mA·h/g,100 次充/放电循环后容量140.6 mA·h/g,容量保持率约为88%,相比于LNMO,G-LNMO展示出更高的放电容量和更优异的循环稳定性。图4(b)对比了LNMO 和G-LNMO 材料在0.1 C 倍率充电,不同倍率放电的容量。可以看出,LNMO 材料在0.1 C、0.5 C 和1 C 倍率下的首次循环放电容量分别为199.8 mA·h/g、146.0 mA·h/g 和87.1 mA·h/g,而GLNMO材料在0.1 C、0.5 C和1 C倍率下首次放电容量分别为220.2 mA·h/g、159.5 mA·h/g 和117.6 mA·h/g。以上结果说明,通过石墨烯包覆有效提升了材料的循环稳定性和倍率性能。
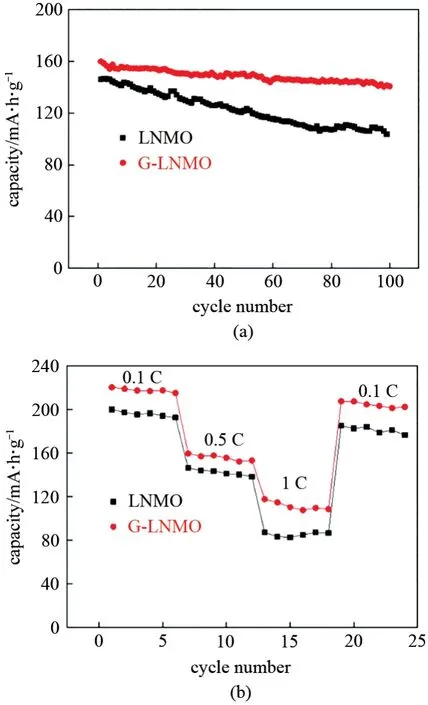
图5 LNMO和G-LNMO材料的(a)0.5 C倍率下的循环性能曲线图;(b)倍率性能曲线图Fig.5 (a)cycling performance of LNMO and G-LNMO at 0.5 C;(b)rate performance of LNMO and G-LNMO at 0.1~1 C

图6 LNMO和G-LNMO材料的(a)0.1 C倍率下首次充/放电曲线图;(b)0.5 C倍率下的库仑效率曲线;(c)0.5 C倍率下第100次循环时的充/放电曲线;(d)0.5 C倍率下100次循环后的电化学交流阻抗谱图(荷电态为50%)Fig.6 (a)initial charge-discharge curves of LNMO and G-LNMO electrodes at 0.1 C;(b)coulombic efficiency profiles of LNMO and G-LNMO electrodes at 0.5 C;(c)100th charge-discharge curves of LNMO and G-LNMO electrodes at 0.5 C;(d)Nyquist plots of LNMO and G-LNMO electrodes after 100 cycles at 0.5 C(SOC is 50%)
图6(a)展示了LNMO 和G-LNMO 材料所组装的电池在0.1 C 倍率下,2.0~4.8 V 电压区间内的首次充/放电曲线,可以看出,LNMO和G-LNMO样品的首次循环充放电曲线呈相似特征:在电压小于4.5 V时,电压持续上升,这对应于过渡金属Ni2+的氧化[24-25];当电压上升到4.5 V 时,开始出现一个平台段,这对应于Li2MnO3结构组分的活化[26-27]。从图6(a)中可以清晰地看到,LNMO 材料在0.1 C 下充电容量为306 mA·h/g,首次放电容量为200 mA·h/g,库仑效率为65%。G-LMNCO材料在0.1 C下充电容量为319 mA·h/g,首次放电容量为223 mA·h/g,库仑效率为70%,高于LNMO材料。充电曲线与放电曲线之间的电压差ΔV代表着电池在充/放电过程中的极化程度,也能够反映充/放电过程中Li+嵌脱的动力学过程和可逆性,可以看出,G-LNMO 材料的充/放电曲线之间的ΔV更小,这说明G-LNMO电极具有更快的电化学反应动力学和可逆性,这也与库仑效率的提升相呼应。究其原因可能有以下三点:首先,石墨烯包覆后与Super P形成复合导电网络,改善了LNMO材料较差的电导率,提升了电极的电化学反应速率,增加了材料的充/放电容量[18];其次,在LNMO颗粒与片状结构的石墨烯之间存在大量空隙,可以容纳电解液,加快电化学反应中Li+迁移速度;此外,G-LNMO材料较低的电极极化会减少界面不可逆副反应的发生,进而提升电化学反应的可逆性和循环稳定性[28]。图6(b)为LNMO和GLNMO材料电池在0.5 C(100 mA/g)倍率下的库仑效率曲线,可以看出G-LNMO 材料的库仑效率高于LNMO材料,具有更优异的循环稳定性。图6(c)为LNMO和G-LNMO材料电池在0.5 C倍率下,2.0~4.8 V 电压区间内的第100 次充/放电曲线,可以看到,100次循环后G-LNMO电极依然表现出更低的充电平台电压和更小的ΔV,展示出更优异的动力学性能。为了进一步分析石墨烯包覆前后材料的电化学性质差异,图6(d)为LNMO和G-LNMO电极在0.5 C 倍率下经过100 次充/放电循环后的电化学交流阻抗(EIS)谱图,在测试前,电池均被预先充电至50%的荷电态(SOC)。其中,EIS谱图上高频区的半圆对应电极的界面电阻(Rsf),低频区的半圆对应电极的电荷转移电阻(Rct)[29],可以看出,经过100 次循环后,G-LNMO 的Rsf及Rct均远小于LNMO。经过石墨烯包覆后,Rct的降低主要归因于石墨烯包覆对电导率的提升,因此G-LNMO 电极具有更快的电化学反应动力学和更加优异的倍率性能;而经过100次循环后,G-LNMO材料的Rsf也远低于LNMO材料。Rsf的增加主要与电极/电解液界面副反应相关,副反应的产物会导致界面膜的增厚,进而导致Li+脱嵌困难和电化学性质的恶化[28,30-31]。由此可以说明G-LNMO 电极具有更高的电化学稳定性和可逆性,电极/电解液界面副反应得到了抑制。
3 结 论
(1)采用喷雾干燥法成功制备了石墨烯包覆的富锂锰基材料Li1.22Mn0.52Ni0.26O2,在G-LNMO 材料中,小片径的石墨烯纳米片贴附于富锂锰基材料颗粒表面,且G-LNMO 材料中未见石墨烯纳米片团聚体的存在,实现了石墨烯纳米片与富锂锰基材料的均匀复合,该工艺过程简单可控,易于进一步放大。
(2)未进行包覆的LNMO 材料在0.1 C 和1 C倍率下的首次循环放电容量分别为199.8 mA·h/g和87.1 mA·h/g,0.5 C 倍率下100 次循环后容量保持率为71%;而包覆后的G-LNMO 材料在0.1 C 和1 C 倍率下首次放电容量分别为220.2 mA·h/g 和117.6 mA·h/g,0.5 C 倍率下100 次循环后容量保持率为88%。经过石墨烯包覆后,富锂锰基材料的容量、循环和倍率性能均得到提升。
(3)电化学分析发现,石墨烯包覆后电极动力学特性得到改善,充/放电过程中的表面副反应得到抑制,进而使材料的循环性能和倍率性能都得到明显提高。
