阿帕替尼联合FOLFOX6方案化疗对晚期胃癌患者疾病控制率及无进展生存期的影响
2021-01-15张晨冲
马 馨,张晨冲
(焦作市第二人民医院a.全科医学科;b.脊椎外科,河南 焦作 454000)
胃癌发病率在男性恶性肿瘤中排第2位,女性第5位,研究显示幽门螺杆菌感染、饮食结构、社会压力大是导致目前胃癌高发的主要因素,且在恶性肿瘤中具有较高的死亡率,严重威胁人类生命安全[1]。由于胃癌早期常无症状,临床就诊时多是晚期,已失去手术切除的机会,而化疗是晚期胃癌患者治疗的主要手段,可缓解肿瘤发展速度,具有一定近期效果,但化疗会使肿瘤细胞产生耐药性,且不良反应强烈,影响整体效果。现阶段分子靶向治疗是临床癌症治疗新方向,阿帕替尼属于新型小分子抗血管生成剂,在胃癌治疗中取得肯定效果[2-3]。本研究进一步探讨阿帕替尼联合FOLFOX6方案化疗在晚期胃癌患者中的应用效果。现报告如下。
1 资料与方法
1.1 一般资料
选取2017年7月至2018年9月本院收治的晚期胃癌患者83例,予以FOLFOX6方案化疗治疗的41例为对照组,接受阿帕替尼联合FOLFOX6方案化疗治疗的42例为研究组。研究组男25例,女17例;年龄42~70岁,平均(55.71±6.79)岁;病理分期:Ⅲb期24例,Ⅳ期18例。对照组男26例,女15例;年龄43~70岁,平均(56.12±6.43)岁;病理分期:Ⅲb期25例,Ⅳ期16例。两组基线资料比较差异无统计学意义(P>0.05),均衡可比。
1.2 选取标准
①纳入标准:经CT等影像学显示多发占位,经病理活检确诊为胃癌,处于Ⅲb~Ⅳ期;患者卡氏评分(KPS)≥60分,无脑转移与骨髓肿瘤浸润,无化疗禁忌证,临床预计患者生存期>3个月;临床资料完整。②排除标准:认知功能障碍或智力低下者;合并其他恶性肿瘤者;伴有血液系统疾病与免疫功能不全者;合并肠穿孔、肠梗阻、溃疡性结肠炎等消化系统疾病者;重度肝肾功能不全者;伴有心肌梗死、脑卒中等严重心脑血管疾病者。
1.3 方法
1.3.1 研究组 予以阿帕替尼[国药准字 H20140105,规格:0.425 g(以阿帕替尼计)/片,江苏恒瑞医药股份有限公司]联合FOLFOX6方案化疗治疗,静脉滴注奥沙利铂(国药准字H20000337,规格:50 mg,江苏恒瑞医药股份有限公司),亚叶酸钙(国药准字H20000584,规格:10 ml∶0.1 g,江苏恒瑞医药股份有限公司),5-氟尿嘧啶[国药准字 H20051626,规格:0.25 g(以氟尿嘧啶计),海南中化联合制药工业股份有限公司]组成的FOLFOX6方案,方法具体如下:奥沙利铂130 mg/m2溶于5%萄糖溶液(500 ml),静脉滴注4 h,第1天;亚叶酸钙200 mg/m2予以静脉注射,时间>3 min;5-氟尿嘧啶400 mg/m2静脉注射,第1天,之后2 400~3 000 mg/m2,连续46 h。口服阿帕替尼850 mg/次,1次/d,每3周为1个周期。
1.3.2 对照组 给予FOLFOX6方案化疗治疗,FOLFOX6方案同研究组,两组均治疗4个周期。
1.4 观察指标
①疾病控制率,依据实体瘤疗效标准判定,完全缓解(CR):肿瘤目标病灶消失,且持续时间≥4周;部分缓解(PR):病灶最大径缩小>30%,且持续时间≥4周;进展(PD):出现新病灶,或病灶最大径增加>20%;稳定(SD):病灶最大径介于PR与PD之间,本次将CR、PR与SD计为疾病控制率。②肿瘤标志物,采集治疗前后两组空腹静脉血5 ml,离心取上清液,冰箱冷藏待检,使用电化学发光法测定患者血清癌胚抗原(CEA)与糖链多肽抗原19-9(CA19-9)水平,采用双抗体夹心酶联免疫法检测患者血清血管内皮生长因子(VEGF)水平。③不良反应发生情况,统计两组胃肠道反应、皮肤黏膜反应、骨髓抑制、肝功能损伤、出血发生情况。④统计比较两组中位无进展生存期,无进展生存期:从治疗后开始到第一次发生疾病进展(肿瘤增长或复发病灶转移)的时间。
1.5 统计学方法
2 结果
2.1 疾病控制率
研究组疾病控制率73.81%高于对照组46.34%(P<0.05)。详见表1。
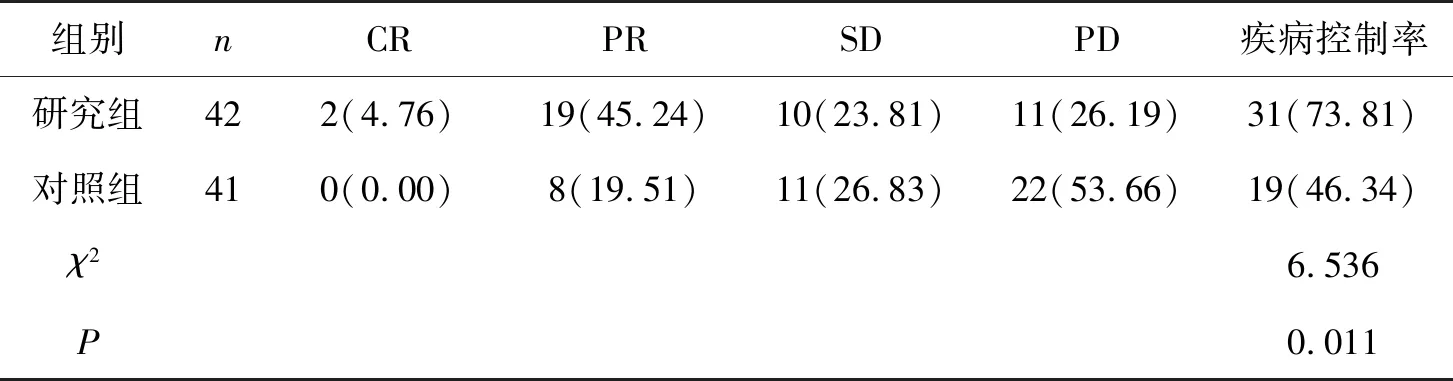
表1 两组疾病控制率比较(n,%)
2.2 肿瘤标志物
治疗前两组血清CA19-9、CEA及VEGF水平比较无显著差异(P>0.05);治疗后研究组血清CA19-9、CEA及VEGF水平低于对照组(P<0.05)。详见表2。
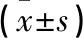
表2 两组肿瘤标志物水平比较
2.3 不良反应
两组不良反应(胃肠道反应、皮肤黏膜反应、骨髓抑制、肝功能损伤、出血)发生率比较无显著差异(P>0.05)。详见表3。
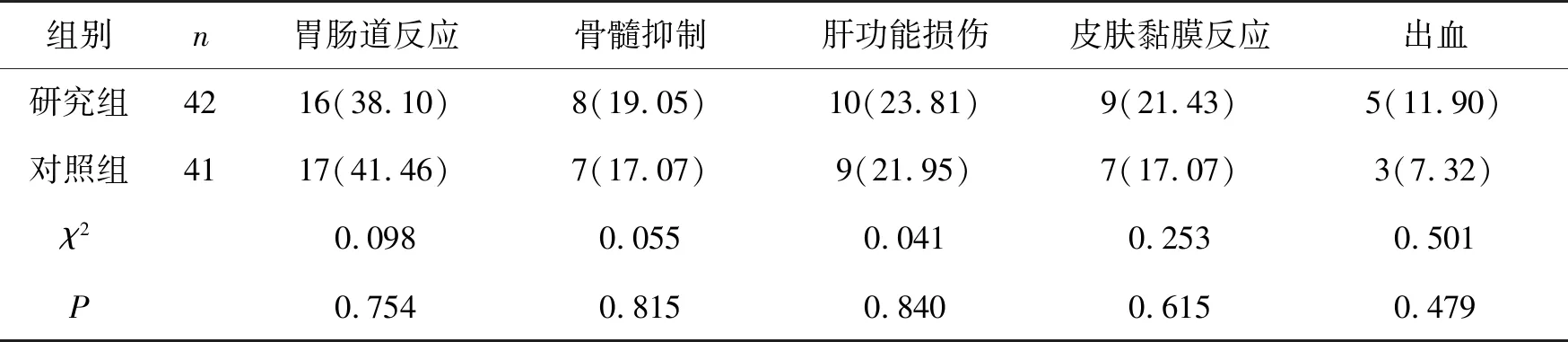
表3 两组不良反应比较(n,%)
2.4 中位无进展生存期
研究组中位无进展生存期为10.5个月,长于对照组8.5个月(P<0.05)。
3 讨论
由于胃癌早期症状与慢性胃炎、胃溃疡等疾病相似,常被忽略或误诊,常在患者胃癌发展到晚期,出现较为频繁与严重的症状时才被发现。对于失去手术治疗的晚期胃癌患者,化疗是其主要治疗方法,虽然有较高的不良反应发生,但其在延缓肿瘤进展上有着不可替代的地位,其中FOLFOX6方案是临床常用的典型化疗方案,可延长患者生存时间,但整体疗效有待提高[4]。
经临床研究发现,肿瘤生长与转移主要依赖新生血管生成,可通过抑制肿瘤新生血管生成以阻碍肿瘤进展,此类靶向治疗成为近年实体瘤治疗研究的热点[5]。阿帕替尼是我国研发的具有自主产权的小分子靶向抗血管生成药物,作用靶点主要是血管内皮生长因子受体-2(VEGFR-2),通过阻碍丝裂原活化蛋白激酶活化,来抑制血管内皮细胞增殖,从而发挥抗肿瘤作用[6]。本研究将阿帕替尼联合FOLFOX6方案化疗应用于晚期胃癌患者,结果发现,研究组疾病控制率高于对照组,无进展生存期长于对照组(P<0.05),说明在奥沙利铂、5-氟尿嘧啶、亚叶酸钙共同作用下可发挥协同抗肿瘤作用,加上阿帕替尼靶向阻止VEGFR-2磷酸化与下游信号传导,针对性阻碍新血管形成,联合起效,提高疾病控制率,延长患者生存时间。另外,本研究通过统计两组不良反应发现,两组不良反应发生率比较无显著差异(P>0.05),提示加用阿帕替尼并未增加患者不良反应发生率,与化疗药物不同,阿帕替尼毒副作用相对较轻,其出现的不良反应对症处理或暂停给药,便可得到缓解,靶向针对治疗,安全有效。
VEGF主要是肿瘤基质细胞与肿瘤细胞分泌,当肿瘤进展时,营养肿瘤的血管异常活跃,VEGF水平上升,促进肿瘤新生血管生成,尤其在晚期胃癌中VEGF呈异常高表达;而CA19-9是大分子特异性糖蛋白抗原,CEA是内胚层细胞分化的酸性糖蛋白,两者均为常见消化系统肿瘤标志物,在晚期胃癌中异常增高[7-8]。应用阿帕替尼联合FOLFOX6方案化疗后,血清CA19-9、CEA及VEGF水平低于对照组(P<0.05),说明本研究方案可有效降低晚期胃癌患者肿瘤标志物,FOLFOX6方案化疗阻碍肿瘤进展与阿帕替尼靶向阻断癌肿血管异生的作用联合,从而明显降低肿瘤标志物生成。
综上所述,对晚期胃癌患者应用阿帕替尼联合FOLFOX6方案化疗治疗,可提高疾病控制率,降低血清肿瘤标志物水平,进而延长无进展生存期,且未增加不良反应发生率,值得推广。
