安罗替尼与安维汀分别联合化疗治疗非鳞状非小细胞肺癌的疗效及安全性
2021-01-09蒙冲董文黄奕江刘凯
蒙冲 董文 黄奕江 刘凯
肺癌是全球范围内常见、致死率较高的恶性肿瘤之一,其患病率多年来始终位居国内男性恶性肿瘤榜首,长期吸烟、慢性肺部疾病及职业高危因素均与疾病发生发展密切相关[1]。根据生物学特征、临床治疗与预后情况,WHO将其分为非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC),前者约占所有肺癌的85%以上,又可分为非鳞状细胞癌(腺癌、大细胞癌及其他类型)和鳞状细胞癌(表皮癌等),其中非鳞状NSCLC发病率最高[2]。目前,对于局部晚期(ⅢA、ⅢB期)或晚期(Ⅳ期)NSCLC患者常采用培美曲赛、顺铂等一线药物化疗以延长生存期,但化疗疗效仍有限,且个体差异较大[3-4]。盐酸安罗替尼为我国自主研发的用于治疗晚期或转移性NSCLC的创新药物,属于多靶点受体酪氨酸激酶抑制剂,对血管形成相关的激酶[如血管内皮生长因子(VEGF)受体(VEGFR)、血小板衍生生长因子受体(PDGFR)、表皮生长因子(EGF)受体(EGFR)及其他与肿瘤细胞增殖相关的激酶如干细胞因子(c-Kit)、间质-上皮细胞转化因子(Met)等]有显著的抑制作用[5-6]。2018年5月盐酸安罗替尼通过国家药品监督管理局审评上市后引起广泛关注,但临床应用报道较少。本研究选择与安罗替尼有类似生物学作用的安维汀为对照,分析安罗替尼联合培美曲赛、顺铂一线治疗非鳞状NSCLC的疗效与安全性,以期为新药安罗替尼的临床应用及相关治疗提供依据。
对象与方法
1.对象:纳入2018年6月~12月于我院接受化疗的72例非鳞状NSCLC患者。纳入标准:(1)常规胸部CT检查显示肺内肿块,通过细胞学检验和病理检查证实为非鳞状NSCLC,即病理类型为腺癌或大细胞癌;(2)符合2015年国际肺癌研究学会(IASLC)颁布的肺癌TNM分期标准[7]中ⅢA期、ⅢB期、Ⅳ期的相关要求;(3)预估生存期>3个月;(4)功能状态(PS)评分≤4分;(5)临床检查、化疗及采血配合度良好。排除标准:(1)病理检查明确的鳞癌或非NSCLC;(2)入选前即已接受过放化疗、中药治疗等综合治疗;(3)对本研究化疗方案不耐受;(4)合并严重的慢性感染、肺部感染、肺水肿;(5)合并其他恶性肿瘤;(6)严重的血液疾病及肝肾功能不全;(7)合并严重心血管疾病、意识模糊、肢体功能障碍。按入院顺序编号后采用随机数表法将其分为安罗替尼组和安维汀组,各36例,其中安罗替尼组男21例,女15例,年龄43~75岁,中位年龄64岁,BMI 18~26 kg/m2,平均BMI(23.32±2.05)kg/m2;腺癌26例,大细胞癌10例;ⅢA期10例、ⅢB期14例、Ⅳ期12例;长期吸烟20例。安维汀组男18例,女18例,年龄42~77岁,中位年龄65岁,BMI 18~25 kg/m2,平均BMI(23.09±1.99)kg/m2;腺癌24例,大细胞癌12例;ⅢA期8例、ⅢB期16例、Ⅳ期12例;长期吸烟22例。两组患者上述基线资料比较差异均无统计学意义(P>0.05)。本研究经我院伦理委员会审核批准,所有患者及家属均签署知情同意书。
2.方法
(1)化疗方法:所有患者化疗前1天针对性实施保肝(还原性谷胱甘肽)、保护胃黏膜(泮托拉唑)治疗,必要时给予补充维生素;化疗前30 min给予5-羟色胺3受体拮抗剂、地塞米松以控制或减轻化疗引起的胃肠道反应。安罗替尼组患者给予盐酸安罗替尼胶囊(国药准字H20180004,正大天晴药业集团股份有限公司)口服,每次12 mg,每天1次,连续服药2周后停药1周;于治疗第1天同时给予培美曲塞(国药准字H20123010,上海凯茂生物医药有限公司)500 mg/m2加生理盐水100 ml静脉滴注(滴注时间30 min内),第3天给予顺铂(国药准字H20073652,齐鲁制药有限公司)75 mg/m2加5%葡萄糖溶液500 ml静脉滴注(滴注时间2 h内)。安维汀组患者于第1天给予安维汀[贝伐珠单抗,注册证号:S20120068,德国Roche Pharma(Schweiz)Ltd.公司]7.5 mg/kg加生理盐水250 ml静脉滴注,于治疗第1天同时给予培美曲塞、第3天给予顺铂静脉滴注,剂量和周期同安罗替尼组。两组均以21天为1个治疗周期,均治疗2个周期后评价疗效,若治疗期间血红蛋白<80 g/L,则予以输注悬浮红细胞。
(2)疗效评估:治疗2个周期后参考1.1版实体瘤疗效评价标准[8]判断疗效,分为4个等级,目标病灶消失为完全缓解(CR),基线病灶长径总和至少缩小30%为部分缓解(PR),介于PR与疾病进展(PD)之间为疾病稳定(SD),基线病灶长径总和至少增加20%为疾病进展(PD),治疗有效率(RR,%)=(CR+PR)/总例数(100%),疾病控制率(DCR,%)=(CR+PR+SD)/总例数(100%)。
(3)观察指标:治疗前、治疗2个周期后采集所有患者清晨空腹外周静脉血5 ml,以3 000 r/min离心15 min(离心半径15 cm)后取上层血清于-20 ℃冰箱冷冻储存待检。采用酶联免疫吸附试验检测血清血管VEGF、EGF水平。治疗2个周期后根据欧洲癌症治疗研究组织(EORTC)生存质量核心量表(QLQC30)[9]评估患者的生存质量,包括情绪、认知、疼痛、呼吸及疲劳5个方面的内容。
(4)安全性评价:每天观察记录患者症状、体征,复查血生化、血常规,依据美国国立癌症研究所常见毒性标准(CTCAE)[10]评估治疗期间患者不良反应的发生情况。

结 果
1.两组患者临床疗效比较:两组患者的RR比较差异无统计学意义(41.67%比30.56%,χ2=0.963,P=0.326),但安罗替尼组患者的DCR高于安维汀组(75.00%比52.78%,χ2=3.853,P=0.049)。见表1。

表1 两组患者临床疗效比较[例,(%)]
2.两组患者治疗前后血清VEGF、EGF水平比较:两组患者治疗前血清VEGF、EGF水平比较差异均无统计学意义(P>0.05)。两组患者治疗后血清VEGF、EGF水平均低于同组治疗前(P<0.05),且治疗后安罗替尼组患者血清VEGF、EGF水平均低于安维汀组(P<0.05)。见表2。
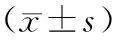
表2 两组患者治疗前后血清VEGF、EGF水平比较
3.两组患者治疗前后生存质量比较:两组患者治疗前情绪、认知、疼痛、呼吸、疲劳评分比较差异均无统计学意义(P>0.05)。安罗替尼组患者治疗后认知、疼痛、呼吸评分低于同组治疗前(P<0.05),而安罗替尼组患者治疗前后情绪、疲劳评分比较差异均无统计学意义(P>0.05)。安维汀组患者治疗后情绪、认知、疼痛、呼吸评分低于同组治疗前(P<0.05),而安维汀组患者治疗前后疲劳评分比较差异无统计学意义(P>0.05)。治疗后安罗替尼组患者情绪评分高于安维汀组,疼痛、疲劳、呼吸评分均低于安维汀组(P<0.05),而治疗后两组患者认知评分比较差异无统计学意义(P>0.05)。见表3。
4.两组患者不良反应发生情况比较:两组患者治疗期间骨髓抑制、肝功能异常、胃肠道反应、出血或血栓发生率比较差异均无统计学意义(P>0.05)。除安维汀组患者出现Ⅲ级胃肠道反应、Ⅲ级骨髓抑制各1例外,安罗替尼组及安维汀组患者其余不良反应均为Ⅰ~Ⅱ级。见表4。

表3 两组患者治疗前后生存质量比较(分,
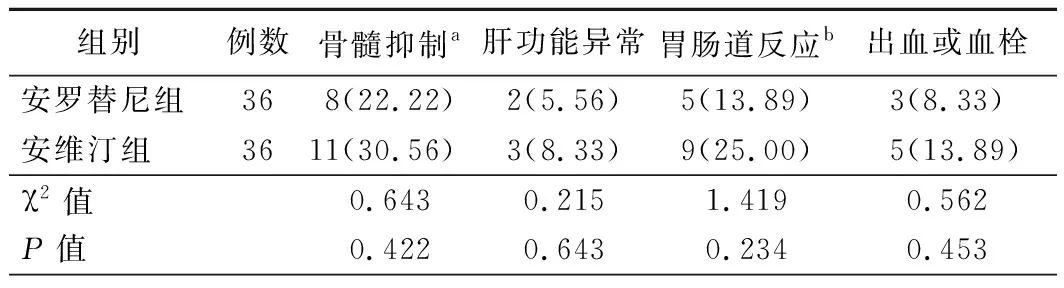
表4 两组患者不良反应发生情况比较[例,(%)]
讨 论
无论是晚期NSCLC或非NSCLC,还是晚期肺鳞癌或腺癌,治疗都应以化疗为主,尤其多种化疗药物联用(目前多主张含铂的多药联合化疗)能明显延长患者的生存期,提高其生存质量。顺铂主要通过抑制DNA复制而产生抗肿瘤活性,因具有广谱抗肿瘤活性而成为临床常用一线药物[11]。培美曲塞属于叶酸抑制剂,可通过抑制多种酶如胸苷酸合酶、二氢叶酸还原酶等参与嘌呤、嘧啶的合成,从而能够多靶点、多方位抑制肿瘤细胞的生长,故逐渐成为治疗肺腺癌的首选药物[12]。但以铂类为基础的化疗方案几乎无法避免不良反应,且通常多种化疗药物联用的不良反应问题更为突出[13],加之目前尚无指南明确指出何种铂类联合化疗方案更具优势,因此,肺癌治疗方案的探索仍在进行中,三线药物的应用也逐渐引起临床的关注。
安维汀是针对VEGF的重组人源化单克隆IgG1抗体,可降低VEGF表达并阻断VEGF促进肿瘤血管生成的生物学作用;同时,对于NSCLC,应用安维汀能够提升化疗药物到达肿瘤细胞的浓度,促进肿瘤血管正常化[14]。安罗替尼是一个多靶点的受体酪氨酸激酶抑制剂,而酪氨酸激酶信号通路与肿瘤细胞的增殖、分化、迁移密切相关,故安罗替尼可通过干扰或阻断该信号通路而实现抑制肿瘤细胞生长的作用[15]。安罗替尼为新上市的三线药物,虽然关于其的临床研究尚不多见,但已有越来越多的研究证实其对血管形成相关激酶[如VEGFR、成纤维细胞生长因子受体(FGFR)、PDGFRα/β、c-Kit、转导重排基因(Ret)等]的抑制作用突出[16]。基于我院病例实际,本研究以72例晚期非鳞状NSCLC患者作为研究对象,结果显示,两组患者RR比较差异无统计学意义,但安罗替尼组DCR高于安维汀组,提示安罗替尼联合一线药物治疗非鳞状NSCLC的临床疗效优于安维汀,可有效控制肿瘤进展。辛涛等[17]的研究结果显示,与安慰剂组比较,安罗替尼治疗晚期NSCLC的疗效及安全性均更突出,认为安罗替尼可作为多线化疗失败及难治性NSCLC患者新的治疗选择。苏雨栋等[18]详细报道了1例应用安罗替尼治疗晚期肺腺癌的效果,结果显示,安罗替尼对延长患者的总生存期和无进展生存期有显著助益。本研究结果显示,治疗后安罗替尼组患者血清VEGF、EGF水平均低于安维汀组,情绪评分高于安维汀组,疼痛、疲劳、呼吸评分低于安维汀组,表明应用安罗替尼可有效降低血清VEGF、EGF水平,提高患者生存质量,这与安罗替尼突出的抗肿瘤血管生成、抑制肿瘤生长作用密不可分。VEGF、EGF可反映人体血管内皮细胞迁移、增殖、分裂及血管通透性情况,与血管生成、肿瘤迁移的关系尤为密切。既往研究结果显示,VEGF、EGF表达水平与癌组织增殖程度、侵袭能力呈正相关[19]。故进一步推断降低血清VEGF、EGF水平可能为安罗替尼辅助治疗非鳞状NSCLC疗效可观的重要原因。此外,Han等[20]对来自中国13个医学临床中心的117例符合条件的NSCLC患者进行分析,发现与安慰剂组比较,安罗替尼组患者的RR更高,中位无进展生存期(4.8个月比1.2个月)、中位总生存期(9.3个月比6.3个月)更理想,由此认为安罗替尼作为三线治疗药物可带给NSCLC患者显著的生存获益,且毒性曲线也显示出良好的耐受性。因安罗替尼上市时间不长,本院最早应用该药的时间为2018年6月,且目前大部分患者仍在随访中,其生存情况数据尚未统计完全,故安罗替尼对相关非鳞状NSCLC患者生存及远期预后的影响将在后期补充论证。
在安全性方面,有学者认为安罗替尼作用于FGFR、VEGFR等靶点的半数抑制浓度值较低,加之给药方式为口服,推荐剂量为12 mg/d,服用2周后停药1周,通常耐受性更好,无显著不良反应[21]。本研究治疗期间两组患者骨髓抑制、肝功能异常、胃肠道反应、出血或血栓发生率比较差异均无统计学意义,可能与本研究入选样本量轻较小有关。但值得关注的是,安维汀组出现Ⅲ级胃肠道反应、Ⅲ级骨髓抑制各1例,而安罗替尼组不良反应均为Ⅰ~Ⅱ级,提示安罗替尼的安全性尚可。由此可见,应用安罗替尼联合培美曲赛、顺铂化疗治疗非鳞状NSCLC的临床疗效可观,安全性尚可,具有推广价值,但相关结论及此药的优势人群选择仍有待扩大样本量、多中心的研究深入分析。
