门脉高压症少见病因的影像学分析
2021-01-09颜荣华
颜荣华
门脉高压症(PH)是由各种原因引起的门静脉系统血流受阻和(或)血流量增加导致压力增高的一组综合征,根据压力来源的解剖部位可分为肝前性、肝内性及肝后性,病因多样。部分少见原因引起的PH临床表现复杂,个体差异显著,也可能与常见的病毒性肝炎等其他获得性肝损伤重叠发生,常规的病史询问、体格检查和实验室检查缺乏特异性。肝脏组织病理检查是诊断PH的“金标准”,但其为有创检查,部分患者存在穿刺活检禁忌证,且结果可能出现“假阴性”或异常原因不明。影像学诊断则相对简单,门静脉主干内径≥13 mm、脾静脉内径≥10 mm可提示门脉高压。对于原因不明的PH患者,无创的影像学检查联合生化检测、酶学分析等可缩小诊断范围,指明诊断方向,为进一步肝脏组织病理活检及基因检测提供依据,对其确诊具有重要价值,可用于病情评估和疗效评价。为了更有针对性地分析病因,本文根据不同类型PH的影像学特点,重点关注肝脏改变、血管病变、侧支循环开放特点及其他间接或继发征象,探讨其诊断和鉴别诊断要点,以供临床医生参考。
一、影像学检查方法的选择
肝脏疾病的无创影像学检查技术主要包括超声、CT和MRI等。超声检查常被视为疾病筛查的首选方法,具有廉价、快速、能实时动态观察肝脏血流动力学改变等优点,超声弹性成像可作为评估肝纤维化的无创检查手段,但易受腹腔积液、肠气干扰,软组织分辨率较低,定性诊断常需进一步检查。CT检查被认为是肝脏疾病的一线检查技术,其扫描速度快、密度分辨率高、对高密度病变(钙化、急性出血、阳性结石、骨性结构等)显示清晰,CT血管成像(CTA)对肝内血管结构显示具有优势,缺点是有电离辐射、骨骼和金属伪影及碘对比剂过敏风险。MRI为多参数、多序列、多平面成像模式,软组织解剖分辨率高,对微小病变的检出最敏感,随着MRI新技术和对比剂的迅速发展,能同时提供解剖和功能信息,实现定性诊断和定量检测:磁共振胰胆管成像(MRCP)可无创显示肝内外胆管完整结构和病变,诊断效能与ERCP相当,但无ERCP相关并发症风险;弥散成像(DWI)及其相关衍生技术可用于鉴别肝胆良恶性病变,能更灵敏地显示细胞水肿,有望在形态学变化前发现早期肝纤维化[1];使用肝胆特异性对比剂增强检查能帮助鉴别肝脏良恶性病变、对肝纤维化进行量化分期、无创评价肝脏功能[2],对于胆道术后或MRCP显示欠佳的患者,基于肝胆特异期的增强胆道成像(CE-MRCP)还能辅助显示胆管解剖结构和通畅情况;MRI定量序列(IDEAL-IQ、mDIXON-Quant等)可无创、准确检测全肝脂肪和铁含量,与肝脏组织病理活检结果一致性好,重复性高,已被越来越多地用于肝脏弥漫性病变的早期诊断、病情评估和疗效监测;磁共振弹性成像(MRE)可绝对定量测量肝、脾的弹性值,是目前无创量化分析组织硬度最准确的手段,与肝纤维化病理分期呈显著正相关,能准确评估不同类型肝纤维化程度,已被认为可取代肝脏病理组织活检,与食管胃底静脉曲张程度(反映门脉高压程度)也具有正相关性[3]。但MRI的缺点是扫描时间长,且体内金属植入、幽闭恐惧症患者检查受限。总之,超声、CT、MRI技术,尤其是CT、MRI的恰当应用将有助于肝脏疾病的正确诊断。
二、不同类型PH的影像学特点
(一)肝内性PH:最为常见,主要是由肝内门静脉和(或)肝内小静脉(肝窦)梗阻所致,多见于肝炎后肝硬化、酒精性肝病、非酒精性脂肪肝和胆道梗阻继发的胆汁性肝硬化等,其少见原因包括肝脏血管性病变、遗传代谢性肝病、自身免疫性肝病及系统性疾病累及肝脏等。
1.肝脏血管性病变
(1)肝窦阻塞综合征(SOS):又称肝小静脉闭塞病,是以肝窦、肝小静脉和小叶间静脉内皮细胞损伤导致管腔狭窄闭塞,引起肝淤血、肝损伤和门脉高压为特征的肝脏非血栓性血管性疾病。病因包括服用含吡咯烷生物碱的中草药(土三七等)、使用奥沙利铂等化疗药物、造血干细胞移植及肝移植等。临床上该病患者起病突然,病情较重,且肝内病变分布不均,可导致穿刺活检出现假阴性;患者服用中草药成分复杂,含吡咯烷生物碱情况有时难以确定,因此影像学诊断价值高。CT、MRI表现包括以下方面:①肝脏改变:肝弥漫性肿大,肝叶比例协调,尾状叶增大不明显,肝淤血,增强扫描呈特征性的“地图样”强化,或以第二肝门为中心沿3支肝静脉呈“爪状”渐进性强化,延迟期更明显[4]。②血管病变:肝静脉模糊、狭窄、显示不清,下腔静脉肝内段受压变细,管腔旁见低强化;门静脉周围T2加权像(T2WI)高信号水肿带;肝动脉可代偿性增粗。③侧支循环开放特点:食管-胃底静脉曲张发生率低,程度轻[5]。④间接或继发征象:脾脏增大程度轻,大量腹腔和胸腔积液、胆囊壁水肿和胃肠壁水肿等(图1)。主要与布-加综合征鉴别诊断。
(2)特发性PH(IPH):细小门静脉分支非特异性炎症引起血管纤维化及狭窄、闭塞,导致肝内窦前性门静脉血流阻力增大及以门脉高压、脾脏显著增大和脾功能亢进为特征的慢性肝病综合征,但不发生肝硬化,肝功能或无明显异常,预后良好。影像学检查的作用主要在于证实门静脉和肝静脉通畅,评价有无门脉高压,排除导致肝硬化或非肝硬化性PH的其他常见疾病。CT、MRI表现包括以下方面:①肝脏改变:早期基本正常,肝硬化表现轻,晚期包膜下肝实质萎缩,可出现局灶性结节样改变,但无尾状叶肥大和左内叶萎缩。②血管病变:相对具有特征性,肝静脉、门静脉大分支和属支通畅,门静脉肝内二、三级小分支狭窄、闭塞,肝外门静脉管壁增厚、钙化,晚期血栓形成[6];约1/3患者可出现门静脉周围T2WI信号增高,提示纤维化和异常新生血管生成[7]。③侧支循环开放:食管-胃底静脉曲张,部分患者门静脉主干通畅却发生海绵样变性。④间接或继发征象:脾脏显著增大,硬度明显增加,程度远超肝硬化[8];脾内多发Gamna-Gandy小体,即铁质沉着性结节(图2)。这些影像学表现可帮助IPH与其他常见原因所致肝硬化相鉴别。
2.遗传代谢性肝病
(1)先天性肝纤维化(CHF):一种少见的常染色体隐性遗传病,以儿童及青少年发病为主,由于肝组织大量纤维化,导致肝内血流阻力增加,引起门脉高压,病变可累及门静脉、肾脏和肝内胆管等多器官。其临床特点是肝纤维化、门脉高压,而肝功能受损较轻,可伴肾功能损害。CT和MRI表现包括以下方面:①肝脏改变:早期肝脏形态可正常,随着病情进展,出现肝硬化,出现形态异常,肝右叶萎缩,尾状叶及肝左外叶肥大,左内叶正常或肥大。相对特征性的改变是肝内胆管扩张,部分呈囊状,MRCP显示囊性病变与扩张的胆管相通,胆管扩张的程度随肝功能受损的程度而变化。②血管病变:肝内门静脉分支受压、减少、纤细;肝动脉增粗、迂曲。③侧支循环开放特点:食管-胃底静脉曲张明显,脾肾分流。④间接或继发征象:超过50%的患者可见肾脏病变,包括多囊肾、髓质海绵肾、肾结石、脾脏增大(图3)。由于CHF临床症状缺乏特异性,若影像学检查结果同时出现上述肝脏、胆管、肾脏病变及PH,而肝功能受损轻,则有助于CHF的诊断。鉴别诊断包括:①肝硬化性PH:肝硬化表现更重,合并肝功能异常,无胆管和肾脏囊性病变。②Caroli病:肝内多发大小不等囊性病变,与胆管相通,增强扫描可见囊内点状强化,即“中心点征”。③胆管错构瘤:少见的小叶间胆管畸形,好发于老年女性,肝内弥漫性粟粒状小囊性病变,呈“满天星”样,可融合,与胆管树不相通,MRCP可帮助鉴别。
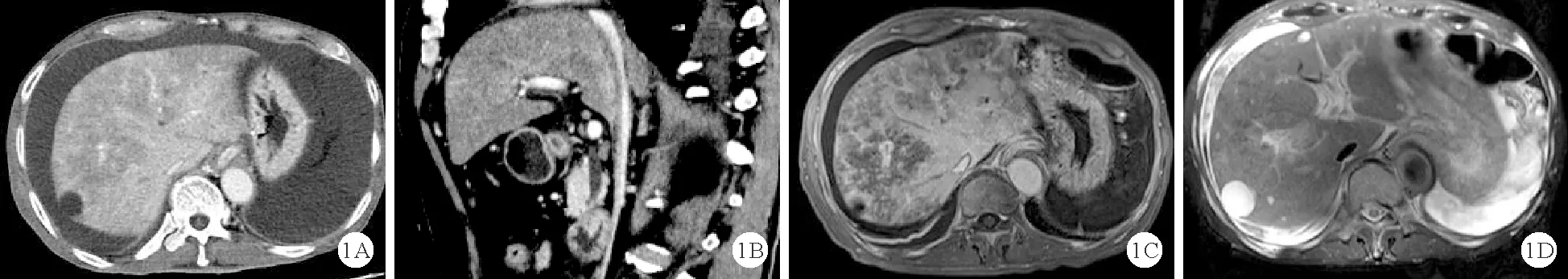
图1 25岁男性SOS患者影像学表现:A:CT增强扫描结果显示肝淤血、肝硬化,肝实质“地图样”强化,沿3支肝静脉“爪状”分布,肝静脉显示不清;食管-胃底静脉曲张轻;B:CT增强扫描结果显示下腔静脉肝内段受压、变细,周围见低强化;C:MRI增强扫描结果显示肝淤血,肝实质异常强化与CT类似;D:MRI T2WI示门静脉周围高信号水肿带

图2 65岁女性IPH患者CT影像学表现:PH,门静脉主干增宽,食管下段-胃底静脉、胃冠状静脉重度曲张,脾静脉曲张,附脐静脉开放,巨脾;门静脉及其属支、肝静脉、下腔静脉通畅,肝硬化改变轻(A、B:横断面;C、D:冠状面)
(2)肝豆状核变性(HLD):我国最常见的遗传性肝病,是少数可治疗的PH病因之一。游离铜离子在肝细胞大量蓄积引起肝细胞肿胀、坏死和小叶中心静脉周围纤维组织增生,晚期表现为间质纤维化和坏死后肝硬化。肝型HLD CT及MRI表现包括以下方面:①肝脏改变:早期肝脏肿大,右肝增大为主;脂肪肝,CT平扫示肝实质密度减低,MRI肝实质脂肪含量增高(>5%);典型表现是结节性肝硬化,肝内多发大小不等、直径1~3 cm的再生结节,在低密度脂肪肝背景上,CT平扫结节呈稍高密度,MRI呈T2WI低、T1WI等稍高信号,CT或MRI增强扫描无异常强化。②血管病变:门静脉直径增宽。③侧支循环开放特点:程度较轻。④间接或继发征象:颅脑MRI双侧豆状核对称性异常信号。HLD影像学表现不具有更多特异性,但对于年轻患者,出现原因不明的肝脏、脾脏增大和其他慢性肝病表现,在排除肝炎感染和自身免疫性病变后,若影像检查发现脂肪肝或结节性肝硬化,即使双侧豆状核改变不典型,仍需注意该病可能。
3.自身免疫性肝病
(1)原发性胆汁性肝硬化(PBC):一种慢性进行性胆汁淤积性肝病,病理改变为肝内肉芽肿、小叶间和胆管的破坏性炎症。好发于40岁左右的女性,临床症状包括肝功能损害、皮肤瘙痒、进行性黄疸,PH发生率高,易发展为胆汁性肝硬化。PBC的CT检查结果可显示肝硬化,但与其他类型肝硬化差别不大。MRI诊断价值高,特异性征象包括以下方面:①肝脏改变:肝脏肿大;MRCP肝内胆管多发狭窄,走行僵直,肝内2~3级胆管显示不清,与PBC淤胆、胆汁分泌减少有关。②血管病变:肝内门静脉周围“晕征”,T1WI和T2WI均呈低信号,病理基础是门静脉周围肝细胞坏死;肝外门静脉周围T2WI高信号,提示门静脉周围炎性水肿;上述征象是PBC高度特异性表现,分别出现于66.7%和72.7%的患者[9]。③侧支循环开放特点:PH表现,门-体静脉侧支开放。④间接或继发征象:脾脏增大;腹腔淋巴结增大,与自身免疫功能紊乱、门脉高压有关;胆囊壁水肿、增厚。典型的MRI表现结合患者临床症状和血液中抗线粒体抗体(AMA)阳性,需考虑PBC,但最终确诊有赖于病理组织穿刺活检结果。
(2)原发性硬化性胆管炎(PSC):一种慢性胆汁淤积性肝病,病理改变为胆管进行性增生性炎症和纤维化,肝内外胆管均可受累,导致胆管的狭窄及肝脾肿大,可发展为胆汁性肝硬化、PH及肝衰竭,临床上多见于25~45岁男性。常见症状有黄疸、乏力、皮肤瘙痒,PSC根据病变部位分为肝内型(最常见)、肝外型和混合型(肝内外胆管均受累)。MRI和MRCP检查是诊断PSC最主要手段,可观察胆管狭窄的部位、程度,随访PH和胆管癌的发生,其表现包括以下方面:①肝脏改变:不同程度肝硬化,肝叶体积缩小,尾状叶肥大,肝实质局灶性异常高灌注,晚期会出现肝硬化结节;典型表现是MRCP胆管“串珠状”改变[10],即胆管多节段或弥漫性胆管狭窄,其间胆管正常或继发性扩张,可呈憩室样,伴胆管壁向心性增厚,可达3~4 mm,明显持续性强化;小胆管闭塞导致肝内胆管分支减少,较大胆管狭窄、僵直似“枯枝”状,称为“剪枝征”;肝外胆管病变表现类似。②血管病变:门静脉周围水肿,T2WI呈高信号,门静脉周围淋巴结增大。③侧支循环开放特点:PH表现。④间接或继发征象:约20%的PSC患者可并发胆管癌,60%~80%的PSC患者可伴发炎性肠病(IBD),以溃疡性结肠炎多见[11](图4)。对于临床疑似PSC的患者应首先行MRI及MRCP检查,排除由胆道手术、缺血、结石、损伤导致的继发性硬化性胆管炎及IgG4相关性硬化性胆管炎、寄生虫感染等,不能确诊时可考虑行组织穿刺病理活检。
4.系统性疾病累及肝脏
(1)肝结节病:结节病是一类发病机制未知的多系统肉芽肿增生性疾病,肺结节病最为常见,肝结节病相对少见。其病理特征是非干酪性肉芽肿在门静脉周围发展,引起门静脉周围纤维化、肝硬化,从而导致PH。CT、MRI表现包括以下方面:①肝脏改变:肝肿大,肝脏弥漫性小结节,门静脉周围分布为主,直径从数毫米至1~2 cm不等,CT平扫呈低密度,MRI呈斑片状、结节状异常信号,活动期T2WI呈高信号,DWI高信号,CT及MRI增强扫描呈低强化,还可出现大的再生结节和外周实质萎缩。②血管病变:MRI可见门静脉周围T2WI高信号。③侧支循环开放特点:晚期有PH表现。④间接或继发征象:脾脏增大,脾脏弥漫性多发结节,与肝内病变类似。鉴别诊断要首先排除肝脏原发和继发肿瘤,及肝结核、炎性假瘤等肉芽肿性病变,若患者胸部CT同时有肺结节病表现,则有助于本病的诊断。

图3 8岁女性CHF患者MRI影像学表现:A:T2WI示肝内胆管扩张,部分呈囊状;B:MRCP示肝内病变与胆管相通;C:T1WI增强扫描示门静脉分支纤细;D:T1WI增强扫描示PH,巨脾,食管-胃底静脉重度曲张;E:T1WI增强扫描示双侧肾脏多发小囊性病变

图4 20岁男性PSC患者影像学表现:A:MRCP示肝内外胆管多节段性狭窄,呈“串珠状”改变,肝内胆管分支僵直,呈“剪枝征”;B、C:MRI T1WI增强扫描示肝内外胆管壁增厚、明显强化
(2)肝脏淀粉样变:淀粉样变是淀粉样物质在多脏器细胞间的沉积,肝脏淀粉样变临床表现多样,误诊率较高。CT主要表现为肝脏弥漫性肿大、密度减低,类似脂肪肝的表现,增强不明显,伴或不伴广泛性钙化,肝内血管不受累、移位。可伴PH的表现,如食管、胃底静脉曲张和腹腔积液等。影像学表现和实验室检查缺乏特异性,若合并心肌、肾脏等其他部位的淀粉样改变,则有助于该病的诊断。确诊需依靠病理学检查结果,但若影像学检查发现患者肝脏明显肿大,肝包膜紧张,有引发肝破裂或出血风险,在肝脏穿刺活检时应慎重[12]。
(二)肝前性PH:约占PH的10%,是由于肝外门静脉及属支阻塞或狭窄导致,多继发于肝硬化或腹部恶性肿瘤的门静脉栓子形成,但无肝病基础的血管病变,如门静脉系统血栓形成(PVT)、门静脉海绵样变性、区域性PH、肝动脉-门静脉瘘等不容忽视。
1.PVT:血液高凝状态、炎症(克罗恩病、憩室炎、阑尾炎等)、损伤等是非肝硬化PVT的主要病因,可导致肝瘀血、肝细胞损伤及PH,甚至导致肠缺血坏死、梗阻。影像学检查需要区分有无肝硬化基础、发现恶性肿瘤、确定血栓形成时间(急/慢性)和内脏肠系膜静脉血栓范围,是评估预后和指导治疗决策的关键。CT、MRI表现包括以下方面:①肝脏改变:可无明显异常。②血管病变:急性期PVT血管管径增宽,CT平扫示腔内密度增高,超过正常血管;门静脉系统中若出现气体,强烈提示门静脉炎;MRI急性期(<24小时)、亚急性期(2~14天)血栓为T1WI、T2WI高信号,流空信号消失;慢性期血栓(15天以上)为T1WI混杂信号、T2WI低信号,提示血栓机化、钙化及血管再通,增强检查为血管腔内充盈缺损,血管壁“轨道样”强化。可累及肠系膜静脉、脾静脉。③侧支循环开放特点:食管胃底静脉曲张,慢性期广泛侧支循环形成。④间接或继发征象:与血栓部位和程度有关,如累及肠系膜上静脉可引起小肠壁水肿、强化减低,提示肠缺血;肠系膜水肿、渗出;肠壁菲薄呈纸样,肠壁、肠系膜积气,提示肠坏死。鉴别诊断主要包括门静脉癌栓,若有肝硬化背景、甲胎蛋白等肿瘤标志物水平增高,出现栓子强化、新生血管生成、肝动脉-门静脉瘘、栓子附近有肿块时,需注意癌栓可能。
2.门静脉海绵样变:血栓形成6天以上即可导致门静脉海绵样变,CT和MRI表现包括以下方面:①肝脏改变:原发性门静脉海绵样变患者肝脏形态多数正常,肝实质可出现动脉期异常高灌注灶。②血管病变:门静脉行程区结构紊乱,正常门静脉结构闭塞、消失,肝内分支变细、减少。③侧支循环开放的特点:门静脉引流区及门-体分流区广泛侧支血管,门静脉、胆囊窝、胆管周围迂曲、扩张的侧支静脉和血管团,具有特征性。④间接或继发征象:胆总管不规则、波浪状受压、管腔变窄,近段胆管可轻度扩张,当继发胆管周围纤维化时,胆管壁不规则增厚,范围较广,呈“假胆管癌征”(图5)。
3.区域性PH:又称胰源性PH、左侧PH,是极少数可治愈的PH之一。脾静脉或其属支狭窄、闭塞,回流障碍,导致门静脉系统的压力增高。主要病因是胰腺病变(约占90%),包括急慢性胰腺炎、体尾部癌、假性囊肿、胰腺手术等,少见原因包括脾血管性病变和腹膜后炎症、肿瘤、特发性纤维化等。CT和MRI表现具有特征性,包括以下3个方面:①肝脏改变:肝脏可无异常,肝硬化改变轻。②血管病变:脾静脉或其属支狭窄、闭塞,显示不清,而门静脉主干及肠系膜静脉管腔通畅;脾动脉可同时受累、狭窄或闭塞,导致脾脏供血异常、动脉扩张,甚至形成动脉瘤,因为本病有效的治疗手段之一是脾切除,术前CTA明确脾脏异常供血的动脉对于确定手术方案十分重要。③侧支循环开放的特点:局限性、孤立性胃底、胃周静脉重度曲张,而食管下段、肠系膜静脉曲张少见[13]。④间接或继发征象:脾脏增大显著、脾脏灌注异常;胰腺或腹膜后原发病灶等(图6)。

图5 31岁男性慢性PVT门静脉海绵样变患者CT影像学表现:门静脉、肠系膜上静脉闭塞,门静脉、胆囊窝、胆管周围可见迂曲、扩张的侧支静脉和血管团,肝内、外广泛侧支循环形成,胆丛和胆总管周围侧支血管开放,“假胆管癌征”(A、B:横断面;C、D:冠状面)
4.肝动脉-门静脉瘘:患者Glisson鞘内肝动脉和门静脉间交通支广泛开放、扩张,大量肝动脉血分流入门静脉,使其血流量增加、压力增高,引起PH。后天性肝动脉-门静脉瘘较为常见,可为先天性,包括遗传性疾病、先天性动静脉畸形和血管瘤等,其中一个罕见原因是遗传性出血性毛细血管扩张症(HHT)。HHT是常染色体显性遗传病,其病理改变为全身多部位的小血管管壁发育异常、菲薄,导致毛细血管扩张、动静脉畸形和动脉瘤,遗传性、血管畸形和出血素质三联征为其特征[14]。由于HHT患者有较高的出血风险,如非必要应避免肝脏病理组织活检,影像学检查对早期发现内脏病变、确诊疾病、预防出血并发症有重要意义。CT和CTA检查最具价值,影像学表现包括以下4个方面:①肝脏改变:肝淤血,肝窦扩张,动脉期肝实质弥漫性异常高灌注灶;长期可发展为淤血性肝硬化,再生结节或局灶性增生结节形成;胆管缺血,出现类似硬化性胆管炎改变。②血管病变:动脉期观察最佳,肝总动脉及其分支增粗、增多、迂曲,达肝脏边缘,肝固有动脉直径大于脾动脉,肝总动脉直径>7 mm、肝左和肝右动脉直径>5 mm是可靠的诊断指标[15];肝动脉-肝静脉瘘、肝动脉-门静脉瘘、动脉解剖变异,常合并肝内、外动脉瘤。③侧支循环开放特点:食管-胃底静脉曲张显著。④间接或继发征象:脾脏增大,腹腔积液;肠系膜动脉受累,导致肠缺血(图7)。鉴别诊断包括其他原因如肝硬化、血管瘤、肝细胞肝癌、多发血管畸形导致的动静脉分流。
(三)肝后性PH:肝静脉或下腔静脉肝后段梗阻、肝静脉向右心回流受阻导致,布-加综合征(BCS)是主要原因,其他还包括被动性肝淤血、缩窄性心包炎、右心衰竭等。
肝静脉主干和(或)下腔静脉肝静脉入口处到与右心房交汇处任何部位阻塞都可引起BCS,根据梗阻部位分为肝静脉型、下腔静脉型和混合型,隔膜和血栓形成是常见的病理改变。CT和CTA为本病最主要无创诊断手段,主要影像学表现包括以下4个方面:①肝脏改变:急性期肝脏肿大,慢性期其他肝叶萎缩,尾状叶肥大,肝叶比例失调;肝淤血,肝实质灌注不均,呈“扇形”,特征性中央部分强化,周边部分低强化。②血管病变:肝静脉主干和(或)下腔静脉肝后段狭窄、充盈缺损或线样低密度隔膜;副肝静脉开放。③侧支循环开放的特点:肝静脉型BCS肝包膜下肝静脉-体循环及肝内肝静脉-门静脉、梗阻-未梗阻肝静脉之间侧支开放,呈“蜘蛛网”样;下腔静脉型肝外体循环侧支开放更明显;混合型则二者兼具。④间接或继发征象:PH表现,肝静脉型更显著(图8)。MRI表现与CT相似,但肝淤血、肝静脉和下腔静脉的血栓、隔膜显示更好,肝特异性对比剂增强检查有助于鉴别肝内增生结节和肝细胞肝癌。鉴别诊断包括以下3个方面:①肝炎后肝硬化、肝内良恶性结节压迫可引起肝静脉狭窄,但肝淤血和肝内外侧支循环开放表现不明显;②肝功能损害、对比剂充盈不良,肝静脉或下腔静脉有时也可显示不清,但无血管病变;③SOS与BCS临床表现相近,但受累血管不同,BCS累及肝静脉主干及下腔静脉,SOS累及肝窦及小肝静脉;肝静脉型BCS肝叶比例失调,肝尾状叶肥大具有特征性,而SOS肝脏体积增大,但比例协调,尾状叶不大,增强扫描呈特征性的“地图样”或“爪状”。
综上所述,无创的影像学检查,尤其是CT、MRI是PH各类病因诊断的重要方法,在密切结合临床病史与实验室检查的基础上,仔细观察影像征象,准确分析影像特征,是实现准确诊断和鉴别诊断的根本。影像学新技术和新应用有望为解决PH疑难诊断问题及全面评价病情严重程度、疗效及预后带来新的机遇。

图6 39岁女性区域性PH患者(既往胰腺肿瘤切除)影像学表现:A、B:CT增强扫描结果示脾静脉闭塞,门静脉及肠系膜上静脉通畅;C:门脉高压,胃底、胃网膜静脉侧支明显增多、迂曲、扩张,但食管静脉曲张轻,无肝硬化改变;D:CTA检查结果示脾动脉闭塞,胃左、胃十二指肠动脉明显增粗,供血脾脏,脾动脉瘤形成

图7 15岁男性HHT患者影像学表现:A:CT增强扫描结果示动脉期肝门部肝动脉明显增粗,门静脉早显、增粗,强化程度与肝动脉相似,提示肝动脉-门静脉瘘;肝硬化,巨脾;B:CT增强扫描结果显示动脉期肝动脉肝内分支增多、迂曲,达肝脏边缘;C:CTA示肝动脉及其分支明显增粗迂曲,腹主动脉小分支、肠系膜上动脉分支与肝动脉沟通;D:CT静脉成像(CTV)示门静脉主干显著增宽,广泛侧支循环形成,食道胃底静脉、胃冠状静脉、脾静脉重度曲张,脾肾分流

图8 57岁男性混合型BCS患者增强CT影像学表现:A、B:肝静脉根部及下腔静脉肝后段狭窄,肝内、肝外侧支循环形成,肝淤血;C:肝硬化,尾状叶明显增大,PH,脾脏增大;D:CTV示下腔静脉肝后段狭窄、闭塞,肝内、肝外广泛侧支循环形成
