顺式曲札茋苷的制备及其热稳定性、抗凝血酶活性
2021-01-08张晓蕾郭明里茜龚云麒李陈云建张建文杨兆祥
张晓蕾 郭明里 黄 茜龚云麒李 宁*陈云建*张建文杨兆祥
(1.昆药集团股份有限公司,云南 昆明 650100;2.昆明医科大学药学院,云南 昆明 650500;3.大理大学药学与化学学院,云南 大理 671000)
曲札茋苷(白皮杉醇-3′-O-β-D-吡喃葡萄糖苷) 是从我国西藏特有植物拉萨大黄Rheum lhasaense A.J.Li et P.K.Hsiao 中提取得到的活性成分[1-2],为茋苷(二苯乙烯苷)类化合物,其结构中2 个苯环之间存在1 个双键,故理论上存在顺式、反式2 种异构体(图1)。由于反式异构体在热力学上较顺式稳定,以往研究中获得的均为前者,故不考虑构型,以曲札茋苷指代反式曲札茋苷。
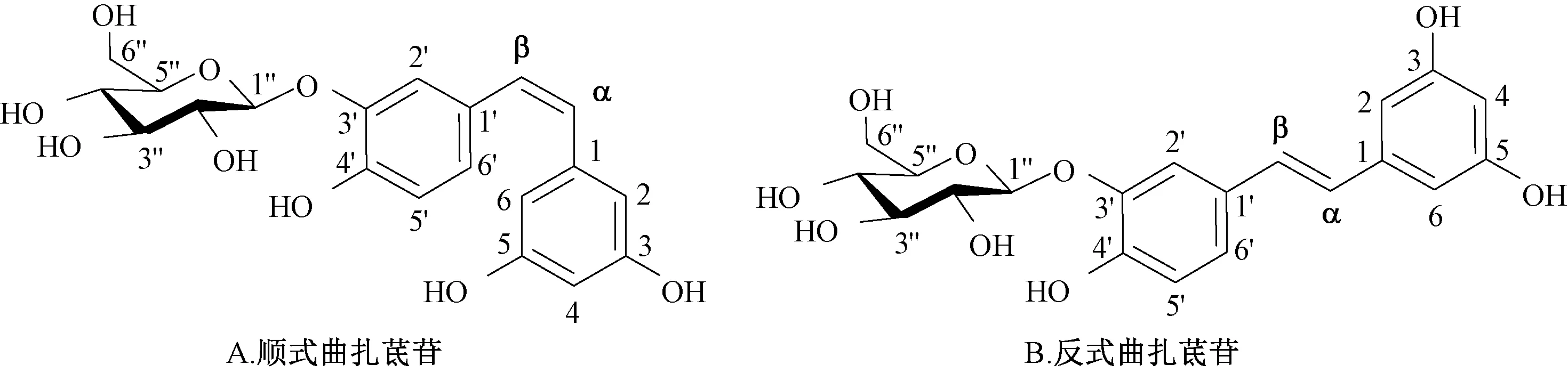
图1 顺式、反式曲札茋苷结构
研究表明,曲札茋苷在心脑血管[2-3]、神经系统[4]、呼吸系统[5]、消化系统[6]、肿瘤[7]等诸多重大疾病领域中有着广阔的应用前景。昆药集团股份有限公司对其进行了持续的考察,在云南丽江引种栽培了拉萨大黄[8],对其质量进行了较为系统的研究[9],建立了该药材中曲札茋苷的工业化提取纯化工艺[10],可大规模制备纯度98%以上者[11]。同时,在此基础上开发了注射用曲札茋苷,以期形成具有我国自主知识产权的天然创新药物。
杂质是药物质量研究的重要组成部分,注射用曲札茋苷中该类成分能否被全面、准确地控制直接关系到其有效性与安全性。前期发现,注射用曲札茋苷中的杂质大部分是拉萨大黄原有成分,随着工艺过程进入成品,但有少量并非来源于原药材。在工艺及贮存过程中,经强烈日光照射后的原料药、中间体、制剂中反式曲札茋苷含有量明显降低,杂质谱也发生较大的变化。理论上,光照可诱导二苯乙烯类化合物顺反异构化,电子首先受光照从基态激发到激发态,再经过无辐射跃迁返回分子基态,导致分子可从反式转化为顺式,或从顺式变为反式[12],故顺式曲札茋苷是注射用曲札茋苷中潜在的杂质。
近年来,有采用光化学反应制备高纯度二苯乙烯苷类化合物顺式异构体的研究[13],但尚无关于顺式曲札茋苷的报道。因此,本实验通过光化学反应将反式曲札茋苷转化为顺式后,对其进行分离纯化及结构鉴定,并考察其热稳定性及抗凝血酶活性,以期为进一步相关研发提供理论依据与技术支持。
1 材料
1.1 仪器 Agilent 1100 高效液相色谱仪(配置在线脱气机、四元泵、自动进样器、VWD 检测器)、Agilent QTOF 6540 质谱仪(美国安捷伦公司);Avance 800 MHz 核磁共振仪(德国Bruker 公司);CP225D 分析天平(德国赛多利斯公司);XPE26 分析天平(瑞士梅特勒-托利多公司);Milli-Q 超纯水机(美国Millipore 公司);ZF-6 紫外灯(上海嘉鹏科技有限公司);Buchi R-3 旋转蒸发仪(瑞士Buchi公司);ED-IE-50 冻干机(上海比郎仪器有限公司);HS-25 PH 计(丹佛仪器有限公司);Synergy HT 酶标仪(美国BioTek 公司);IMS-70 全自动雪花制冰机(常熟市雪科电器有限公司);Eppendorf 移液器(德国Sartorius 公司)。
1.2 试剂与药物 反式曲札茋苷对照品(纯度≥99.0%)及原料药(批号20140104、20140104-UV-1、20140104-UV-2、20140104-UV-3) (昆药集团股份有限公司自制)。人凝血酶 (美国Hyphen 公司,Vial of 10 NIH);荧光底物thrombin substrate 2 (FR-2) Cbz-Gly-Gly-Arg-AMC (加拿大Biomatik 公司)。阿加曲班(湖北鑫源顺医药化工有限公司,纯度≥99%)。色谱纯乙腈(德国默克公司);色谱纯乙醇(赛默飞世尔科技有限公司);氘代甲醇(美国Sigma-Aldrich 公司);三羟甲基氨基甲烷(Tris,美国Amresco 公司,纯度≥99.9%);其他试剂均为分析纯;水为超纯水。
2 方法与结果
2.1 顺式曲札茋苷制备 称取反式曲札茋苷对照品150 mg,置于200 mL 玻璃烧杯中,加入100 mL 甲醇充分溶解,将烧杯敞口置于紫外灯下,以365 nm 紫外光照射4 h,反应后的溶液在35 ℃以下减压浓缩至2 mL,浓缩液通过HPLC 法分离纯化。色谱条件为Phenomenex Luna Su C18(2)色谱柱(250 mm×4.6 mm,5 μm);流动相95%乙醇-水(30∶70);柱温20 ℃;检测波长319 nm;进样量50 μL;目标峰(顺式曲札茋苷) 保留时间约16 min。收集目标峰洗脱液,立即以氮气吹扫挥去乙醇,于黑暗环境中冷冻干燥,合并冻干粉,即得(20 mg)。
2.2 结构鉴定
2.2.1 顺式曲札茋 白色粉末(乙醇-水),溶于甲醇、乙醇、乙腈中。UV (乙腈-水) λmax:285 nm。HRESI-MS m/z:405.119 8[M-H]-(计算值405.119 1),分子式C20H22O9。1HNMR (800 MHz,CD3OD) δ:7.21 (1H,d,J=1.6 Hz,H-2′),6.81 (1H,dd,J=8.0,1.6 Hz,H-6′),6.72 (1H,d,J=8.0 Hz,H-5′),6.39 (1H,d,J=12.0 Hz,H-β),6.34(1H,d,J=12.0 Hz,H-α),6.24 (2H,d,J=1.6 Hz,H-2,6),6.14 (1H,t,J=1.6 Hz,H-4),4.47 (1H,d,J=7.2 Hz,H-1″),3.72 (1H,dd,J=12.0,3.2 Hz,H-6″a),3.60(1H,dd,J=12.0,2.4 Hz,H-6″b),3.49 (1H,m,H-2″),3.41 (2H,m,H-3″,5″),3.10 (1H,m,H-4″);13C-NMR(200 MHz,CD3OD) δ:141.3 (C-1),108.2 (C-2,6),159.5 (C-3,5),102.6 (C-4),130.7 (C-1′),116.5 (C-2′),146.4 (C-3′),147.4 (C-4′),118.4 (C-5′),126.1 (C-6′),129.4 (C-α),130.3 (C-β),104.3 (C-1″),74.8 (C-2″),77.4 (C-3″),70.4 (C-4″),77.4 (C-5″),61.6 (C-6″)。
2.2.2 反式曲札茋 淡黄色粉末(乙醇-水),溶于甲醇、乙醇、乙腈中。UV (乙腈-水) λmax:319 nm。HRESI-MS m/z:405.119 3 [M-H]-(计算值405.119 1),分子式C20H22O9。1H-NMR (800 MHz,CD3OD) δ:7.45 (1H,d,J=1.6 Hz,H-2′),7.06 (1H,dd,J=8.0,1.6 Hz,H-6′),6.81 (1H,d,J=8.0 Hz,H-5′),6.93 (1H,d,J=16.0 Hz,H-β),6.84 (1H,d,J=16.0 Hz,H-α),6.45 (2H,d,J=2.4 Hz,H-2,6),6.16 (1H,t,J=2.4 Hz,H-4),4.80(1H,d,J=7.2 Hz,H-1″),3.95 (1H,dd,J=12.0,2.4 Hz,H-6″a),3.73 (1H,dd,J=12.0,5.6 Hz,H-6″b),3.51(1H,m,H-2″),3.49 (2H,m,H-3″,5″),3.39 (1H,t,J=8.8 Hz,H-4″);13C-NMR (200 MHz,CD3OD) δ:141.6 (C-1),106.4 (C-2,6),160.1 (C-3,5),103.3 (C-4),131.8(C-1′),117.1 (C-2′),147.5 (C-3′),148.7 (C-4′),117.7(C-5′),124.1 (C-6′),128.4 (C-α),129.6 (C-β),105.0(C-1″),75.5 (C-2″),78.1 (C-3″),72.0 (C-4″),79.0 (C-5″),63.1 (C-6″)。
2.2.3 数据归属 通过DEPT、HSQC、HMBC、1D-TOCSY等核磁共振实验对反式曲札茋的1H-NMR、13C-NMR 数据进行归属,主要HMBC 相关见图2。顺式曲札茋苷的核磁数据与反式曲札茋苷的相似,主要区别在于前者1H-NMR 中δ 6.34、6.39 可见1 对相互偶合的烯氢信号,偶合常数为12.0 Hz,提示双键构型为顺式,参照反式曲札茋核磁数据及文献[14]中类似结构的化合物,对该成分1H-NMR、13C-NMR数据进行了归属,经文献检索可知它为首次获得,而且是新化合物。

图2 反式曲扎茋苷主要HMBC 相关
2.3 顺式曲札茋苷含有量测定及其热稳定性研究 精密称取“2.1” 项下样品适量,甲醇制成40 μg/mL 溶液,即得供试品溶液;精密称取反式曲札茋苷对照品适量,甲醇制成40 μg/mL 溶液,即得对照品溶液。色谱条件为Grace Apollo C18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A) -0.1%磷酸(B),梯度洗脱(0~25 min,15%~30%A;25~30 min,30%~40% A;30~35 min,40%~15% A;35~40 min,15% A);体积流量1.0 mL/min;检测波长319 nm;进样量10 μL。
取“2.1” 项下样品适量,于温度25 ℃、相对湿度60%环境中贮存,于0、24 h 在上述色谱条件下进样测定,测得顺式曲札茋苷纯度分别为97.1%、84.2%,表明该成分稳定性较差。
取避光保存(批号20140104) 及经强烈日光照射过(批号 20140104-UV-1、20140104-UV-2、20140104-UV-3,分别于约100 000 lx 日光下直射约1 h、15 min、5 min) 的反式曲札茋苷原料药进行测定,色谱图见图3。结果,避光保存的原料药中顺式曲札茋苷质量分数为0.18%,而3 批经强烈日光照射者分别为33.15%、9.16%、4.12%,表明光照会诱导反式曲札茋苷异构化,增加顺式曲札茋苷杂质含有量。
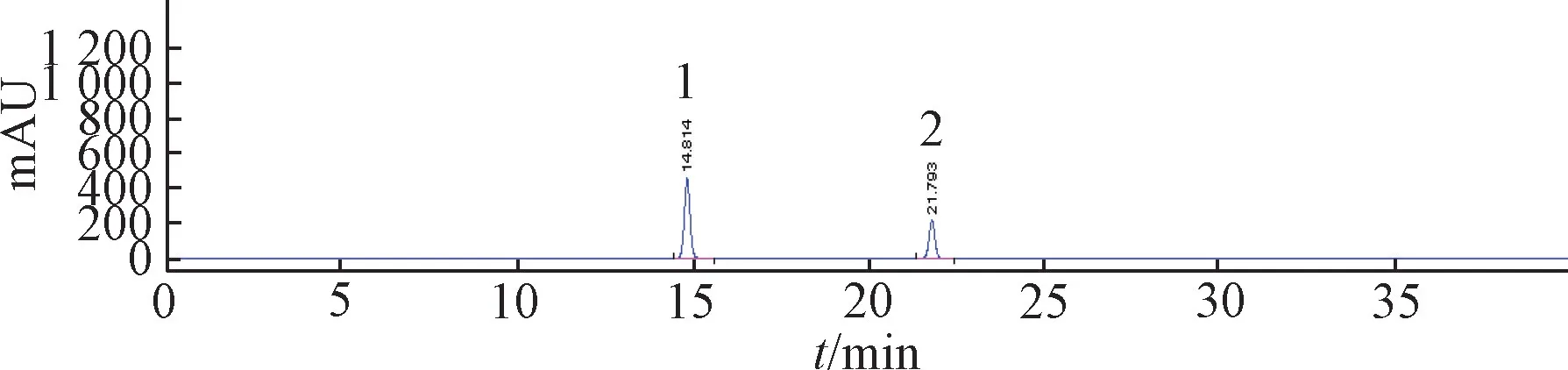
图3 供试品溶液(经强烈日光照射过的) 中2 种成分HPLC 色谱图
取原料药(批号20140104-UV-2) 2 份,25%乙醇制成0.5 mg/mL 溶液,分别置于80、100 ℃水浴中加热1 h,减压蒸干,测得顺式曲札茋苷质量分数分别为3.69%、0.77%。由此表明,加热会促进顺式曲札茋苷转为反式,而且温度越高,转化率越高,同时提高反式曲札茋苷纯度。
2.4 顺式曲札茋苷抗凝血活性研究 参考文献 [15]报道。
2.4.1 Tris-NaCl 缓冲液制备 称取Tris 适量,加入NaCl适量后用水溶解,浓HCl 调节pH 至8.40,即得(含Tris 0.05 mol/L、NaCl 0.3 mol/L),在4 ℃下保存。
2.4.2 荧光底物溶液制备 称取Cbz-Gly-Gly-Arg-AMC适量,加水溶解,制成4 mmol/L 溶液,即得,在4 ℃下保存,临用前用水稀释到所需浓度。
2.4.3 凝血酶溶液制备 临用前取10 IU/mL 人凝血酶原液适量,加水稀释至所需浓度,即得,置于冰上待用。
2.4.4 待测溶液制备 取阿加曲班(阳性对照)、顺式曲札茋苷、反式曲札茋苷适量,DMSO 分别制成50 μmol/L、30 mmol/L、3 mmol/L 母液,临用前用DMSO 稀释至所需浓度,即得(以DMSO 为空白对照组)。
2.4.5 测定方法 采用荧光法测定。反应体系为样品溶液及阳性、空白对照溶液各1 μL,酶溶液5 μL (1 IU/mL),缓冲液24 μL,水50 μL,加到96 孔板中,再加入底物溶液20 μL (200 μmol/L),立即置于酶标仪上测定。设置样品孔(样品+酶)、标准孔(DMSO+酶)、空白孔(DMSO+水),激发光390/40 nm,发射光460/40 nm,测定时间间隔51 s,顶部检测,增益70,在25 ℃下反应10 min,每个浓度设置2 个副孔,测定凝血酶抑制率,取平均值,公式为抑制率=[(△V标准孔-△V样品孔)/ (△V标准孔-△V空白孔) ]×100%,其中△V 为平均反应速度,通过GraphPad Prism 6 软件对样品反应浓度对数与抑制率作图,计算IC50。结果,阿加曲班IC50为29.63 nmol/L,表明造模成功,顺式曲札茋苷、反式曲札茋苷IC50分别为48.42、3.40 μmol/L。
3 讨论
文献[16]对顺式曲札茋苷的抗氧化活性进行了模拟预测,但该研究是基于理论推断,并未获得具体化学实体。本实验通过光化学反应首次将反式曲札茋苷转化为顺式异构体,经HPLC 分离后在低温条件下回收溶剂,并通过高分辨质谱、核磁共振、紫外光谱等技术对其结构进行鉴定,可为进一步考察相关分析方法和生物活性奠定基础。
前期对光化学反应的转化条件进行了考察,比较了254、365 nm 紫外光源及日光(约100 000 lx),发现365 nm紫外光源及日光的转化效率远高于254 nm 紫外光,为确保反应可控性,最终采用365 nm 紫外光源;比较了15 min~10 h 的照射效果,发现15 min 内即有顺式曲札茋苷产生,随着照射时间延长其得率增加,但过长(>8 h) 时溶剂颜色加深,表明有其他微量成分产生,增加后续色谱分离难度,最终确定转化时间为4 h;比较了甲醇、甲醇-水、乙醇、乙醇-水、丙酮等多种溶剂,发现甲醇、甲醇-水、乙醇、乙醇-水的提取效率高于丙酮,为方便溶剂回收,最终选择甲醇。
通过HPLC 法对光化学反应后的混合物进行分离,考虑到未来工艺,流动相采用廉价、低毒的95% 乙醇-水体系;为保证连续进针以缩短分析时间,采用了等度洗脱;在顺式曲札茋苷的制备过程中温度控制非常关键,故将洗脱液用氮气吹扫后在黑暗环境中冷冻干燥,以避免洗脱液中的该成分再次异构化。另外,顺式曲札茋苷在室温下稳定性较差,虽然最初获得该成分时纯度可高于95%,但24 h内会降低至85% 以下,因条件所限,目前无法获得其准确可靠的熔点、红外光谱、旋光等数据,故建议在条件允许的情况下其贮存和使用应尽量处于低温、避光环境。
由于顺式曲札茋苷热稳定性较差,故现阶段该成分成药性不理想,但常作为杂质出现于反式曲札茋苷中。本实验初步摸索了顺式曲札茋苷杂质的检测方法,该方法在拉萨大黄指纹图谱[9]的基础上对洗脱梯度进行了调整,发现各色谱峰峰形、分离度良好,保留时间适中,能满足分析要求,并首次证实经强烈日光照射后反式曲札茋苷中含有顺式异构体,而且可通过加热工艺使后者质量分数降低至1%以下。由此提示,在注射用曲札茋苷的生产、贮存过程中应注意避光,而且加热工艺可降低杂质含有量,与成品质量有较大关联,故应进一步重点考察并确定参数范围。
凝血酶是机体凝血系统中的重要组成因子,是触发凝血反应的效应器,抗凝血酶活性与注射用曲札茋苷防治心脑血管疾病,特别是缺血性脑卒中的药效密切相关。本实验发现,顺式、反式曲札茋苷均具有抗凝血酶活性,但前者较后者大致降低了1 个数量级。有研究表明,二苯乙烯类化合物顺反异构体在实验动物中的药动学、组织分布等体内过程有较大差异[17],其安全性也有明显的不同,如何首乌中顺式二苯乙烯苷对3D 培育的肝细胞模型的毒性大于反式异构体,具有更大的肝损伤风险[18],表明顺反异构化不但会影响注射用曲札茋苷药效,对其安全性也有潜在的重要影响。
综上所述,本实验为注射用曲札茋苷质量标准的进一步提高,特别是杂质成分的控制提供了参考。今后,将围绕顺式曲札茋苷开展进一步研究,以期提高注射用曲札茋苷质量,保障用药安全。
致谢:感谢中国药科大学生药学研究室、上海中医药大学中药研究所李娟博士对本文的审阅与指导。
