磁性介孔氧化硅的合成及其对有机染料吸附性能研究*
2021-01-08党韶丽
党韶丽
(宝鸡职业技术学院 生物与建筑工程学院,陕西 宝鸡 721013)
近年来,随着中国工业化的快速发展,环境污染问题越发严重,尤其是纺织工业中产生的有机染料废水是不容忽视的水污染问题。染料废水中的有害化学物质进入人体,会诱发癌症、基因突变等一系列问题,严重影响到人类健康和生命安全[1,2]。
目前,处理有机染料废水的方法主要有:高级氧化法、微生物降解、吸附分离和光催化降解等[3-5]。其中,吸附分离技术因其成本低、效率高、可循环好、操作简单等优点,已成为处理有机废水的一项重要技术方法,引起了研究者的广泛关注[6-8]。其中,磁性吸附材料作为一种新兴有机吸附材料,对有机污染物有着良好的吸附性能,而且该材料能够快速方便的与水体分离,有利于吸附材料的重复利用和污染物的集中处理[9,10]。
介孔SiO2由于比表面积高、孔容大、介孔孔道规整、生物相容性好、表面易修饰、易再生循环利用及热稳定性良好等优点,已经成为当前国内外极具发展潜力的吸附材料[11,12]。但是,该类材料存在明显的缺陷亟待研究和解决:(1)纯介孔氧化硅本身缺乏化学活性位点,限制了其在化学工业中的应用;(2)如何对介孔SiO2材料进行改性修饰,使其具有较高的选择性吸附能力,同时使该材料易于分离、再生,进而提高介孔SiO2的重复利用。
本文利用溶剂热法合成了亚微米级磁性Fe3O4,以Fe3O4为“芯”,通过溶胶凝胶法合成了“芯-壳”结构的Fe3O4@SiO2@mSiO2磁性介孔SiO2,并研究了磁性介孔SiO2对有机染料甲基橙、亚甲基蓝及罗丹明B 的吸附性能。
1 实验部分
1.1 试剂与仪器
六水三氯化铁(FeCl3·6H2O)、十六烷基三甲基溴化铵(C19H42BrN,CTAB)、乙二醇((CH2OH)2)、正硅酸四乙酯(C8H12O4Si),国药集团化学试剂有限公司;亚甲基蓝(C16H18N3ClS,MB),阿拉丁;罗丹明 B(C28H30N2O3,RhB)、甲基橙(C14H14N3SO3Na,MO)、氨水(NH3·H2O,30%)天津市天力化学试剂有限公司;以上试剂均为分析纯。
D8 Advance 型 X 射线粉末衍射仪(XRD)(德国布鲁克公司);JSM-2010 型透射电子显微镜(TEM)(日本电子公司);SU8010 型高分辨冷场发射扫描电子显微镜(SEM)(日本日立公司);ASAP-2460 型比表面积测试仪(麦克公司);U-3900 型紫外可见分光光度计(日本日立公司)。
1.2 磁性介孔SiO2 的制备
1.2.1 Fe3O4的制备 将 11g FeCl3·6H2O 溶于乙二醇中搅拌30min 得到澄清溶液,接着添加18g NaAc,继续搅拌1h,再加入2.5g 柠檬酸三钠于水浴50℃下搅拌5h;将上述悬浊液封装于聚四氟乙烯反应釜中,在200℃下反应8h,冷却至室温,取黑色固体用H2O 和乙醇循环洗涤数6 次,磁分离,40℃烘干,得到磁性Fe3O4。
1.2.2 Fe3O4@SiO2的制备 将 0.15g Fe3O4纳米颗粒分散在 80mL 乙醇和20mL 去离子水混合溶液中,再加入1mL NH3·H2O,超声40min,然后加入0.2mL 正硅酸乙酯,搅拌反应6h;将所得产物进行磁分离,用乙醇和离子水反复洗涤,在60℃温度下干燥6h,得Fe3O4@SiO2磁性复合材料。
1.2.3 Fe3O4@SiO2@mSiO2的制备 将0.1g Fe3O4@SiO2分散在 60mL 乙醇和80mL 去离子水混合溶液中,再加入 1mL NH3·H2O 和 0.3g 十六烷基三甲基溴化铵,超声搅拌30min,然后滴加0.4mL 正硅酸乙酯,搅拌反应2h;将所得产物进行磁分离,用乙醇和离子水反复洗涤,在 60℃温度下干燥 6h,得Fe3O4@SiO2@mSiO2磁性介孔SiO2复合材料。
1.3 有机染料的吸附实验
分别量取 50mL 20mg·L-1的 MB、MO 与 RhB 溶液(20mg·L-1),各添加 20mg 的 Fe3O4@SiO2@mSiO2磁性介孔SiO2,在室温下搅拌反应,每反应5min,取样进行磁分离,取上清液,采用紫外可见分光光度计测定,计算其脱色率。
2 结果与讨论
2.1 Fe3O4@SiO2@mSiO2 磁性介孔 SiO2 的物相研究
图1 为 Fe3O4与 Fe3O4@SiO2@mSiO2样品的 XRD谱图。
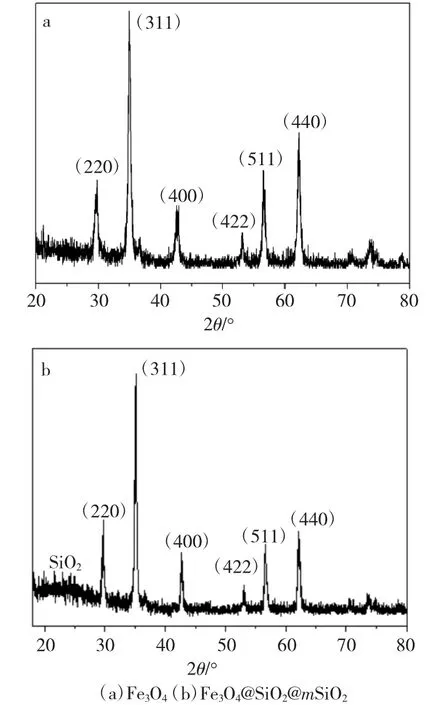
图1 样品的XRD 谱图Fig.1 XRD patterns of samples
由 XRD 图 1(a)可见,所得样品的 XRD 谱图在20°~80°范围出现了 (220)、(311)、(400)、(422)、(511)与(440)晶面所对应的6 个衍射峰,以上衍射峰与Fe3O4的特征衍射峰相对应,说明所得样品为纯相的Fe3O4。由图1(b)可知,所得样品除了呈现出Fe3O46 个晶面 (220)、(311)、(400)、(422)、(511)、(440)对应的特征衍射峰,还在2θ=23°附近呈现出非晶态SiO2的衍射峰,表明所得样品为Fe3O4与SiO2复合材料。
2.2 Fe3O4@SiO2@mSiO2 磁性介孔 SiO2 的微观结构研究
图2 为Fe3O4(a)、Fe3O4@SiO2(b)与Fe3O4@SiO2@mSiO2(c)样品的SEM 图。

图2 样品的SEM 与TEM 图Fig.2 SEM and TEM patterns of samples
由图 2(a)可见,Fe3O4呈现出球形状形貌,平均粒径约275nm,表面粗糙不光滑。由图2(b)可见,Fe3O4@SiO2仍然保持球形形貌,平均粒径约290nm,表面光滑,表明在Fe3O4表面形成了厚度约为15nm SiO2壳层。壳层SiO2不仅可以提高Fe3O4的生物相容性,还能够防止Fe3O4溶解漏磁。从图2(c)可看出,所得样品Fe3O4@SiO2@mSiO2具有明显的“芯”-“壳”结构,“壳”层呈现出大量孔状结构。图2(d)为Fe3O4@SiO2@mSiO2样品的 TEM 图。由图 2 可知,球形Fe3O4表面包覆了一层厚度约为15nm 的SiO2,然后在SiO2壳层生长形成了无序的介孔SiO2,该结果与XRD 和SEM 的分析结果相一致。
将 Fe3O4与 Fe3O4@SiO2@mSiO2样品进行 N2物理吸附测试,所得结果见图3。
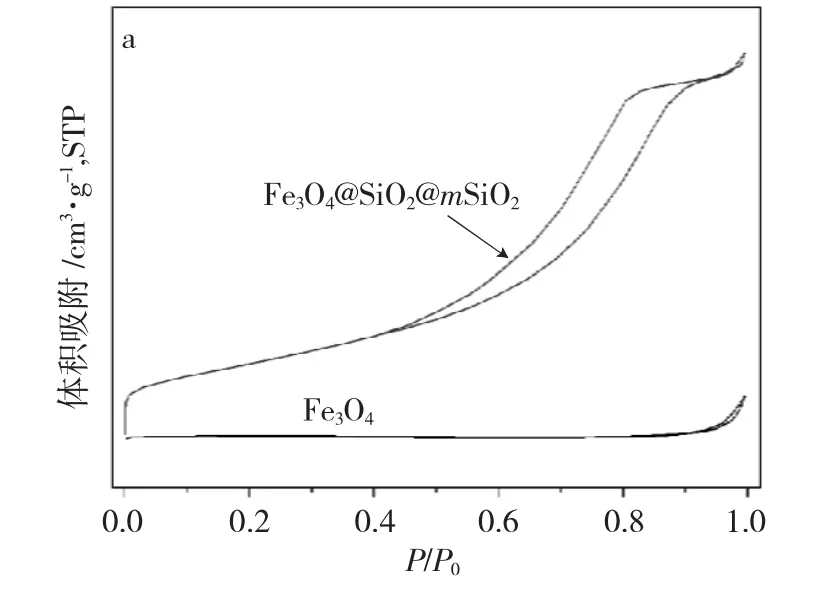
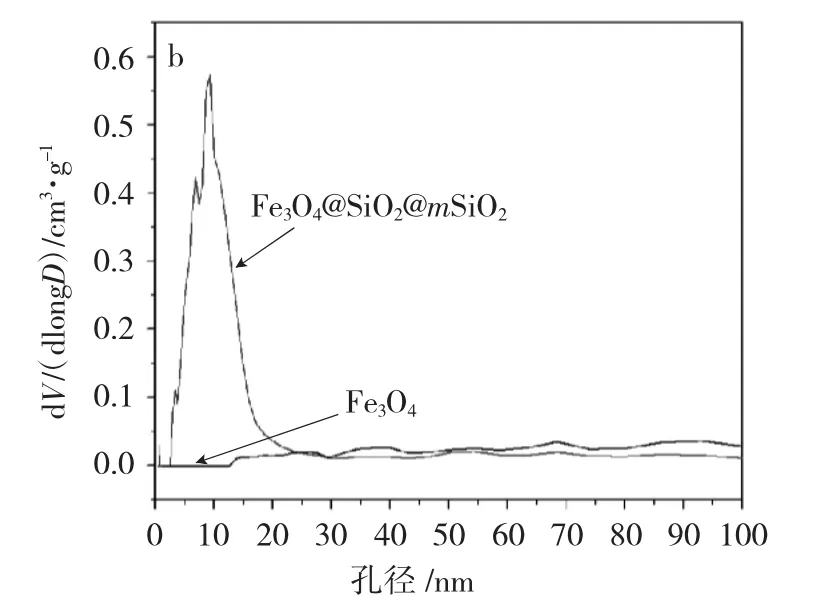
图3 样品Fe3O4 与Fe3O4@SiO2@mSiO2 的N2 吸附等温线(a)与孔径分布(b)图Fig.3 Physical adsorption diagram(a)and pore size distribution(b)patterns of the Fe3O4 and Fe3O4@SiO2@mSiO2 samples
由图 3(a)可知,样品 Fe3O4的 N2吸附/脱附等温线在P/P0为0.9~1.0 之间形成滞后环,表明只形成了堆积孔。样品Fe3O4@SiO2@mSiO2的N2吸附/脱附等温线在P/P0为0.6~0.8 之间形成明显滞后环,这是由于N2分子在介孔中的毛细凝聚现象导致的,表明Fe3O4@SiO2@mSiO2为介孔材料,但是在P/P0大于0.8 处Fe3O4@SiO2@mSiO2吸附-脱附等温线的滞后环没有闭合,出现了堆积孔,表明所得Fe3O4@SiO2@mSiO2介孔材料的有序度较低,这与TEM 表征结果是一致的。图 3(b)为 Fe3O4与 Fe3O4@SiO2@mSiO2样品的孔径分布曲线,由图可知,Fe3O4样品没有形成孔径,而Fe3O4@SiO2@mSiO2样品的孔径主要分布于 2~14nm 之间。由 BET 测试可知,Fe3O4与 Fe3O4@SiO2@mSiO2样品的比表面积分别为 4.5cm2·g-1与121cm2·g-1,这是由于 Fe3O4@SiO2@mSiO2样品形成了介孔孔道导致其比表面积的成倍增加。
2.3 Fe3O4@SiO2@mSiO2 磁性介孔 SiO2 对有机染料的吸附性能研究
图4(a)为 Fe3O4、Fe3O4@SiO2与 Fe3O4@SiO2@mSiO2样品对MB 的吸附性能图。
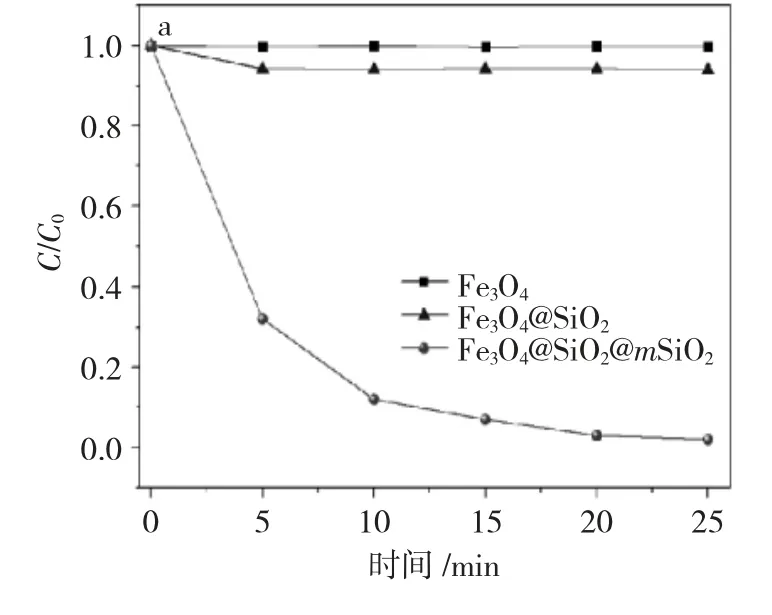
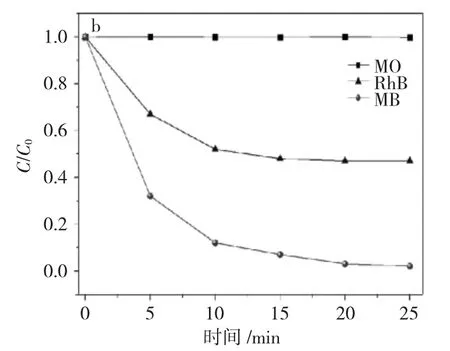
图4 磁性介孔氧化硅对有机染料的吸附性能图Fig.4 Adsorption performance of magnetic mesoporous silica on organic dyes
由图 4(a)可见,在相同吸附时间 25min 内,Fe3O4与 Fe3O4@SiO2对 MB 吸附率分别为 0 和 8.2%,而Fe3O4@SiO2@mSiO2样品对MB 吸附率达到99%,这主要是由于Fe3O4@SiO2@mSiO2样品具有介孔结构,比表面积达到121cm2·g-1,在单位时间内,更容易吸附 MB。图 4(b)为 Fe3O4@SiO2@mSiO2样品对 MO、RhB 与MB 的吸附性能图。由图可见,在相同吸附时间25min 内,所得磁性吸附剂对MO 无吸附性能,而对RhB 与MB 的吸附率分别达到52.3%与99%。这是因为SiO2电动电势为2,当溶液的pH 值大于2时,其表面带负电荷,而MO 的显色基团也带负电荷,RhB 与MB 显色基团分别带弱负电荷与强负电荷,同电荷相互排斥,异电荷相互吸引,从而导致吸附率的明显差异。
3 结论
利用溶剂热法合成了亚微米级磁性Fe3O4,以Fe3O4为“芯”,通过溶胶凝胶法合成了“芯-壳”结构的Fe3O4@SiO2@mSiO2磁性介孔SiO2。该磁性介孔SiO2的比表面积达到121cm2·g-1,孔径主要分布于2~14nm 之间,对有机染料甲基橙无吸附性能,对亚甲基蓝(MB)展现出较好的吸附性能,25min 后对MB 的吸附率可达99%。
