UPLC-MS/MS法检测禽蛋中10种大环内酯类药物多残留的研究
2021-01-06王亦琳王鹤佳
尹 晖, 王亦琳, 叶 妮, 孙 雷, 王鹤佳
(中国兽医药品监察所, 北京海淀100081)
大环内酯类药物 (Macrolides)具有抗革兰阳性菌和抗支原体活性,广泛应用于临床兽药领域[1-3],常用于治疗上呼吸道感染、泌尿道感染及胃肠道感染等[4]。大环内酯类药物通过和细菌核糖体50S亚基发生不可逆结合,阻断转肽及mRNA位移,选择性地抑制蛋白质合成,从而发挥抗菌作用[5]。由于大环内酯类药物在可食用动物中的广泛使用,以及目前存在的阿奇霉素等人用药在家禽中滥用的现状,禽蛋中的兽药残留问题愈加凸显,这是危害人类健康的隐患。另外,动物源食品中大环内酯类药物残留还可导致携带耐药因子的菌株扩散[6-7]。
为了提供禽蛋中大环内酯类药物残留监控手段,本文首次建立了鸡蛋和鸭蛋中红霉素、替米考星、泰乐菌素、克拉霉素、螺旋霉素、阿奇霉素、罗红霉素、吉他霉素、加米霉素和泰万菌素共10种大环内酯类药物残留的UPLC-MS/MS检测方法,能够快速、简便地进行大环内酯类药物多残留监控。其中,阿奇霉素、罗红霉素和克拉霉素为人用药,未批准使用于动物 ; 替米考星在鸡产蛋期禁用 ; 泰万菌素的残留标志物为泰万菌素和3-O-乙酰泰乐菌素的总和。
1 材料与方法
1.1 材料与试剂 红霉素、替米考星、泰乐菌素、克拉霉素、螺旋霉素、阿奇霉素、罗红霉素、吉他霉素、加米霉素、泰万菌素及3-O-乙酰泰乐菌素,纯度均大于99.0%,均购自北京振翔科技有限公司;甲酸、乙腈为色谱纯,均购自美国默克公司;所用水为超纯水。
1.2 仪器与设备 Shimadzu 30A-QTRAP 6500液相色谱-串联质谱仪,日本岛津公司-美国爱博才思公司;AE260电子天平,梅特勒-托利多公司;Biofuge Strators高速冷冻离心机,贺利氏公司;SIR4涡旋混合器,艾卡公司;Cleanert MAS-Q净化管,艾杰尔公司。
1.3 对照溶液配制 精密称取红霉素、替米考星、泰乐菌素、克拉霉素、螺旋霉素、阿奇霉素、罗红霉素、吉他霉素、加米霉素、泰万菌素及3-O-乙酰泰乐菌素共10种大环内酯类标准品适量,置于10 mL棕色量瓶中,用甲醇溶解并稀释成浓度为1 mg/mL的标准储备液;量取标准储备液适量,用甲醇稀释成10 μg/mL的标准工作液,再用40%乙腈水溶液稀释成100 ng/mL的标准工作液。
1.4 测定方法
1.4.1 色谱条件 色谱柱:BEH C18 (50×2.1 mm,1.7 μm);流动相:A:0.1%甲酸水溶液,B:0.1%甲酸乙腈溶液;柱温:40 ℃;进样量:5 μL;流动相梯度洗脱条件见表1。
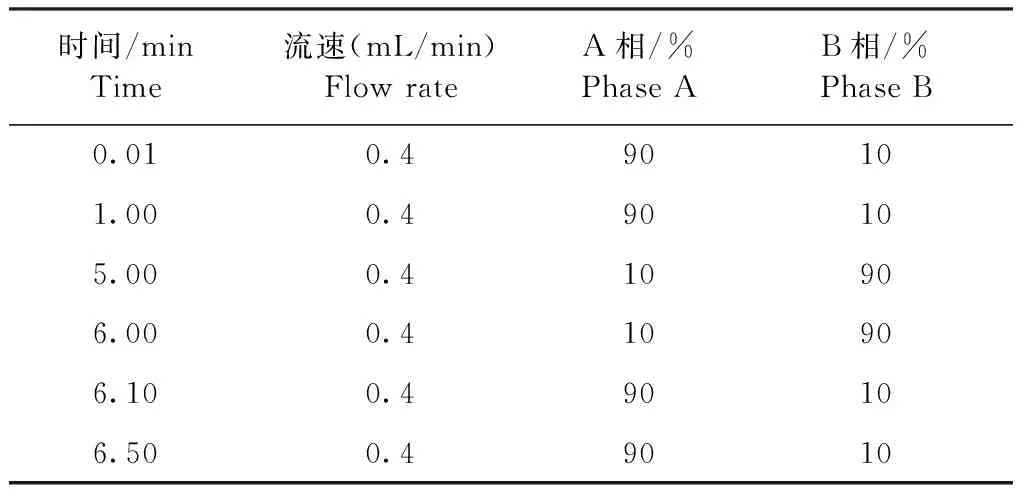
表1 流动相梯度洗脱条件Table 1 Gradient elution conditions of mobile phase
1.4.2 质谱条件 离子源:电喷雾离子源,扫描方式:正离子扫描,检测方式:多反应监测,气帘气CUR:30 psi,碰撞气(CAD):中等(Medium),电喷雾电压(IS):5 500 V,离子源温度:550 ℃,辅助气(GS1):50 psi,辅助气(GS2):50 psi,EP电压:10 V,CXP电压:10 V,待测药物定性定量离子对及对应的去簇电压(DP)和碰撞能量(CE)见表2。
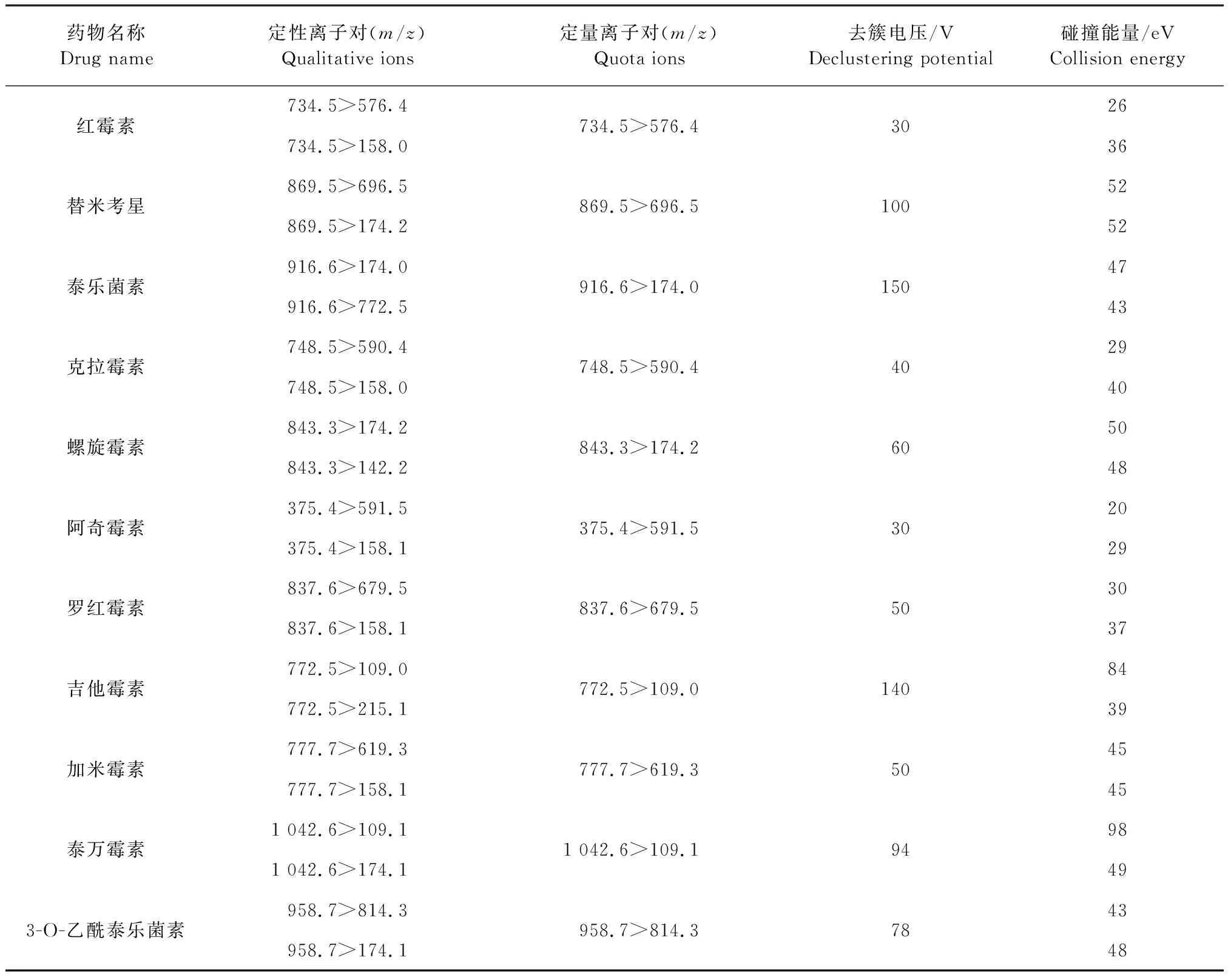
表2 10种大环内酯类定性定量离子对及对应的去簇电压(DP)和碰撞能量(CE)Table 2 Qualitative ions,corresponding quota ions of 10 macrolides and corresponding declustering potential(DP),collision energy(CE)
1.4.3 定性与定量 定性时试样溶液中色谱峰的保留时间,应与校正溶液的保留时间一致,容许偏差为±5%,试样溶液中的离子丰度比应与校正溶液的一致,容许偏差符合欧盟2002/657/EC决议要求。定量方法采用外标法定量。
1.4.4 基质匹配标准曲线绘制 精密量取大环内酯类标准工作液适量,用40%乙腈水溶液稀释成含各药物浓度分别为0.2、2、5、10 ng/mL和20 ng/mL的系列混合标准工作液,从中各取1.0 mL,分别加入到空白组织经提取、净化和吹干后的残余物中,充分溶解,0.2 μm滤膜过滤后,作为基质匹配标准溶液上机测定。每一浓度进样3针,按所得峰面积与相应的对照溶液浓度作标准曲线,并依次计算回归方程及相关系数。
1.4.5 样品前处理过程 称取试料鸡蛋或鸭蛋(2±0.02)g于50 mL离心管中,加入80%乙腈水溶液10 mL,涡旋振荡1 min,8 000 r/min离心8 min。取上清液1.0 mL至Cleanert MAS-Q净化管中,涡旋振荡1 min,8 000 r/min离心8 min,取上清液0.5 mL,加水0.5 mL,混匀,备用,取适量体积过微孔滤膜后,供液相色谱-串联质谱仪测定。
1.4.6 方法灵敏度确定 将适量大环内酯类标准工作液加入到空白试料鸡蛋中,经上述方法进行前处理后,用UPLC-MS/MS检测,观察药物特征离子质量色谱峰信噪比(S/N)和对应药物浓度,S/N>3者定其为方法的检测限,S/N>10者为方法的定量限。
1.4.7 准确度和精密度的测定 采用标准添加法,在空白试料鸡蛋和鸭蛋中各添加2、20、200 μg/kg三个不同浓度药物进行回收率试验,各浓度进行5个样品平行试验,重复3次,求批内、批间RSD。
2 结果
2.1 基质匹配标准曲线 按照上述系列基质匹配标准溶液浓度进行线性回归,得到的回归方程及相关系数见表3、表4。从表中可以看出,10种大环内酯类药物于鸡蛋和鸭蛋中在0.2~20 ng/mL的浓度范围内呈现良好的线性关系,R2均大于0.990。
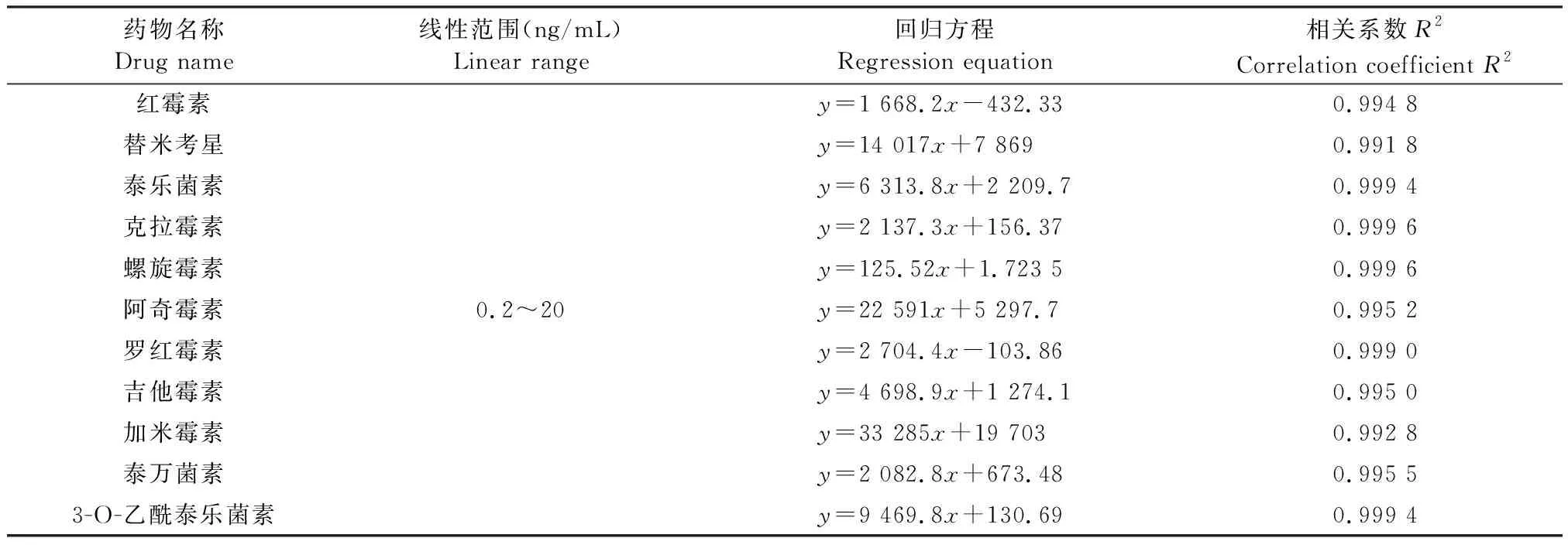
表3 鸡蛋中10种大环内酯类药物基质匹配标准曲线Table 3 Matrix-matched standard curve of 10 macrolides and a metabolite in eggs

表4 鸭蛋中10种大环内酯类药物基质匹配标准曲线Table 4 Matrix-matched standard curve of 10 macrolides and a metabolite in duck eggs
2.2 方法灵敏度 按上述方法进行处理,当添加浓度为1 μg/kg时,测得大环内酯类药物的S/N>3,说明方法检测限为1 μg/kg。当添加浓度为2 μg/kg时,测得大环内酯类药物的S/N>10,说明方法定量限为2 μg/kg。20 μg/kg空白鸡蛋添加试液中10种大环内酯类药物的特征离子质量色谱图见图1。
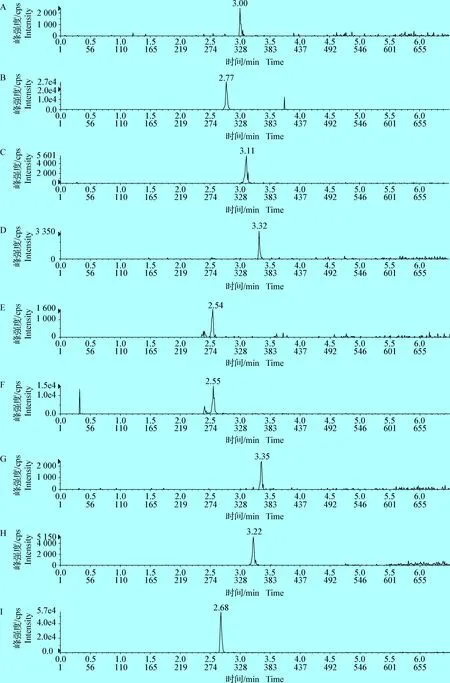
(转下页 Carried forwoud)
(续图1 Continued)
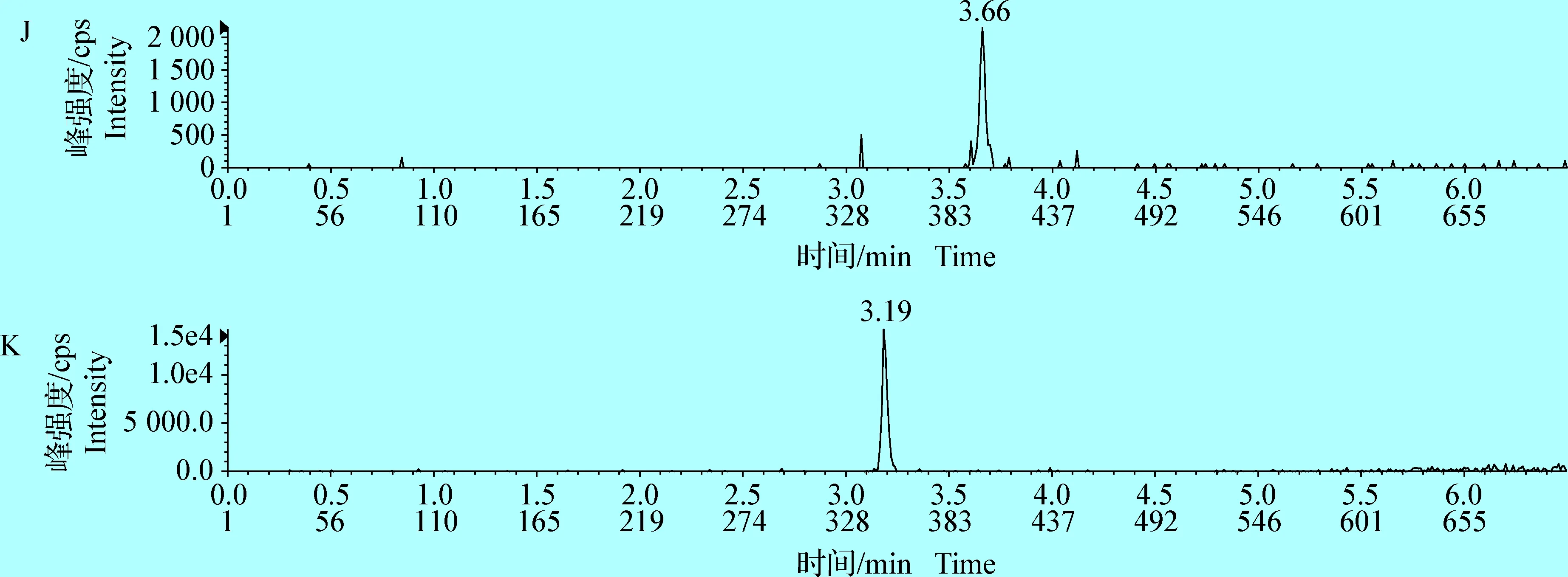
图1 空白鸡蛋添加试样溶液中得到的特征离子质量色谱图(20 μg/kg)Fig.1 Qualitative ions of 10 macrolides in spiked eggs(20 μg/kg)A:红霉素(734.5>576.4); B:替米考星(869.5>696.5); C:泰乐菌素(916.6>174.0); D:克拉霉素(748.5>590.4); E:螺旋霉素(843.3>174.2); F:阿奇霉素(375.4>591.5); G:罗红霉素(837.6>679.5); H:吉他霉素(772.5>109.0); I:加米霉素(777.7>619.3); J:泰万菌素(142.6>109.1); K:3-O-乙酰泰乐菌素(958.7>814.3)A:Erythromycin(734.5>576.4); B:Tilmicosin(869.5>696.5); C:Tylosin(916.6>174.0); D:Clarithromycin(748.5>590.4); E:Spiramycin(843.3>174.2); F:Azithromycin(375.4>591.5); G:Roxithromycin(837.6>679.5); H:Guitamycin(772.5>109.0); I:Gamithromycin(777.7>619.3); J:Tylvalosin(142.6>109.1); K:3-O-Acetyltylosin(958.7>814.3)
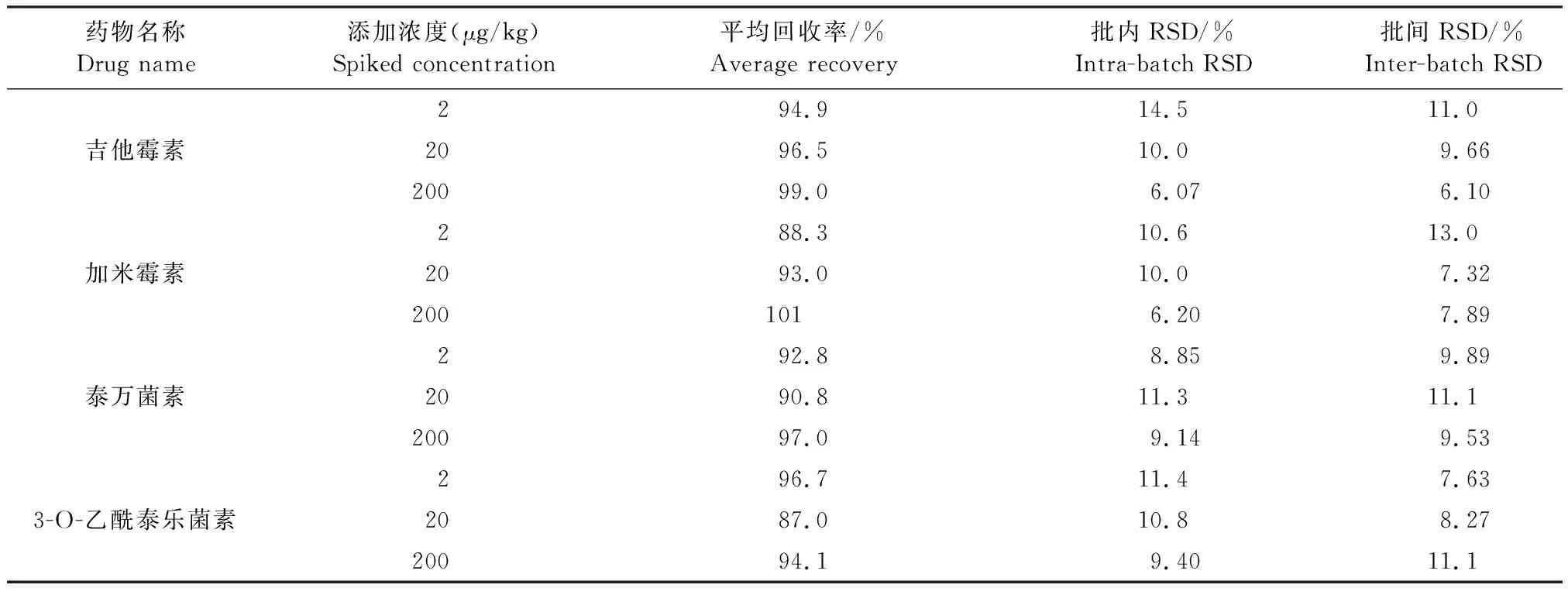
2.3 方法精确度 在空白鸡蛋和鸭蛋中各添加3个不同浓度大环内酯类药物进行回收率试验,结果见表5、表6。可以看出,鸡蛋中10种大环内酯类药物平均回收率为65.1%~115%,鸭蛋中10种大环内酯类药物平均回收率为67.5%~117%,本方法的回收率范围都在60%~120%,批内批间RSD均小于20%。
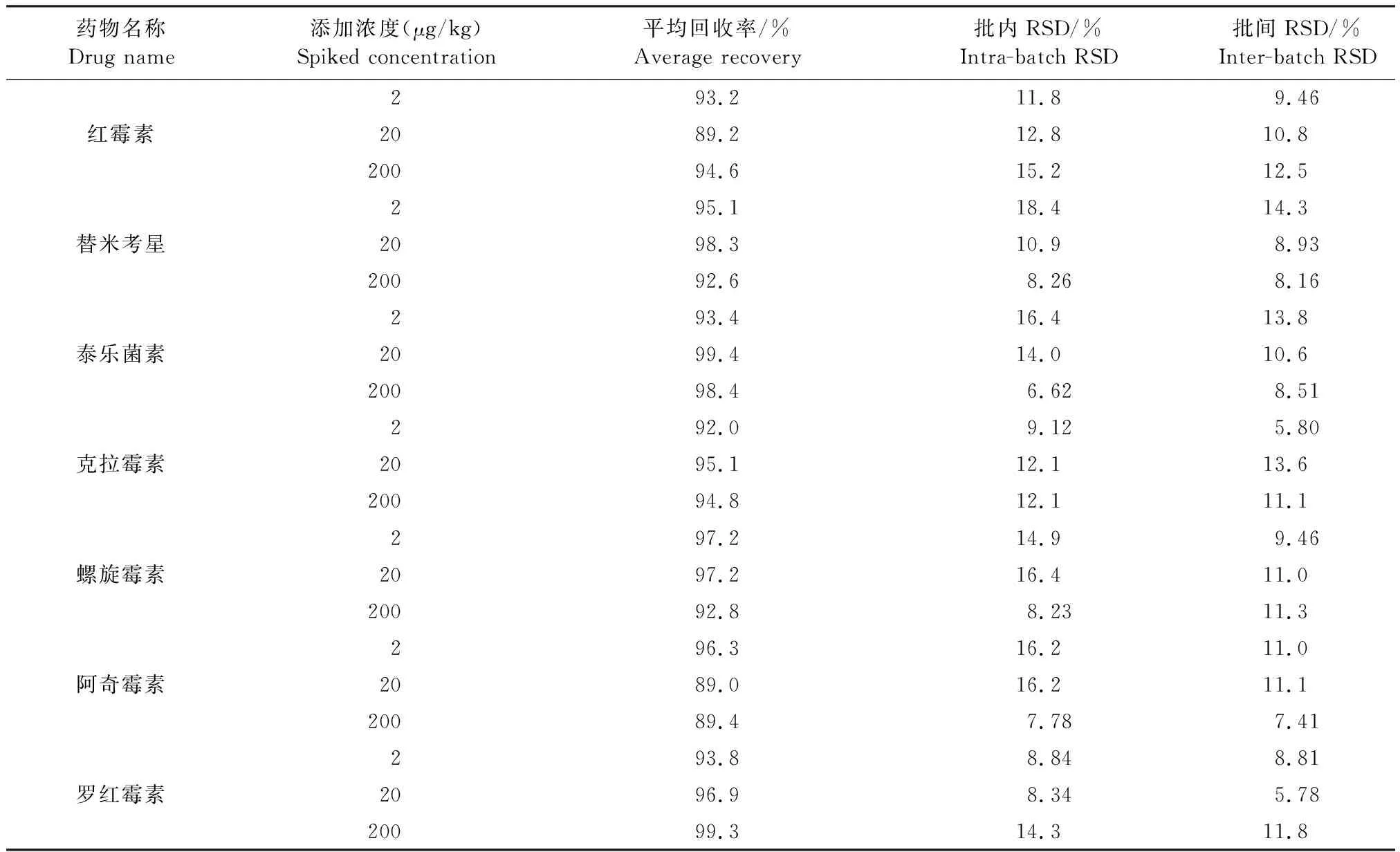
表5 空白鸡蛋中10种大环内酯类药物添加的回收率Table 5 Recoveries of 10 macrolides and a metabolite in spiked eggs
(转下页 Carried forwoud)
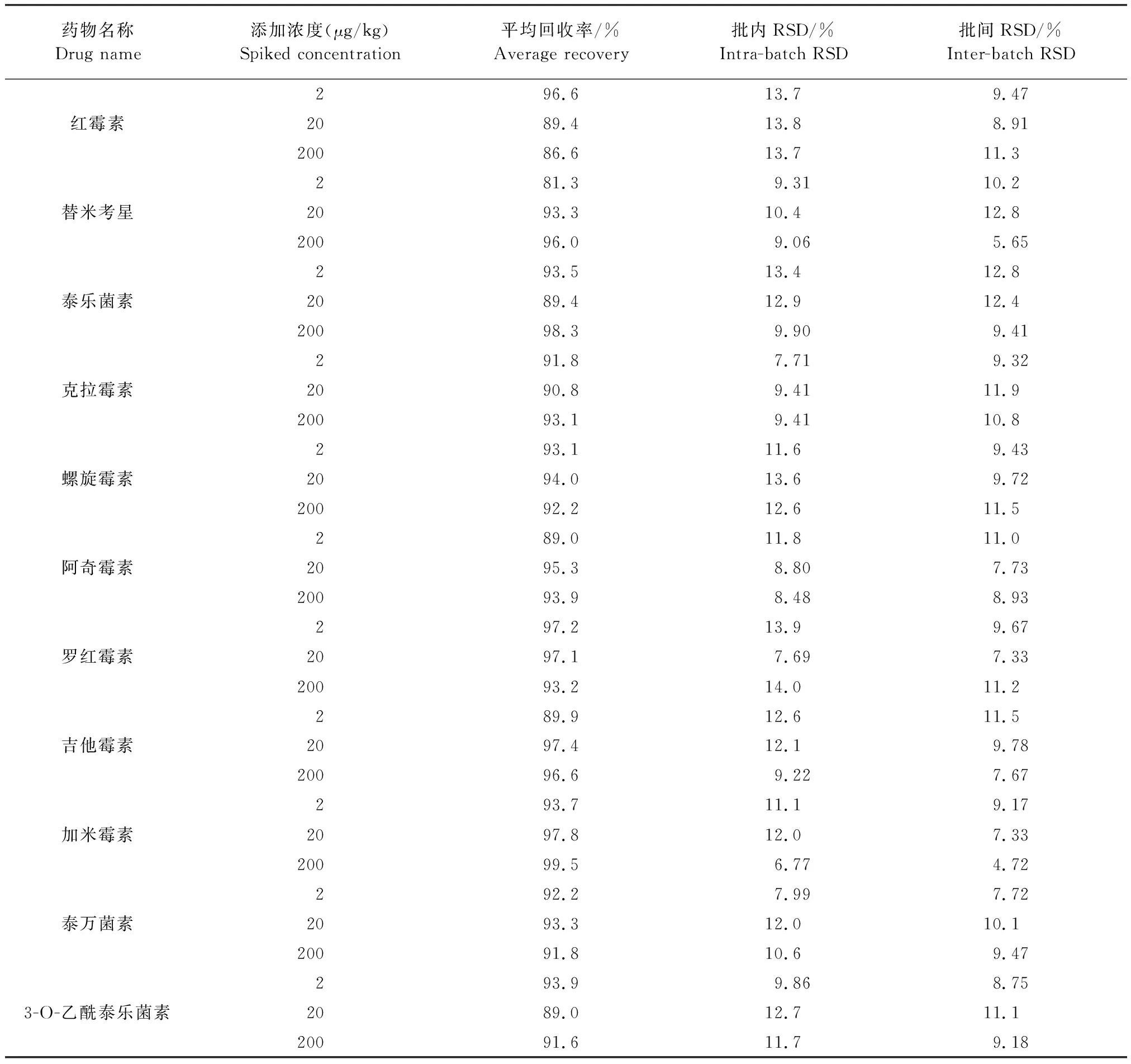
表6 空白鸭蛋中10种大环内酯类药物添加的回收率Table 6 Recoveries of 10 macrolides and a metabolite in spiked duck eggs
3 讨论
目前,我国动物可食性组织中大环内酯类药物残留检测方法的现行标准大部分是高效液相色谱法,多针对动物性食品中的单一药物或某几种药物[8-9],已有的液相色谱-串联质谱法标准也只针对单一药物或某几种药物[10-11],仅有少量文献对同时检测大环内酯类抗生素及其代谢物进行报道[12]。
目前还没有鸡蛋和鸭蛋中大环内酯类药物残留检测方法的报道,本文创新性地首次建立了鸡蛋和鸭蛋中红霉素、替米考星、泰乐菌素、克拉霉素、螺旋霉素、阿奇霉素、罗红霉素、吉他霉素、加米霉素和泰万菌素共10种药物残留的UPLC-MS/MS检测方法,为动物性食品中大环内酯类药物的残留监控提供了关键的技术支持。
液-液萃取常用于大环内酯类药物残留的定量检测,但是有机溶剂消耗大,操作耗时[13]。本方法根据称样量,选择适宜体积的80%乙腈水溶液提取1次,可以有效提取大环内酯类药物,提取步骤简便,同时通过高速离心又能很好的去除蛋白质等大量杂质的干扰,并且在不影响回收率的情况下尽可能减少过柱体积,为实际应用中大批量样品检测提供了便捷操作性。
固相萃取法是最常见的净化方式,大环内酯类药物可采用HLB柱[14]或C18柱[15]净化,经过比较试验,本方法采用Cleanert MAS-Q净化管,有效吸附备用液中脂肪及其他杂质,有效去除禽蛋样品中的大部分基质干扰,直接收集上清并过滤膜后上机检测,节省了固相萃取和浓缩步骤,有利于提高回收率。本方法定性、定量准确,前处理方法简便,是一种高灵敏度、高选择性的检测方法,对动物性食品中兽药残留风险监测提供了科学依据。
