壳聚糖纳米粒子的制备和在食品抑菌中的研究进展
2020-12-31邱婷婷李若男周丽莎赵艳云陈舜胜张洪才
谭 啸,邱婷婷,李若男,周丽莎,赵艳云,陈舜胜,张洪才,*
(1.上海海洋大学食品学院,上海 201306;2.上海水产品加工及贮藏工程技术研究中心,上海 201306;3.国家淡水水产品加工技术研发分中心(上海),上海 201306;4.俄勒冈州立大学食品科技学院,美国 俄勒冈 科瓦利斯 97331-6602)
壳聚糖是甲壳素脱乙酰基形成的产物,是常用的天然生物高分子聚合物材料,因其具有无毒、吸附性强、可降解和生物活性高等特性,近年来在食品、医药、环境和农业等领域已得到广泛应用。尽管壳聚糖具有一定的广谱抑菌性能,但与脱乙酰程度和分子质量有密切关系,此外,由于壳聚糖水溶性差,其应用也受到了很大的限制。
近年来壳聚糖纳米粒子包埋抑菌活性物质已成为国内外研究的热点,离子交联法是制备壳聚糖纳米粒子常用的方式之一(粒径小于200 nm)。如Zhang Hongcai等通过离子交联法制备儿茶素-Zn复合物装载的β-壳聚糖纳米粒子(粒径在100 nm左右),研究表明β-壳聚糖纳米粒子可显著提高儿茶素-Zn的抑菌活性,它可作为食品抑菌剂用于食品包装材料中[1]。Orellano等研究发现壳聚糖对金黄色葡萄球菌的最小抑菌浓度(minimum inhibitory concentration,MIC)为1 600 μg/mL,而壳聚糖纳米粒子为200 μg/mL,表明壳聚糖纳米粒子的抑菌效果比壳聚糖强[2]。Omidi等制备由新型吡啶类化合物接枝的壳聚糖和壳聚糖纳米粒子,研究表明新型壳聚糖衍生物纳米粒子抑菌效果和抗氧化性都得到显著提高,其中,对金黄色葡萄球菌的MIC达到81.25 μg/mL[3]。壳聚糖纳米粒子不仅具有纳米材料的体积效应、表面效应、量子尺寸效应和介电限域效应等优点,且存在抗菌性强、包埋率和灵敏度高等特点,已成为食品和农业等领域研究的热点。因此,本文综合国内外研究介绍了壳聚糖纳米粒子的制备方法和壳聚糖纳米粒子在食品抑菌应用中的研究进展,为天然抑菌剂的开发提供新的研究思路和理论参考。
1 壳聚糖纳米粒子的制备方法
1.1 离子交联法
1988 年Bodmeier等首次通过离子交联法制备壳聚糖纳米粒子[4],其原理为当壳聚糖溶解在酸性介质中时,壳聚糖上的氨基转化成带正电荷的NH3+,并与带负电荷的三聚磷酸钠(sodium tripolyphosphate,TPP)相互吸引,二者通过分子间的静电作用相互交联形成壳聚糖纳米粒子(图1)。该反应条件温和,可在室温中进行,TPP无毒且不需要添加其他化学交联剂,可应用于食品等领域中。制备壳聚糖纳米粒子有诸多影响因素,如壳聚糖的分子质量、脱乙酰程度、初始浓度、与TPP的浓度和体积比、体系pH值、搅拌速率和TPP加入方式等。Mohammadi等使用分子质量70、190 kDa和684 kDa的壳聚糖分别制备粒径为60、78 nm和105 nm的纳米粒子,结果表明分子质量越低,粒径越小,抗菌性越强[5]。Fan Wen等研究不同壳聚糖和TPP的比例制备纳米粒子,结果表明当壳聚糖和TPP的质量比在3:1时,纳米粒子的粒径最小(138 nm)[6]。Sreekumar等研究了壳聚糖质量浓度、壳聚糖的脱乙酰程度、壳聚糖和TPP的物质的量之比对离子交联法制备壳聚糖纳米粒子的影响以及各因素之间的相互作用,结果表明对于当NH2∶PO4物质的量之比为3∶2时,壳聚糖质量浓度对粒径的影响较大,且随壳聚糖浓度的增加粒径也增加,不同浓度的壳聚糖都能得到从微米到纳米的颗粒,但是需要特定的NH2与PO4物质的量之比。此外,其还发现纳米颗粒的形成及其粒径与溶液中盐的存在有一定的关系[7]。Kaloti等研究了不同壳聚糖质量浓度、壳聚糖与TPP体积比例以及pH值条件下制备纳米粒子,纳米粒子的尺寸受壳聚糖浓度和混合物比例影响较大,高浓度的壳聚糖和高的壳聚糖与TPP体积比导致纳米粒子的尺寸变大。当壳聚糖质量浓度大于0.5 mg/mL,壳聚糖与TPP的体积比大于2∶1,壳聚糖纳米粒子的粒径为150~350 nm[8]。此外,Fàbregas等研究不同搅拌速率对壳聚糖纳米粒子粒径的影响,在相同条件下,当搅拌速率为800 r/min时,粒径105~209 nm的粒子分布最广[9]。

图1 TPP与壳聚糖离子交联制备纳米粒子Fig.1 Cross-linking of sodium tripolyphosphate and chitosan for the preparation of nanoparticles

表1 离子交联法制备壳聚糖纳米粒子的条件Table 1 Preparation conditions for chitosan nanoparticles by ionic cross-linking
纳米粒子的粒径越小,Zeta-电位越高,包埋率和装载量越高且具有缓释作用。陈文彬等制备α-生育酚装载的壳聚糖纳米粒子,平均粒径和包埋率分别为214 nm和51.65%,体外缓释实验发现在12 h内,纳米粒子存在明显的突释,此后缓慢释放,且在不同的酸碱性环境中纳米粒子呈现不同的缓释速率[10]。这主要是由于前期纳米粒子表面会附着包埋物,较易从体系中释放出来,而后物质的释放分为体系瓦解、表面侵蚀、扩散等阶段,因此较为缓慢。Zhang Hongcai等采用离子交联法,使用两种不同分子质量的壳聚糖制备出包埋β-半乳糖苷酶的壳聚糖纳米粒子,粒径分别为584.37 nm和652.46 nm、Zeta-电位分别为26.37 mV和16.46 mV、包埋率分别为68.32%和58.64%。研究表明包埋体系具有良好的缓释效果,可用于治疗乳糖不耐症或用于奶制品[11]。离子交联法制备壳聚糖纳米粒子的条件如表1所示。离子交联法由于具有制备过程简单、条件可控、细胞毒性低、生物相容性好和包埋率高等优点,已广泛应用于医药、农业、环境和食品等领域。
1.2 其他制备方法
除了离子交联法外,乳化交联法、化学交联法、凝聚法、喷雾干燥法、乳液液滴聚合法和层层自组装法也可用来制备壳聚糖纳米粒子。
乳化交联法是将包埋物与壳聚糖制备成不同类型的乳液。根据乳液的类型分为单乳法(O/W型、W/O型和O/O型)和复乳法(W/O/W型和O/W/O型)。然后通过连续搅拌加入交联剂使内相固化制备纳米粒。常用的交联剂有戊二醛、甲醛等。Riegger等采用乳化交联法成功制备了壳聚糖纳米粒子并装载了双氯芬酸和卡马西平,壳聚糖纳米粒子的粒径随着壳聚糖分子质量的增加而增加,最低粒径为109.9 nm,最高为200.3 nm[19]。
化学交联法是利用壳聚糖氨基与醛类化合物(戊二醛)进行交联发生氨醛缩合反应制备壳聚糖纳米粒子的方法。Sadighian等以戊二醛为交联剂,与壳聚糖溶液(含铁离子)进行交联反应,制备包埋了阿霉素的磁性壳聚糖纳米颗粒,阿霉素的有效载药量达到71%[20]。尽管化学交联法制备的纳米粒子稳定性好且吸附能力强,但粒径较大,且戊二醛的添加限制了其在食品中的应用。
凝聚法是通过降低壳聚糖在溶液中的溶解度,而析出沉淀制备壳聚糖颗粒,可分为单凝聚和复凝聚。单凝聚法是将芯材分散于高分子壁材中,通过加入凝聚剂(硫酸盐等)降低壳聚糖溶解度从而析出制备微球。复凝聚法是指采用两种带有不同电荷的壁材包埋芯材,通过调节体系的pH值、溶液浓度及温度等条件,使不同材料之间相互交联,溶解度降低,分离得到微粒。Butstraen等采用复凝聚法制备阿拉伯树胶-壳聚糖微胶囊,研究了相体积比、搅拌速率和搅拌时间、pH值、反应时间、交联剂等条件对微胶囊形成的影响,在最佳条件下微胶囊粒径在5~10 μm之间[21]。虽然凝聚法包埋率较高但制备的粒子粒径较大,用于食品抑菌中会出现包埋的抑菌剂释放速率慢和短期抑菌效果差等缺陷。
喷雾干燥法是将芯材分散在壁材溶液中,然后在热气流作用下使溶剂迅速蒸发,壁材将芯材包埋形成微球粉末。喷雾干燥法具有操作简单、成本低、利于规模化生产等优点。Tavares等采用喷雾干燥法制备乳清蛋白和壳聚糖复合纳米颗粒包埋大蒜提取物,纳米颗粒包封性好、表面无裂纹,对大蒜提取物有良好的保护作用且微粒有较好的水溶性,可用于食品工业中[22]。Li Yue等采用喷雾干燥法制备壳聚糖包埋橘油的微胶囊,微胶囊平均粒径小于20 μm,具有规则的形态,橘油包埋率在90%以上[23]。尽管喷雾干燥法可批量生产,但粒径大,且包埋物暴露在高温中易被破坏(氧化、分解),因此不适用于包埋热敏性物质,在食品中的应用受到限制。
自组装是大分子物质通过分子间弱的非共价键作用,如氢键作用、静电作用和范德华作用等自发形成特定结构和功能的有序聚集体。Zou Liqiang等采用层层自主装法将表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)包埋在壳聚糖纳米粒子中,包埋率达到90.8%,能有效地减缓EGCG在模拟肠液中的降解[24]。张力等以明胶和壳聚糖为载体,采用自组装法制备丁香酚-明胶-壳聚糖纳米胶囊。壳聚糖、明胶和丁香酚质量浓度分别为2、2、5 mg/mL,交联30 min制得的纳米粒子粒径为229.09 nm,包埋率达到50.69%,具有一定的缓释效果。该工艺提高了丁香酚生物利用度,拓宽了其在食品防腐中的应用范围[25]。
自组装法制备的聚集体,因不需要添加表面活性剂或乳化剂,具有工艺简单和可调控等优点,是制备纳米粒子的重要手段。此外,壳聚糖分子中存在大量的氨基和羟基,可以接枝众多官能团从而使壳聚糖具有新的功能。然而,自组装法制备的聚集体粒径大、物理稳定性能差等缺点使其在食品中的应用受到限制。但随着科技的不断发展,自组装法将会在不同领域发挥重要的作用。
2 壳聚糖纳米粒子包埋物的体外释放
包埋物装载的壳聚糖纳米粒子可改变包裹物质的释放方式,从而具有明显控制其释放和延长包裹物质的体内外作用。包裹的纳米粒子主要通过4 种方式进行释放:1)从完整的纳米粒子基质中扩散;2)通过纳米粒子的溶胀进行释放;3)通过纳米粒子的分裂进行释放;4)通过纳米粒子的腐蚀进行释放(图2[26])。
包裹物质的溶出度是壳聚糖纳米粒子的重要质量指标,能直接反映壳聚糖纳米粒子中包裹物质的释放速率,可用于比较壳聚糖纳米粒子的性能。包裹物质的释放速率、壳聚糖纳米粒子的理化性质(如粒径尺寸和溶液物化性质等)和包埋药物的比例有密切关系。如亲水性物质比亲脂性物质释放速率快,粒径越小、纳米粒子表面积越大,药物释放速率越快。传统的溶剂蒸发和喷雾干燥等技术制备的壳聚糖纳米粒子因骨架密度低,活性物质只能吸附在壳聚糖纳米粒子表面,无法避免突然释放,而离子交联法可在一定程度上避免上述缺陷。

图2 包裹在壳聚糖纳米粒子中活性成分的释放机制[26]Fig.2 Release mechanism of active components in chitosan nanoparticles[26]
3 壳聚糖在食品抑菌中的应用
3.1 壳聚糖纳米粒子的抑菌机理
壳聚糖纳米粒子的抑菌机理见图3[27]。壳聚糖的氨基(—NH3+)带正电荷,而细胞壁中的磷脂带负电荷,两者的电荷相互吸引导致细胞膜破裂,从而起到抑菌作用;壳聚糖能够在细胞核中阻止遗传因子的转录进而阻碍蛋白质合成;此外,壳聚糖的抑菌特性受诸多因素(脱乙酰程度、分子质量、微生物种类、离子强度和pH值等)影响[28]。抑菌机理主要依靠壳聚糖纳米粒子的尺寸效应,纳米尺寸的壳聚糖粒子可进入细菌细胞膜的内部,引起细胞表面磷脂双分子层破裂而导致细胞内容物的渗漏,使细胞膜内外的渗透压不平衡而导致细菌死亡。

图3 壳聚糖纳米粒子抗菌活性的可能机制[27]Fig.3 Suggested mechanism of antibacterial activity of chitosan nanoparticles[27]
3.2 壳聚糖纳米粒子在食品抗菌中的应用
壳聚糖纳米粒子比壳聚糖具有更强的抗菌性,在食品保鲜包装中得到广泛应用。Hajji等采用离子交联法制备了最小粒径为121.6 nm的壳聚糖纳米粒子,并在4 ℃下对鱼糜进行保藏,发现在9 d的贮藏期内壳聚糖纳米粒子的涂覆可以抑制微生物的生长和鱼糜脂质的氧化,有效延长货架期[29]。此外,由于壳聚糖纳米粒子包埋率高、缓释性好和条件可控等特性,将壳聚糖纳米粒子作为包埋物的输送和缓释载体也是国内外研究的热点。Liu Yong等以壳聚糖纳米粒子作为α-半乳糖苷酶的包埋材料,在最优条件下(pH 5.5、壳聚糖质量浓度2 mg/mL、α-半乳糖苷酶质量浓度0.2 mg/mL、壳聚糖与TPP体积比为4∶1),酶的包埋率超过60%,活性和热稳定性都得到显著提高[30]。壳聚糖纳米粒子可用于包埋各类精油、溶菌酶、鱼精蛋白和多酚类物质等天然抑菌剂,用于保鲜果蔬、肉制品、奶制品和水产品。
壳聚糖纳米粒子包埋抗菌剂不仅可提高活性物质的稳定性和延长活性物质的释放时间,也可起到缓释抗菌剂的作用(图4)。朱玉林等采用聚合物静电自组装法制备乳酸链球菌肽(Nisin)-壳聚糖纳米颗粒,3 d后Nisin-壳聚糖纳米颗粒处理的样品菌落数仍在3.7(lg(CFU/mL))左右,表明Nisin(乳酸链球菌素)可缓慢释放,对模拟炼乳体系中的李斯特菌具有较好的抑菌效果[31]。Lin Lin等通过离子交联法制备包埋辣木精油的壳聚糖纳米粒子,最高包埋率(41.3%)时粒径为143.8 nm,抗菌实验表明,壳聚糖纳米粒子包埋辣木精油用于奶酪在4 ℃下保藏10 d时,李斯特菌和金黄色葡萄球菌分别减少78.63%和98.67%,且对奶酪的感官品质几乎无影响[32]。Li Feng等通过离子交联法制备儿茶素和槲皮素同时装载的壳聚糖纳米颗粒,平均粒径为180.4 nm,儿茶素和槲皮素的包埋率分别为76.35%和52.23%,且均可在体外持续释放,包埋后抑菌性能显著增强,儿茶素和槲皮素装载的壳聚糖纳米粒子对大肠杆菌和金黄色葡萄球菌抑菌圈直径分别为13.2 mm和12.85 mm[33]。

图4 壳聚糖纳米粒子中生物活性物质的释放Fig.4 Schematic diagram showing the release of bioactive ingredients from chitosan nanoparticles
肉桂精油作为一种有效的抗菌剂,存在高挥发性和低稳定性的缺点。Matshetshe等利用β-环糊精改性壳聚糖纳米粒子并包埋肉桂精油,包埋体系的最大包埋率和最优粒径范围分别达到58.03%和216.14~591.92 nm,其体外释放依赖于环境的pH值,当pH 4.5时,肉桂精油在120 h内的释放量为71%。壳聚糖纳米粒子可有效保护肉桂精油以提高其抗菌效果[34]。Hasheminejad等分两步制备丁香精油装载的壳聚糖纳米粒子,首先以壳聚糖和丁香精油制备成W/O体系,调节pH为4.6,以Tween-80作为表面活性剂,然后加入TPP自发形成纳米粒子。在壳聚糖、丁香精油、TPP质量比为1∶1∶1时粒径为268.47 nm,包埋率为31%。抗菌实验表明与游离精油和壳聚糖纳米粒子相比,壳聚糖纳米粒子包埋的丁香精油对黑曲霉的抑制作用得到显著增强,这种良好的抑菌效果与纳米粒子对丁香精油的控释以及壳聚糖纳米粒子本身的抑菌特性有关[35]。Paomephan等研究表明大粒径和小粒径的壳聚糖纳米粒子对蔬菜中大肠肝菌(减少3.38(lg(CFU/mL)))和沙门氏菌具有显著的抑菌效果[36]。Kavaz等制备节莎草根精油装载的壳聚糖纳米粒子(0.25∶1,m/m),粒径和包埋率分别为119 nm和40.28%,对大肠杆菌的MIC从10 mg/L减少到5 mg/L[37]。已有较多研究表明壳聚糖纳米粒子可作为多种抑菌活性物质的包埋体系用于保护和提高抗菌性,并广泛应用于食品保鲜中,然而关于其可控释放、更深层次的抗菌机理以及安全性还有待进一步研究。包裹活性物质的壳聚糖纳米粒子制备方法及其抑菌性能如表2所示,壳聚糖纳米粒子的包埋在保护生物活性物质的同时,还具有很好的缓释效果。
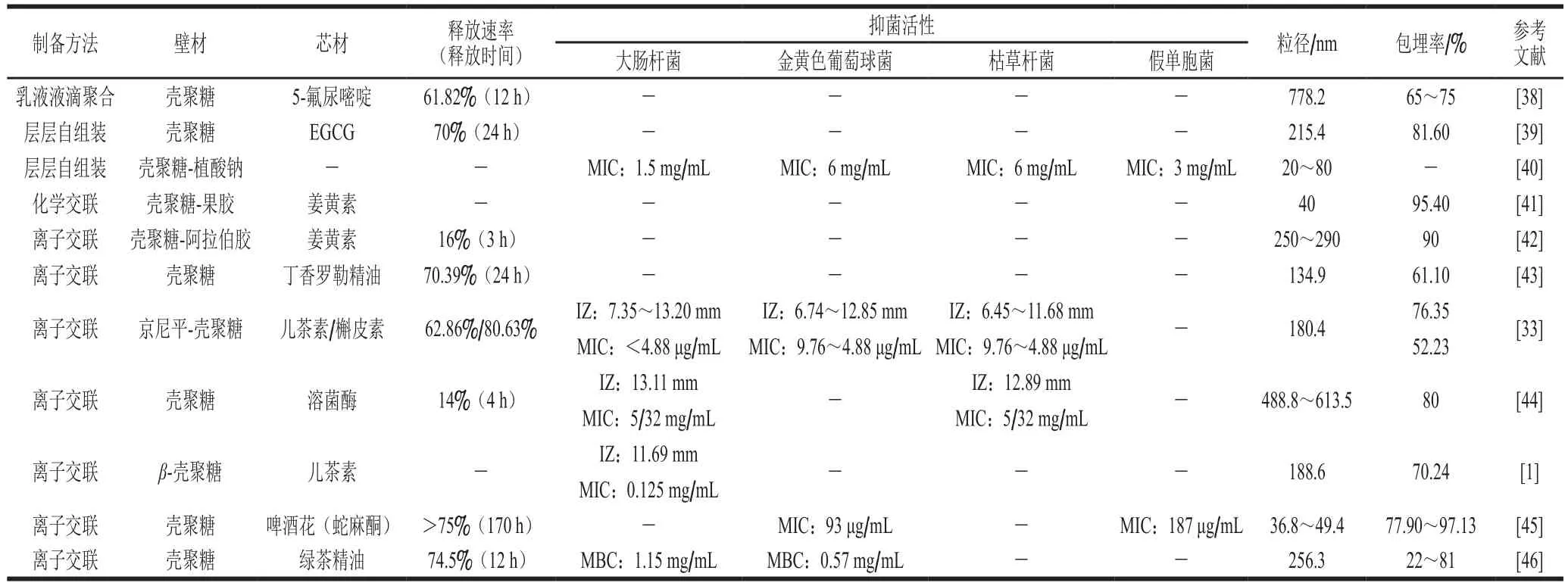
表2 壳聚糖纳米粒子的制备方法和抑菌性能Table 2 Preparation methods and antibacterial properties of chitosan nanoparticles
4 结 语
壳聚糖具有可食性、生物相容性、无毒、抗氧化和抗菌性等优点,已广泛应用于食品、环境、医药和纺织等领域。近年来对壳聚糖的研究不局限于壳聚糖本身,对于壳聚糖衍生物、壳聚糖复合膜和壳聚糖纳米粒子国内外都有广泛报道。其中壳聚糖纳米粒子是近5 年来研究的热点。尽管壳聚糖纳米粒子的制备方法较多,但离子交联法制备的壳聚糖纳米粒子因具有生物安全性高、粒径小、条件可控和包埋率高等优点,在食品领域中得到广泛应用。
天然抑菌剂稳定性差、易受外界环境(温度、光照和pH值等)的影响,壳聚糖纳米粒子可作为抑菌剂的载体,用于提高包埋物的生物可利用度和拓宽抑菌剂的应用领域。此外,纳米粒子还可延缓抑菌剂的释放从而延长食品的货架期。如何更加有效地控制活性物质的释放和探讨壳聚糖纳米粒子的抑菌机制仍是后续需要解决的难题。
壳聚糖纳米粒子的生物安全性问题近年来也受到广泛关注,有研究报道壳聚糖纳米粒子可能会对保鲜对象的组织细胞有杀伤作用。尽管已有大量文献报道通过细胞噻唑蓝检测和组织切片发现壳聚糖纳米粒子对细胞活性基本没有影响,但对纳米粒子的生物安全性综合评价也是其在食品抑菌应用中需要重视的问题。
