复合凝聚法制备绿咖啡油微胶囊及其性能
2020-12-31董文江龙宇宙胡荣锁陈治华蒋快乐
谭 睿,申 瑾,董文江*,章 中,*,龙宇宙,胡荣锁,3,陈治华,蒋快乐
(1.宁夏大学农学院,宁夏 银川 750021;2.中国热带农业科学院香料饮料研究所,海南 万宁 571533;3.海南省热带作物工程技术研究中心,海南 万宁 571533;4.云南农业大学热带作物学院,云南 普洱 665000)
咖啡为茜草科、咖啡属植物,起源于埃塞俄比亚和刚果,由于咖啡独特的风味,以及具有提神醒脑、减肥、抗氧化等各种生理功能而被人们所喜爱[1]。咖啡为我国重要的特色热带饮料作物,亦是海南和云南地区农民增收致富的优势特色产业,目前我国咖啡种植面积已达180万 亩,年产咖啡15.0万 t,产值超过25.8亿 元。但我国咖啡豆主要以初级原料豆出口为主,深加工研究较少,绿咖啡油是从生咖啡豆中提取的油脂,导致其综合效益偏低;中粒种和小粒种咖啡油中脂肪酸组分分别为亚油酸(46.3%和44.0%)、棕榈酸(30.2%和31.3%)、油酸(10.6%和12.5%)和硬脂酸(8.0%和5.9%)[2],绿咖啡油具有润肤和防紫外线辐射作用,已被广泛用于化妆品工业。由于绿咖啡油中不饱和脂肪酸含量较高,易氧化变质,进而影响其感官和风味品质,氧化酸败产生的醛酮类挥发性物质亦对人体有害,因此采用微胶囊化包埋绿咖啡油,提高其氧化稳定性尤为必要。
微胶囊化被定义为一个过程,在此过程中,微小的颗粒或液滴被涂层包围,或嵌入均匀或非均匀的基质中,从而使小胶囊具有较多优异的性能[3]。微胶囊化的咖啡油比未胶囊化的咖啡油具有更高的氧化稳定性,并能在高双萜的情况下保持较高的日光防护系数。Frascareli等[4]采用响应面法优化了喷雾干燥法使用阿拉伯胶作为壁材制备绿咖啡油微胶囊的工艺条件;Carvalho等[5]采用静电逐层沉积技术,采用喷雾干燥法制备绿咖啡油微胶囊,以卵磷脂壳聚糖稳定的Hi-Cap100和玉米糖浆/Hi-Cap100制备的微颗粒氧化稳定性最高。微胶囊的防晒系数在1.52~2.45之间,接近纯绿咖啡油;Freiberger等[6]用聚乳酸和聚羟基丁酸酯-羟基戊酸酯为包封剂,采用微乳化-溶剂蒸发技术制备了烘烤咖啡油纳米胶囊,这种油的微胶囊化改善了其在粉状化妆品中的应用,并减少了肉桂酸的过敏反应,当直接应用于皮肤上时,可导致过敏。
复凝聚法制备微胶囊是利用两种水溶性高分子,在改变溶液pH值时生成的相反电荷通过静电作用引起凝聚而形成聚合物的反应。当带正电荷的胶体溶液与带负电荷的胶体溶液相混合时,异种电荷的相互作用形成聚电解质复合物而发生分离,壁材在芯材周围沉积而得到微胶囊。复合凝聚法具有操作简单、成本低、可扩展性和可重复性等优点,可用于食品配料的封装,即使在非常高的负载下也能产生较高的封装效率[7]。复合凝聚法是包埋脂溶性食品配料的常用方法,该方法不需要专用设备,工艺条件较为温和,工艺过程对芯材品质的损伤较小,且得到的微胶囊产品载量较高,对于脂溶性芯材具有良好的延缓氧化以及控制释放的功能[8]。然而,到目前为止还鲜见采用复合凝聚法制备绿咖啡油微胶囊方面的报道。
本实验通过明胶(gelatin,G)结合3 种多糖阿拉伯胶(gum arabic,GA)、果胶(pectin,P)、羧甲基纤维素钠(sodium carboxymethyl cellulose,CMC)3 种壁材,采用复合凝聚法制备绿咖啡油微胶囊,通过对微胶囊形态表征、包埋率、粒径等进行比较,筛选出包埋绿咖啡油的最适壁材。本研究通过制备出性能优良的绿咖啡油微胶囊,以期为绿咖啡油的高值化利用提供理论依据和技术支撑。
1 材料与方法
1.1 材料与试剂
绿咖啡油 雅克耶提芳香医药科技(青岛)有限公司;明胶、阿拉伯胶 中国医药集团上海化学试剂有限公司;高酯果胶(121型) 美国斯比凯克公司;羧甲基纤维素钠(FL9、黏度300) 上海申光食品化学品有限公司;实验用水全部为超纯水;其他试剂均为分析纯。
1.2 仪器与设备
Magic LAB多功能乳化分散机、RW20.n悬臂式搅拌器德国IKA公司;SevenCompact S220 pH计 Mettler-Toledo仪器(上海)有限公司;UV-2450紫外分光光度计日本岛津公司;SCIENTZ-18ND真空冷冻干燥机宁波新芝生物科技股份有限公司;R-215旋转蒸发仪瑞士BUCHI有限公司;RS552NRUAWW/SC冰箱 苏州三星电子有限公司;DF-101集热式恒温加热磁力搅拌器巩义市予华仪器责任有限公司;Mastersizer 3000激光粒度仪 英国马尔文仪器有限公司;CX23生物显微镜日本奥林巴斯公司;JXN-26高速冷冻型离心机 美国贝克曼库尔特有限公司;Nicolet 6700傅里叶变换红外光谱仪 美国Thermo Fisher公司;STA 449F3热分析仪德国NETZSCH公司。
1.3 方法
1.3.1 反应pH值的确定
在对绿咖啡油进行包埋之前,需要确定明胶与阿拉伯胶、果胶、羧甲基纤维素钠的最佳反应pH值条件;壁材组成和反应pH值条件是影响复凝聚反应的关键因素,壁材组成不同,发生复凝聚的pH值范围就不同。参考杜歌[9]、Muhoza[10]和赖凌峰[11]等的方法,以1 g/L的总生物聚合物质量浓度,分别制备了明胶/阿拉伯胶(质量比1∶1)、明胶/果胶(3∶1)、明胶/羧甲基纤维素钠(9∶1)的混合物,在45 ℃水浴下,以体积分数分别为10%、1%、0.1%的醋酸对生物聚合物溶液进行浊度滴定。
1.3.2 复聚物及微胶囊制备
复聚物的制备:参照Dong Die等[12]方法,并稍作修改。将壁材按表1中比例混合均匀制成1%溶液,明胶、果胶原液混合前pH值分别调整至7.0,其中果胶溶液pH值为3.5,将pH值调整为7.0,以防止混合过程中明胶和果胶之间静电吸引而形成复合物。保持体系温度40 ℃,搅拌速率400 r/min,用10%醋酸调节pH值,凝聚20 min。冰水浴降温至15 ℃以下,保持30 min。用1% NaOH调节体系pH值至6.0,静置,分层,离心分离,去除上清液后,均匀平铺于培养皿内,在贮藏温度为-16 ℃时预冻过夜后,-4 ℃时冷冻干燥,干燥时间48 h。所得样品置于高密度聚乙烯袋装中并保存于冰箱(-20 ℃)。
微胶囊的制备:按表1配制1%的壁材溶液后,以芯壁质量比1∶1加入绿咖啡油,在20 000 r/min下高速分散均质乳化3 min。后续制备过程同上。

表1 复合凝聚法制备绿咖啡油微胶囊工艺参数Table 1 Process parameters for the preparation of green coffee oil microcapsules by complex coacervation
1.3.3 形态表征
光学显微镜观察:采用光学显微镜对湿囊形态进行形态观察,并将相机与电脑连接,以400 倍的放大倍数收集湿囊的图像。
1.3.4 微胶囊水分质量分数测定
精密称取0.5 g真空冷冻干燥好的微胶囊样品,均匀置于快速水分测定仪样品盘上进行水分质量分数测定。每个样品平行测定3 次。
1.3.5 产率、包埋率、壁材利用率、载量的测定
将干燥后的总油质量除以初始油质量来计算油的产率(式(1)):

壁材利用率指微胶囊去除总油后与加入的初始壁材质量之比(式(3)):

载量按式(4)计算:

表面油含量根据QB/T 4791—2015《植脂末》测定[13]。
采用GB 5009.6—2016《食品安全国家标准 食品中脂肪的测定》的酸水解法测定微胶囊中总油含量[14]。
1.3.6 微胶囊的粒度分布
通过Mastersizer 3000激光粒度仪对微胶囊湿囊进行测定,去离子水作为分散剂,设置材料折射率为1.59,水分散剂折射率为1.33[15],将微胶囊湿囊缓慢加入到去离子水中至适宜浓度,直至遮光度达到适宜测定范围内。每个样品的粒度平行测定3 次。
1.3.7 微胶囊的傅里叶变换红外光谱分析
将微胶囊分别通过傅里叶变换红外光谱仪在室温下进行测定,加入样品质量50~100 倍的溴化钾后进行研磨,压片机压制成片,选用空白溴化钾片作为对照。置于红外光谱仪上,于400~4 000 cm-1范围内进行扫描,扫描次数为32 次,分辨率为4 cm-1。利用PeakFit v4.12软件在谱带范围内(酰胺I带1 600~1 700 cm-1)校正基线,然后用Gaussian去卷积,进行二阶导数拟合,多次拟合使残差最小。根据峰面积计算出明胶及其复聚物蛋白质二级结构相对含量。
1.3.8 热重分析
将壁材、复聚物、咖啡油微胶囊(3~5 mg)置于小坩埚中,设置仪器参数温度范围30~600 ℃,升温速率10 ℃/min,载气为氮气,流速为20 mL/min,测定样品的热释放曲线。
1.4 数据统计分析
数据的显著性分析均采用SPSS 24.0软件进行处理和分析,并采用Origin 9.0软件作图。所有实验均进行3 次重复实验,结果以平均值±标准偏差表示。
2 结果与分析
2.1 明胶与3 种多糖复合凝聚的pH值

图1 明胶/阿拉伯胶、明胶/果胶、明胶/羧甲基纤维素钠多糖浊度滴定曲线Fig.1 Turbidity versus pH curves of gelatin combined with each of three polysaccharides
发生于生物大分子之间的复合凝聚反应,随着pH值的改变会经历若干胶体形态,而这些转变从外观上可表现为体系浊度的变化。因此,浊度滴定被广泛应用于追踪复合凝聚反应的整体过程,同时浊度滴定曲线被用作选择最适混合比例及相应的pH值条件,所得出的最适条件即可应用于微胶囊的制备。图1所示即为明胶/阿拉伯胶、明胶/果胶、明胶/羧甲基纤维素钠不同比例下的pH值浊度曲线。在滴定开始阶段,浊度值几乎为0,溶液呈现均一、透明外观,这是因为明胶与阴离子多糖均带负电,相互之间的静电排斥力使得体系没有复聚物产生,该阶段被称为分离的相行为[16]。随着pH值的缓慢下降,少量的可溶性复聚物产生,溶液开始略微泛白,体系浊度开始缓慢上升,开始形成可溶性复合物。当pH值继续下降时,形成的可溶性复合物发生了结构间的重排,形成相对紧密的结构,即不可溶性复合物,此时,浊度急速上升,溶液逐渐变为不透光的乳白色。浊度的峰值意味着明胶与阴离子多糖之间的静电相互作用达到了最大值,当浊度跨越峰值,进入下降阶段,生物聚合物溶液开始变得透明。明胶/阿拉伯胶、明胶/果胶、明胶/羧甲基纤维素钠的最适pH值分别为4.00、4.23、4.85。本实验的研究结果与杜歌[9]和Muhoza[10]等报道相一致,明胶/羧甲基纤维素钠的最适pH值与赖凌峰[11]研究结果略有不同,可能是由于在选择的羧甲基纤维素钠种类中型号不同,最佳条件也会发生细微变化[17]。
2.2 微胶囊形态光学显微镜观察结果
由于芯材、壁材不同,微胶囊的大小和形态变化较大。图2所示为光学显微镜下明胶结合不同阴离子多糖阿拉伯胶、果胶、羧甲基纤维素钠复合凝聚法制备的微胶囊空囊及咖啡油微胶囊形态图。在光学显微图像中,不同壁材组合通过复合凝聚法制得微胶囊空囊及咖啡油微胶囊的形态都呈规则的圆形。Lü Yi等[17]研究得出通过复合凝聚得到的粒子呈球形的。单位表面积下,球状结构由于具有相对更大的体积,因而具有更大的包覆芯材物质的潜能[10],并具有更好的缓释性能;3 种壁材组合制备的咖啡油微胶囊显微图像呈球形多核结构,囊壁结构完整,芯材被包裹在囊壁中,因此认为咖啡油被成功胶囊化,对芯材产生良好的保护作用,并且粒径具有明显区别,说明不同壁材组合对微胶囊产品的大小有显著影响。

图2 明胶/阿拉伯胶、明胶/果胶、明胶/羧甲基纤维素钠复聚物及其绿咖啡油微胶囊显微镜图Fig.2 Micrographs of G/GA, G/P and G/CMC complexes, and green coffee oil microcapsules
由图2可知,咖啡油完全被复聚物包裹,复聚物和微胶囊都呈球形,单位表面积下,球状结构由于具有相对更大的体积,因而这3 种复聚物具有更大的包覆芯材物质的潜能。芯材咖啡油对微胶囊颗粒大小与形状影响不明显,但是不同壁材组合对复聚物和微胶囊的颗粒尺寸影响较为明显,其中明胶/羧甲基纤维素钠的颗粒最大,明胶/阿拉伯胶次之,明胶/果胶最小,通过使用不同的壁材组合,可以使稳定的输送系统具有理想的尺寸。已有报道表明[18-19],生物聚合物的黏度、分子质量和乳化性能对复合凝聚法制备微胶囊大小具有显著影响。
2.3 绿咖啡油微胶囊产品理化指标

表2 绿咖啡油微胶囊产品理化指标Table 2 Physicochemical indexes of green coffee oil microcapsules
微胶囊产品的水分质量分数是一个很重要的指标,过高的水分质量分数会让产品在储藏过程中结块,霉变,也会增加油脂的氧化速率。表2中微胶囊的水分质量分数表明,干燥后的微胶囊中水分质量分数较低,使微胶囊较为容易保存。微胶囊的产率和包埋率是评价包埋效果的重要指标,它能够反应芯材被包埋的程度,也是微胶囊制备工艺中的重要指标,可影响到生产工艺及最终产品的性质[20]。由表2可知,明胶结合不同阴离子多糖阿拉伯胶、果胶、羧甲基纤维素钠的不同壁材组合,复合凝聚法制备的微胶囊产率都达到了90%以上,包埋率85%以上,可以得出3 种壁材包埋绿咖啡油都比较适合制备微胶囊,该结果与Yuan Yuan等[21]的研究结果相一致。对微胶囊产品特性进行显著性分析,得出3 种不同壁材组合制备的微胶囊产率没有显著性差异(P>0.05),其载量、包埋率、壁材利用率具有显著性差异(P<0.05)。明胶/阿拉伯胶的载量最高,明胶/果胶的载量最低,这是由于三者壁芯比相同,在产率相差不大情况下,明胶/阿拉伯胶的壁材利用率最低,明胶/果胶的壁材利用率最高,所导致的芯材占比不同。静电吸引是复合凝聚过程中的主要驱动力之一,在相分离的情况下,电荷密度尤为重要。高电荷密度通常会导致沉淀,而在低电荷密度下,则很容易诱发液体凝聚[17],果胶、羧甲基纤维素钠的电荷密度比阿拉伯胶大,会导致其壁材利用率比较大。明胶/果胶的壁材利用率最高,较高的复聚物利用率为芯材的包覆提供了更多的壁材,同时为获得高载量的复合凝聚微胶囊创造了条件[11],且壁材利用率较高可以降低生产成本。
2.4 粒径分布分析
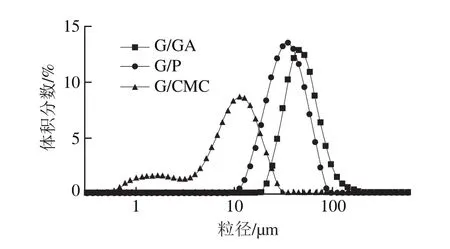
图3 绿咖啡油微胶囊的粒径分布Fig.3 Particle size distribution of green coffee oil microcapsules

表3 不同壁材复合凝聚绿咖啡油的平均粒径Table 3 Average particle sizes of green coffee oil microcapsules prepared with different wall material combinations
微胶囊的粒径及其分布状态是微胶囊产品的重要参数。粒径是评价微胶囊乳液体系质量的一个重要参数,特别是从食品配料的应用角度来看,因为颗粒过大可能会造成口感不适[22]。此外,大颗粒可以延长活性化合物的释放时间[23]。粒径分布结果如图3所示,明胶/阿拉伯胶、明胶/羧甲基纤维素钠微胶囊的粒径呈正态分布并且相对较为狭窄,说明在最佳工艺条件下制备的微胶囊粒径大小较为均匀,分散性良好。3 种壁材组合制得的微胶囊平均粒径(D4.3)和径距如表3所示,平均粒径不同,明胶/羧甲基纤维素钠>明胶/阿拉伯胶>明胶/果胶,粒径在60 μm以下。明胶/阿拉伯胶、明胶/羧甲基纤维素钠具有更低的径距(1.1左右),而明胶/果胶的径距最大(1.8),体系粒径的多分散性更加明显,更高的跨度值意味着更广泛的粒子分布。
2.5 壁材、明胶/多糖复聚物的红外光谱图分析

图4 明胶、阿拉伯胶、果胶、羧甲基纤维素钠的红外光谱图Fig.4 Infrared spectra of gelatin, arabic gum, pectin and sodium methylcellulose

图5 复聚物的红外光谱图Fig.5 Infrared spectra of complexes
红外光谱是生物高分子和其聚合物结构分析的有力工具,通过红外光谱的扫描分析,可以显示出各物质的分子结构和具有特征性的化学键[24]。本实验通过红外光谱分析可获取有关明胶、阴离子多糖和咖啡油之间复合凝聚过程中相互作用的信息。图4、5分别表示的是明胶、阴离子多糖及其各自复聚物的红外光谱图[25]。从3 种复聚物图谱中可看出,复聚物的红外谱图类似于明胶与阴离子多糖的叠加,但仍有一些吸收峰位置发生了改变。复聚物光谱中明胶代表N-H键伸缩振动的3 444 cm-1被移至较低的波数。阿拉伯胶、羧甲基纤维素中代表受氢键影响的-OH伸缩振动峰3 413、3 420 cm-1也被移至较低波数,而果胶的3 389 cm-1升高至3 433 cm-1。这可能是由于明胶和多糖分子构象的改变,以及在凝聚过程中分子间相互作用能量的降低。复聚物中代表C-H拉伸振动的2 930 cm-1左右的峰被移至较高的波数,C-H键的这种变化反映了明胶与多糖在复合凝聚形成过程中构象的变化,这是明胶和阴离子聚合物相互作用的又一迹象,新的峰值也被认为是一个指标的蛋白质过量电荷和更高的相互作用[26]。
在明胶/多糖复聚物中,可以观察到酰胺I带代表-C=O的伸缩振动峰从1 643 cm-1位移至1 659~1 669 cm-1范围。这一变化可能是由于在复杂的凝聚过程中,带负电荷的多糖与带正电荷的明胶相结合。多糖分子中代表-COO-伸缩振动的峰1 615、1 635、1 647 cm-1被移至较高的波数以及1 423、1 441、1 423 cm-1处峰的消失,表明了羧基参与了复合凝聚物的形成。此外,这两种生物聚合物之间的复杂凝聚改变了羰基-酰胺区的红外光谱[18]。在明胶光谱中,在1 542 cm-1处的NH振动带和在1 454 cm-1处的CH振动带在形成复合物后仍基本保持其位置。然而,在1 200~400 cm-1区域的复合凝聚物图谱与明胶和多糖图谱的模式完全不同。这可能是络合过程中明胶和多糖分子重排的结果[18],因此,这些组分可能形成稳定的复合凝聚体。对比壁材与复聚物的红外光谱可以看出,在复合凝聚物的红外光谱上未发现不存在明胶、阴离子多糖的特殊峰值,这说明了没有新的化学键生成,进一步证实了明胶、阴离子多糖是通过静电相互作用等物理相互作用形成的,而非通过化学相互作用联接的。

图6 绿咖啡油及其微胶囊的红外光谱图Fig.6 Infrared spectra of free and microencapsulated green coffee oil
对比明胶/阿拉伯胶复聚物及微胶囊红外图谱发现,复聚物1 669 cm-1的吸收峰位移至1 647 cm-1;对比明胶/果胶复聚物及微胶囊红外图谱发现,复聚物1 659 cm-1的吸收峰位移至1 647 cm-1;对比明胶/羧甲基纤维素钠复聚物及微胶囊红外图谱发现,复聚物1 669 cm-1的吸收峰位移至1 660 cm-1。以上峰位移的原因可能是-NH3+发生了不对称变角振动。3 种微胶囊的1 542 cm-1的吸收峰与明胶的红外光谱的峰值相同,说明微胶囊中都含有明胶。图6表示的是咖啡油及明胶/阿拉伯胶、明胶/果胶、明胶/羧甲基纤维素钠包埋所得的微胶囊红外谱图。从图中可以看出咖啡油微胶囊在波数为2 925、2 854、1 746、1 464、1 377、1 238、1 163、1 099、722 cm-1处与咖啡油的红外光谱的峰值相近,可以说明微胶囊中含有咖啡油。咖啡油中含有亚油酸,亚油酸中含有两个双键,由咖啡油的红外光谱可以看出在波数为3 009 cm-1处有极强的振动峰,这是=C-H键伸缩振动形成的,而在形成的微胶囊产品中没有看到此波长处的伸缩振动现象,并且咖啡油的羰基峰在1 746 cm-1处减弱,这与已有关于咖啡油的报道一致[5],表明咖啡油已被包埋。
3 种壁材组合的绿咖啡油微胶囊图谱主要特征峰在壁材、芯材的光谱图上均有所显示,只是不同程度地被隐藏或削弱,这可能是多种物质混合所致,由此可以初步判定,咖啡油被成功包埋,包埋过程中未与壁材发生化学反应。这与郭阳等[27]报道一致。
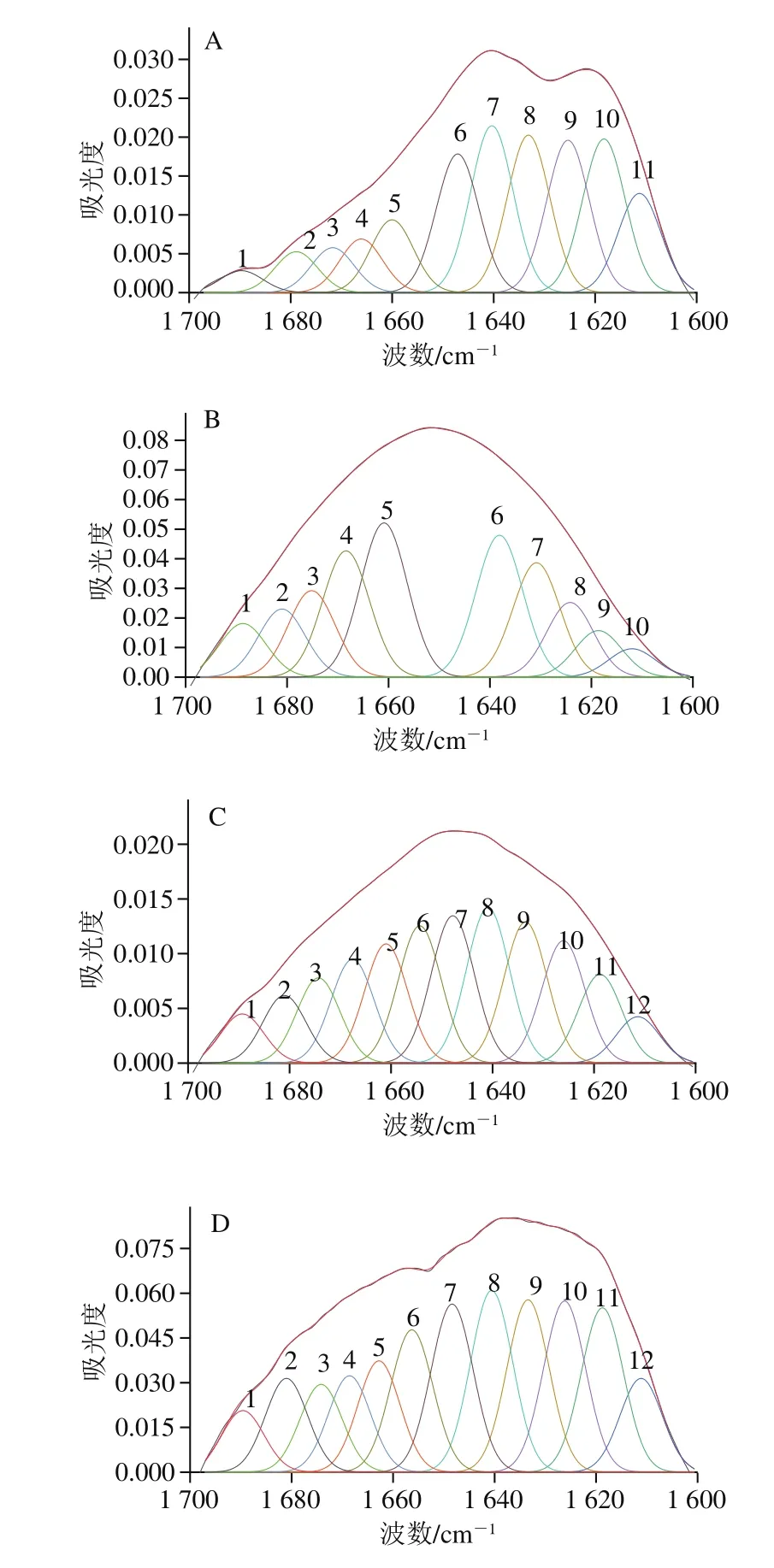
图7 蛋白质酰胺I带(1 700~1 600 cm-1)拟合傅里叶变换红外光谱图Fig.7 Curve-fitting of amide I (1 700–1 600 cm-1) in FTIR spectra
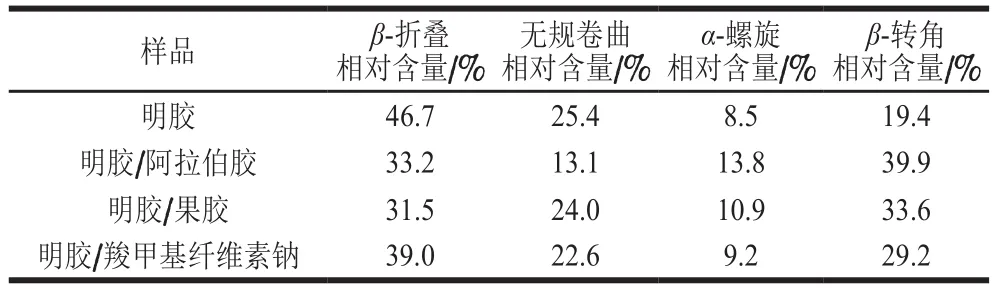
表4 明胶及复聚物中蛋白质二级结构相对含量Table 4 structure contents in gelatin and complexes
蛋白质酰胺的光谱区间为1 700~1 600 cm-1,主要包含了的C=O伸缩振动,对蛋白质二级结构的变化非常敏感,对于研究二级结构最有价值。应用二阶导数和曲线拟合的方法对明胶及3 种复聚物酰胺Ⅰ带曲线拟合。酰胺I带是由多个子峰重叠而成的宽峰,从图7得出分别有11、10、12、12 个自带峰,对自带峰进行指认,计算各子峰和总峰的峰面积,求得各二级结构相对含量[28]。从表4中得出明胶中β-折叠、无规卷曲、α-螺旋、β-转角相对含量分别为46.7%、25.4%、8.5%、19.4%,经复合凝聚后复聚物中β-折叠、无规卷曲相对含量都相对减少,α-螺旋和β-转角相对含量增加。表明α-螺旋结构和β-转角结构是明胶与多糖相互作用的重要结构区域,同时,复合凝聚反应对明胶的α-螺旋结构和β-转角结构具有一定的稳定作用[29],而对于无规卷曲和β-折叠影响较小,这与明胶和多糖的静电相互作用有关。
2.6 微胶囊的热稳定性分析
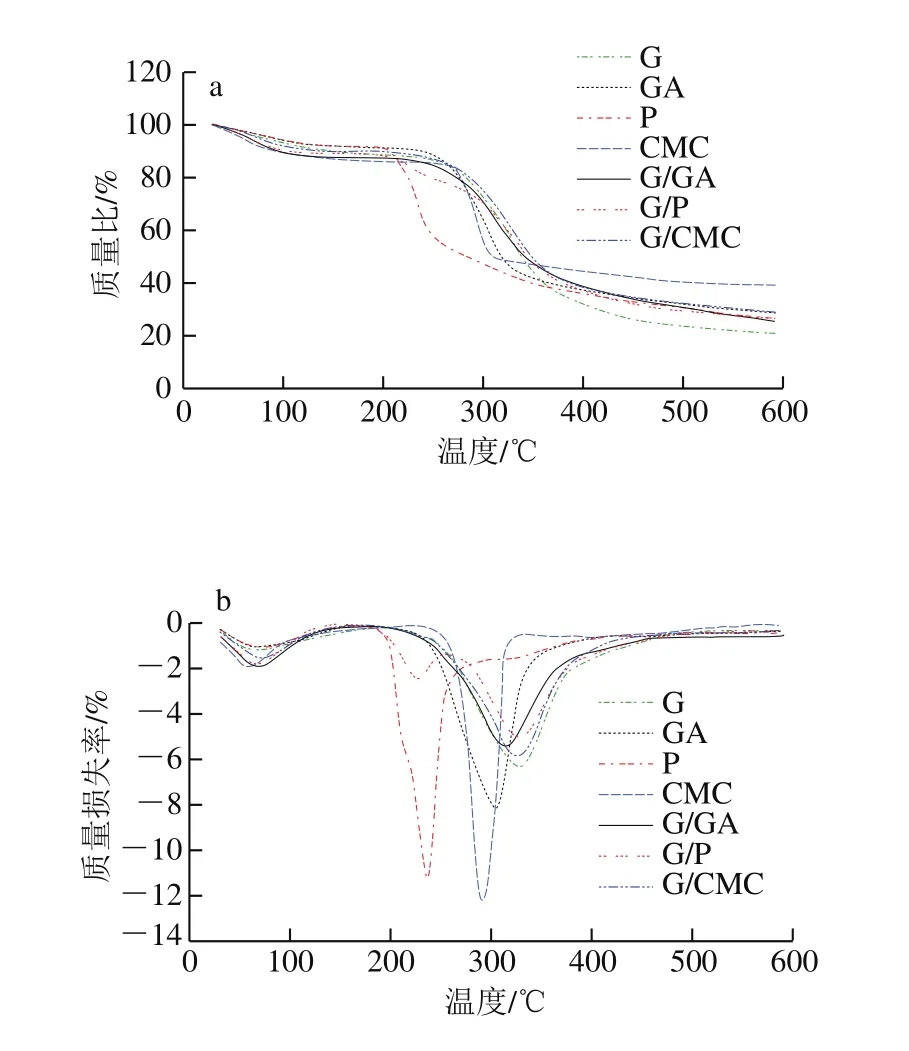
图8 壁材及其复聚物的残余失重随温度变化的热重分析曲线(a)和对应的微商热重曲线(b)Fig.8 Thermogravimetric analysis (TGA) curves (a) and corresponding derivative thermogravimetry (DTG) curves (b) of residual weightlessness of individual wall materials and complexes with increasing temperature

图9 绿咖啡油及其微胶囊的残余失重随温度变化的热重分析曲线(a)和对应的微商热重曲线(b)Fig.9 TGA curves (a) and corresponding DTG curves (b) of residual weightlessness of free and microencapsulated green coffee oil with increasing temperature
热重法可用于测定样品的热解温度和速率,不同的热降解阶段可以通过微商热重曲线的显著峰值来区分,这些信息对评价不同大分子的热稳定性是有用的[30]。对探明羧酸盐对微胶囊的保护作用,并指导工业生产具有实际意义,同时微胶囊的缓热分解形式也决定了微胶囊未来的控释特性。热重分析曲线与相应样品的一阶微分曲线如图8、9所示,在100 ℃左右,由于所有样品的水分蒸发,显示吸热峰,继续升温后,样品开始分解,出现样品分解的吸热峰。其中,明胶的热稳定性最好,质量损失峰值温度为326 ℃,3 种多糖稍差,其中果胶的热稳定性最差,在235 ℃达到最大质量损失速率,阿拉伯胶和羧甲基纤维素钠热稳定性最高,分别在304 ℃和291 ℃时达到最大质量损失速率,对比壁材与复聚物的微商热重曲线可以看出,壁材在经过复凝聚后,增加了其热稳定性,且它们的热稳定性与壁材本身的热稳定性相关,明胶/果胶复聚物在226 ℃达到一个质量损失峰值,与单独果胶在235 ℃达到最大质量损失峰值相符,然而其最大的质量损失峰被延长至328 ℃,与明胶/阿拉伯胶、明胶/羧甲基纤维素钠复聚物的最大质量损失峰相似,其中热稳定性最好的复聚物为明胶/羧甲基纤维素钠,失重峰值温度达到325 ℃。复凝物质量损失平缓在温度范围内,表明复凝物在这一范围内不会分解,能基本保持稳定[31],明胶/阿拉伯胶和明胶/羧甲基纤维素钠组合的复聚物在250 ℃前都可保持较为稳定的状态。Duhoranimana等[32]研究证明了复聚物的热稳定性与pH值无关,因此3 种复聚物不同的热稳定性是由不同的壁材组合所导致的,通过使用不同的壁材组合,可以使稳定的输送系统具有理想的释放模式。复凝聚法制备的微胶囊绿咖啡油在380~480 ℃几乎被完全分解,最大损失在417 ℃,而咖啡油微胶囊的分解温度被延长至500 ℃,说明微胶囊具有较强的耐热性,提高了绿咖啡油的热稳定性。
3 结 论
本实验以明胶分别与阿拉伯胶、果胶、羧甲基纤维素钠3 种阴离子多糖组合为壁材,绿咖啡油为芯材,研究了3 种壁材组合对复合凝聚法微胶囊化绿咖啡油形态、产率、包埋率、粒径及结构的影响。经光学显微镜形态观察,其空囊及绿咖啡油微胶囊结构完整、形态呈球状、囊壁明显、分散均匀;其产率达到90.0%以上,包埋率均达到85.0%以上,但其壁材利用率不同,明胶/果胶最高,为76.6%,都能较好地进行包埋。
通过傅里叶变换红外光谱对其结构进行分析,证实了明胶与3 种多糖的静电相互作用,且复凝聚反应只是壁材间的相互作用,芯材未与壁材发生其他化学反应。进一步证明所选择的技术和所用的材料能够成功封装绿咖啡油,从而保证了对萃取物的保护作用。应用二阶导数和曲线拟合的方法对明胶及复聚物蛋白质酰胺I带二级结构进行拟合,结果表明明胶中β-折叠、无规卷曲、α-螺旋、β-转角相对含量分别为46.7%、25.4%、8.5%、19.4%,经复合凝聚后,复聚物中β-折叠、无规卷曲相对含量减少,α-螺旋和β-转角相对含量增加。
通过热重分析对复聚物形成的热稳定性进行分析,证实了壁材热稳定性与复聚物热稳定性的相关性,通过对咖啡油进行包埋可以提高其热稳定性,其中3 种壁材组合的复聚物中明胶/果胶的热稳定性最差。
