银杏叶提取物治疗阿尔茨海默病有效性、安全性和经济性的快速卫生技术评估
2020-12-28任晓蕾刘一詹轶秋张春燕黄琳封宇飞
任晓蕾 刘一 詹轶秋 张春燕 黄琳 封宇飞


摘 要 目的:快速評价银杏叶提取物(EGb)治疗阿尔茨海默病(AD)的有效性、安全性和经济性,为临床药物选择和决策提供循证依据。方法:系统检索PubMed、Embase、Cochrane 图书馆、Web of Science、中国知网、中国生物医学数据库、万方数据等中英文数据库,同时检索国内外快速卫生技术评估(HTA)机构官方网站及相关数据库,检索时限均为建库起至2020年8月10日,收集EGb对比安慰剂治疗AD的HTA报告、系统评价/Meta分析和药物经济学研究。筛选文献、提取资料后,分别采用HTA核查清单、系统综述质量评价工具量表2、综合卫生经济评价报告标准量表评价纳入HTA报告、系统评价/Meta分析和药物经济学研究的质量,采用定性描述方法汇总纳入研究的结论。结果:共纳入9篇文献,其中8篇为系统评价、1篇为药物经济学研究。有效性方面,EGb组患者的简易智能状态检查评分、120 mg EGb组患者的阿尔茨海默氏病评估量表-认知分量表(ADAS-Cog)评分与安慰剂组比较,差异均无统计学意义(P>0.05);EGb组患者的痴呆生活质量量表评分显著高于安慰剂组,简短认知能力测试评分、神经精神科问卷(NPI)评分、NPI-照顾者版评分、160 mg EGb组和240 mg EGb组患者的ADAS-Cog评分均显著低于对照组(P<0.05)。患者的日常生活活动能力(ADL)评分结果不一致,EGb组患者的ADL评分显著低于安慰剂组(P<0.05)或两组比较差异无统计学意义(P>0.05);按剂量进行亚组分析结果显示,120 mg EGb组患者的ADL评分与安慰剂组比较,差异无统计学意义(P>0.05);而240 mg EGb组患者的ADL评分显著低于安慰剂组(P<0.05)。临床总体印象改变(CGIC)评分的亚组分析结果显示,小于200 mg EGb和治疗26周时EGb组患者的CGIC评分与安慰剂组比较,差异均无统计学意义(P>0.05);大于200 mg EGb和治疗24周时EGb组患者的CGIC评分均显著高于安慰剂组(P<0.05)。安全性方面,EGb组患者的不良反应发生率、严重不良反应发生率与安慰剂组比较,差异均无统计学意义(P>0.05);按剂量进行亚组分析结果显示,240 mg EGb组患者的不良反应发生率显著高于安慰剂组(P<0.05)。经济学方面,EGb治疗AD具有成本-效益,可间接节省AD患者的护理费用。结论:EGb治疗AD的有效性尚不确切,但安全性与经济性均较好。
关键词 银杏叶提取物;阿尔茨海默病;快速卫生技术评估;有效性;安全性;经济性
中图分类号 R742 文献标志码 A 文章编号 1001-0408(2020)22-2786-05
DOI 10.6039/j.issn.1001-0408.2020.22.17
ABSTRACT OBJECTIVE: To rapidly evaluate the effectiveness,safety and economics of Ginkgo biloba extract (EGb) in the treatment of Alzheimers disease (AD) patients, and to provide evidence-based reference for clinical drug selection and decision. METHODS: Retrieved from PubMed, Embase, Cochrane Library, Web of Science, CNKI, CBM, Wanfang database, health technology assessment (HTA) organization websites and database during the inception to Aug. 10, 2020, HTA reports, systematic reviews/Meta-analysis, and pharmacoeconomic studies of EGb versus placebo in the treatment of AD were collected. After literature screening and data extration, HTA checklist, AMSTAR-2 scale and CHEERS scale were used respectively to evaluate the literature quality of the included HTA report, systematic review/Meta-analysis and pharmacoeconomics studies. The conclusion of the included studies were summarized by using qualitative description. RESULTS: A total of 9 literatures were included, involving 8 systematic reviews and 1 economic studies. In terms of effectiveness, there was no statistical significance in MMSE score of EGb group, ADAS-Cog score of 120 mg EGb group, compared with placebo group (P>0.05). Dementia Quality of Life (DQoL) score of EGb group was significantly higher than that of placebo group. The scores of short cognitive aptitude tests, neuropsychiatric inventory (NPI), NPI caregiver version score, ADAS-Cog score of 160 mg EGb group and 240 mg EGb group were significantly lower than those of control group (P<0.05). ADL scores of patients were inconsistent; ADL scores of EGb group were significantly lower than those of placebo group (P<0.05), or there was no significant difference between 2 groups (P>0.05); subgroup analysis by dose showed that there was no significant difference in ADL score between 120 mg EGb group and placebo group (P>0.05); ADL score of 240 mg EGb group were signicantly lower than that of placebo group (P<0.05). Subgroup analysis of clinical global impression change (CGIC) score showed that there was no significant difference in CGIC score between EGb group and placebo group after receiving <200 mg EGb and 26 weeks of treatment (P>0.05); CGIC score of EGb group was significantly higher than that of placebo group after receiving >200 mg EGb and 24 weeks of treatment (P<0.05). In terms of safety, there was no statistical significance in the incidence of ADR or the incidence of severe ADR between EGb group and placebo group (P>0.05). Subgroup analysis by dose showed that the incidence of ADR in 240 mg EGb group was significantly higher than placebo group (P<0.05). Economically, EGb treatment for AD is cost-effective, which could indirectly save the nursing costs of AD patients. CONCLUSIONS: The efficacy of EGb in the treatment of AD is uncertain, and the safety and economy are good.
KEYWORDS Ginkgo biloba extract; Alzheimers disease; Rapid health technology assessment; Effectiveness; Safety; Economics
阿尔茨海默病(Alzheimers disease,AD)是一种主要发生于老年人的神经退行性疾病,是痴呆的最常见病因,其病因和发病机制尚不明确[1]。美国AD学会发布的数据显示,2018年共有122 019名美国人因AD死亡,AD是65岁以上老年人群的第五大死因;该数据还显示,2019年有超过1 600万名家庭成员和其他无偿照顾者为AD或其他痴呆患者提供了约186亿小时的护理,这项护理的价值接近2 440亿美元[2]。目前,已获批准用于治疗AD的药物包括乙酰胆碱酯酶抑制剂(Acetylcholinesterase inhibitors,AChEI)和N-甲基-D-天冬氨酸(N-methyl-D-aspartic acid,NMDA)受体拮抗剂,除上述药物外,还有改善脑代谢/循环药物及神经保护剂等在临床中应用,但这些药物的疗效及安全性尚不确切[3]。有研究发现,银杏叶提取物(Ginkgo biloba extract,EGb)对痴呆有一定的疗效[3],但各研究结果不一致。2019年亚洲神经认知障碍临床专家组相关共识推荐,EGb为综合治疗AD的一部分,特别是对于未能从AChEI、NMDA 受体拮抗剂治疗中受益的患者[4],但此推荐缺乏足够的循证医学证据支撑。
卫生技术评估(Health technology assessment,HTA)是指对包括药品在内的各种卫生技术的技术特性、临床有效性、安全性、经济性和社会属性进行全面系统的评价,为各层次的决策者提供合理选择卫生技术的科学信息和决策依据[5]。快速HTA是一种快速决策工具,可相对高效地对现有的主要证据进行梳理和分析,现已被日益重视并用于决策制定[6]。基于此,本研究采用快速HTA的方法对EGb治疗AD的有效性、安全性和经济性进行评估,旨在为临床药物选择和决策提供循证依据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型 HTA报告、系统评价(SR)/Meta分析、药物经济学研究。语种限定为中文和英文。
1.1.2 研究对象 AD患者。
1.1.3 干预措施 干预组患者给予EGb,对照组患者给予安慰剂;两组患者用药剂量、疗程不限。
1.1.4 结局指标 有效性指标:①认知功能,包括简易智能状态检查(MMSE)评分、阿尔茨海默病评估量表-认知分量表(ADAS-Cog)评分、简短认知能力测试(SKT)评分;②日常生活活动能力(ADL)评分;③临床总体印象改变(CGIC)评分;④生活质量,包括神经精神科问卷(NPI)评分、NPI-照顾者版评分、痴呆生活质量量表(DQoL)评分。安全性指标:⑤不良反应发生情况。⑥经济性指标,包括增量成本-效果、成本-效用、成本-效益等。
1.1.5 排除标准 ①重复发表的文献;②数据缺乏或无法获取全文的文献;③非中、英文文献。
1.2 文献检索策略
计算机检索PubMed、Embase、Cochrane图书馆、Web of Science、中国知网(CNKI)、中国生物医学数据库(CMB)、万方数据等数据库,以“银杏叶提取物”“阿尔茨海默病”“痴呆”为中文检索词,“Ginkgo biloba extract”“Alzheimers disease”“Dementia”为英文检索词进行全文检索或者主题检索;同时,检索国内外HTA机构官方网站及相关数据库。检索时限均为各数据库建库起至2020年8月10日。必要时限制研究类型,并手工检索纳入研究的参考文献列表。
1.3 文献筛选、资料提取和质量评价
由2位评价者独立按纳入与排除标准筛选文献,共同决定纳入的文献;如遇分歧,则通过讨论或咨询第3位评价者解决。按预先设计的资料提取表提取资料和数据,包括第一作者、发表年份、研究人群、纳入研究个数、患者例数、干预措施及结局指标等。采用国际卫生技术评估组织协会制定的HTA核查清单(HTA checklist)[6]评价HTA报告,采用系统综述质量评价工具2(AMSTAR-2)量表[7]评价SR/Meta分析,采用综合卫生经济评价报告标准(CHEERS)量表[8]评价药物经济学研究的质量。
1.4 数据分析
对本研究的结局指标采用定性描述的方法汇总纳入研究的结论,得出研究结果。统计学检验水平为α=0.05。
2 結果
2.1 文献筛选流程与纳入研究的基本信息
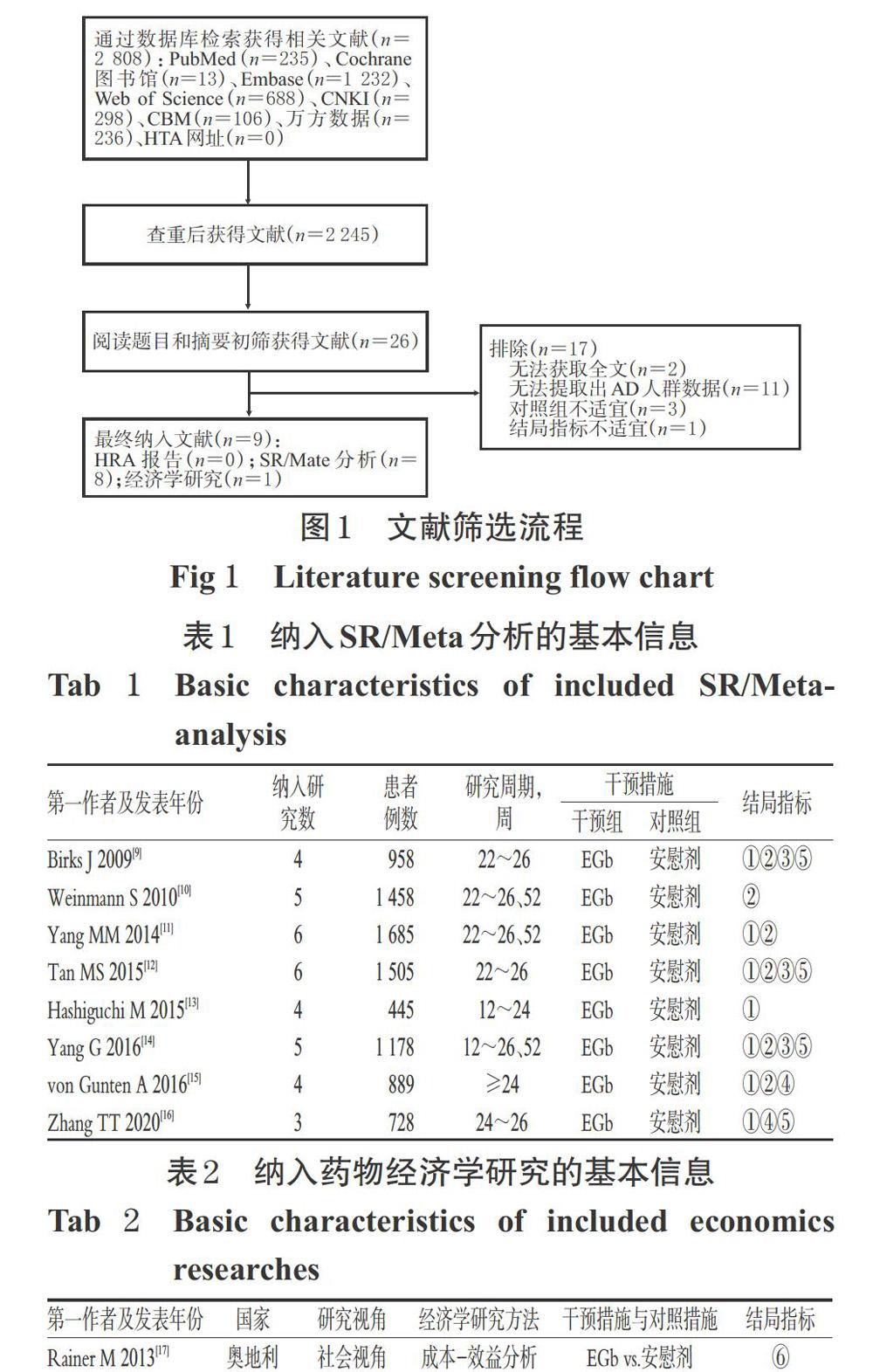
初检共获得相关文献2 808篇,经阅读文题和摘要后获得文献26篇;进一步阅读全文后,最终纳入9篇文献[9-17],其中8篇[9-16]为SR/Meta分析,1篇[17]为药物经济学研究。文献筛选流程见图1,纳入研究的基本信息见表1、表2。
2.2 纳入研究质量评价结果
2.2.1 SR/Meta分析 SR/Meta分析的质量评价结果见表3。该表中,“1”为研究问题和纳入标准是否包括了 PICO(即人群、干预措施、对照组以及结果结论)部分;“2”为是否声明在系统评价实施前确定了系统评价的研究方法,对于与研究方案不一致处是否进行了说明;“3”为系统评价作者在纳入文献时是否说明了纳入研究的类型;“4”为系统评价作者是否采用了全面的检索策略;“5”为是否采用了双人重复式文献选择;“6”为是否采用了双人重复式文献提取;“7”为系统评价作者是否提供了排除文献清单并说明其原因;“8”为系统评价作者是否详细地描述了纳入的研究;“9”为系统评价作者是否采用合适工具评估了每个纳入研究的偏倚风险;“10”为系统评价作者是否报告了纳入各个研究的资助来源;“11”为进行Meta分析时,系统评价作者是否采用了合适的统计学方法合并研究结果;“12”为进行Meta分析时,系统评价作者是否评估了每个纳入研究的偏倚风险对Meta分析结果或其他证据综合结果潜在的影响;“13”为系统评价作者在解释或讨论每个研究结果时是否考虑了纳入研究的偏倚风险;“14”为系统评价作者是否对研究结果的任何异质性进行了合理的解释和讨论;“15”为如果系统评价作者在进行定量合并时是否对发表偏倚(小样本研究偏倚)进行了充分的调查,并讨论了其对结果可能的影响;“16”为系统评价作者是否报告了所有潜在利益冲突的来源,包括所接受的用于制作系统评价的任何资助。由表3可知,2篇[9,14]为高质量文献,6篇[10-13,15-16]为中等质量文献(具体质量评价标准来源于文献[7])。
2.2.2 药物经济学研究 1篇药物经济学研究[17]从社会视角出发,采用成本-效益分析对奥地利的痴呆患者使用EGb可获得的治疗效果进行了经济学评价,该文献质量良好,详见表4(具体质量评价标准来源于文献[8])。
2.3 有效性评价
2.3.1 认知功能 ①MMSE评分——1项SR/Meta分析[16]报道了MMSE评分。结果显示,EGb组患者的MMSE评分与安慰剂组比较,差异无统计学意义[SMD=0.144,95%CI(-0.407,0.694),P>0.05]。②ADAS-Cog评分——5项SR/Meta分析[9,11-12,14,16]报道了ADAS-Cog评分。结果显示,EGb组患者的ADAS-Cog评分与安慰剂组比较,差异无统计学意义[MD=-0.21,95%CI(-1.05,0.63),P=0.63][9]。亚组分析结果显示,120 mg EGb组患者的ADAS-Cog评分与安慰剂组比较,差异无统计学意义[MD=-0.29,95%CI(-1.21,0.64),P=0.54];而160 mg EGb组[MD=-5.60,95%CI(-6.95,-4.25),P<0.000 01]、240 mg EGb组[MD=-2.76,95%CI(-3.24,-2.28),P<0.000 01]患者的ADAS-Cog评分均较安慰剂组显著降低[12]。③SKT评分——4项SR/Meta分析[9,11,13,15]报道了SKT评分。结果显示,与安慰剂组比较,EGb组患者的SKT评分显著降低[MD=-2.74,95%CI(-3.46,-2.03),P<0.000 1][9]。
2.3.2 ADL评分 6项SR/Meta分析[9-12,14-15]报道了ADL评分。结果显示,与安慰剂组比较,EGb患者的ADL评分显著降低[SMD=-1.55,95%CI(-2.55,-0.55),P=0.002][11];但也有研究指出,EGb组患者的ADL评分与安慰剂组比较,差异无统计学意义[SMD=-0.09,95%CI(-0.26,0.09),P=0.33][9]。1项SR/Meta分析[12]按照EGb剂量进行的亚组分析结果显示,120 mg EGb组患者的ADL评分与安慰剂组比较,差异无统计学意义[SMD=-0.15,95%CI(-0.32,0.02),P=0.07],而240 mg EGb组患者的ADL评分较安慰剂组显著降低[SMD=-0.39,95%CI(-0.52,-0.27),P<0.000 01]。
2.3.3 CGIC 评分 3项SR/Meta分析[9,12,14]报道了CGIC评分。2项SR/Meta分析[9,12]按照EGb剂量进行的分析结果显示,小于200 mg EGb组患者的CGIC评分与安慰剂组比较,差异无统计学意义[OR=1.35,95%CI(0.88,2.07),P=0.17];而大于200 mg EGb组患者的CGIC评分较安慰剂组显著增加[OR=1.79,95%CI(1.21,2.65),P<0.01][9]。1项SR/Meta分析[14]按照疗程进行的亚组分析结果显示,与安慰剂组比较,治疗24周时 EGb组患者的CGIC评分显著增加[OR=3.32,95%CI(2.09,5.29),P<0.05];而治疗26周时EGb组患者的CGIC评分与安慰剂组比较,差异无统计学意义[OR=1.47,95%CI(0.96,2.26),P>0.05]。
2.3.4 生活质量 ①NPI评分——2项SR/Meta分析[15-16]报道了NPI评分。结果显示,与安慰剂组比较,EGb组患者的NPI评分显著降低[SMD=-3.72,95%CI(-4.81, -2.62),P<0.05][15]。②NPI-照顾者版评分——1项SR/Meta分析[15]报道了NPI-照顾者版评分。结果显示,与安慰剂组比较,EGb组患者的NPI-照顾者版评分显著降低[SMD=-1.84,95%CI(-2.52,-1.17),P<0.05]。③DQoL评分——1项SR/Meta分析[15]报道了DQoL评分。结果显示,与安慰剂组比较,EGb患者的DQoL评分显著升高[SMD=2.40,95%CI(0.85,3.95),P<0.05]。
2.4 安全性评价
4项SR/Meta分析[9,12,14,16]报道了不良反应发生情况。結果显示,EGb组患者的不良反应发生率与安慰剂组比较,差异无统计学意义[OR=0.82,95%CI(0.62,1.06),P=0.13][14]。1项SR/Meta分析[9]按照EGb剂量进行的亚组分析结果显示,小于200 mg EGb组[OR=0.84,95%CI(0.53,1.32),P=0.44]或大于200 mg EGb组[OR=0.78,95%CI(0.49,1.23),P=0.28]患者的不良反应发生率与安慰剂组比较,差异均无统计学意义。1项SR/Meta分析[16]同样按照EGb剂量进行的分组分析结果显示,120 mg EGb组患者的不良反应发生率与安慰剂组比较,差异无统计学意义[OR=0.84,95%CI(0.53,1.32),P=0.44];而240 mg EGb组患者的不良反应发生率较安慰剂组显著增加[OR=0.70,95%CI(0.52,0.93),P=0.02]。2项SR/Meta分析[12,14]报道了严重不良反应发生情况。结果显示,EGb组患者的严重不良反应发生率与安慰剂组比较,差异无统计学意义[OR=0.82,95%CI(0.39,1.74),P=0.60][14]。
2.5 经济性评价
Rainer M等[17]采用成本-效益的方法研究了EGb治疗以AD为主的痴呆的经济性。结果显示,EGb可降低治疗成本,减缓疾病的发展,与安慰剂组比较,240 mg/d EGb组患者ADL恶化延迟时间达22.3个月,且可减少患者对更高级别家庭护理费用的需求,护理费用的总净节省额为3 692~29 577欧元。另外有两项研究[18-19]也得出相同结果,即不论疾病持续时间、治疗开始时间、EGb使用剂量等是否相同,节省的护理费用均超过了EGb的治疗费用,但由于无法获取全文,故这两项研究未纳入经济性评价。综上,对AD患者使用EGb有利于节省成本,尤其是AD患者的护理费用。
3 讨论
EGb是从银杏科植物银杏的叶中提取的具有独特药理活性的混合物,有研究发现,EGb可提高AD患者认知和记忆功能,改善脑部血液循环,促进脑部损伤后的功能恢复及脑代谢[20]。
本研究结果显示,在有效性方面,(1)EGb对AD患者的认知功能改善疗效虽然尚不确切,但研究结果提示高剂量(160、240 mg)的EGb疗效可能更好。(2)除1项研究[9]外,5项研究[10-12,14-15]结果均显示,EGb可降低患者的ADL评分,且1项研究[12]按剂量进行的亚组分析结果提示,高剂量(240 mg)的EGb疗效可能更好。(3)大于200 mg的EGb可提高患者的CGIC评分,提示高剂量的EGb疗效可能更好。(4)EGb可显著改善AD患者及照顾者的生活质量。有研究发现,EGb可多环节、多靶点地防治心脑血管疾病,具有清除自由基、抗氧化、改善血流动力学、抗血小板聚集、抗炎、抗凋亡、调节血脂、防治动脉粥样硬化、保护线粒体和减少组织耗能等作用[21]。这提示EGb可能是通过上述多重作用机制实现治疗AD 的目的[4],但尚需相关研究进一步验证。
在安全性方面,有3项研究[9,12,14]显示,EGb组患者的不良反应发生率与安慰剂组比较,差异无统计学意义;仅有1项研究[16]提示,与安慰剂组比较,240 mg EGb组患者的不良反应发生率显著增加。2项研究[12,14]显示,EGb组患者的严重不良反应发生率与安慰剂组比较,差异无统计学意义。这提示,EGb治疗AD的安全性尚可,但240 mg剂量可能会增加不良反应的发生风险。
在经济性方面,仅有1项[17]研究表明,EGb治疗AD具有成本-效益优势,主要体现在应用EGb治疗可间接节省AD患者的护理费用。目前,国内尚无EGb治疗AD的经济学研究报道,因此缺乏我国医疗环境下EGb治疗AD的经济性评价结果,这提示我国可开展基于实际情况的药物经济学研究。
综上所述,EGb治疗AD的有效性尚不确切,但安全性与经济性均较好。本研究存在的局限性為:(1)本研究为快速HTA,对纳入的研究仅作定性描述分析,未进行系统的定量评价,且本研究纳入文献的药物治疗剂量、治疗周期等均不同,因此仍需进行Meta分析及亚组分析;(2)国内外关于EGb治疗AD的经济学研究较少。因此,本结论有待更多高质量研究进一步验证。
参考文献
[ 1 ] BALLARD C,GAUTHIER S,CORBETT A,et al. Alzheimers disease[J]. Lancet,2011,377(9770):1019- 1031.
[ 2 ] 2020 Alzheimers disease facts and figures[J]. Alzheimer s Dementia,2020. DOI:10.1002/alz.12068.
[ 3 ] 殷贺,刘广志.银杏叶提取物治疗阿尔茨海默病的作用机制研究进展[J].中国医药,2020,15(1):151-152.
[ 4 ] KANDIAH N,ONG PA,YUDA T,et al. Treatment of dementia and mild cognitive impairment with or without cerebrovascular disease:expert consensus on the use of Ginkgo biloba extract,EGb 761?[J]. CNS Neurosci Ther,2019,25(2):288-298.
[ 5 ] 唐惠林,门鹏,翟所迪.药物快速卫生技术评估方法及应用[J].临床药物治疗杂志,2016,14(2):1-4.
[ 6 ] HAILEY D. Toward transparency in health technology assessment:a checklist for HTA reports[J]. Int J Technol Assess Health Care,2003,19(1):1-7.
[ 7 ] 葛龙,潘蓓,潘佳雪,等.解读AMSTAR-2:基于随机和(或)非随机对照试验系统评价的质量评价工具[J].中国药物评价,2017,34(5):334-338.
[ 8 ] HUSEREAU D,DRUMMOND M,PETROU S,et al.Consolidated health economic evaluation reporting standards(CHEERS)statement[J]. J Med Econ,2013,16(6):713- 719.
[ 9 ] BIRKS J,GRIMLEY EVANS J. Ginkgo biloba for cognitive impairment and dementia[J]. Cochrane Database Syst Rev,2009. DOI:10.1002/14651858.CD003120.
[10] WEINMANN S,ROLL S,SCHWARZBACH C,et al. Effects of Ginkgo biloba in dementia:systematic review and meta-analysis[J]. BMC Geriatr,2010. DOI:10.1186/1471- 2318-10-14.
[11] YANG MM,XU DD,ZHANG Y,et al. A systematic review on natural medicines for the prevention and treatment of Alzheimers disease with meta-analyses of intervention effect of ginkgo[J]. Am J Chin Med,2014,42(3):505-521.
[12] TAN MS,YU JT,TAN CC,et al. Efficacy and adverse effects of Ginkgo biloba for cognitive impairment and dementia:a systematic review and meta-analysis[J]. J Alzheimers Dis,2015,43(2):589-603.
[13] HASHIGUCHI1 M,OHTA Y,SHIMIZU M,et al. Meta- analysis of the efficacy and safety of Ginkgo biloba extract for the treatment of dementia[J]. J Pharm Health Care Sci,2015. DOI:10.1186/s40780-015-0014-7.
[14] YANG G,WANG Y,SUN J,et al. Ginkgo biloba for mild cognitive impairment and Alzheimers disease:a systematic review and meta-analysis of randomized controlled trials[J]. Curr Top Med Chem,2016,16(5):520-528.
[15] VON GUNTEN A,SCHLAEFKE S,?BERLA K. Efficacy of Ginkgo biloba extract EGb 761? in dementia with behavioural and psychological symptoms:a systematic review[J]. World J Biol Psychiatry,2016,17(8):622-633
[16] ZHANG TT,LIU NY,CAO HF,et al. Different doses of pharmacological treatments for mild to moderate Alzheimers disease:a bayesian network meta-analysis[J]. Front Pharmacol,2020. DOI:10.3389/fphar.
[17] RAINER M,MUCKE H,SCHLAEFKE S. Ginkgo biloba extract EGb 761? in the treatment of dementia:a pharmacoeconomic analysis of the austrian setting[J]. Wien Klin Wochenschr,2013. DOI:10.1007/s00508-012-0307-x.
[18] H?RR R,KIESER M. Pharmaco-economic evaluation of ginkgo special extract EGb 761? for dementias in Austria[J]. Wien Med Wochenschr,2002. DOI:10.1046/j.1563- 258x.
[19] HEINEN-KAMMERER T,MOTZKAT K,DANIEL D, et al. The situation of patients with dementia may be rectified by Ginkgo biloba:results of a health services research study concerning the ability of patients with dementia,quality of life of the nursing family members and total treatment costs[J]. MMW Fortschr Med,2005,147(Suppl 3):127-133.
[20] 劉丹,王佳贺.银杏叶提取物防治阿尔茨海默病的研究进展[J].实用老年医学,2017,31(7):609-612.
[21] 李淑琴,朱嘉宝,武宇洲.银杏叶提取物防治心脑血管疾病的研究进展[J].中国新药杂志,2016,25(1):76-80.
(收稿日期:2020-08-24 修回日期:2020-10-26)
(编辑:陈 宏)
