新型凝血因子Ⅺ、Ⅻ靶向药物在早期临床试验中的研究进展
2020-12-16马宇飞洛佳坤杨雯伊曹剑
马宇飞,洛佳坤,杨雯伊,曹剑
心血管疾病和静脉血栓栓塞症(VTE)是导致死亡和残疾的主要原因,占全球死亡人数的四分之一[1,2],其二级预防,如抗凝和抗血小板治疗,虽然有效,但普遍会增加出血风险。抗凝治疗的核心即在预防血栓形成和消除出血风险之间取得平衡。维生素K拮抗剂(如华法林),通过监测凝血酶原时间(PT)和国际标准化比值(INR)来体现这种平衡。近年随着直接口服抗凝剂(DOACs)的广泛应用,极大提高了预防和治疗血栓性疾病的安全性。与维生素K拮抗剂相比,DOACs每年发生颅内出血的风险至少降低了一半[3]。尽管如此,DOACs的问题仍然存在:据报道每年DOACs的主要出血事件为4%,颅内出血后的死亡率达到25%[4];缺乏对DOACs明确的实验室监测技术;在诸多领域还未有突破,如预防血管内装置(如血液透析、机械心脏瓣膜和心室辅助装置)血栓形成[5];以及逆转DOACs抗凝作用。在一定比例的患者中,出血似乎是任何抗凝方案都无法避免的副作用,特别是高龄、贫血和肾脏疾病患者[6,7]。因此人们期待凝血接触途径能为这一临床困境提供解决方案。
接触系统由凝血因子Ⅺ(FⅪ)、凝血因子Ⅻ(FⅫ)、前激肽释放酶和高分子激肽原组成[8,9],属于内源性凝血途径,位于传统抗凝靶点,即外源性(组织因子)和共同凝血途径的上游。内源性凝血途径由FⅫ活化而启动,目前已知的FⅫ激活物包括表面带负电荷的异物(如血管内导管、透析回路等)、血小板衍生的短链和细菌性的长链聚磷酸盐(polyP)、游离RNA/DNA以及感染性病原体[10]。活化的FⅫ(FⅫa)可以激活FⅪ(FⅪa);FⅪa通过促进凝血酶介导的纤维蛋白生成而促进凝血。同时,FⅪ与凝血酶和FⅫ之间可以相互激活[11]。此外,FⅪ和FⅫ与炎症和补体系统密切相关。因此,接触系统,特别是FⅪ,被视为连接众多病理生理过程的中心节点[12]。
有人认为,止血过程主要依赖于组织因子,而内源性凝血途径则是对这一过程实施了放大效应[13]。就临床出血事件或出血时间而言,动物模型确实未显示FⅪ基因敲除或药物诱导FⅪ缺乏的不良影响。与缺乏FⅧ和FⅨ(血友病A、B)不同,先天性FⅪ缺乏(血友病C)的人通常在重大创伤时才可能出现轻微出血[14]。FⅪ缺乏症最常见于德系犹太人,一项大型回顾性队列研究显示,与FⅪ水平正常的患者相比,FⅪ缺乏症患者的静脉和动脉血栓栓塞率显著降低[15]。换言之,FⅪ似乎在病理性血栓形成中起关键作用,但对止血影响很小[16]。
综上,抑制接触途径是极具吸引力的抗凝策略。目前,几种面向FⅪ和FⅫ的药物正在开发中,本文收集了8种该类药物已公开的相关数据,其作用机制包括抑制FⅫa介导的FⅪ激活(CSLl312、AB023);抑制肝脏合成FⅪ(ISIS 416858);以及抑制FXIa的催化活性(MAA868、BAY 1213790、EP-7041、BMS-986177、BAY 2433334)。
1 抑制FⅫa介导的FⅪ激活的药物
1.1 AB023(抗FⅪ单克隆抗体)AB023是一种IgG2b抗体,其作用机制不同于传统意义上的抗FⅪ抗体MAA868和BAY 1213790(见下文),它与FⅪ的A2结构域结合,特异性抑制FⅫa介导的FXI激活、FⅪa对FⅫ的激活以及FⅪa与高分子激肽原之间的相互作用,但不会影响凝血酶激活FⅪ和FⅪa对FⅨ的作用[17]。AB023被证明在几种动物模型中预防血栓形成是有效的。AB023前体14E11,可显著增加动脉模型的颈动脉通畅性,延长肺动脉栓塞模型的呼吸停止时间。尽管活化部分凝血活酶时间(APTT)有所延长,但均没有观察到出血[17-19]。
在狒狒模型中,与对照组相比,AB023减少了75%的移植物内血小板和纤维蛋白的积聚,虽然APTT在给药24 h后仍升高,但未观察到出血差异。随后在一项随机双盲、安慰剂对照、单次递增剂量Ⅰ期试验中对AB023进行了评估,涉及21名健康的成年志愿者。当剂量≥0.5 mg/kg时,APTT在0.25~24 h内达最大延长值。AB023的血药浓度呈剂量依赖性,最大血药浓度出现在给药后0.08~0.65 h间。药物半衰期也随剂量增加而增加,0.1 mg/kg剂量时约为1.3 h,5.0 mg/kg时约为121.5 h。药物血浆清除率随着剂量的增加而降低。AB023对凝血酶原时间(PT)和出血时间(BT)没有明显影响。报告中未提及FⅪ活性。与对照组相比,AB023未观察到严重不良反应,最常见的不良反应是排痰性咳嗽,但这被认为与治疗无关。总体而言,AB023在健康人类志愿者中是安全且耐受性良好的[20]。
AB023通过选择性抑制FⅫa对FⅪ的激活,中止了原本由接触激活启动的凝血,但它保留了FⅪ的活性,所以与其说AB023是FⅪ抑制剂,不如称其为FⅫa抑制剂。虽然先天FⅫ缺乏的患者很少见,但有研究显示FⅫ缺乏者可以在无干预的情况下接受大手术[21-23]。这表示,使用AB023的患者发生出血时很可能可以与凝血系统正常的患者进行类似处理。AB023作用机制的另一个潜在好处是避免了抗体与其它FⅫa底物之间的竞争。另外,AB023保留了FⅫa的其他功能,包括激活激肽-激肽释放酶系统,可能具有较少的非靶点效应。
一项对终末期肾病慢性血液透析患者的Ⅱ期试验正在进行,目的是评估AB023在减少透析回路血栓形成方面的安全性和有效性。
1.2 CSL312(抗FⅫa单克隆抗体)CSL312是IgG4抗体,可结合并抑制FⅫa活性。CSL312及其前体3F7已经在许多动物模型中被评价,包括血栓形成模型、遗传性血管性水肿(HAE)模型。与对照组相比,3F7能有效减少兔体外膜肺氧合(ECMO)回路血栓形成,出血次数低于普通肝素组[24]。最近,一种更有效的抗FⅫ抗体CSL312正在开发当中,与3F7相比,CSL312与FⅫa的亲和力提高了44倍。这两种抗体在HAE动物模型中进行了试验。与传统治疗血管水肿药物相比,在减轻小鼠耳朵水肿方面,3F7展现出更深远持久的作用。CSL312在体外人血浆中对产生缓激肽的抑制作用也强于传统药物。同时,CSL312以剂量依赖的方式延长了食蟹猴的APTT,但不影响PT,并且注射了耐受性良好[25]。CSL312的Ⅰ期临床数据尚未公布。
CSL312的功能与AB023极为相似,二者基本上消除了FⅫa对FⅪ的作用,但FⅪ活性不受影响,且在动物模型中都表现出能够减少病理性血栓形成。然而,CSL312对激肽/激肽释放酶途径的抑制,虽然为HAE等疾病提供了治疗可能,但同时也产生了不确定的非靶点效应,这方面正在积累临床前数据。FⅫa靶向药物的另一个缺陷是可能与其他底物竞争FⅫa催化域。
一项旨在调查CSL312预防HAE患者发作的临床疗效、药代动力学和安全性的Ⅱ期试验正在招募。另外一项评估CSL312在预防PICC相关血栓形成方面的研究在今年3月因与安全性无关的业务决策被撤回。
2 抑制FⅪ合成的药物——ISIS 416858(FⅪ反义寡核苷酸)
反义寡核苷酸(ASO)通过降解特定的mRNA,最终干扰目标蛋白合成[26]。ISIS 416858是针对FⅪ的第二代ASO,结合FⅪ对应mRNA,刺激核糖核酸酶H1分解,阻止了mRNA翻译,以降低FⅪ水平。
在一项Ⅱ期随机开放平行组研究中,对300例接受择期单侧全膝关节置换术的成年受试者,分别皮下注射200 mg或300 mg的ISIS,或40 mg依诺肝素,并至少持续8 d。疗效终点是VTE的发生率,安全终点是临床相关出血的发生率。200 mg ISIS(VTE发生率为27%)的疗效与依诺肝素(30%)相当,300 mg ISIS的VTE发生降低(4%)。与依诺肝素(8%)相比,ISIS的出血风险较低(分别为200 mg 4%,300 mg 3%),差异无统计学意义,其血浆FⅪ水平呈剂量性递减,APTT明显延长,而PT、FⅧ、FⅨ和FⅫ值在各组间无明显差异。ISIS组偶会有轻微注射反应[27]。
当发生组织损伤或血小板激活时,便有更多的FⅫ或凝血酶激活FⅪ,因此,对于预防外科手术相关的VTE,并非专注于激活FⅪ这一过程,选择降低FⅪ水平可能更有效。ISIS的缺点包括:降低FⅪ水平所需时间过长;可能导致类似FXI缺乏症患者的出血风险[28],即在某些情况下,虽然出血很轻微,但临床意义重大,当然这一假设需要进一步临床数据来支持或驳斥。
两项以评估ISIS 416858在进行血液透析的终末期肾病患者当中的安全性、药代动力学和药效学的Ⅱ期试验,目前已完成招募正在进行当中。
3 靶向抑制FXIa催化活性的药物
3.1 MAA868(抗FXI和FXIa单克隆抗体)MAA868是IgG1抗体,它的Fab片段高亲和力结合FⅪ和FⅪa的催化域,使其变构,将FⅪa锁定在酶原状态,并抑制凝血酶→FⅪa前馈环路,阻止凝血的进一步激活。但MAA868不会阻断FⅫa激活FⅪ的能力。
在Ⅰ期随机、盲法、安慰剂对照、单次剂量递增研究中,对61名成人受试者(包括1组严重肥胖者)皮下注射MAA868。MAA868以剂量和时间依赖的方式延长APTT,还可抑制血浆中游离FⅪ水平及其活性,FⅪ最大抑制水平为基线的3%,在任何时间点均未观察到完全抑制(FⅪ水平<1%)。该药对PT和凝血酶时间(TT)均无影响。MAA868血药浓度达峰时间为7~21 d,且与剂量无关。重度肥胖组药物最大浓度和抑制效应相对较低。药物半衰期为20.1~28.6 d。治疗组有7起药物相关轻微不良事件,而安慰剂组有两起,其中头痛最常见。一名MAA868受试者发生了致命性心脏骤停,但被认为与药物无关。治疗组未报告注射反应或过敏反应。研究人员表示,虽然MAA868的出血风险大大下降,但逆转其抗凝作用仍具临床必要性。为此,他们对MAA868和重组活化FⅦ(rFⅦa)处理后的人血进行了体外血栓弹力图检查,提示rFⅦa能够将凝血时间校正回正常参考范围内[29]。
MAA868能够在FⅪ酶原和活化形式上均有效抑制其促凝作用,通过与FⅪa特异性抗体DEF比较表明,MAA868能够更为全面的抑制FⅪ。但与其他FXI抑制剂相比,MAA868的这种与众不同是否能够提高临床疗效,仍有待观察。同样,尽管研究人员在尝试探索可能的逆转方案,但在rFⅦa对凝血时间的校正并不能证明其在严重出血情况下的临床有效性。肥胖患者MAA868血药暴露的降低也可能限制其使用,需要进一步研究来确定是否需要对严重肥胖症患者进行剂量调整。MAA868的优势是每月一次皮下注射使其具备更好的依从性和疗效。
MAA868计划用于房颤和全膝关节置换术血栓栓塞预防的两项Ⅱ期试验被撤回。日前,诺华宣布与黑石生命科学公司合作继续开发MAA868。一项评估MAA868对存在低风险血栓栓塞性卒中或外周栓塞的房颤或房扑患者的安全性、耐受性、药代动力学和药效学的Ⅱ期试验正在招募中。
3.2 BAY 1213790(抗FⅪa单克隆抗体)BAY 1213790也是一种IgG1抗体,它与FⅨa活性位点相邻的区域结合,从而引起别构调节,使FⅪa失去活性。目前尚无法获得更加具体的作用机制。在兔肝切开模型中,与对照组相比,BAY 1213790不会增加出血时间,还能够减少颈动脉FeCl3诱导的小鼠模型发生血栓形成[30]。
对83名健康的高加索成年男性进行了Ⅰ期单盲、平行安慰剂对照、单次剂量递增研究,以评估BAY 1213790的安全性、药效学及药代动力学。治疗组按剂量分组静脉滴注BAY 1213790。给药后APTT和全血凝血时间延长,FXI活性降低,呈剂量依赖关系。最大APTT倍数变化为2.17(65.4 s),且至少20 d内保持高于基线水平。与安慰剂相比,FXI活性在剂量大于0.15 mg/kg时开始显著下降,这几乎是在给药后立即发生的,并在约55 d后逐渐恢复到基线值。BAY 1213790达最大浓度的时间为1.05~4 h(依赖于剂量),半衰期为30~44 d。未观察到任何临床出血事件,出血时间也没有增加。不论是治疗组还是安慰剂组,不良反应均常见,但都很轻微,其中以头痛和鼻咽炎最为多见。同时未观察到剂量和不良事件发生频率之间存在明显联系[31]。
虽然目前还不能获得BAY 1213790结构和作用机制的细节,但该药物与MAA868不同,它对酶原FⅪ没有抑制作用,只抑制FⅪa活性。与MAA868相同的是,BAY 1213790的动物和人类Ⅰ期试验数据均未提示明显的出血信号。此外,作为一种单克隆抗体,BAY 1213790的优势在于与肾或肝无关的代谢方式[32],使其适用于肝肾功能不全患者。其较长的半衰期方便了给药,如每月一次即可达到稳定的药物血浆水平,这是长期血栓预防所需要的。
但是,在接受BAY 1213790治疗的患者中,APTT或FⅪ活性检测结果与临床之间的关联尚不清楚。一种特异性BAY 1213790逆转剂正在评估中,但这种药物的真正临床需求仍待探究。并且需要进一步研究BAY 1213790在不同患者群体中的安全性、药效学和药代动力学。评估BAY 1213790在进行血液透析的终末期肾病患者中的安全性和耐受性的Ⅰ期试验正在招募。Ⅱ期FOXTROT试验,比较BAY 1213790与依诺肝素或阿派沙班在预防接受全膝关节置换术患者静脉血栓栓塞时的有效性和安全性,目前已经完成受试者招募。
3.3 EP-7041(小分子FXIa活性位点抑制剂)至少已经有三种选择性小分子FXI抑制剂在进行人体试验,尽管到目前为止关于它们安全性和有效性的数据公布还很少。EP-7041便是其中一类,已经完成了初步Ⅰ期试验。在仅以摘要形式发表的Ⅰa、Ⅰb期临床试验报告中,健康志愿者接受单次递增剂量的EP-7041静脉注射,或连续5 d接受安慰剂静脉注射[33]。试验过程中未发生严重的不良反应事件。该药呈剂量相关的APTT延长,且起效迅速,半衰期较短,其作用可以通过简单的方法逆转,对PT无影响。目前尚不清楚是否有其它EP-7041的Ⅰ期或Ⅱ期试验在进行。
3.4 BMS-986177(小分子FⅪa活性位点抑制剂)第二种选择性小分子FⅪ抑制剂,BMS-986177,高亲和力结合、抑制活化形式的FⅪ。BMS-986177已经完成了多项Ⅰ期临床试验,在健康受试者(临床试验注册号:NCT02608970,N C T 0 3 3 6 2 4 3 7、N C T 0 3 2 2 4 2 6 0)、肾功能损害者(NCT03196206)、血液透析中的肾损害(NCT03000673)、可能存在相互作用的药物(NCT02959060)以及与阿司匹林联合使用(NCT03341390、NCT03698513)等方面进行了试验,但是还没有公布任何数据。目前,针对BMS-986177的多项Ⅱ期试验正在招募,例如在阿司匹林或氯吡格雷的基础上加用BMS-986177用于中风二级预防,在预防全静脉血栓栓塞事件方面的疗效。
3.5 BAY 2433334(小分子FⅪa抑制剂)BAY 2433334是一类口服小分子FⅪa抑制剂,其具体作用机制尚不清楚。BAY 2433334已经完成了多项Ⅰ期临床试验,但是相关数据还未公布。一项评估BAY 2433334最佳剂量、并对房颤患者就安全性、疗效与阿派沙班比较的Ⅱ期试验目前正在招募。另外两项Ⅱ期试验,旨在评估BAY 2433334在双重抗血小板疗法的基础上对心肌梗死患者的安全性和疗效以及在非心源性缺血性卒中患者中的正确剂量和安全性,即将招募受试者。近日,中国国家药监局药品审评中心(CDE)公示,BAY 2433334的3项临床申报已获得受理[34]。
4 总结与展望
人们对抗栓治疗安全性的不断追求,以及对凝血过程更深入的了解,促进了新型抗凝剂的发展。当肝素和华法林效果较差时,具有选择性靶点和明确机制的DOACs成为选择[35]。然而,DOACs抗凝治疗的诸多问题仍然存在,特别是对出血风险的一贯担忧促使人们对于作为潜在治疗靶点的接触途径的研究[36]。大量的临床前和早期临床数据证明,选择性抑制内源性凝血途径可以限制受损血管表面的初始凝块形成[37],且同时不影响外源性和共同凝血途径,这将降低出血的可能性。接触因子FⅫ、FⅪ的抑制剂正在开发,在早期临床数据中,这些药物展现了多方面优势,例如更好的抗凝效果,出血风险的下降,便利的给药方式,不依赖肝、肾的代谢形式等,使其适用于各种可能的临床方案,包括预防手术和血管内装置源性的血栓形成,以及预防和治疗与传染病相关的凝血功能异常。但这些药物仍需要进行大量研究(表1),当中部分药物目前正在接受更大规模的Ⅱ期临床试验,以进一步评估它们的安全性和有效性,似乎只有时间才能证明靶向抑制FⅪ和/或FⅫ是否能为抗凝治疗提供新的解决方案。抗凝的前景充满光明,大量研究支持抗凝剂在未来将更加多样化,针对不同患者确保更合理和更有益的治疗。
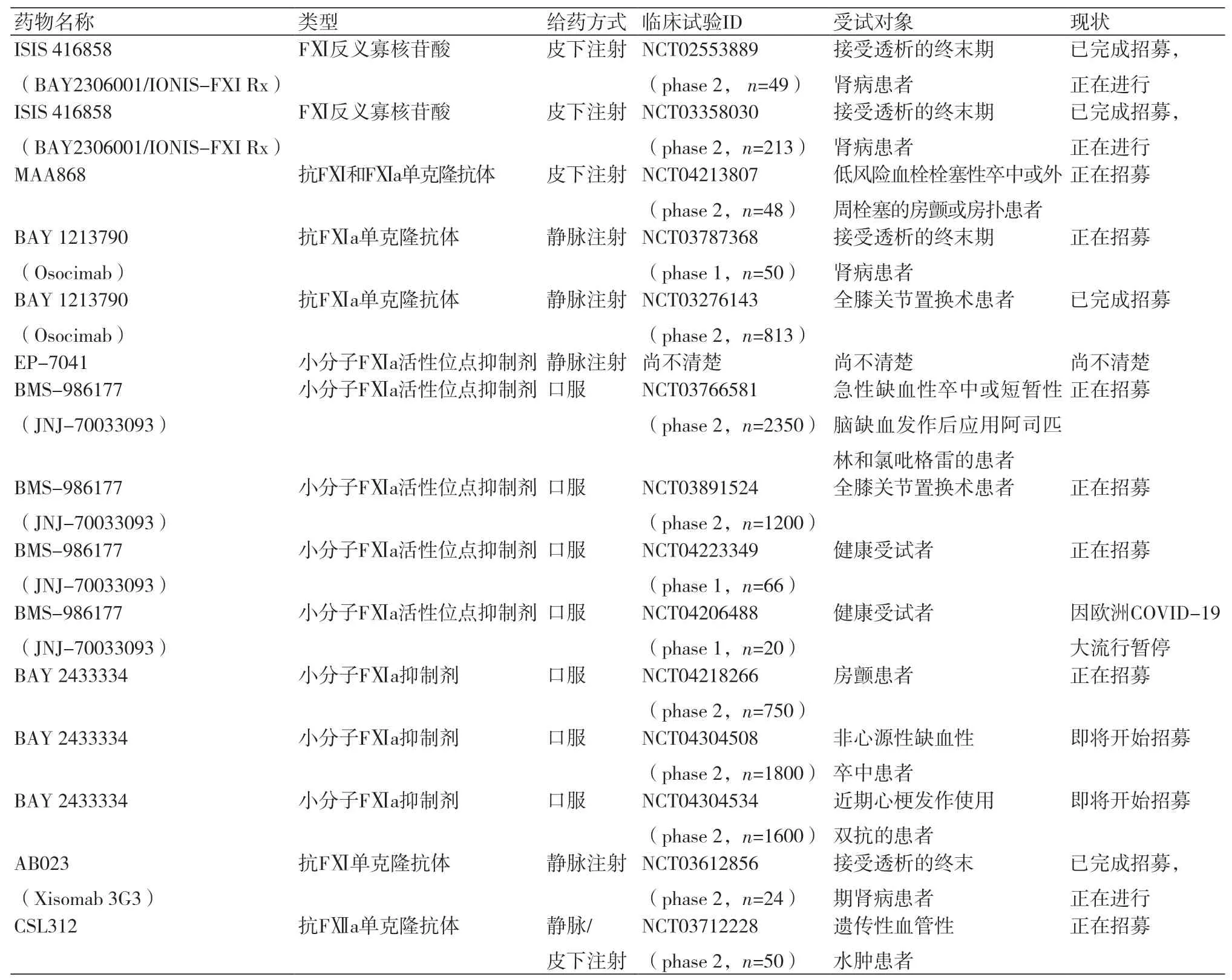
表1 正在进行或即将进行的凝血因子Ⅺ、Ⅻ靶向药物临床试验
