ICP-MS法测定复方氨基酸注射液(18AA)中14种金属元素含量
2020-12-15周敏熊欣程奇珍
周敏,熊欣,程奇珍
江西省药品检验检测研究院,国家药品监督管理局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,南昌 330029
复方氨基酸注射液(18AA)是肠外营养制剂,属于营养用氨基酸注射液,用于各种应激状态和危重患者的营养支持,临床使用较广[1,2]。氨基酸独特的分子结构,可加速包装材料中金属离子溶出[3]。同时,金属元素也可能在原辅料中带入和生产设备引入。某些金属元素不仅对药品的稳定性、保质期产生不利影响,还可能因为潜在的毒性引发药物毒副作用[4]。从药物安全性及稳定性考虑,有必要对复方氨基酸注射液(18AA)中的金属元素进行分析考察。
电感耦合等离子体质谱法(ICP-MS)是目前最强有力的多元素快速分析技术之一。它可以同时测定元素周期表中的大部分金属元素,具有灵敏度高、背景计数低、检出限低、线性动态范围宽等优势[5]。本次实验采用电感耦合等离子体质谱(ICP-MS)法建立测定复方氨基酸注射液(18AA)中镁、铝、钾、钙、铬、锰、铁、镍、铜、锌、砷、镉、钡、铅14种金属元素含量的方法,以期为该制剂质量控制提供参考。
1 材料
1.1 仪器
Synergguv millipore超纯水制水机(密理博中国有限公司);MAS-xpress型微波消解仪(美国CEM公司);GST25-20A型赶酸仪(天津市莱玻特瑞仪器设备有限公司);7700X型ICP-MS仪(安捷伦科技有限公司)。
1.2 标准物质与试剂
混合对照标准溶液(包含镁、铝、钾、钙、铬、锰、铁、镍、铜、锌、砷、镉、钡、铅等元素,安捷伦科技有限公司,批号:51-005CRY2,浓度:10 μg/mL);标准内标溶液[含铋(Bi)、锗(Ge)、铟(In)、铑(Rh)、钪(Sc)等内标元素,安捷伦科技股份有限公司,浓度:100 μg/mL,批号:5-67MKBY2];硝酸(色谱纯,瑞士Fluka公司,批号:BCBP0680V);水(纯化水,自制)。
1.3 样品信息
复方氨基酸注射液(18AA)(A企业,批号2018011261、2019022064、2020010964,编 号Y1~Y3;B企业,批号1608182041,编号Y4;C企业,批号16092408,编号Y5;D企业,批号16918824,编号Y6。)
2 试验方法
2.1 仪器条件设置
2.1.1 ICP-MS条件设置射频功率:1 530 W;冷却温度:4 ℃;碰撞气:氦气;载气:氩气;载气流量:1.08 L/min;积分时间:0.3 s;等离子气流量:15 L/min;采样锥孔径:1.0 mm;截取锥孔径:0.4 mm;数据采集重复次数:3次;入口温度:33.8 ℃;出口温度:41.5 ℃。
2.1.2 内标及同位素设置测定时选取的同位素为24Mg、27Al、31K、40Ca、53Cr、55Mn、56Fe、60Ni、63Cu、66Zn、75As、111Cd、137Ba、208Pb,其 中23Na、24Mg、27Al、31K、40Ca、53Cr、55Mn、56Fe以45Sc作为内标,60Ni、63Cu、66Zn、75As以72Ge作为内标,111Cd、137Ba以115In作为内标,208Pb以209Bi作为内标。
2.1.3 微波消解程序设置消解功率:1 600 W;升温程序:15 min内由室温升至160 ℃,保持5 min,再以5 ℃/min的速度升温至190 ℃,保持25 min。
2.2 溶液的制备
2.2.1 内标溶液精密量取1 mL内标对照品溶液,置100 mL量瓶中,用2%硝酸稀释至刻度,摇匀,即得浓度为1 μg/mL的混合内标溶液。
2.2.2 混合对照溶液精密量取10 mL混合对照标准溶液,置100 mL量瓶中,用2%硝酸稀释至刻度,摇匀,即得浓度为1 μg/mL的混合对照溶液。
2.2.3 样品溶液精密取样品溶液10 mL,置微波消解罐中,置于赶酸仪中,100 ℃下浓缩至约1 mL,精密加入硝酸10 mL,在100 ℃下预消解1 h,取出,盖上内盖并旋紧外盖,按“2.1.3”项下微波消解程序消解,取出,放至室温,开盖,置于赶酸仪中,140 ℃赶酸至硝酸近干,用2%硝酸分次转移至25 mL量瓶中并稀释至刻度,摇匀即得。同法制备空白溶液。
2.3 测定方法
仪器的内标进样管在仪器分析过程中始终插入内标溶液中,依次将仪器的样品管插入系列混合对照溶液中进行测定,绘制标准曲线。之后将仪器的样品管依次插入样品溶液中,测定,从标准曲线上计算得相应的浓度。在同样的分析条件下测定空白溶液进行空白校正。
3 方法学验证
3.1 线性关系与检测限
分别精密量取混合对照标准溶液(1 μg/mL)适量,用2%硝酸溶液稀释制成浓度为0、1、4、8、10、20、40、60、80、100、200、400 ng/mL系 列混合对照品溶液。以测定元素响应值与对应内标元素响应值比值为纵坐标,以溶液元素浓度(ng/mL)为横坐标,制作标准曲线。以3倍信噪比计算检测限。试验结果见表1。
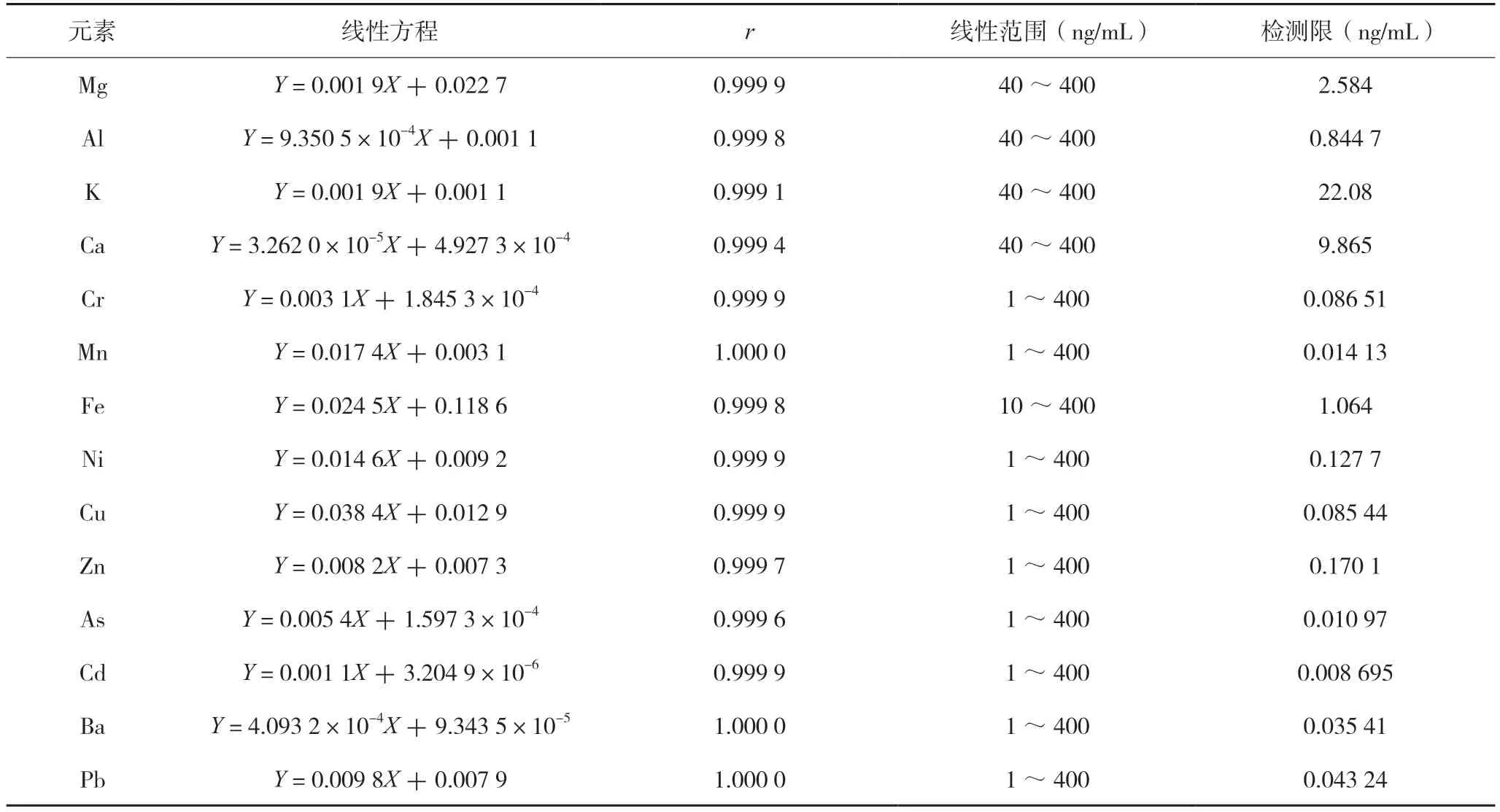
表1 线性关系与检测限
3.2 回收率试验
精密量取样品溶液(Y1)10 mL(共6份),置微波消解罐中,分别精密加入混合对照标准溶液(浓度均为10 μg/mL)0.25、0.25、0.5、0.5、0.75、0.75 mL,按“2.2.3”项下方法制备,作为各元素的回收试验溶液;回收试验结果详见表2。
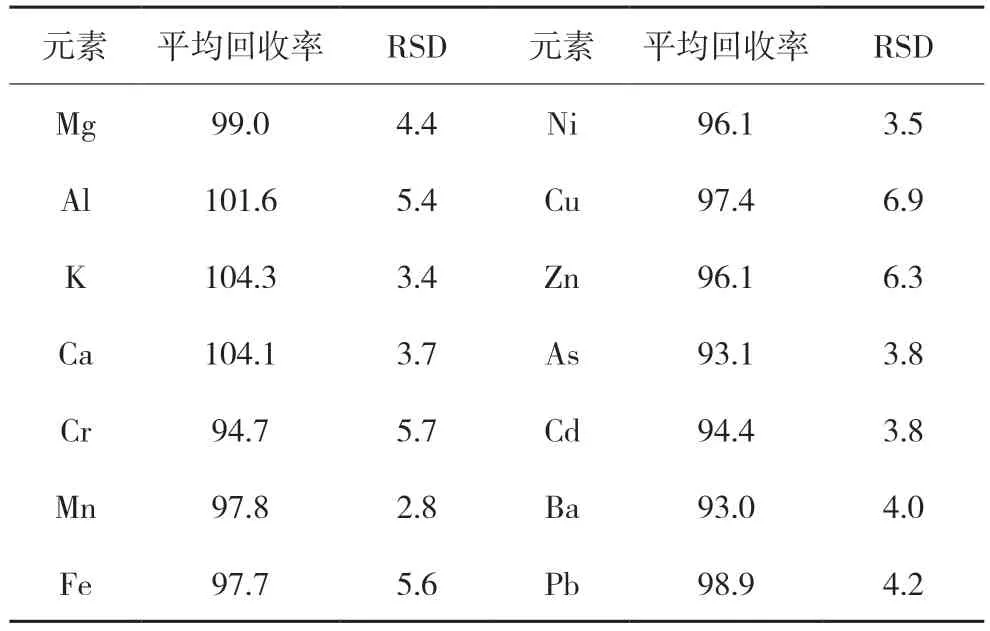
表2 加样回收率与重复性试验结果(n=6) %
3.3 重现性试验
因样品中部分元素含量低于检出限,使用回收率及RSD表示。结果见表2,方法重复性良好。
3.4 精密度试验
取3.1项下混合对照品溶液(200 ng/mL),重复进样测定6次,记录测定结果。结果详见表3,表明仪器精密度良好。
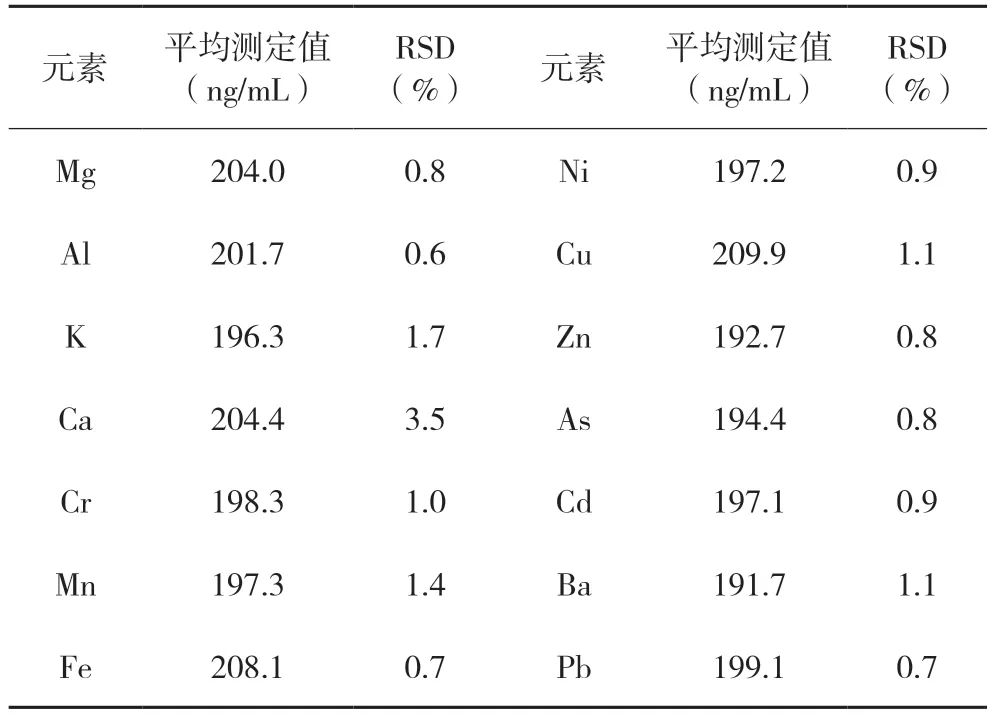
表3 精密度试验结果(n=6)
4 样品测定与结果
取6批样品,按“2.2.3”项下方法制备供试品溶液(每批制备2份),测定结果,记录仪器响应值并计算各批样品中各元素含量。样品测定结果见表4。
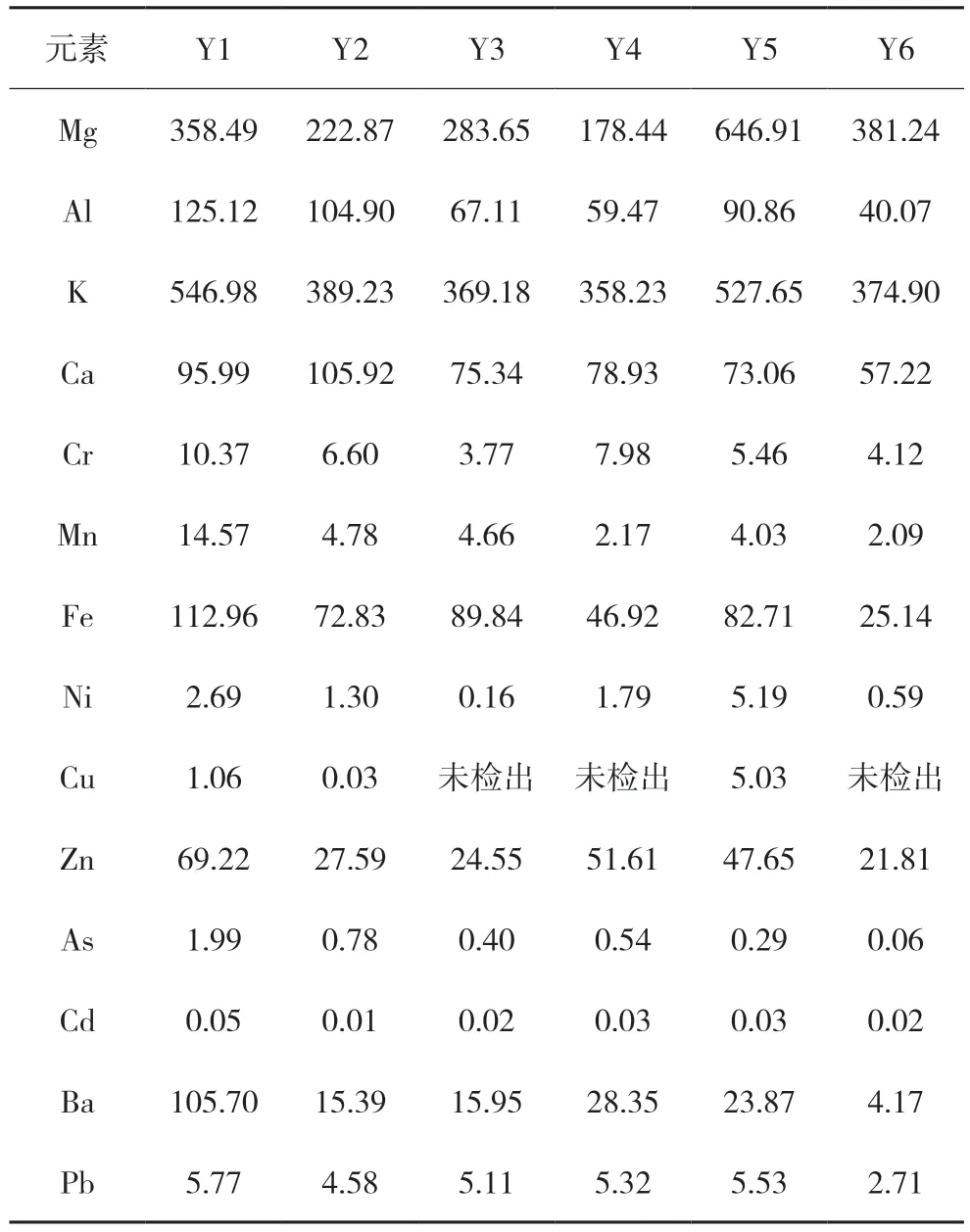
表4 样品测定结果(n=2) ng/mL
5 结论
5.1 方法分析
复方氨基酸注射液(18AA)虽是澄清透明液体,但样品直接使用ICP-MS测定,对金属元素测定干扰较大,加样回收率低,对测定造成干扰。同时,由于样品中元素含量均为微量,为提高检测准确度,选择先浓缩样品溶液,再进行酸破坏。经方法学评价显示此方法线性回归良好,灵敏度高、准确性好,各元素加样回收率均较理想,表明专属性较好。该方法适用于复方氨基酸注射液(18AA)中多种金属元素的检测分析。
5.2 结果分析
本次实验共采用来自四家企业6批样品测定,结果表明不同企业间样品中微量金属元素含量存在一定差异,其中含量较高的为镁、钾、铝、铁、钙、锌与钡,其余各金属元素含量均较低。参照ICH Q3D元素杂质指南对制剂金属元素杂质限度规定[11],各微量元素均低于限度。
USP 41 版要求用于全肠外营养的大容量注射液中铝的含量不得超过25 μg/L,并且应在说明书和标签中警示[9]。复方氨基酸注射液(18AA)现行标准[10]中对复方氨基酸注射液中铝元素的限度未进行控制,根据实验结果,6批样品中铝元素含量均超过了FDA规定量,存在一定的用药风险。
复方氨基酸注射液(18AA)的包装材料主要为钠钙玻璃输液瓶和注射液用卤化丁基橡胶塞,二者中常会加入少量三氧化二铝[6,7]。复方氨基酸注射液由多种氨基酸组成,由于氨基酸的分子结构,对金属离子具有一定的螯合作用,可加速包装材料中的金属离子溶出。同时,产品中含有较高浓度的氯离子和醋酸根离子,药液的离子强度大,较易破坏包装材料的结构层[8]。本次实验选取来自同一企业的相邻年份生产的三批样品[Y1(2018),Y2(2019),Y3(2020)],从实验结果看到,样品中微量元素含量随年份均明显增加,证明包材中金属离子随时间放置有明显溶出。
为确保复方氨基酸注射液在效期内的质量可控,同时确保临床用药安全,建议制剂生产商在质量标准(货架期标准)中增加主要金属元素含量测定,对金属离子溶出量进行追踪分析。国家也应尽快制订相关的文件及标准,对注射液中元素尤其是铝元素含量进行控制。
