胎儿先天性血管环的产前超声诊断分析
2020-12-11孙碧云朱向明朱菲菲
孙碧云,洪 云,朱向明,江 峰,朱菲菲
(皖南医学院第一附属医院 弋矶山医院 超声医学科,安徽 芜湖 241001)
先天性血管环(congenital vascular ring,CVR)是一种罕见的心血管畸形,约占先天性心血管异常的1%,系主动脉弓及其分支完全或不完全地包围并压迫气管、食管甚至迷走神经和喉返神经,常并发其他心内外畸形或染色体异常[1-2]。CVR患儿出生后临床表现取决于血管环的分型和周围器官的受压程度,常见症状包括在婴儿早期引起呼吸窘迫和进食问题、反复发作的上呼吸道感染、声音嘶哑等,容易被漏诊、误诊,严重者可危及生命[3]。随着二孩政策的开放,产前准确诊断血管环对于优生优育及早期治疗干预方式选择有指导价值。本研究回顾性分析中孕期胎儿CVR的超声影像学特征,探讨规范化产前超声筛查在胎儿CVR诊断及预后评估中的应用价值。
1 资料与方法
1.1 一般资料 收集2017年6月~ 2019年6月在弋矶山医院经产前超声诊断的37例CVR胎儿患者,孕妇年龄22~39岁,平均(29.5±4.2)岁,孕20~28周,平均(23.6±2.8)周。纳入标准:①产前超声诊断经两位资深产前超声筛查医师共同确诊,二维超声图像清晰显示心脏结构、血管、气管及食管等结构,三血管气管切面显示异常血管环绕气管周围;②胎儿超声估测孕周与月经龄相符合。排除标准:妊娠后进行过治疗(药物或侵入性治疗)的自然受孕孕妇、试管辅助受孕者等。
1.2 仪器和方法 应用三星麦迪逊WS80A超声诊断仪,选用单晶体容积探头,频带宽1.0~8.0 MHz。首先确定胎儿方位、进行产前超声常规检查并评估孕周大小;再进行胎儿心脏筛查,检查流程先在胎儿胸部行横切面扫查,确定标准四腔心切面,在此基础上寻找三血管-气管切面,再完善左右心室流出道切面、主动脉弓切面、动脉导管弓长轴切面等标准切面扫查,应用彩色多普勒血流显像以及高级精细血流成像技术(S-Flow)显像观察各血管的血流动力学情况。重点观察三血管气管切面,明确主动脉弓在此切面的走形、分支,判断气管食管的位置及其与血管之间的相对位置关系。若正常导管弓与主动脉弓的V字形结构消失,气管后方存在血管结构走行,围绕气管或支气管,即可诊断为血管环形成。辅助应用S-Flow技术可以检测出平时难以监测的细微血管和低速血流信号。
1.3 随访 对超声诊断CVR胎儿行定期超声监测,建议孕妇完善胎儿染色体检查,统计终止妊娠孕妇并尽量完善病理结果,产后对患儿呼吸情况进行评估,并随访6个月。
2 结果
2.1 确诊孕妇胎儿超声表现 37例CVR患者中,右位主动脉弓(right aortic arch,RAA)、左位动脉导管(left duct artery,LDA) 29例,其中13例伴迷走左锁骨下动脉(aberrant left subclavicular artery,ALSA),即RAA-LDA-ALSA;双主动脉弓(double aortic arch,DAA) 5例;左主动脉弓、左位动脉导管并迷走右锁骨下动脉(aberrant right subclavicular artery,ARSA) 3例。在二维超声三血管气管切面(3VT)观察,血管、气管及食管表现为无回声,辅助彩色多普勒血流及S-Flow技术可以清晰显示血管的走行及血管与气管的位置关系。正常主动脉弓与导管弓的“V”形结构(图1)消失,不同类型的血管环在超声图像上形成的环状结构有所差异(图2、3)。合并肺动脉狭窄、永存左上腔静脉、室间隔缺损等心脏畸形的有6例,单纯合并唇腭裂畸形1例,详见表1。
2.2 随访结果 37例CVR胎儿中,32例完善胎儿染色体检查,合并染色体异常2例,均为13-三体综合征。合并严重心脏畸形或染色体异常选择引产终止妊娠5例, 2例失访。30例活产儿中,28例无症状,2例伴有喘鸣症状。
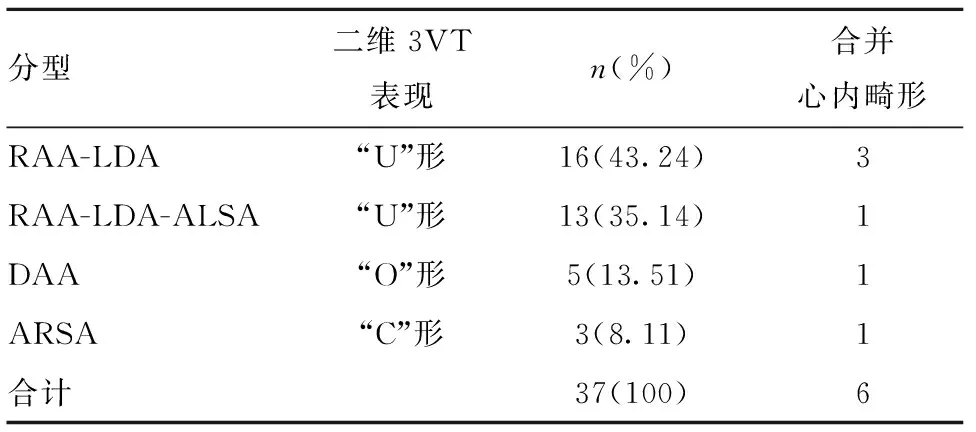
表1 37例CVR分型及合并畸形情况
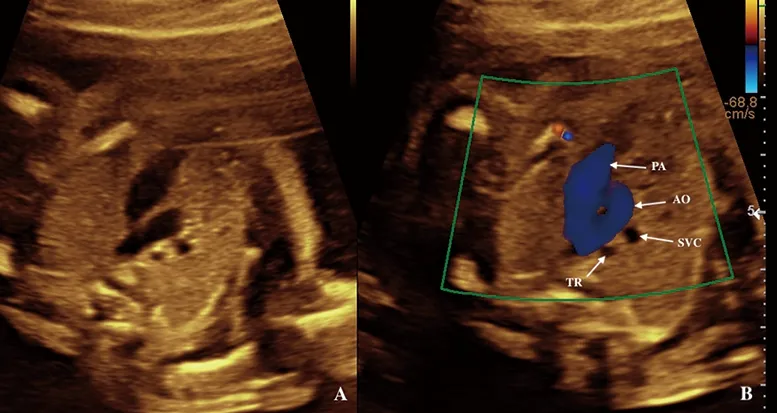
A.二维声像图显示三血管气管切面“V”形结构;B.彩色多普勒声像图显示三血管气管切面主动脉弓与导管弓的“V”形结构。其中AO为主动脉,PA为肺主动脉,SVC为上腔静脉,TR为气管。
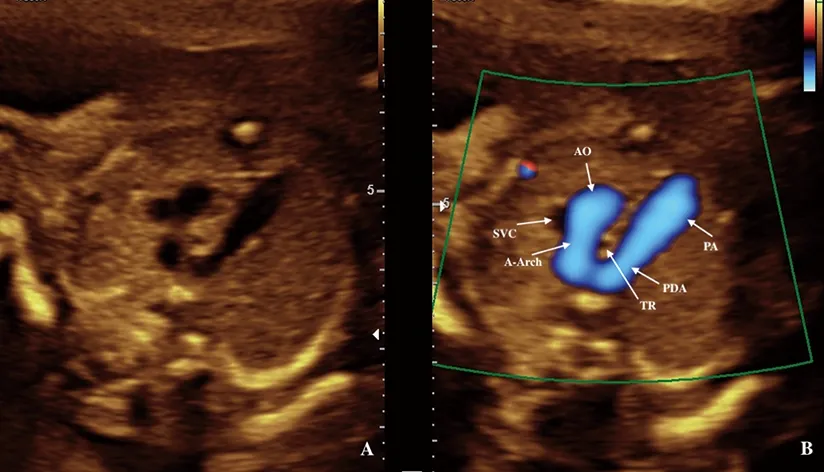
A.二维声像图显示主动脉弓走行于气管的右侧;B.S-Flow多普勒声像图显示“U”形血管环结构,气管被U字包绕。其中AO为主动脉,A-Arch为主动脉弓,PA为肺主动脉,PDA为动脉导管,SVC为上腔静脉,TR为气管。
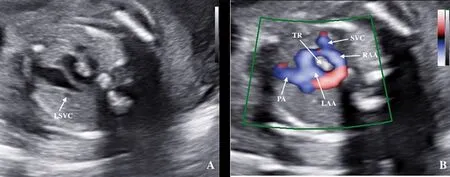
A.二维声像图显示双主动脉弓型血管环,呈“O”形结构;B.S-Flow多普勒声像图显示主动脉与动脉导管弓形成“O”形血管环结构。其中AO为主动脉,LAA为左侧主动脉弓,RAA为右侧主动脉弓,PA为肺主动脉,SVC为上腔静脉,TR为气管,本病例可见合并永存左上腔静脉畸形(LSVC)。
3 讨论
3.1 血管环的胚胎发育及病理机制 血管环的形成与胚胎主动脉弓系统的发育有关。胚胎在发育过程中形成六对原始主动脉弓。随着胚胎的发育,第1、2、3、5对弓动脉相继退化消失。正常情况下,主动脉弓位于气管左侧,第3对动脉弓退化形成颈总动脉和颈内动脉持续存在[4-5]。左侧第4对动脉弓产生左主动脉弓和左锁骨下动脉,右第四弓退化为右锁骨下动脉持续存在。胚胎发育过程中正常应予保留的却退化消失,或应该消失的仍然保留,则形成了主动脉弓走形异常,与气管、食管的相对位置关系发生改变,将气管或食管包绕,形成了完整或不完整的动脉环。根据血管环的发育特点,血管环病理类型众多,有学者将CVR主要归纳为4种病理类型即RAA-LDA-ALSA、DAA、无名动脉压迫、肺动脉吊带[6]。此外,还可以根据血管环包绕气管或食管的程度分为完全性和不完全性血管环。
3.2 超声监测胎儿CVR的体会 胎儿心脏超声检查要求包括众多切面,规范完整的切面扫查可以减少血管环的产前漏诊率[7-8]。超声心动图检查胎儿CVR的关键在于正确扫查确定三血管气管切面,重点观察气管与主动脉弓的位置关系,典型表现为气管后方存在血管结构走行,围绕气管、食管形成“U”形、“O”形或“C”形环状。除常规心脏横断面扫查外,可以辅以冠状位扫查,特别是经胎儿降主动脉起始部冠状面的扫查,从不同切面观察血管与气管、食管的空间位置关系[9-11]。标准的胎儿心脏切面对血管走形和空间构象的判断至关重要。二维图像联合彩色多普勒声像图可以清晰显示血管环及血流方向,利用灵敏度高的S-Flow技术能够全面提升血流的空间分辨率,便于观察细小动脉的走行分支。有研究表明,大多数血管环的主要血管构成是右位主动脉弓[12-13]。Backer等[6]将双动脉弓分为三种类型即右弓优势型、左弓优势型和左、右弓均衡型。不完全型血管环图像表现为“C”形,常见于一侧主动脉弓伴对侧迷走锁骨下动脉或无名动脉且伴同侧动脉导管,亦可见于绕食管主动脉弓伴对侧降主动脉、同侧动脉导管。本组病例中完全性血管环34例,其中“U”形血管环29例,13例合并左锁骨下动脉迷走,“O”形血管环5例;不完全性血管环3例,呈“C”形。血管环构成类型与文献报道一致,但因血管环发病率较低,因此本组资料中存在的血管环类型较少。此外,超声诊断血管环的患儿合并心脏其他畸形的风险增高,本组中6例合并永存左上腔静脉、法洛四联症等其他心脏畸形,故应注意排除是否合并其他心脏畸形。有文献报道部分双主动脉弓患儿可伴有22q11基因的微小缺失,患儿表现为神经发育迟缓、语言障碍等症状[14]。CVR胎儿条件允许的情况下建议完善染色体检查,排除染色体异常。
综上所述,产前超声检查可以明确显示CVR的形状,评估其与周围气管、食管的空间位置关系,规范化的超声操作流程以及结合S-Flow技术多普勒显像可以减少CVR的漏诊。对胎儿主动脉弓部的胚胎发育过程及血管的病理分型的理解,有助于超声医师做出正确诊断,为胎儿优生优育及后续治疗提供指导。
