采用葡萄糖参考方法为室间质量评价样本确定靶值的应用初探
2020-12-03金中淦张素洁欧元祝虞啸炫孙贺伟范霄宇虞科颖
金中淦, 居 漪, 张素洁, 李 卿, 欧元祝, 虞啸炫, 孙贺伟, 范霄宇, 虞科颖
(1. 上海市临床检验中心参考测量实验室,上海 200126;2.上海市临床检验中心临床生化免疫学研究室,上海 200126)
葡萄糖(glucose,Glu)是临床实验中重要的检测项目,血糖监测是糖尿病诊断和治疗的重要环节,其结果有助于评估糖尿病患者血糖代谢情况,可帮助临床制定治疗方案,并监测疗效。因此,临床实验室Glu检测质量在糖尿病管理中具有重要作用[1-2]。能力比对检验(proficiency testing,PT)/室间质量评价(external quality assessment,EQA)活动是目前管理和提高临床实验室检测质量的常用方式,通常依据方法学或检测系统进行分组统计,靶值为组内均值或中位值[3]。本研究拟运用国际检验医学溯源联合委员会(the Joint Committee for Traceability in Laboratory Medicine,JCTLM)公布的同位素稀释气相色谱串联质谱(isotope dilution gas chromatography tandem mass spectrometry,IDGC/MS)Glu参考方法[4]确定EQA样本靶值,探索其在EQA中的可行性。
1 材料和方法
1.1 研究对象
收集参加上海市临床检验中心2018年第2次常规化学EQA活动的509家各级、各类医院的医学实验室及独立实验室反馈结果。
1.2 样品
正确度物质为美国国家标准与技术研究院(the National Institute of Standards and Technology,NIST)标准物质SRM 965b(-70℃保存)及国际临床化学协会(the International Federation of Clinical Chemistry and Laboratory Medicine,IFCC)提供的RELA-A和RELA-B。EQA样品为2018年第2次EQA活动的5份样本,编号分别为EQA1、EQA2、EQA3、EQA4和EQA5,均为冻干血清,依据中国合格评定国家认可委员会(China National Accreditation Service for Conformity Assessment,CNAS)-GL03-2006《能力验证计划样品均匀性和稳定性评价指南》评估样品的均一性和稳定性[5]。
1.3 仪器与试剂
Glu标准品SRM 917c,纯度为(99.7±0.3)%,购自NIST;13C6-D-Glu标记物同位素丰度为99%,购自美国Cambridge Isotope laboratories公司;乙腈(质谱级)、乙酸(质谱级)购自美国Fisher公司,乙酸酐购自国药集团。Agilent G7000B气相质谱仪、HP-5MS UI毛细管柱(30 m×0.25 mm,0.25 μm)均购自美国Agilent公司,梅特勒-托勒多分析天平(Max=220 g,d=0.1 mg)购自德国METTLER公司,氮气仪购自美国THERMO公司。
1.4 参考方法赋值
上海市临床检验中心参考测量实验室是通过CNAS ISO/IEC17025/15195认可的实验室,被认可的项目包括血清Glu。赋值过程:(1)样品前处理,在血清样品中加入适量Glu标记物溶液,使血清中Glu的含量与Glu标记物含量之比约为1,加入适量无水乙醇去除蛋白质,10 000×g离心10 min,收集上清液至另一管中;(2)衍生化反应,取收集的上清液200 μL至另一样品瓶中,60 ℃氮气吹干后,加入盐酸羟氨吡啶溶液(0.6 mol/L)200 μL,混匀,90 ℃条件下反应1.5 h,冷却后加乙酸酐300 μL,90 ℃条件下反应1 h,60 ℃氮气吹干,用400 μL二氯甲烷复溶,进行ID-GC/MS分析;(3)ID-GC/MS条件,以分流模式进样,分样流比为20∶l。进样口温度设定为270 ℃,氦气流速为1.0 mL/min,初始炉温为150 ℃,持续1 min,再以30 ℃/min的速率升至180 ℃,持续1 min,再以20 ℃/min的速率升至280 ℃,持续1 min。离子源温度250 ℃,电离能为70 eV。选择离子监测模式下采集质荷比(m/z)314和319,扫描时间为200 ms。进样量为1 μL;(4)测定过程,参考方法赋值过程依据本实验质谱法样品赋值标准操作规程进行,分3批次测定,每批次每个浓度样品重复前处理3份样本,每份样本与标样同步测定,按低标-样品(含质控)-高标的次序进样,每份样本最少重复测定3次,要求3次进样检测结果的变异系数(coefficient of variation,CV)<2%,否则需要再增加进样次数至满足要求,以3次进样的均值作为每份样本的有效实验结果。
1.5 临床实验室EQA过程
样本通过上海市临床检验中心指定冷链系统运送到参评实验室,各参评实验室按照标准操作规程测量样本,记录测量结果,并通过网络平台上传测定结果、所用仪器、方法等相关信息。
1.6 统计学方法
使用上海市临床检验中心EQA评价管理平台及Excel 2016软件进行数据的分析处理,计算中位数及偏移。
2 结果
2.1 参考方法性能
Glu参考方法测量不精密度≤2.0%,测量参考物质相对偏移<1.0%。本实验室参加IFCC参考实验室网络比对,测定结果均在规定的等效限内。见表1。

表1 参考方法主要性能评价
2.2 EQA样本赋值结果
实验过程中同步测定正确度物质,要求正确度物质测定结果在靶值允许偏移范围内,否则该批次实验结果无效。参考方法为EQA样本定值结果。见表2。
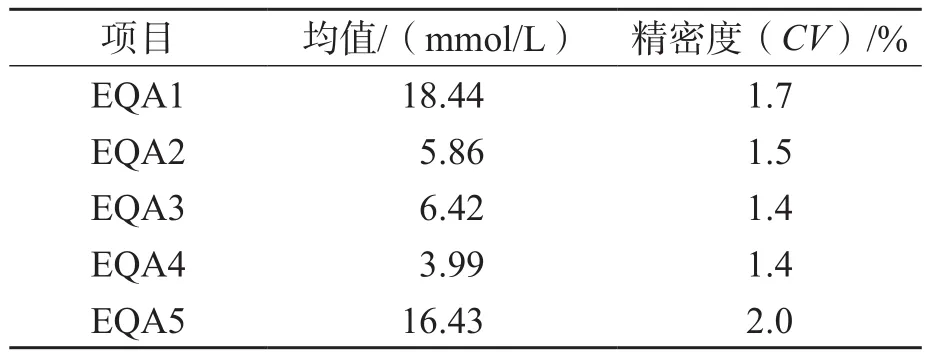
表2 参考方法测定血清Glu结果
2.3 EQA结果分析
2.3.1 按照Glu检测的不同方法对调查结果进行分析 按照Glu检测方法对检测结果进行分析,不同方法测定的Glu水平中位值与参考方法定值结果的相对偏移为-2.22%~4.51%,见图1。按WS/T 403-2012[6]中偏移2%的评价标准,其中己糖激酶法5个浓度的测定值与参考方法确定靶值的相对偏移均<2%。

图1 不同方法测定的Glu浓度与参考方法确定靶值的相对偏移
2.3.2 按照不同检测系统对结果进行分析 不同常规分析系统测定的血清Glu浓度中位数与参考方法确定靶值的相对偏移见图2。13个系统检测EQA1~5结果中位数与参考方法确定靶值的相对偏移分别为-1.71%~3.47%、-0.17%~3.75%、-2.3%~3.60%、0.50%~7.52%、-1.70%~3.23%。按WS/T 403-2012[6]中偏移2%的评价标准,只有7.69%(1/13)的常规分析系统测定的5个Glu结果与参考方法定值的相对偏移<2%,有61.54%(8/13)的系统只有1个结果与参考方法定值的相对偏移>2%,有15.38%(2/13)的系统2个结果与参考方法定值的相对偏移均>2%,有7.69%(1/13)的系统3个结果与参考方法定值的相对偏移>2%,有7.69%(1/13)的系统测定的5个Glu浓度与参考方法定值的相对偏移>2%。

图2 不同常规分析系统测定的血清Glu浓度与参考方法赋值结果的相对偏移
2.3.3 EQA结果分析 分别以实验室所有数据中位数、参考方法定值为靶值,并且以WS/T 403-2012[6]中允许总误差的7%评价实验室合格率,结果见表3。
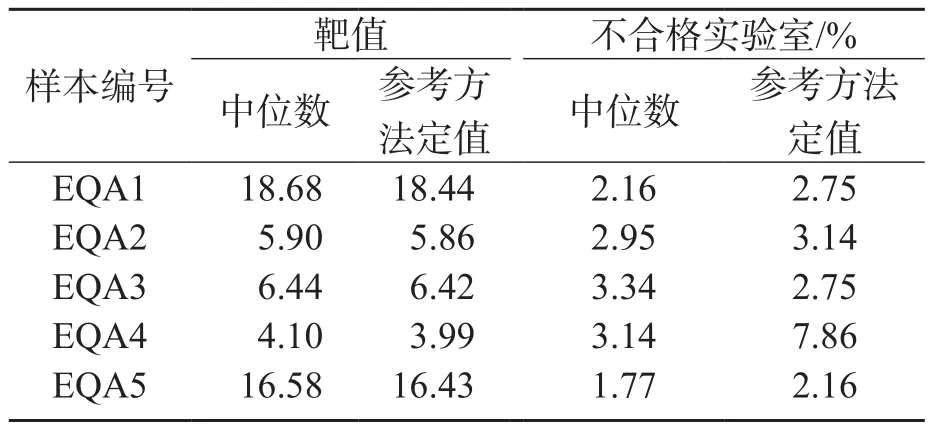
表3 实验室合格率
3 讨论
EQA中靶值的正确性、客观性一直是质量评价机构努力的方向。本研究主要利用Glu参考方法确定EQA样本靶值,初步探讨其在上海地区EQA工作中的可行性。
本实验室Glu参考方法已通过2018年CNAS ISO/IEC17025/15195认可[7],并于2019年通过JCTLM评审认可,该项目的检测能力已获得国际组织认可,可以为全球提供赋值服务,保证了本实验室检测靶值的可靠性。我们所分析的上海地区509家临床实验室的数据,不同检测原理测定的Glu浓度中位数与参考方法确定靶值的相对偏移为-2.22%~4.51%,己糖激酶法5个浓度的测定值与参考方法确定靶值的相对偏移均<2%,显示出较好的正确性。己糖激酶法的特异性高于葡萄糖氧化酶法,是公认的血糖测定的参考方法,己糖激酶法常规分析方法原理与参考方法类似,因此其测定准确性是比较高的。
按照检测系统进行分组分析,大部分系统测定的Glu浓度与参考方法赋值结果的相对偏移与行业标准中2%偏移的要求还存在一定距离,但大部分系统是能够满足1/2允许总误差的要求。张传宝等[8]用参考方法对血清进行赋值,并用标准物质SRM 965a对系统进行校准,评价了13种Glu常规检测系统的正确性,校准前大部分系统为正偏移,与我们的研究结果一致,常规方法测定Glu的特异性问题可能是主要原因。另外,目前大部分体外诊断试剂均采用的是单一校准品,该校准品的浓度和定值准确性是临床实验室检测结果的重要保证。
以行业标准中允许总误差7%来评价实验室合格率,当靶值为所有实验室检测结果的中位数时,EQA1~5不合格率分别为2.16%、2.95%、3.34%、3.14 %、1.77%;当靶值为参考方法赋值结果评价时,EQA1~5不合格率分别为2.75%、3.14%、2.75%、7.86%、2.16%。提示不同的靶值对实验室来讲,可能会导致不同的质量评价结果。CNAS-GL002:2018《能力验证结果的统计处理和能力评价指南》[9]指出,在能力验证中指定值的确定方式有多种,除去采用已知值和有证参考值外,参考方法赋值比采用参加者公议值为指定值等级高,不确定度要小[9],可以适当减少均值或中位数的偏移导致靶值出现偏差的情况,提高靶值和质量评价的客观性。EQA的关键是掌握样本的互换性及靶值的设定过程,本研究主要探讨靶值的设定过程,对于样本的互换性,需进一步探讨。值得注意的是,EQA样品虽为人血清基质,但为了满足保存和运输的要求,可能会添加一定的稳定剂,因此对于临床实验室检测EQA4样本出现的较大偏差是来自于系统的正确性问题还是样本存在的互通性问题,仍需进一步研究。EQA4样本浓度在4 mmol/L左右,为较低水平的浓度,而本实验室认可的参考测量范围是1.8~26.3 mmol/L,校准和测量能力为1.4%,故参考方法定值的准确性比较高。对于低浓度Glu的准确测量是值得被关注的。当血糖浓度为3.4~3.9 mmol/L时,约有29.92%糖尿病住院患者易发生有症状低血糖;而当血糖值为2.8~3.3 mmol/L时,约31.80%糖尿病住院患者易发生无症状低血糖[10]。低血糖的危害主要是对神经系统的损伤,因此应及时检测血糖,提高低血糖的诊断准确率,以达到早期预防、及时干预的目的,减少低血糖的临床危害[2]。后续我们将着手2方面的工作:一是尝试开展正确度验证工作,使用新鲜冰冻血清考察临床实验室检测水平;二是研究EQA样本的互换性,因常规EQA样本在保存、运输及成本上相对正确度样本具有较大优势,因此有必要评价选择质量较高的EQA样本,并且制定合理的EQA评价方案,为提高临床实验室检测质量发挥作用。目前较高质量EQA样本的获得需要实验室、质量评价机构及体外诊断试剂企业的共同努力[11]。
综上所述,如何确立靶值在临床实验室质量管理中有重要意义。参考方法可在推动临床实验室量值溯源工作、提高实验室检测质量中起一定作用。质量监管机构应关注EQA样本的质量,临床实验室应关注低浓度Glu测量的可靠性。
