铑催化的3-乙烯基吲哚与芳基三氮唑交换环合制备3-(2,3-二氢吡咯)吲哚衍生物
2020-12-01潘乐昊田世杰
邵 莺, 潘乐昊, 田世杰, 吴 锦
(常州大学 石油化工学院 江苏省精细石油化工重点实验室,江苏 常州 213164)
含氮杂环化合物广泛存在于多种具有生物活性的天然产物和药物中间体之中。取代吲哚作为一类重要的含氮杂环,具有广泛的生物活性和药理活性,在临床上广泛用于治疗艾滋病和癌症等疾病[1]。其中同时含有吡咯和吲哚结构的天然产物,如吡咯并吲哚生物碱naseseazineA/B和pestalazineA/B[2]都具有相当高的生物活性和实用价值。
烯基吲哚是个构建含吲哚及其他杂环或多环的重要合成子。Sun等[3]于2018年实现了铑催化下与烯基重氮衍生物反应,生成的Rh(II)卡宾物种插入3-乙烯基吲哚的乙烯基形成环丙烷结构中间体,然后经历cope重排,最终得到新型的[4+3]环合产物环庚烷并[b]吲哚衍生物。缺电子三氮唑衍生物与α-重氮氮杂烯化合物存在平衡,可在铑催化作用下放出N2后形成Rh(II)亚氨基卡宾中间体,从而发生一系列交换环合反应[4-6]。特别是该卡宾产物可与烯烃、二烯烃等,发生一系列[2+1][7], [3+2][8]和[4+3][9]的环加成反应,得到各种环合化合物。2019年,Anbarasan等[10]以Rh催化缺电子芳基三氮唑形成卡宾物种后,与烯基上连有吸电子基团的2-烯基吲哚的3位发生C—H插入反应,然后不经分离直接在有机碱作用下发生分子内的氮杂Michael加成反应,最终实现了对三氮唑的交换环合反应,一锅两步制备二氢-β-咔啉和二氢异喹啉。

Scheme 1
以醋酸铑为催化剂,3-乙烯基吲哚与芳基三氮唑为底物,氩气保护下在1,2-二氯乙烷中发生交换环合反应(Scheme 1)。与Anbaransan等[10]的工作不同,最终以中等到较高的产率得到[3+2]环加成产物,生成一类新型的3-(2,3-二氢吡咯)吲哚衍生物(3aa~3al,3ba~3da),其结构经1H NMR,13C NMR和HR-MS(ESI)表征。
1 实验部分
1.1 仪器与试剂
SGW X-4B型熔点仪;Bruker ARX-300/400 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);Agilent 6540 Q-TOF(ESI)型质谱仪。
底物1a~1f,1a′,1a″和1a‴按照文献[11-14]方法制备,2a~2l按照文献[15]方法制备;其余所用试剂均为分析纯。
1.2 合成
(1) 化合物3aa~3al和3ba~3da的合成(以3aa为例)
依次加入1a23.3 mg(0.1 mmol),2a59.9 mg(0.2 mmol)和含有Rh2(OAc)41.1 mg(0.0025 mmol)的1,2-二氯乙烷(2 mL)。体系置换氩气后60 ℃反应6 h(TLC监测)。冷却至室温,过滤,滤饼用乙酸乙酯(3×10 mL)洗涤,合并有机相。减压蒸去溶剂,残余经硅胶柱层析[洗脱剂:V(乙酸乙酯)/V(石油醚)=1/30]纯化得黄色固体3aa41 mg,收率81%, m.p.112~113 ℃;1H NMR(300 MHz, CDCl3)δ: 7.47(d,J=8.0 Hz, 2H), 7.40(d,J=7.9 Hz, 1H), 7.36~7.27(m, 7H), 7.24~7.06(m, 7H), 7.03~6.89(m, 3H), 5.33(dd,J=11.0 Hz, 6.2 Hz, 1H), 5.26(s, 2H), 3.35(ddd,J=15.7 Hz, 11.0 Hz, 2.0 Hz, 1H), 3.14(ddd,J=15.8 Hz, 6.2 Hz, 1.5 Hz, 1H), 2.27(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.2, 137.3, 137.1, 134.7, 134.0, 129.2, 128.8, 128.7, 127.8, 127.1, 127.0, 126.9, 125.8, 125.4, 124.7, 122.4, 121.8, 119.7, 119.5, 115.7, 109.9, 57.6, 50.2, 39.4, 21.5; HR-MS(ESI)m/z: Calcd for C32H29N2O2S{[M+H]+}505.1944, found 505.1942。
用类似方法合成3ab~3al和3ba~3da
3ab: 黄色固体,收率54%, m.p.100~101 ℃;1H NMR(400 MHz, CDCl3)δ: 7.51(d,J=8.1 Hz, 2H), 7.43(d,J=7.9 Hz, 1H), 7.38~7.26(m, 5H), 7.24~7.16(m, 5H), 7.15~7.08(m, 3H), 7.02(d,J=8.1 Hz, 2H), 7.00~6.93(m, 1H), 5.35~5.31(m, 1H), 5.28(s, 2H), 3.33(dd,J=13.9 Hz, 11.3 Hz, 1H), 3.13(dd,J=15.8 Hz, 5.8 Hz, 1H), 2.59(t,J=7.6 Hz, 2H), 2.30(s, 3H), 1.66(dd,J=15.0 Hz, 7.5 Hz, 2H), 0.97(t,J=6.0 Hz, 3H);13C NMR(75 MHz, CDCl3)δ: 143.2, 141.7, 137.3, 137.1, 134.6, 131.3, 129.2, 128.8, 128.75, 127.72, 127.1, 127.0, 125.8, 124.6, 122.7, 121.8, 119.7, 119.5, 115.9, 109.9, 57.6, 50.1, 39.5, 37.8, 24.6, 21.5, 13.9; HR-MS(ESI)m/z: Calcd for C35H35N2O2S{[M+H]+}547.2414, found 547.2415。
3ac: 黄色固体,收率59%, m.p. 90~91 ℃;1H NMR(400 MHz, CDCl3)δ: 7.56(dd,J=8.1 Hz, 2.0 Hz, 2H), 7.48(dd,J=7.7 Hz, 3.2 Hz, 1H), 7.44~7.39(m, 2H), 7.38~7.30(m, 5H), 7.28~7.20(m, 4H), 7.16(s, 2H), 7.08~6.98(m, 3H), 5.40~5.32(m, 1H), 5.30(s, 2H), 3.37(m, 1H), 3.23~3.12(m, 1H), 2.33(s, 3H), 1.38(s, 9H);13C NMR(75 MHz, CDCl3)δ: 150.2, 143.2, 137.3, 137.1, 134.6, 131.1, 129.2, 128.8, 127.7, 127.2, 127.04, 127.01, 125.8, 125.6, 124.8, 124.5, 122.6, 121.9, 119.8, 119.5, 115.9, 109.9, 57.6, 50.2, 39.5, 34.6, 31.3, 21.5; HR-MS(ESI)m/z: Calcd for C36H37N2O2S {[M+H]+}561.2570, found 561.2568。
3ad: 黄色固体,收率42%, m.p.106~108 ℃;1H NMR(400 MHz, CDCl3)δ: 7.49(d,J=8.1 Hz, 2H), 7.41(d,J=7.9 Hz, 1H), 7.33~7.27(m, 2H), 7.26~7.19(m, 4H), 7.19(m, 3H), 7.09~7.12(t,J=7.6 Hz, 1H), 7.02~6.90(m, 4H), 6.83(d,J=8.6 Hz, 2H), 5.27(dd,J=10.9 Hz, 5.9 Hz, 1H), 5.22(s, 2H), 4.09~3.91(m, 2H), 3.26(dd,J=14.7 Hz, 12.0 Hz, 1H), 3.06(dd,J=15.7 Hz, 5.8 Hz, 1H), 2.26(s, 3H), 1.39(t,J=7.0 Hz, 3H);13C NMR(75 MHz, CDCl3)δ: 158.2, 143.2, 137.4, 137.1, 134.6, 129.2, 128.8, 127.7, 127.2, 127.1, 127.0, 126.4, 126.0, 125.8, 123.5, 122.7, 121.9, 119.7, 119.5, 116.0, 114.7, 110.0, 63.6, 57.5, 50.2, 39.6, 21.5, 14.9; HR-MS(ESI)m/z: Calcd for C34H33N2O2S{[M+H]+}549.2206, found 549.2207。
3ae: 黄色固体,收率76%, m.p.117~118 ℃;1H NMR(400 MHz, CDCl3)δ: 7.49(d,J=8.1 Hz, 2H), 7.42~7.30(m, 6H), 7.28(s, 2H), 7.25~7.12(m, 6H), 6.99(d,J=8.1 Hz, 3H), 5.41(dd,J=11.1 Hz, 6.2 Hz, 1H), 5.28(s, 2H), 3.44~3.29(m, 1H), 3.15(dd,J=15.7 Hz, 6.1 Hz, 1H), 2.30(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.3, 137.3, 137.1, 134.8, 132.5, 132.4, 129.2, 128.9, 128.8, 127.8, 127.2, 127.07, 127.05, 126.1, 125.9, 125.7, 121.9, 121.0, 119.7, 119.6, 115.4, 110.0, 57.8, 50.2, 39.4, 21.5; HR-MS(ESI)m/z: Calcd for C32H28N2O2SCl{[M+H]+}539.1555, found 539.1557。
3af: 黄色固体,收率69%, m.p.124~125 ℃;1H NMR(300 MHz, CDCl3)δ: 7.46~7.39(m, 3H), 7.34~7.24(m, 7H), 7.23~7.18(m, 2H), 7.15~7.08(m, 4H), 7.00(d,J=8.7 Hz, 1H), 6.95(d,J=8.0 Hz, 2H), 5.26(dd,J=11.0 Hz, 6.6 Hz, 1H), 5.18(s, 2H), 3.30(ddd,J=15.7 Hz, 11.0 Hz, 2.0 Hz, 1H), 3.01(ddd,J=15.8 Hz, 6.7 Hz, 1.6 Hz, 1H), 2.24(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.4, 136.8, 135.7, 134.7, 133.8, 129.3, 129.0, 128.7, 128.4, 128.0, 127.5, 127.1, 127.0, 125.5, 124.74, 124.69, 122.3, 122.2, 115.2, 113.0, 111.5, 57.5, 50.4, 39.7, 21.5; HR-MS(ESI)m/z: Calcd for C32H28N2O2SBr{[M+H]+}583.1049, found 583.1050。
3ag: 棕色粘稠液体,收率86%;1H NMR(300 MHz, CDCl3)δ: 7.43(d,J=8.3 Hz, 2H), 7.37~7.30(m, 2H), 7.29~7.27(m, 2H), 7.25~7.22(m, 3H), 7.21~7.05(m, 7H), 6.96~6.88(m, 3H), 5.35(dd,J=11.1 Hz, 6.2 Hz, 1H), 5.22(s, 2H), 3.37~3.25(m, 1H), 3.14~3.05(m, 1H), 2.24(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.3, 137.6, 137.2, 137.1, 134.9, 129.1, 128.9, 128.6, 128.2, 127.8, 127.75, 127.3, 127.1, 126.9, 125.7, 125.6, 124.6, 121.9, 120.2, 119.6, 115.0, 110.0, 57.9, 50.2, 39.2, 21.4; HR-MS(ESI)m/z: Calcd for C33H28N2O2SF3{[M+H]+}573.1818, found 573.1821。
3ah: 黄色固体,收率83%, m.p.112~114 ℃;1H NMR(300 MHz, CDCl3)δ: 7.62~7.53(m, 2H), 7.44~7.28(m, 8H), 7.27~7.21(m, 2H), 7.20~7.15(m, 3H), 7.11~7.04(m, 1H), 6.92~6.78(m, 3H), 5.44(dd,J=11.3 Hz, 6.6 Hz, 1H), 5.24(s, 2H), 3.40(ddd,J=15.6 Hz, 11.3 Hz, 1.8 Hz, 1H), 3.16(ddd,J=15.7 Hz, 6.6 Hz, 1.5 Hz, 1H), 2.21(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.3, 138.8, 137.08, 137.1, 134.9, 132.9, 132.4, 130.6, 129.0, 128.9, 127.9, 127.4, 127.1, 126.8, 126.5, 125.6, 124.7, 122.0, 119.6, 119.4, 114.6, 110.0, 109.5, 58.0, 50.2, 39.0, 21.4; HR-MS(ESI)m/z: Calcd for C33H28N3O2S{[M+H]+}530.1897, found 530.1899。
3ai: 黄色固体,收率77%, m.p.125~126 ℃;1H NMR(300 MHz, CDCl3)δ: 7.45~7.37(m, 3H), 7.35~7.24(m, 5H), 7.23~7.12(m, 7H), 7.11~7.03(m, 1H), 6.98~6.85(m, 3H), 5.34(dd,J=11.1 Hz, 6.3 Hz, 1H), 5.20(s, 2H), 3.29(ddd,J=15.7 Hz, 11.1 Hz, 2.0 Hz, 1H), 3.07(ddd,J=15.8 Hz, 6.3 Hz, 1.5 Hz, 1H), 2.21(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.3, 137.3, 137.1, 136.3, 134.8, 130.2, 129.6, 129.2, 128.9, 127.8, 127.5, 127.3, 127.1, 127.0, 126.8, 125.7, 123.1, 122.9, 122.0, 120.5, 119.7, 119.6, 115.3, 110.0, 57.8, 50.2, 39.3, 21.5; HR-MS(ESI)m/z: Calcd for C32H28N2O2SBr{[M+H]+}583.1049, found 583.1050。
3aj: 黄色固体,收率56%, m.p.101~102 ℃;1H NMR(400 MHz, CDCl3)δ: 7.47(d,J=8.1 Hz, 2H), 7.39(d,J=7.9 Hz, 1H), 7.36~7.25(m, 3H), 7.22~7.14(m, 5H), 7.13~7.06(m, 4H), 7.03(d,J=7.4 Hz, 1H), 7.00~6.91(m, 3H), 5.31(dd,J=11.0 Hz, 6.0 Hz, 1H), 5.24(s, 2H), 3.32(dd,J=14.7 Hz, 12.1 Hz, 1H), 3.11(dd,J=15.8 Hz, 6.0 Hz, 1H), 2.33(s, 3H), 2.26(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.2, 138.2, 137.3, 137.1, 134.7, 133.9, 129.2, 128.8, 128.6, 127.8, 127.7, 127.11, 127.08, 127.0, 125.8, 125.4, 125.3, 122.6, 121.9, 121.8, 119.7, 119.5, 115.8, 110.0, 57.6, 50.2, 39.5, 21.5, 21.4; HR-MS(ESI)m/z: Calcd for C33H31N2O2S{[M+H]+}519.2101, found 519.2102。
3ak: 黄色固体,收率51%, m.p.117~118 ℃;1H NMR(300 MHz, CDCl3)δ: 7.47(d,J=8.3 Hz, 2H), 7.38(d,J=7.9 Hz, 1H), 7.32~7.29(m, 1H), 7.29~7.27(m, 1H), 7.22(s, 1H), 7.19(s, 1H), 7.17~7.08(m, 4H), 7.00~6.91(m, 4H), 6.85(d,J=1.5 Hz, 1H), 6.76~6.64(m, 2H), 5.94(s, 2H), 5.28(dd,J=11.0 Hz, 6.1 Hz, 1H), 5.23(s, 2H), 3.25(ddd,J=15.6 Hz, 11.0 Hz, 2.0 Hz, 1H), 3.13~2.94(ddd, J=15.7 Hz, 6.1 Hz, 1.4 Hz, 1H), 2.26(s, 3H);13C NMR(75 MHz, CDCl3)δ: 148.0, 146.8, 143.2, 137.3, 137.1, 134.6, 129.2, 128.8, 128.2, 127.8, 127.14, 127.09, 127.02, 125.8, 124.2, 122.6, 121.9, 119.7, 119.5, 118.4, 115.8, 110.0, 108.4, 105.1, 101.2, 57.6, 50.2, 39.7, 21.5; HR-MS(ESI)m/z: Calcd for C33H29N2O4S {[M+H]+}549.1843, found 549.1845。
3al: 黄色固体,收率65%, m.p.104 ~105 ℃;1H NMR(300 MHz, CDCl3)δ: 7.47(d,J=8.3 Hz, 2H), 7.39(d,J=7.9 Hz, 1H), 7.32~7.25(m, 3H), 7.25~7.19(m, 2H), 7.17(d,J=7.3 Hz, 3H), 7.14~7.04(m, 2H), 7.00~6.91(m, 4H), 6.86(dd,J=2.7 Hz, 1.0 Hz, 1H), 5.27(dd,J=11.0 Hz, 6.2 Hz, 1H), 5.22(s, 2H), 3.28(ddd,J=15.6 Hz, 11.0 Hz, 2.0 Hz, 1H), 3.06(ddd,J=15.7 Hz, 6.2 Hz, 1.4 Hz, 1H), 2.26(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.3, 137.3, 137.1, 135.6, 134.7, 129.3, 128.9, 127.7, 127.2, 127.1, 127.0, 126.4, 125.8, 125.1, 124.9, 121.9, 119.7, 119.5, 119.3, 118.9, 115.7, 110.0, 57.5, 50.2, 40.0, 21.5; HR-MS(ESI)m/z: Calcd for C30H27N2O2S2{[M+H]+}511.1508, found 511.1507。

表1 合成条件的优化
3ba: 黄色固体,收率40%, m.p.106~107 ℃;1H NMR(300 MHz, CDCl3)δ: 7.44(d,J=8.3 Hz, 2H), 7.36~7.27(m, 7H), 7.25~7.20(m, 1H), 7.19(s, 2H), 7.17~7.13(m, 2H), 7.05(d,J=8.8 Hz, 1H), 6.93(d,J=8.0 Hz, 2H), 6.79(d,J=2.3 Hz, 1H), 6.73(dd,J=8.9 Hz, 2.4 Hz, 1H), 5.36(dd,J=11.0 Hz, 5.6 Hz, 1H), 5.21(s, 2H), 3.58(s, 3H), 3.43~3.29(m, 1H), 3.18~3.06(m, 1H), 2.26(s, 3H);13C NMR(75 MHz, CDCl3)δ: 153.8, 143.1, 137.3, 135.1, 133.9, 132.3, 129.1, 128.8, 128.7, 127.82, 127.76, 127.99, 126.96, 126.1, 125.4, 124.6, 122.4, 115.0, 111.9, 110.7, 101.7, 57.8, 55.5, 50.4, 39.1, 21.4; HR-MS(ESI)m/z: Calcd for C33H31N2O2S{[M+H]+}535.2050, found 535.2051。
3ca: 黄色固体,收率56%, m.p.98~100 ℃;1H NMR(300 MHz, CDCl3)δ: 7.45(d,J=8.3 Hz, 2H), 7.34~7.25(m, 7H), 7.25~7.19(m, 2H), 7.18~7.08(m, 4H), 6.96(d,J=7.8 Hz, 3H), 6.75(dt,J=13.5 Hz, 6.8 Hz, 1H), 5.29(dd,J=11.0 Hz, 6.2 Hz, 1H), 5.20(s, 2H), 3.31(ddd,J=15.7 Hz, 11.0 Hz, 2.0 Hz, 1H), 3.11(ddd,J=15.8 Hz, 6.2 Hz, 1.5 Hz, 1H), 2.37(s, 3H), 2.26(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.2, 137.6, 137.5, 134.8, 134.0, 131.8, 129.2, 128.8, 128.7,127.7, 127.1, 127.0, 126.9, 126.5, 125.5, 124.7, 123.6, 122.3, 121.3, 119.4, 115.6, 109.8, 57.7, 49.9, 39.4, 21.9, 21.5; HR-MS(ESI)m/z: Calcd for C33H31N2O2S{[M+H]+}519.2101, found 519.2102。
Scheme 2
Scheme 3
3da: 黄色固体,收率74%, m.p. 121~122 ℃;1H NMR(300 MHz, CDCl3)δ: 7.40(d,J=8.3 Hz, 2H), 7.38~7.28(m, 7H), 7.26~7.24(m, 1H), 7.24~7.20(m, 1H), 7.19~7.14(m, 4H), 7.12(t,J=1.7 Hz, 1H), 6.93(d,J=8.0 Hz, 2H), 6.87(dd,J=8.5 Hz, 1.8 Hz, 1H), 5.30(dd,J=11.1 Hz, 6.2 Hz, 1H), 5.20(s, 2H), 3.35(ddd,J=15.8 Hz, 11.1 Hz, 2.0 Hz, 1H), 3.07(ddd,J=15.8 Hz, 6.2 Hz, 1.6 Hz, 1H), 2.27(s, 3H);13C NMR(75 MHz, CDCl3)δ: 143.3, 137.5, 136.6, 134.8, 133.8, 129.1, 129.0, 128.7, 128.03, 128.01, 127.9, 127.0, 126.95, 125.4, 124.6, 124.4, 122.0, 120.7, 120.2, 115.8, 109.8, 57.4, 50.2, 39.4, 21.4; HR-MS(ESI)m/z: Calcd for C32H28N2O2ClS{[M+H]+}539.1555, found 539.1557。
2 结果与讨论
2.1 化合物3aa的反应条件优化
以1a和2a反应为例,对反应条件进行了优化,结果见表1。在80 ℃条件下,以Rh2(OAc)4为催化剂,DCE作为反应溶剂,当量比为1/1.2,在氩气氛围下反应6 h。催化剂种类对产率的影响(Entry 1~6),可见Rh2(OAc)4为催化剂时,产率最优,相应的产物3aa的产率可达75%。3-乙烯基吲哚的N上不同保护基对产率的影响(Entry 7~9),保护基为苄基时产率较高,当保护基为Boc, Ts和2-pym时,仅能得到痕量的对应产物。反应温度对产率的影响(Entry10~11),当温度降低至60 ℃时,结果产率提升至77%,升温至100 ℃时,产率略有下降,可见在60 ℃下,反应产率最高(Entry 10)。溶剂种类对产率的影响(Entry 12~18),当溶剂为甲苯时,产率可达71%(Entry 13),其余的溶剂产率均不高甚至仅得到痕量的产率。筛选了1a和2a的当量比对反应产率的影响(Entry 19~21),当1a和2a的当量比升高至1/2时产率可达81%(Entry 20),若其当量比增加至1/2.5,产率有所下降(Entry 21),因此选择1a和2a的当量比为1/2作为最佳当量比。该反应在空气条件下的情况(Entry 21)。若在空气的氛围下反应,则仅能得到痕量产物。因此最终确定了模板反应的最佳反应条件为:氩气保护下,Rh2(OAc)4为催化剂,无水DCE为溶剂,60 ℃反应6 h,1a和2a的当量比为1/2。
2.2 底物拓展
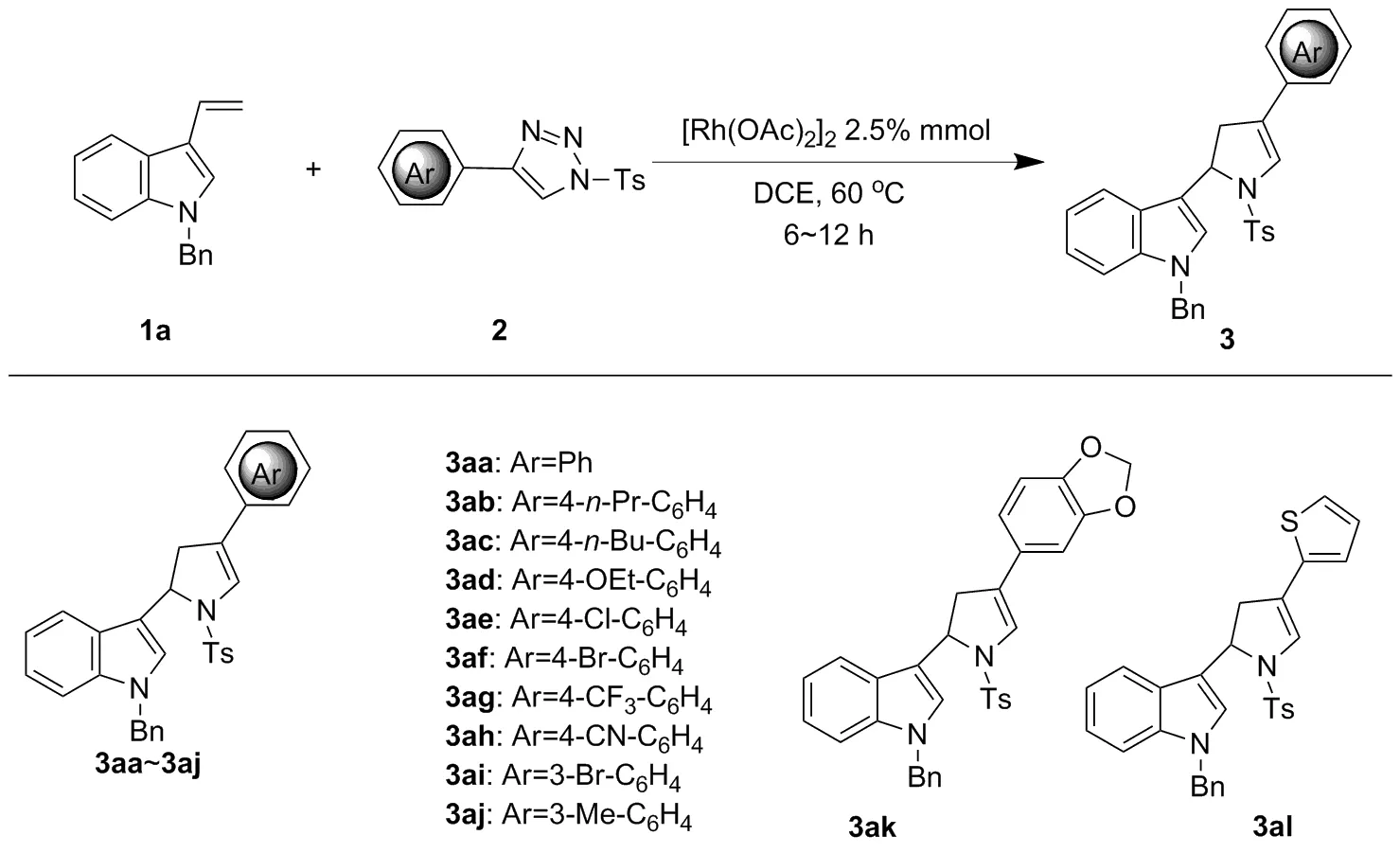
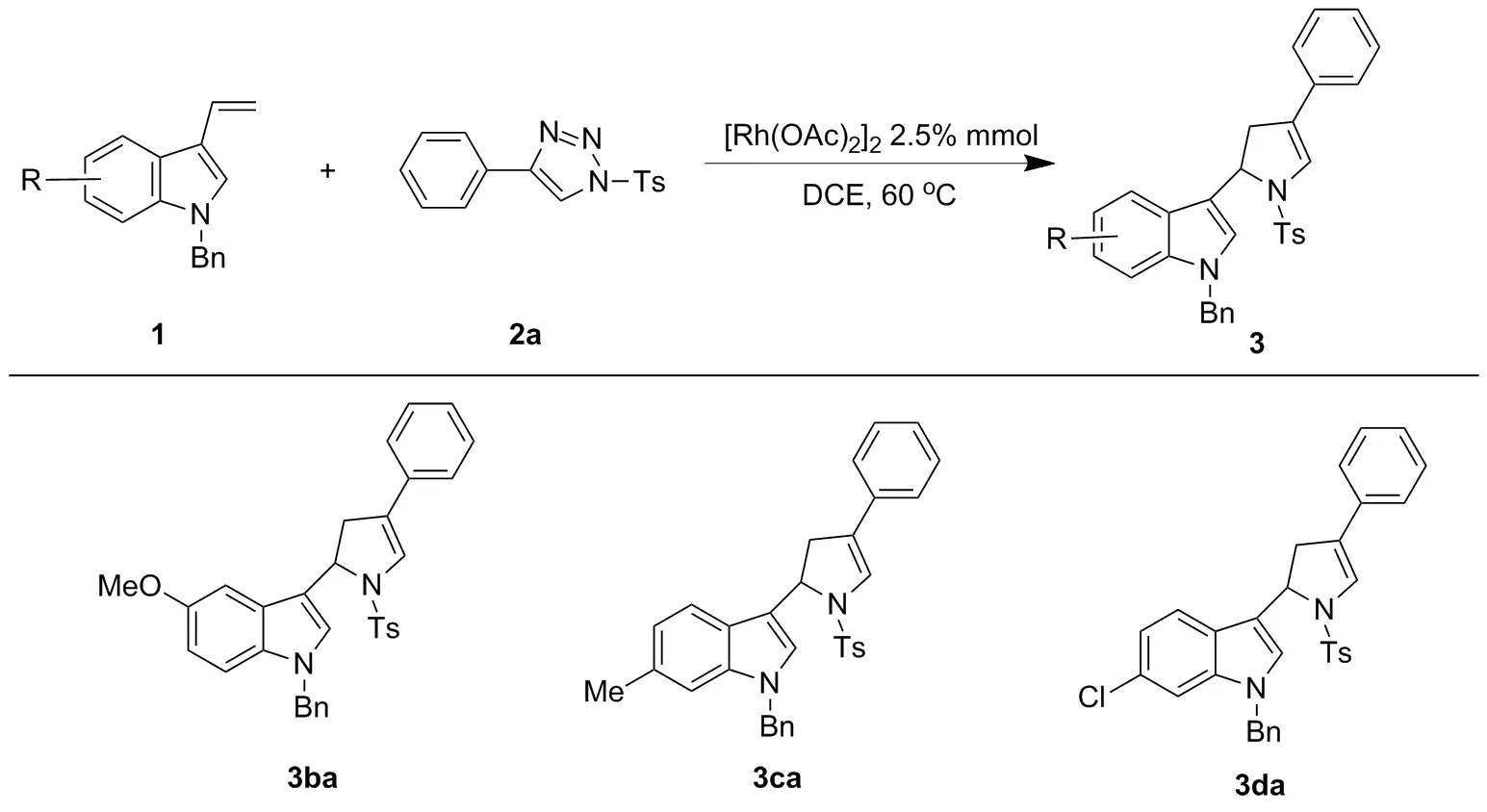
在最佳条件下,进行三氮唑底物(Scheme 2)和3-乙烯基吲哚底物(Scheme 3)的拓展。如Scheme 2中所示,当芳基三氮唑的苯环上的3或4位取代基为氯、溴、三氟甲基、氰基等吸电子的取代基时,得到相应的产物(3ae~3ai),产率较高,达69%~86%;而当芳基三氮唑苯环上的3或4位的取代基为给甲氧基,烷基等给电子基团时(3ab~3ad,3aj),产率中等,为42%~59%。而如Scheme 3中所示,当3-乙烯基吲哚上的6号位为氯这种吸电子基团时(3da),产率较高,达74%;而当乙烯基吲哚的5-位或6-位换为甲氧基或甲基这类给电子的取代基时(3ba和3ca),产率中等,分别为40%和56%。所以推测吸电子基团的存在可以使反应产率提高。而当以7号位有甲基或者氟取代基的3-乙烯基吲哚为底物(2e和2f)时,未能与底物2a反应得到相应的产物3ea和3fa,推测可能是由于位阻大,不利于反应的进行。
报道了一种以3-乙烯吲哚衍生物和芳基三氮唑为底物通过铑催化一步反应合成3-(2,3-二氢吡咯)吲哚衍生物的方法,该反应合成条件温和,底物适用性较广,丰富了吲哚类生物碱化合物。
