链长和阳离子对胆碱脂肪酸皂的细胞毒性和生物降解力的影响
2020-11-25程书钘
表面活性剂的Krafft点是其应用的关键因素之一,因为其限定了表面活性剂的使用温度。只有当温度高于krafft温度时,胶束才开始形成,溶解度才会大幅度提高,因此表面活性剂才可以发挥其功能。与降低离子液体的熔点(熔点<100℃的盐)类似,可以通过阻碍固态分子规则的晶体堆积来降低表面活性剂的Krafft点。因此,与钠和钾的同系物相比,在简单的脂肪酸皂中使用大体积的胆碱阳离子(如图1所示)作为抗衡离子,对增加相应表面活性剂的水溶性非常有效。例如,在环境温度下,胆碱脂肪酸皂(ChCm)的链长达到m=16时依然是可溶解的,而棕榈酸钠(NaC16)在60℃以下几乎不溶。

图1 胆碱阳离子的结构
胆碱((2-羟乙基)三甲基铵)大量存在于植物、动物和人体组织中,并且具有良好的生化特性。此外,它还是神经传递质乙酰胆碱以及生物膜主要成分磷脂的前体,其衍生物甜菜碱可作为甲基供体,这对蛋白质合成和甲基转移反应很重要。早期研究表明,胆碱在环境中可被某些微生物分解。它们还是在哺乳动物的初级代谢中大量存在的成分组成,因此,胆碱脂肪酸皂也应该是对环境和生理无害的。另外,由于它们的低Krafft点,胆碱脂肪酸皂的合成可以在环境温度下进行,无须额外提供能量。如今,胆碱盐(例如氯化物)是低成本的化学品,每年产量可达数百万吨。因此,胆碱脂肪酸皂不仅具有生物相容性,而且还具有经济优势。
近年来,胆碱在绿色离子液体领域引起了人们极大的兴趣。已评测了胆碱磷酸根离子液体对J774鼠巨噬细胞系的细胞毒性,显示毒性基本上取决于所用的阴离子。Petkovic等实验表明,中短链脂肪酸胆碱盐(从乙酸到癸酸,m=2~10))也是离子液体。此外,他们分别使用丝状真菌和青霉菌作为生物模型对这些化合物的毒性和生物降解性进行了评估,发现这些胆碱离子液体的毒性甚至比钠离子液体低。胆碱盐作为有应用前途的绿色化学品,在过去几年中的多项专利声明中得到了明显体现。但是,欧洲化妆品管理规范76/768/EEC(Anex II/168)仍然禁止在化妆品中使用胆碱盐。这主要是因为胆碱属于季铵化合物(QAC),而季铵化合物通常具有内在的刺激潜力。
为了检验对胆碱脂肪酸皂具有高生物相容性的先验假设是否有效,笔者研究了链长为m=12~18的ChCm盐的生物降解能力,并使用两种不同的人类细胞系子宫颈癌细胞(HeLa)和角质形成细胞(SK-Mel-28)进行了体外细胞毒性分析。这项工作的主要目的是为了证明胆碱羧酸盐表面活性剂对环境和最终用户无害,为其在日常生活产品中的使用提供支持。
根据文献,表面活性剂对HeLa测试通常显示出较高的重现性,并且与体内实验具有良好的相关性。因此,它们被公认为是以兔子为研究对象进行眼刺激实验(Draize实验)的合理替代方法。选择角化细胞系来检查皮肤刺激能力。我们研究了烷基链长为m=8~16的胆碱脂肪酸盐对这两种细胞系的细胞毒性的影响。为了更好地与以前的研究进行比较,我们通过在相同实验条件下测量脂肪酸钠和脂肪酸钾对这两种细胞系的IC50值。此外,为了阐明毒性的潜在机理,即表面活性剂是否仅对细胞外膜具有非特异性破坏,或者表面活性剂是否可以渗透到细胞内更具体地影响细胞功能,我们使用芘取代月桂酸钠和月桂酸胆碱盐进行了细胞荧光显微镜分析。
值得一提的是,以前的研究主要集中在偶数脂肪酸皂的细胞毒性上,因为它们在哺乳动物细胞的天然脂肪酸储库中含量最高。在本研究中,根据结构-活性关系(SAR)对奇数碳同系物进行了评估,以研究这些化合物是否显示出轮廓作用或遵循假定的细胞毒性随着疏水链长度的增加而增加的总体趋势。
1 实验
1.1 试剂和样品准备
按文献的方法,合成胆碱月桂酸盐(ChC12),胆碱肉豆蔻酸盐(C h C 1 4),胆碱棕榈酸盐(ChC16)和胆碱硬脂酸盐(ChC18),并通过两次重结晶纯化。辛酸钠(≥99%),癸酸钠(≥98%)和十二烷酸钠(99%~100%)购自Sigma-Aldrich,并按原样使用。辛酸(≥99%,Sigma),壬酸(≥97%,Sigma-Aldrich),癸酸(99%,Alfa Aesar),十一酸(99%,Aldrich),月桂酸(≥ 99%,Merck),十三烷酸(≥98%,Sigma)和十五烷酸(99%,Aldrich)。氢氧化钠和氢氧化钾用作滴定溶液(0.1 N和1 N(Merck))。从Taminco公司获得氢氧化胆碱,质量分数为46%的水溶液。为了防止胆碱的分解,将储备溶液放在-18℃的氮气下避光保存。胆碱的准确浓度通过用0.1 mol/L HCl(Merck)滴定3次来确定。所得到的肥皂以水溶液的形式存在,对于C11和更长的链长为1质量分数,对于C10为2质量分数,对于C8和C9均为5质量分数。为了更好地进行比较并统一表示,图3仅显示了通过直接中和制备的表面活性剂的数据。
对于荧光显微镜,按原样使用1-吡咯十二烷酸(≥98%,Sigma),然后用胆碱或氢氧化钠中和,分别得到1-吡咯十二烷胆碱(ChPC12)和1-吡咯十二烷酸钠(NaPC12)。在60~80℃时,取代的胆碱和月桂酸钠不溶。因此,将它们与相应的未官能化的脂肪酸皂以1∶2的摩尔比混合,从而在环境温度下得到澄清的溶液。
1.2 生物降解力
按照OCDE 301F规范研究了m=2~18(偶数)ChCm盐的生物降解性,这需要确定生物(BOC)和理论(TOC)耗氧量。乙酸钠用作参考,使用已知的分子结构,可以根据等式(1)计算TOC值(以每毫克产品中的氧气毫克数计),它反映了化合物完全氧化所需的氧气量。

BOC值是通过IBUK呼吸计确定的,呼吸计可检测降解过程中的氧气消耗量。在含有多种盐(磷酸钠和磷酸钾;氯化铵,氯化钙和氯化铁;硫酸镁)以及从当地废水处理厂收集的细菌培养基中,于20℃下进行了28 d的实验。最后,按照以下方程式计算生物降解性值:

为了检查肥皂对细菌可能产生的有害影响,研究了每种化合物的各种浓度。以下3个参数作为实验可靠性的标准:
(1)醋酸钠的降解必须在14 d后达到60%以上的水平。在我们的实验中,这一比例为96.4%;
(2)矿物介质必须在28 d之内显示低于60 mg/L的耗氧量。在我们的实验中,只有6 mg/L;
(3)28 d后,pH必须介于6和8.5之间,我们的每个测定都是如此。
1.3 细胞毒性实验
通过MTT(3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四唑鎓)测定表面活性剂的细胞毒性,所用细胞为HeLa(子宫颈癌细胞,ATCC CCL17)和SK-Mel-28(角质形成细胞,CLS 300337)。在这两种情况下,使用由Mosmann引入并由Vlachy等修改的MTT分析程序。简而言之,将细胞以每孔2.5×103个细胞的密度接种在96孔板中,并与不同浓度的待测化合物一起培养,未处理的细胞用作阴性对照。与测试化合物在37℃下培养68 h后,将15 mL MTT溶液(5 mg/mL)添加到每个孔中。随后培养4 h后,移去培养基,加入150 mL10%的SDS溶液,并将溶液过夜。然后,用酶标仪在560 nm下测量光密度。
根据浓度-响应曲线计算出每种物质的IC50值(以mmol/mL为单位),该曲线是根据8种不同浓度生成的(有关详细信息,请参见ESI)。IC50值与未处理的对照,被测化合物培养72 h后MTT降低50%的浓度。为获得更好的可比性,同一天(一式3份)测定所有物质的IC50值。在数周内重复进行3至5次实验(n=4~6),并记录平均IC50值及其标准偏差(SD)。观察到的最大(绝对)标准偏差约为15%。
通过单向方差分析和Posthoc Scheffe程序确定细胞毒性与测定的IC50值之间的统计差异和一致性。
1.4 荧光显微法
将HeLa细胞以每培养皿1×104个细胞的密度接种在m盘(35 mm,Ibidi GmbH)中,并培养过夜。对于显微镜分析,使用无酚的培养基。使用来自Zeiss(Hallbergmoos,德国)的CellObserver系统进行成像,该系统包括计算机控制的倒置荧光显微镜(AxioObserver),具有AxioVision 4.7软件和AxioCam HRm CCDCamera的全分辨率。 使用63×LCI Plan-Neouar物镜和一组适合荧光的滤光片(HC 340/26,Q380 LP,HQ 420/40)采集图像。
为了监测所研究的肥皂的细胞摄取,将荧光ChPC12和ChC12或NaPC12和NaC12的混合物(均以1:2的摩尔比)添加到培养基中。对于ChPC12/ChC12使用的浓度和IC50值分别为81mmol/L和(115±2) μmol/L,对于NaC12/NaPC12使用的浓度和IC50值分别为102 μmol/L和(154±2) μmol/L。加入表面活性剂后立即拍摄相衬和荧光图像,随后在长达1 h的时间内每10 min从同一皿中随机选择细胞进行拍摄。我们注意到,在培养基中的背景荧光可以忽略不计。
2 结果讨论
2.1 生物降解力
表面活性剂的生物降解性是很重要的性能,这说明了它们在环境中持续存在的能力。 根据REACH(化学品注册、评估和授权)法规,所有新化学品都必须通过最终的生物降解测试才能进入市场,因此,我们用乙酸钠确定了从月桂酸到硬脂酸的胆碱脂肪酸皂的生物降解能力。
通常,就OCDE标准而言,如果在十天内有机物从60%的水平被分解到10%,并且如果28 d后总体上至少分解了60%的有机物,则该有机物是可生物降解的。根据欧洲标准CE2004/648,如果表面活性剂在28 d后有60%被降解(即没有10 d的窗口标准),则表面活性剂可以归类为可生物降解的。图2显示了m=12~18(偶数)的ChCm皂的生物降解曲线随时间的变化。显然,所研究的化合物都在10 d之内达到了后者的标准。此外,无论碳链长短,胆碱脂肪酸皂的生物降解均立即开始,这表明胆碱衍生物的潜在毒性对生物没有抑制作用。

图2 降解时间对月桂酸胆碱(□)、肉豆蔻酸酯(○)、棕榈酸酯(△)和硬脂酸酯(◇)生物降解度的影响,以乙酸钠(○)为标准
在OCDE指南中,建议以100 mg/L的浓度测试产品。如有必要,此后可以降低测试浓度。我们的结果为在50 mg/L和90 mg/L下进行测试的平均值。每种化合物在两种浓度下测试结果的差异非常小(小于5%)。这证实了所研究的胆碱脂肪酸皂的毒性低。关于链长的影响,我们观察到28 d后生物降解性的最终水平还在变化,范围从ChC12的约100%到ChC16的超过85%再到ChC14和ChC18的约80%。然而,由于C14同系物打破了总体趋势,因此无法建立生物降解性和疏水性之间的简单关系。这种现象可能与性能参数(例如Krafft点)或明显的聚集行为有关。实际上,在所研究的胆碱脂肪酸皂中,ChC18是唯一Krafft点高于20℃的化合物。无论如何,当比较ChC12(82%)和NaC12(58%)5 d后的生物降解水平时,胆碱盐的生物降解性明显超过了其对应的钠盐。
在有氧和厌氧的条件下,经典肥皂已被广泛研究,并被称为易于生物降解,但它们容易受到水硬度的影响,因为形成的水溶性钙盐和镁盐很难降解。相对于碱性同系物而言,胆碱脂肪酸皂对二价阳离子的存在也非常敏感,因此可能也会表现出类似的行为。此外,胆碱离子本身不会对环境产生任何有害影响,因为它可以被微生物分解,在土壤中无法积累。
因此,所研究的胆碱脂肪酸皂都可以认为是易于生物降解的,因为它们一方面都通过了10 d的窗口标准,另一方面又在13 d内降解了70%。这一发现与其他胆碱盐(如中短链烷酸衍生物)的早期研究相吻合。
2.2 细胞毒性
表面活性剂良好的水溶性是进行体外细胞毒性实验的必要条件。已知表面活性剂的Krafft温度会随着烷基链长的增加而升高,对于本研究中的胆碱脂肪酸皂,Krafft温度会随着阳离子的尺寸增加而降低。因此,在我们的研究中,烷基链的最大长度限制为钠皂的m=12,钾皂的m=13,胆碱皂的m=16。细胞培养72 h后,胆碱脂肪酸皂、脂肪酸钠和脂肪酸钾对HeLa和SK-Mel-28细胞系的细胞毒性如图3所示(以IC50值表示)。
对于这两种细胞系,在毫摩尔范围内,ChCm表面活性剂的细胞毒性与钠、钾同系物的细胞毒性基本相当(除了m=15和m=16)。表明胆碱脂肪酸皂在所选条件下具有低细胞毒性。
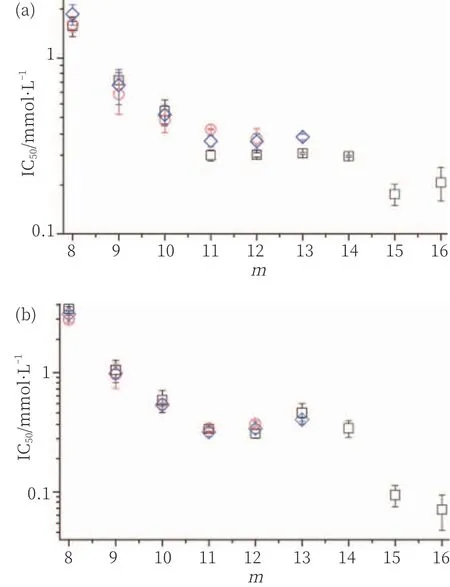
图3 (a)HeLa和(b)SK-Mel-28细胞培养72 h后获得的羧酸盐的IC50值与烷基链长m的关系
对具有羧酸根基团和各种抗衡离子(包括碱金属和季铵离子)的阴离子表面活性剂的细胞毒性测试指出,阳离子越大,毒性越低。这种趋势可以用离子对的形成来解释:可极化的较大离子比较小的碱金属离子更易与羧酸头基结合,且离子对的形成可以降低咪唑鎓盐和吡啶鎓盐离子液体的毒性。Petkovic等检测到胆碱离子液体的毒性比钠离子液体略低,也是相同的原因。与先前的研究相比,我们无法在实验中验证阳离子特异性。这可能是因为所用的细胞培养基含有多种盐(例如NaCl或CaCl2),不会出现明显的离子效应。但是,我们的结果对阳离子的非特异性是合理的,因为至少在相关的浓度范围内,钠、钾和胆碱均未表现出内在的毒性作用。因此,胆碱脂肪酸皂的毒性主要源自阴离子。
根据SAR概念,预期细胞毒性与疏水性呈线性关系。这种趋势在许多离子液体中都可以观察到,尤其是链长为m=10~12时。疏水性通常由辛醇-水系数(P)表示,对于表面活性剂可以用临界胶束浓度(CMC)表示。由于表面活性剂的CMC随着烷基链长度的增加而线性降低,因此IC50值与m的关系图上应该显示出基本相同的变化。然而,对m=8~16的奇数碳和偶数碳脂肪酸胆碱盐的细胞毒性的详细评估表明,对于两种细胞系,文献报道的线性趋势在研究的整个链长范围内均无效(参见图3)。使用方差分析程序进行的数据分析表明,对于m=11~14所获得的值之间在统计学上没有显著差异。因此,我们观察到m=11到m=14之间的趋势是平稳的,而不是线性趋势。反过来,对于m≤11的皂,IC50值可以通过线性关系很好地描述,在胆碱皂和HeLa的情况下细胞的log IC50(mmol/L)=(2.1±0.2)–(0.24±0.02)m(R=0.995)。有人可能会说,奇数碳脂肪酸皂偏离了线性趋势,但它们在脂肪酸的生物合成中并不常见,因此对生物学功能的重要性不如偶数碳脂肪酸皂。同样,经常报道的奇数碳和偶数碳脂肪酸在物理化学性质上(如熔点或krafft点)的锯齿状行为,也无法使IC50值随烷基链长的变化趋势合理化。
据我们所知,迄今尚未报道具有不同链长的表面活性剂的细胞毒性达到平稳状态。一般而言,早期的肥皂和阴离子表面活性剂研究(不幸的是仅在偶数链上进行)确定了m=12~14时细胞毒性最大,这在文献中通常被称为截止效应,为解释这一现象,提出了几个论点,如水溶性不足(即实际测试浓度偏离标称浓度)或动力学方面(例如,在高分子量化合物的情况下,由于空间效应而减速吸收)。对于表面活性剂在中链长度处发现的最大刺激性和毒性还归因于两个因素:一方面,随着烷基链长度的增加,CMC以及可用单体的极限浓度会降低;而另一方面,油水分配系数和疏水性同时增加。
在本研究中,由于我们只研究了Krafft点为室温或更低温度的表面活性剂,因此基本可以排除水溶性不足的影响。考虑到长链脂肪酸钠在40℃以下基本不溶于水,并且无m=11的研究数据,故许多文献将钠皂在m=12时表现出的最大的毒性归结于有限的水溶性可能也是合理的。相比之下,胆碱肥皂的水溶性增加,使我们能够研究碳链更长的脂肪酸皂的细胞毒性。因此,在对脂肪酸胆碱皂进行细胞毒性检测时,不太可能出现简单的截止效应,反而是经过一个平台后,细胞毒性随着烃链长度的增加而进一步增加。同样,由于所有的测试浓度均低于各自的CMC,IC50值的测定并不受胶束形成的影响。此外,表面活性剂的毒性主要归因于单体而不是聚集体。Roberts等人的定量结构-活性关系(QSAR)研究,表明了化合物是否为表面活性剂与其毒性无关,相反疏水性似乎是影响毒性的主要因素。
通常认为阴离子表面活性剂具有极性麻醉剂的作用。Roberts等建议根据溶质在水和细胞膜之间的分配方式来区分普通和极性麻醉剂的机理。他们提出,诸如酒精之类的普通麻醉剂通过在细胞膜内的三维分配来起作用,这意味着它们能够在双层膜的疏水内核中向各个方向移动。反过来,极性麻醉剂仅能凭借溶质的极性基团与膜表面的磷脂酰胆碱头基的结合进行二维分配。仔细观察胆碱脂肪酸皂的剂量反应曲线,可以发现不同m值的曲线变化存在差异:碳链较短时,细胞活力随着表面活性剂浓度的减少而逐渐增加,碳链较长时它们突然升高。这表明,与m≥12的盐相比,m=11的脂肪酸胆碱皂的作用机理不同。一种可能的情况是,如Roberts等人所述的,较短链的衍生物在3D分区的框架中起一般麻醉品的作用,而它们的较长链同系物被膜更有效地结合,因此可以视为2D分区溶质。需要进一步的实验来支持这一假设,并阐明这些脂肪酸系统中烷基链长度变化时观察到的IC50值不常见的变化趋势。
2.3 通过荧光显微镜监测胆碱和钠皂的细胞摄取和在细胞内的分布
为了大致了解胆碱脂肪酸盐和钠皂的细胞毒性,将HeLa细胞与芘取代的月桂酸钠或月桂酸胆碱及相应的非功能化脂肪酸盐以1:2摩尔比混合培养,其浓度略低于其各自的IC50。随后,通过监测荧光随时间的变化来跟踪肥皂在这种细胞内的行为。显微照片如图4所示。

图4 添加表面活性剂后,将HeLa细胞与ChPC12 / ChC12的混合物(摩尔比为1:2)一起培养的相衬(左)和荧光(右)图像
获得的结果表明,肥皂是细胞膜的非特异性破坏剂。根据芘的荧光,我们观察到表面活性剂实际上能够穿透细胞膜并在细胞内部积聚(参见图4)。在这方面,没有发现胆碱和钠盐之间的明显差异,与它们的IC50值趋势一致。细胞摄取非常迅速:培养10 min后,在整个细胞中都可以看到广泛的荧光,然后荧光强度逐渐增加,直到大约30 min后达到某种饱和度。正如阴离子表面活性剂所预期的那样,在检查期间细胞核不受影响。
最值得注意的是,除了细胞内均匀的荧光外,我们还可以识别细胞内的荧光聚集体,这可能代表了所谓的“细胞质脂滴”(CLD)。CLD由中性脂质核心和周围的磷脂单层组成,几乎在每种哺乳动物细胞中都可以找到。它们由内质网形成,并通过掺入三酰基甘油而生长。在我们的实验中观察到的细胞荧光非常类似于CLD的典型现象。由于已知CLD是多余脂质的沉积物,并且就缓冲细胞培养基的中性pH而言,肥皂可能以质子化脂肪酸的形式被吸收到细胞中并掺入CLD中。此外,很可能会发生CLD中荧光的积累。但是,需要更多数据来了解细胞吸收的分子的确切定位。
3 结论
在这项工作中,我们研究了胆碱脂肪酸盐的生物相容性。胆碱脂肪酸盐是一类新的表面活性剂,以前已经证明其比经典的碱皂类似物具有更大的优势,主要是长链衍生物在环境温度下的溶解度更大,这对于洗涤过程尤为重要。我们的研究表明,根据欧洲规范,对于m=12~18的链长胆碱脂肪酸盐,考虑到其组成分子具有生物起源并存在于许多活生物体中(至少是偶数链长)这些表面活性剂可以认为是易于生物降解的。对人体细胞系的细胞毒性测试还证明,胆碱脂肪酸皂的危害性不大于其对应的钠皂和钾皂,而胆碱脂肪酸皂的确在各种配方具有广泛的应用潜力。因此,这些结果为胆碱表面活性剂在客户产品中的应用提供了实质性支持,这与一直存在的禁令相反。
通过对不同碳链长度的胆碱脂肪酸盐细胞毒性数据的分析发现,m≤11时,随着疏水性的增加,毒性或多或少呈线性增加,但是与许多先前研究的结果不同,这种简单的线性趋势不会在较长的链长时继续下去;当m=11~14时,疏水链长与细胞毒性的关系尚不清楚,只能通过研究奇数碳脂肪酸来解决。这一意想不到的特征在统计上得到了验证,在大量的分析中,被证明是独立于阳离子和细胞系的。实际上,无论使用HeLa还是SK-Mel-28细胞,在胆碱、钠和钾的羧酸盐中测定的IC50值都非常相似,或者在实验误差范围内几乎可以认为是相同的。因此,没有观察到阳离子选择性,并且可以得出结论,毒性主要来自阴离子。一个简单的截止效应不能解释我们实验中追踪到的IC50值的异常变化,因为在m=11~14的平台期之后,细胞毒性随着链长的增加而进一步增加(m=15~16)。我们认为m=11的胆碱脂肪酸盐通过不同于m≥12的同系物的细胞毒性机制起作用。具有较长烷基链的表面活性剂最有可能更有效地结合到膜的双层中。通过荧光显微镜研究HeLa细胞摄取芘取代的胆碱盐和十二烷酸钠盐,可以进一步了解这些化合物在体内的行为。相应的数据表明,表面活性剂不会简单地以非特异性方式破坏细胞外膜,而是以相对较快的速度渗透到细胞内部。
综上所述,我们的研究结果证明了胆碱羧酸盐成为有前途的绿色表面活性剂的潜力。当然,这还需要进行其他研究,例如水生生物毒性的测定,以评估把胆碱作为季铵离子的简单分类是否合理,并证明其目前作为化妆品配方中的成分是合理的。此外,还要评估这些胆碱脂肪酸皂的抗菌潜力。无论如何,目前的工作已经迈出了第一步,但还有重要的一步,促进胆碱脂肪酸皂在实际客户产品中的应用。在不久的将来,这些高效表面活性剂的使用将成为可能。
程书钘译自The Royal Society of Chemistry RSC Adv., 2013, 3。
