基础LH水平过高患者拮抗剂方案中全程使用拮抗剂的效果观察
2020-11-24林海燕李予焦雪丹谢言信陈晓莉王文军张清学
林海燕,李予,焦雪丹,谢言信,陈晓莉,王文军,张清学
(中山大学孙逸仙纪念医院生殖医学中心,广州 510120)
辅助生殖技术(ART)中控制性促排卵方案的发展,主要围绕着促排过程中通过不同机制抑制黄体生成素(LH)而展开。促性腺激素释放激素(GnRH-a)降调节长方案中利用GnRH-a与GnRH受体的强亲和力,达到垂体抑制,去除内源性LH峰的影响;GnRH拮抗剂(GnRH-ant)方案则利用了GnRH-ant与垂体上GnRH受体的竞争性结合,抑制内源性早发LH峰;黄体期促排卵及高孕激素状态下促排卵(PPOS)通过内源性、外源性高孕酮水平抑制LH分泌。因此预防早发LH峰是促排卵成功的一个关键内容。
目前拮抗剂方案使用广泛,成为国际上的主流方案之一。按照添加拮抗剂的时间不同主要分为固定方案和灵活方案。固定方案即在给予促性腺激素(Gn)控制性促排卵后的第5~6天加用GnRH-ant;灵活方案即根据最大卵泡的直径和LH水平加用拮抗剂,一般选择当主导卵泡直径达12~14 mm或LH≥10 U/L时加用拮抗剂[1]。在临床工作中,经常会遇到卵巢高反应的患者,如多囊卵巢综合征(PCOS)患者,这类患者基础LH水平过高,拮抗剂方案在月经第2~4天开始使用Gn时,基础LH水平常常超过10 U/L。既往对于这一部分患者大多使用口服避孕药(OC)预处理1~2个月,降低基础LH后再行促排卵。查阅文献尚没有关于基础LH过高是否需要处理及其对IVF/ICSI结局影响的报道[2-4]。近2年,我中心对这类患者的临床处理做了一些尝试,继续按常规灵活方案添加拮抗剂或者选择Gn启动时同时使用拮抗剂。由于目前暂时没有相似文献,本研究首次通过回顾性研究分析本中心近1年的临床相关数据,旨在初步探讨以上处理方式对IVF周期结局的影响。
资料和方法
一、研究对象
收集2018年1~12月在中山大学孙逸仙纪念医院生殖中心行拮抗剂方案IVF/ICSI助孕的Gn启动日LH升高(≥10 U/L)的64例患者资料。其中启动日单用Gn、灵活方案添加GnRH-ant的患者42例为A组,启动日Gn与GnRH-ant同时使用者22例为B组。同时选取2018年8月启动日LH<10 U/L、采用灵活方案添加拮抗剂的患者112例纳入对照组(C组)。
所有患者资料齐全。收集女方年龄、体重指数(BMI)、不孕年限、基础FSH水平、抗苗勒管激素(AMH)水平及Gn启动日、促排卵第5天或第6天、HCG注射日外周血性激素水平、Gn用量等资料。
二、促排卵方案
采用常规的拮抗剂方案。月经周期第2~3天抽血查性激素FSH、LH、E2、P水平,采用阴道B超检查双侧卵巢窦卵泡情况,若卵泡大小2~9 mm,即开始使用FSH(珠海丽珠;或默克雪兰诺,瑞士;或默沙东,美国)每天75~300 U肌肉注射或皮下注射促排卵,每3~5 d监测B超及血性激素水平了解卵泡发育情况。A组患者拮抗剂的添加采用灵活方案,主导卵泡达直径12~14 mm或LH≥10 U/L时加用加尼瑞克(默沙东,美国)或思则凯(默克雪兰诺,瑞士)0.25~0.50 mg/d皮下注射直至HCG日。B组患者Gn启动日同时添加拮抗剂。C组患者拮抗剂添加亦采用灵活方案,与A组相同。当出现至少1个卵泡直径≥18 mm或至少3个卵泡直径≥17 mm时予以HCG(珠海丽珠;或默克雪兰诺,瑞士)4 000~10 000 U或GnRH-a(益普生,法国;或辉凌,瑞士)0.1~0.2 mg 皮下注射扳机。36 h后在阴道B超引导下使用17 G取卵针经阴道穿刺取卵术,取卵后即行胚胎培养3~5 d后行胚胎移植术。黄体支持从取卵日开始使用黄体酮注射液(浙江仙琚)60 mg/d肌肉注射或阴道用黄体酮胶囊(上海博赏)600 mg/d阴道给药直至验孕日。
三、治疗结局及观察指标
比较各组患者的基本资料:年龄、BMI、不孕年限、AMH、基础FSH等;促排卵情况及妊娠结局:Gn启动量、促排卵过程中激素水平、添加HMG比例及天数、获卵数、取消取卵比例,以及临床妊娠率和取消移植、卵巢过度刺激综合征(OHSS)高风险比例等。胚胎移植后12~14 d血HCG>20 U/L诊断为妊娠试验阳性,移植后35 d经阴道B超见宫内妊娠囊者诊断为临床妊娠。临床妊娠率=临床妊娠周期/胚胎移植周期总数×100%。活产指移植后妊娠≥28周分娩至少一活胎。
截至本文撰稿时,仍有部分患者有冷冻胚胎未移植。为了初步评估每个患者的累积活产率,本研究采用了两种计算方式:乐观累积活产率(optimistic cumulative live birth rate),即假设仍有冷冻胚胎未移植患者与已完成治疗患者具有相同的机会获得活产来计算;保守累积活产率(conservative cumulative live birth rate),即假设仍有冷冻胚胎未移植患者,移植完所有冷冻胚胎仍不能获得活产来计算。因此保守累积活产率=已经活产者/周期起始或移植患者总数×100%。乐观累积活产率=[已经活产者+(分析随访期内仍有冷冻胚胎未移植者×保守活产率)]/周期起始或移植患者总数×100%。分别计算每移植患者累积活产率,即分母为总的移植患者数目;每启动周期累积活产率,即分母为总的启动周期数目。
四、统计学分析
结 果
一、各组患者基本资料比较
3组患者的基本资料比较,A组女方年龄中位数显著小于其他两组(P<0.001);3组间BMI、不孕年限及基础FSH比较,均无显著性差异(P>0.05);B组基础LH、AMH显著高于其他两组(P<0.001);A、B两组PCOS患者比例显著高于C组(P<0.001)(表1)。
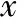
表1 三组患者临床基本资料的比较[(-±s),M(Q25,Q75),n(%)]
二、各组患者促排卵资料比较
C组的Gn启动量中位数水平显著高于其他两组(P<0.001);Gn天数、Gn启动日P水平在3组间比较均无显著性差异(P>0.05);C组的Gn总量中位数水平显著高于其他两组(P<0.001);Gn启动日LH水平3组间比较有显著性差异(P<0.001)(表2)。

表2 三组患者促排卵过程各指标的比较[(-±s),M(Q25,Q75),n(%)]
3组中分别有22例、8例、48例患者在促排卵第5天抽血查性激素,11例、9例、49例在促排卵第6天检测性激素,另外3组中分别有9例、5例、15例患者在促排卵第4天或第7天抽血检测性激素。C组促排卵第5天或第6天及HCG日血LH水平显著低于其他两组(P<0.05);促排卵过程中添加HMG比例、HMG添加天数及总量3组间比较均无显著性差异(P>0.05);其他指标包括Gn天数、Gn启动日E2及P水平,促排卵第5天或第6天E2及P水平,HCG日E2及P水平3组间比较均无显著性差异(P>0.05);促排卵第5~6天,A、B组中LH≥10 U/L患者比例均略高于C组,但尚无显著性差异(P>0.05)(表2)。
促排卵过程中激素变化趋势图显示,B组患者在促排过程中E2及LH水平均略低于A组患者,但尚无显著性差异(P>0.05)(图1)。
三、3组患者临床结局各指标比较
A、B组获卵数显著高于C组(P<0.05);总共6例患者取消取卵周期,A组无取消取卵病例,B组1例患者因早发LH峰取消取卵,另5例患者中均来自于C组,其中4例患者因卵巢反应不良取消周期,1例患者提前排卵取消周期;B、C组取消取卵的比例分别为4.54%、4.46%,取消原因包括提前排卵、卵巢反应不良;B组的取消移植周期比例相对最高(50%),但与其他两组比较尚无显著性差异(P>0.05);B组因OHSS高风险取消移植比例亦最高(45.45%),但与其他两组比较尚无显著性差异(P>0.05);B组患者的乐观累积活产率显著高于A、C组(P<0.05);保守累积活产率亦有高于A、C组的趋势,但尚无显著性差异(P>0.05)(表3)。
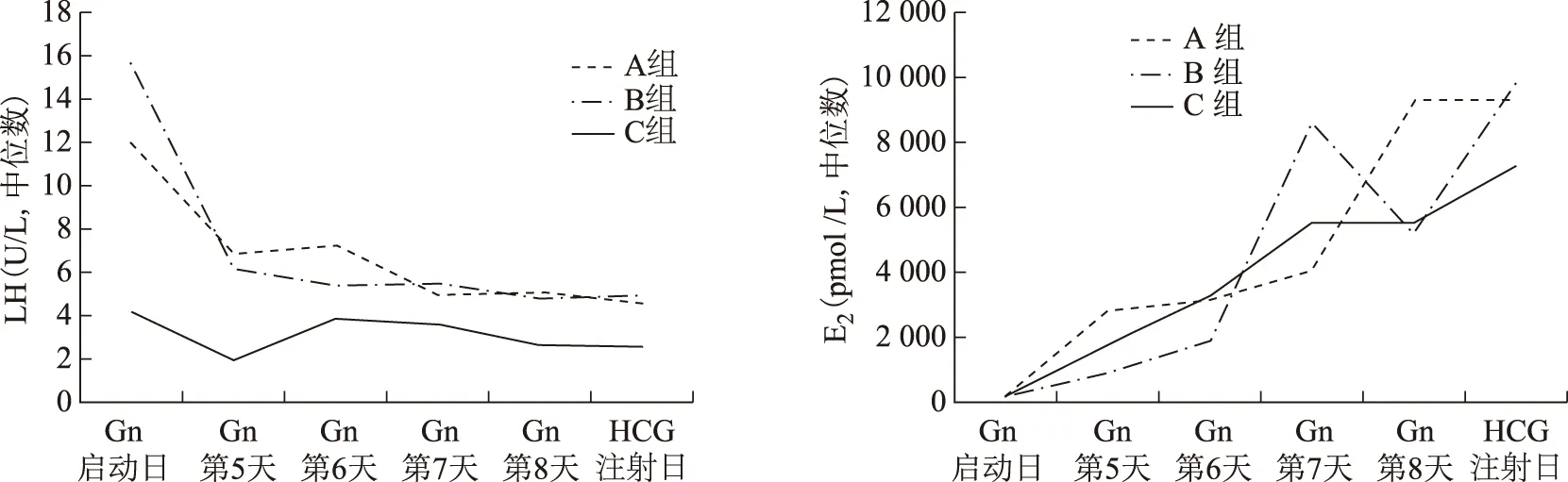
图1 不同组间促排卵过程中血LH和E2水平变化趋势

表3 三组患者临床结局各指标比较[(-±s),%]
讨 论
随着ART快速发展,对于促排卵过程激素变化的探讨越来越深入。卵泡中晚期的早发性LH峰及过早黄素化引起学者们的关注,但对于早卵泡期LH、基础LH水平的关注较少。早发LH峰通常是指卵泡成熟前或卵泡径线未达HCG注射标准前出现的内源性LH峰。早发LH峰可导致过早排卵和黄素化,影响获卵、卵母细胞质量和子宫内膜容受性,导致ART周期取消率增加,出现受精率、胚胎质量、着床率和临床妊娠率下降等不良结局[5]。
外周血基础LH升高(≥10 U/L)主要见于两类患者,一类是临床常见的PCOS患者,另一类是卵巢功能低下或者衰竭的患者,以高龄或围绝经期女性多见。本研究中纳入基础LH升高的患者主要是PCOS患者(A、B组中PCOS患者均占70%以上)。PCOS患者内分泌紊乱的常见性激素表现为LH/FSH倒置、LH大于10 U/L等,其发生率介于35%~90%之间[6]。PCOS患者中早发LH峰发生率达38%[7]。本研究中启动日单用Gn、灵活方案添加GnRH-ant的患者促排卵第5天血LH≥10 U/L占11.9%,高于启动日Gn与GnRH-ant同时使用组患者。因为本研究是回顾性分析,推测之前医嘱是建议多卵泡发育的早发LH峰高危患者促排卵第5天复诊,低危患者第6天复诊,还有少部分患者第4天和第7天测性激素,故检测性激素水平的时间不同。已有文献报道促排卵第5~6天给予GnRH-ant抑制LH,可使LH下降到安全水平,有机会挽救该助孕周期,获得较满意的助孕结局[5,8]。对于基础LH过高的患者,可能高生物活性的LH会增加卵泡募集,常规促排卵4 d后更易出现过多卵泡发育,体内雌激素水平上升迅速并明显增高,易出现垂体正反馈LH峰,且难以抑制,出现过早黄素化。
雌激素对正常女性垂体GnRH敏感性的影响是双相的,可表现刺激性作用即正反馈效应或抑制性作用即负反馈效应,且存在剂量和持续时间的依赖性[6]。促排卵4~5 d后,伴随着多个卵泡生长发育,体内雌激素水平升高明显。在临床上有部分患者基础LH高,未作处理,促排卵4 d后,随着雌激素水平的升高,LH水平有所下降。这部分患者卵泡生长缓慢或卵巢慢反应,E2水平上升慢,推测对垂体GnRH敏感性主要以抑制性为主。若卵巢高反应,多个卵泡同时发育,生长迅速,E2水平上升明显,作用时间长,对垂体GnRH敏感性主要为刺激性作用,正反馈诱发LH峰。既往学者通过回顾性分析发现卵巢高反应患者使用固定方案添加拮抗剂时,雌激素水平高于669 pg/ml(2 448.54 pmol/L)患者易出现早发LH峰[15]。本研究中启动日Gn与GnRH-ant同时使用组患者促排卵第5、6天雌激素水平均较低。由于样本量偏小,3组患者的取消移植率、取消取卵率、OHSS高风险比例比较均无显著性差异。从3组患者年龄预测启动日单用Gn、灵活方案添加GnRH-ant组患者临床妊娠率可能最高,但结果显示3组间每移植周期临床妊娠率比较无显著性差异。乐观及保守累积活产率结果提示全程添加拮抗剂与灵活添加拮抗剂相比,前者的乐观累积活产率明显增高,是否与全程拮抗剂添加有关有待于进一步扩大样本量设计前瞻性研究加以探讨。
GnRH-ant早在1999年开始使用,主要用于IVF/ICSI促排卵中预防早发LH峰。如不使用GnRH类似物,大概20%的IVF促排卵周期会出现LH峰。拮抗剂的使用为控制垂体功能提供了新思路、新方法。动物试验结果证明在动物动情周期早期(1~5 d)使用拮抗剂不影响周期长度,说明早卵泡期使用拮抗剂不影响卵泡生长及排卵[9]。另有研究表明在正常月经周期中卵泡差异化前1~2 d体内LH水平会上升,此时给予单次剂量拮抗剂,LH水平连续两天降低约50%,但并不影响优势卵泡的生长[10]。有研究证实在PCOS患者宫腔内人工授精(IUI)促排中使用全程拮抗剂是有效的方法,可以获得满意的临床妊娠率[11]。即在卵泡早期使用拮抗剂并不影响卵泡生长。早在2003年Kolibianakis等[12]通过小样本随机对照研究 (n=60),发现全程使用拮抗剂(Gn启动日开始)相比固定方案(促排卵第6天开始)添加拮抗剂,前者LH及E2水平均明显降低,而成熟卵子数无明显差异,种植率两组相当(33.9% vs. 30.5%)。但上述研究均排除了PCOS患者,基础LH或启动日LH均小于10 U/L,因此有学者认为需对早卵泡期高LH水平的PCOS患者开展研究[13]。2018年有学者回顾性分析卵巢高反应患者[基础窦卵泡数(AFC)≥15个或预期高反应患者]固定方案添加拮抗剂的临床资料发现,早发LH峰发生率约为15.6%,尤其是AFC≥22个及添加拮抗剂日E2水平≥669 pg/ml(2 448.54 pmol/L)患者易出现早发LH峰[14],因此作者建议对于高反应患者促排第4天或更早添加拮抗剂。本研究纳入人群中PCOS患者比例居多,比较Gn启动日全程使用拮抗剂与灵活方案使用拮抗剂的相关指标,研究结果提示早卵泡期LH及E2水平有降低的趋势。有研究报道卵泡早期高LH及E2可能影响子宫内膜,降低种植率[15-16],低LH水平可获得更高的持续妊娠率[17]。PCOS患者Gn启动日开始使用拮抗剂与长方案比较,两种方案的妊娠结局相当[18]。因此早卵泡期LH水平与妊娠结局的关系尚无定论,PCOS患者全程使用拮抗剂方案值得深入研究。
外周血LH的检测采用的是化学发光法,血清LH水平并不能完全代表具有生物活性的LH。既往研究表明PCOS患者体内LH的生物活性明显增高[6],但亦有研究推测PCOS患者中基础LH高说明存在着LH同分异构体(isoforms)[19-21]。由于LH存在多种酸碱类型,体外生物活性更强,体内半衰期更短,推测这种双重表现,可能通过更快速地清除体内LH而部分减弱过量LH驱动胰岛素致敏的卵泡膜细胞分泌雄激素的作用[19-20]。而PCOS患者高频率、高幅度的LH过量分泌,在雌激素的正反馈下极有可能发生叠加作用,诱发早发LH峰风险增加。临床工作中确实遇到部分患者LH过高,拮抗剂无法抑制,最终取消周期的案例。推测PCOS患者体内存在大量LH同分异构体,半衰期短、体内清除快,导致体内LH相对不足,那么是否需要在促排过程中添加含LH成分的促排卵药物尚无定论。既往研究证实在拮抗剂方案中添加LH仅使高龄人群获益[22]。本研究中,比较了3组添加HMG的比例及天数,3组间无显著性差异。因此,对基础LH高的PCOS患者如何处理可能降低各种风险(包括早发LH峰、卵巢反应不良等),仍值得进一步深入探讨。
在既往的临床工作中,我们认识到PCOS患者基础高LH与胰岛素抵抗及高雄激素血症密切相关,主张纠正胰岛素抵抗及高雄激素血症后再复查基础性激素。但仍有部分特殊患者高LH水平难以纠正,本研究中涉及的全程使用拮抗剂也是针对这一部分特殊患者做的尝试。早发LH峰在整体拮抗剂方案人群中可能并不高,但在特殊人群中发生风险高。全程使用拮抗剂通过进一步降低卵巢高反应患者雌激素水平的快速上升、早发LH峰风险,有改善临床结局的趋势。
因为本研究是回顾性分析,且是对临床特殊病例处理的初步尝试,纳入研究的样本量较小,同时不可避免存在临床医生使用方案时的选择偏倚,因此,研究结论有一定局限性。但从分析的数据来看,对于基础LH水平过高(≥10 U/L)的患者,尝试使用全程拮抗剂平稳控制LH水平是可行的,可能有助于降低高危患者早发LH峰的发生风险及改善助孕结局。但对于全程使用拮抗剂的必要性及高LH的截断值,尚需要大样本的前瞻性对照研究加以探讨。
