狭义水解和广义水解概念及规律
2020-11-17湖北陈功健
湖北 陈功健
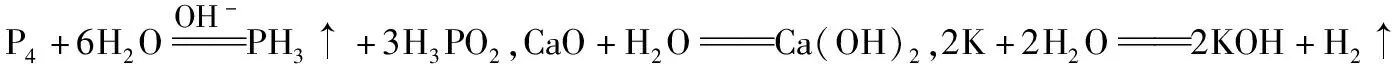
一、狭义水解即盐类水解“概念的界定”
人教版选修4《化学反应原理》第56页文中指出:“综上所述,强酸弱碱盐和强碱弱酸盐溶于水时,电离产生的阳离子、阴离子可分别与水电离产生的OH-或H+生成弱电解质——弱碱或弱酸,使得溶液中c(OH-)≠c(H+),因而这两类盐溶液呈现酸性或碱性。盐与水发生的这种作用叫作盐类的水解。”
抓住盐类水解概念中关键词:
①该盐能“溶于水”
②该盐含有“弱离子”——弱碱阳离子或弱酸根
③盐类水解的“本质”是——“弱离子”与水电离出的OH-或H+生产弱电解质
④盐类水解的“结果”——产生“弱酸或弱碱”
盐类水解模型:




【答案】8.7×10-7

电离与水解的区别在于,弱电解质电离的过程是弱电解质在水中生成对应弱酸阴离子或弱碱阳离子。盐类水解是盐类中弱离子在水中生成对应“弱酸或弱碱”的过程。
由上述高考真题可知,高考中很重视对于教材中化学概念的考查,教师在教学过程和高考备考过程一定要引导学生重视化学学科概念的认知与理解。
二、广义水解的“概念及电化二元论的应用”
1.无机物的水解反应


广义水解理论在无机反应中的应用主要有以下几种类型:







人教版选修4《化学反应原理》第58页还介绍了利用水解原理制备纳米材料。溶液浓度较低,可以利用水解反应来获得纳米材料,此时氢氧化物可变为氧化物。如果水解程度很大,还可用于无机化合物的制备,如制纳米TiO2:
2.有机物的水解反应
“电化二元论”不仅能帮助学生理解无机化学反应中的很多非盐水解反应,还能帮助学生理解很多有机物的水解反应。
(1)酯类在酸性环境下水解:

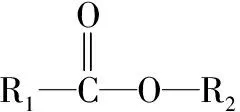
(2)酯类在碱性环境下水解:


(3)氯代烃的水解:

在氯代烃中氯元素显电负性,与水电离出的H+结合生成HCl,而R-与水电离出来的OH-形成ROH。同理,这种处理方式不代表氯代烃水解本质。
(4)醇钠的水解:
例如乙醇钠的水解:

在乙醇钠中,Na+显正电性与水电离出OH-结合生成NaOH,而CH3CH2O-与水电离出H+结合生成CH3CH2OH。
其他的如二糖及多糖、多肽及蛋白质的水解反应均可借助“电化二元论”进行理解。
必须要说明的是,借助瑞典化学家贝采尼乌斯的“电化二元论”书写广义水解反应方程式是一种在高中阶段解决问题的方法,不能认为它就是有机物水解反应的机理或本质。
三、广义水解在高考真题中的考查
【例2】(2019·天津卷·7节选)SbCl3能发生较强烈的水解,生成难溶的SbOCl,写出该反应的化学方程式______________________________。


【例3】(2020年1月浙江省普通高校招生选考科目考试·26节选)(1)比较给出H+能力的相对强弱:H2O________(填“>”“<”或“=”)C2H5OH;用一个化学方程式说明OH-和C2H5O-结合H+能力的相对强弱________。


【例4】(2020年天津市学业水平等级考适应性测试·13节选)(3)CHCl3与SiHCl3空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式________________________________________________。


【例5】(2018·全国卷Ⅲ·28节选)三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料。回答下列问题:
(1)SiHCl3在常温常压下为易挥发的无色透明液体,遇潮气时发烟生成(HSiO)2O等,写出该反应的化学方程式______________________________。


【例6】(2016·天津·7节选)下表为元素周期表的一部分。

碳氮YX硫Z
回答下列问题:
(5)碳与镁形成的1 mol化合物Q与水反应,生成2 mol Mg(OH)2和1 mol烃,该烃分子中碳氢质量比为9∶1。Q与水反应的化学方程式为________________________________________________。


【例7】(2015·浙江·27节选)Ⅱ.化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80 g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
NaAlH4与水发生氧化还原反应的化学方程式____________________________________________。


【例8】(2014·安徽·28节选)LiPF6是锂离子电池中广泛应用的电解质,某工厂用LiF、PCl3为原料,低温反应制备LiPF6,其流程如下:

已知:HCl的沸点是-85.0℃,HF的沸点是19.5℃。
(2)该流程需在无水条件下进行,第③步反应中PF5极易水解,其产物为两种酸,写出PF5水解的化学方程式:______________________________。


【例9】(2013·海南·14节选)溴及其化合物广泛应用于医药、农药、纤维、塑料组燃剂等,回答下列问题:
(2)溴与氯能以共价键结合形成BrCl。BrCl分子中,________显正电性。BrCl与水发生反应的化学方程式为______________________________。



