高浓度HBsAg检测化学发光微粒子免疫分析法的建立及性能评价
2020-11-06张志平彭道荣宋浏伟葛胜祥郝晓柯刘家云
刘 杨, 张志平, 彭道荣, 宋浏伟, 葛胜祥, 郝晓柯, 刘家云
(空军军医大学第一附属医院,陕西 西安 710032)
乙型肝炎表面抗原(hepatitis B surface antigen,HBsAg)是乙型肝炎病毒(hepatitis B virus,HBV)的外膜蛋白,主要用于HBV感染的筛查[1]。血清HBsAg定量检测已成为临床抗病毒治疗疗效监测的重要指标。化学发光微粒子免疫分析法(chemiluminescent microparticle immunoassay,CMIA)是一种高特异性、高灵敏度、重复性好的检测方法,无放射性污染,可快速检测血清中的小分子物质及肿瘤标志物等[2-3]。目前,我国临床实验室广泛使用的是进口化学发光免疫分析系统。由于绝大部分慢性乙型肝炎患者血清HBsAg水平较高,目前临床常用的检测系统需对样本先进行稀释,然后再检测,不仅降低了工作效率,也加大了检测成本。为此,本研究拟建立定量检测中、高值血清HBsAg的CMIA,并对其进行初步的性能评价。
1 材料和方法
1.1 研究对象
选取2014年12月—2015年12月空军军医大学第一附属医院就诊的HBV感染患者268例,其中男135例、女133例,年龄21~67岁,无甲型肝炎病毒(hepatitis A virus,HAV)、丙型肝炎病毒(hepatitis C virus,HCV)、戊型肝炎病毒(hepatitis E virus,HEV)、梅毒螺旋体(Treponema pallidum,TP)、人类免疫缺陷病毒(human immunodeficiency virus,HIV)等合并感染。选取同期空军军医大学第一附属医院进行健康体检的表观健康者146名,其中男75名、女71名,年龄23~74岁。本研究所用的血清样本均为常规检测后的剩余血清,-20 ℃保存待检。
1.2 仪器和试剂
重组HBsAg、羊抗HBsAg多克隆抗体Ab1和7株抗-HBsAg小鼠单克隆抗体(Ab2~Ab8)均购自厦门万泰沧海生物技术有限公司,hepatitis E virus(HEV),human immunodeficiency virus(HIV),human T-lymphotropic virus(HTLV),cytomegalovirus(CMV)and Epstein-Barr virus(EBV)positive samples did not cross-react with this assay. The prepared reagent could be stable for 6 d at 37 ℃,it could be stable for 4 weeks after opening lid at 2-8 ℃,and it could be stable for 6 months when stored in a sealed container at 2-8 ℃. The correlation and consistency between self-established CMIA and electrochemiluminescence method were good(r=0.978,P<0.001).ConclusionsThe self-established CMIA has a wide linear range for determining HBsAg,high concentration samples can be directly determined without dilution,and the determination performance is good,which has certain clinical application prospects.
Key words:Hepatitis B surface antigen;Hepatitis B virus;Chemiluminescent microparticle immunoassay;Performance evaluation纯度均>90%。HBsAg突变株WT、G119R、P120T、C124Y、I126S、Q129R、S136P、C139R、T140I、P144A、G145A、G145R、M204U、M204I购自厦门大学国家传染病与疫苗工程技术研究中心。磁微粒(直径约3 μm,微粒表面为羧基修饰)购自上海立驰高化工有限公司。碳二亚胺盐酸盐[1-ethyl-3-(3-dimethylaminopropyl)carbodiimide,EDC]和N-羟基琥珀酰亚胺(N-hydroxy succinimide,NHS)购自美国Sigma公司。Caris 200全自动化学发光免疫分析仪(厦门优迈克医学仪器有限公司),cobas e601全自动电化学发光免疫分析仪(瑞士罗氏公司)及配套HBsAg试剂盒(电化学发光法)。
1.3 自建CMIA试剂的制备
自建CMIA主要有2种试剂,一种是磁微粒与鼠抗-HBsAg单克隆抗体偶联制备的MB试剂,磁微粒与抗体的化学偶联通过EDC和NHS两者联用进行,步骤参照磁微粒使用说明书;另一种是吖啶酯标记抗-HBsAg多克隆抗体,配制成SEA试剂,步骤如下:将50 μg抗体与5 μL吖啶酯溶液(5 mmol/L)在300 μL磷酸盐缓冲液(pH值8.0)中避光反应30 min,加入终止缓冲液(5%甘氨酸)反应30 min,最后避光透析去除游离吖啶酯。
1.3.1 自建CMIA的检测程序 自建CMIA检测原理为双抗体夹心法,检测程序:(1)向反应杯中加入一定量的样本、MB试剂和反应稀释液,混匀后37 ℃孵育15 min;(2)仪器内置磁铁对反应杯中的磁微粒进行集磁,然后对磁微粒洗涤2次;(3)加入SEA试剂混匀重悬磁微粒,37 ℃孵育10 min;(4)仪器内置磁铁对反应杯中的磁微粒进行集磁,然后对磁微粒洗涤4次;(5)反应杯中加入预激发液和激发液,并检测光子信号。
1.3.2 反应的最佳体系 取重组HBsAg抗原用20%婴牛血清(newborn bovine serum,NBS)进行梯度稀释,得到10份阳性系列标准品(依次编号为S1~S10)。5份表面健康者血清样本依次编号为N1~N5。观察S1~S10的相对发光强度(relative light unit,RLU)值与样本浓度的线性关系。将S1~S10的平均RLU值(记为P值)除以N1~N5的平均RLU值(记为N值),得出P/N比值,综合分析上述线性关系及P/N比值,筛选出最佳反应体系。
1.3.3 抗体筛选 将羊抗HBsAg多克隆抗体Ab1标记吖啶酯制备成SEA试剂,7株抗-HBsAg小鼠单克隆抗体(Ab2~Ab8)包被磁微粒制备为MB试剂,将MB试剂与SEA试剂配对检测1例HBsAg阳性血清样本(P)、1例HBsAg阴性样本(N),以及不同HBsAg突变株,评估不同原料对不同样本的检出能力。
1.3.4 抗体最适浓度的筛选 将不同浓度的磁微粒抗体(0.2、0.4、0.8 mg/mL)与不同稀释比例的吖啶酯抗体(1∶100、1∶200和1∶500)进行两两配对筛选,通过P/N比值及标准品的RLU与浓度的线性关系筛选出抗体的最适浓度。
1.3.5 反应稀释液的用量 分别设置0、25、50、100 μL反应稀释液用量,对S1~S10系列标准品进行检测,通过P/N比值及标准品的RLU与浓度的线性关系筛选出反应稀释液的最适用量。
1.3.6 样本加样量的选择 分别设置20、50、80 μL样本加样量,对S1~S10进行检测,通过P/N比值及标准品的RLU与浓度的线性关系筛选出样本最适加样量。
1.3.7 试剂用量的选择 设置25、50、100 μL试剂用量,分别评价MB试剂与SEA试剂的用量对试剂检测范围的影响,通过P/N比值及标准品的RLU值与浓度的线性关系筛选出试剂最适用量。
1.3.8 标准曲线的建立 将HBsAg纯品梯度稀释,制备成6个不同浓度(100 000、20 000、4 000、800、160、32 IU/mL)的标准品(依次编号为S0~S5),测定S0~S5的RLU值,用四参数拟合方式对校准品的检测结果进行拟合,得到标准曲线。
1.4 自建CMIA的性能评价
参照美国临床实验室标准化协会(the Clinical and Laboratory Standards Institute,CLSI)EP6-A文件[4]、EP15-A2文件[5]、EP5-A2文件[6]、EP7-A2文件[7]评价自建CMIA的检测性能。
1.4.1 线性范围 将高浓度HBsAg标准品梯度稀释,得到10个浓度(100 000、50 000、10 000、5 000、1 000、500、100、20、10、5 IU/mL)的标准品,每个浓度样本平行检测4次,计算。将每个浓度的和RLU值采用Log-Logit数学模型处理后得到剂量-反应曲线及r值。
时间等不起,造价出不起。只有一个办法,自己动手。工程师刘家林、施工队长李德铭和大家一起,研究出一个新的方案:原设计要求在路基2.5米以下用直径1560毫米的钢筋混凝土保护管穿越路基,改用直径377毫米的钢管代替混凝土管,可把管底深度由4.04米减少到2.88米,穿越长度由70米缩短到35米。但是,长距离穿越,稍有疏忽就会造成弯曲,即使缩短为30多米,仍有相当长的距离,如稍有弯曲就会损伤路基。因此,大家仍是提心吊胆,兢兢业业,采取了非常严密的措施,并自己设计制造了一个24米长的顶推滑道,以避免管道穿弯,还选用D80推土机,挑选驾驶技术最熟练的推土机手,把顶推的位置固定死。
1.4.2 检测限 检测HBsAg零浓度值的标准品,重复检测20次,计算RLU的和s,将+2s代入剂量-反应曲线方程,求出对应的浓度值,即为最低检测限。
1.4.3 精密度 分别重复检测高、低值HBsAg阳性样本10次,连续检测10 d,计算批内和批间精密度[以变异系数(coefficient of variation,CV)表示]。
1.4.4 准确度 检测配制的准确度参考品,测量相对偏差=(实测值-理论值)/理论值×100%。
1.4.5 交叉反应 选择可能与自建CMIA检测HBsAg发生交叉反应的其他病毒阳性样本,如HAV、HCV、HIV、人类嗜T淋巴细胞病毒(human T-lymphotropic virus,HTLV)、巨细胞病毒(cytomegalovirus,CMV)、EB病毒(Epstein-Barr virus,EBV),通过检测特异性观察自建CMIA是否会发生交叉反应。
1.4.6 干扰实验 在HBsAg阳性样本中加入不同浓度的干扰物质(血红蛋白、胆红素、三酰甘油、类风湿因子、抗凝剂)制备成干扰样本,对照样本加入同等体积的0.9%氯化钠溶液,同时检测干扰样本和对照样本,计算相对偏差,相对偏差=(干扰样本-对照样本)/对照样本×100%。如相对偏差≤10%,可认为该浓度的干扰物质对检测无干扰。
1.4.7 稳定性实验 将配制好的试剂在37 ℃条件下放置6 d,评估试剂的热稳定性。将试剂2~8 ℃密封保存6个月,每3个月检测1次,观察试剂的长期保存稳定性。将试剂在仪器上冷藏(2~8 ℃)保存4周,每周检测1次,评价试剂的机上保存稳定性。稳定性评估通过检测系列标准品、阴阳性参考品及高值、低值样本,以线性、准确度、检出限、精密度等指标体现。
1.5 统计学方法
采用SPSS 16.0软件和Graphpad Prism 5软件进行统计分析。采用Pearson相关分析及Bland-Altman一致性检验评价2种方法的相关性和一致性。
2 结果
2.1 抗体筛选
7株抗HBsAg小鼠单克隆抗体中Ab2、Ab3、Ab4、Ab5、Ab6和Ab8对阳性样本和阴性样本的区分度较好。进一步检测不同HBsAg突变株,结果显示Ab3、Ab4、Ab6和Ab8对不同突变株具有互补检出能力,可用于包被磁微粒,制备MB试剂。见图1、图2。

图1 不同抗体反应性评估

图2 不同抗体对不同HBsAg突变株的检测能力
2.2 最适反应条件
2.2.1 抗体最适浓度的筛选 磁微粒抗体最适浓度为0.4 mg/mL,吖啶酯抗体最适稀释比例为1∶200(浓度为250 ng/mL)。
2.2.2 反应稀释液最适用量 当反应稀释液用量为100 μL时,试剂检测范围最优。见图3。

图3 不同反应稀释液用量下RLU与HBsAg浓度的关系
2.2.3 样本加样量 随着样本加样量的增加,试剂检测上限逐渐降低,检测范围逐渐缩小,故样本最适加样量选择20 μL。见图4。
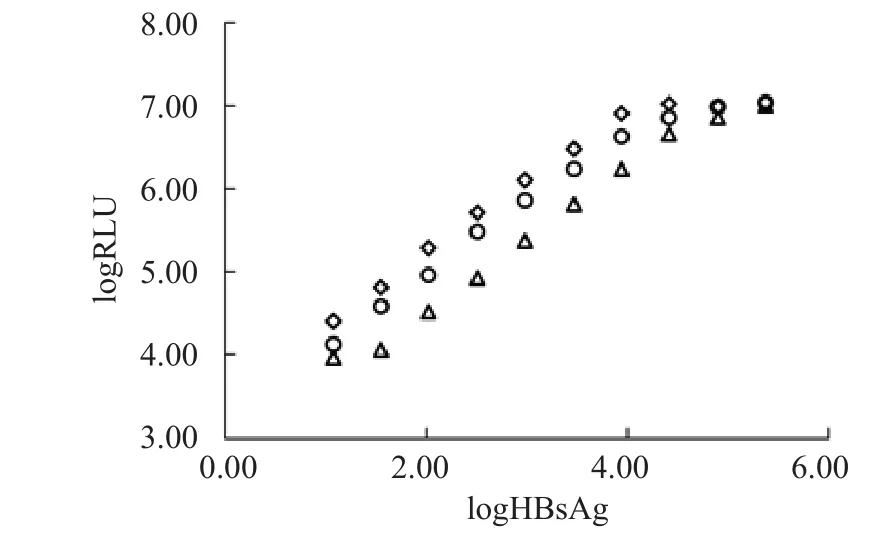
图4 不同样本加样量下RLU和HBsAg浓度的关系
2.2.4 试剂用量 MB试剂用量和SEA试剂用量对检测范围的影响较小,因此2个主要试剂的用量均为50 μL。
2.3 性能评价结果
2.3.1 线性范围 自建CMIA检测HBsAg的线性范围为20~100 000 IU/mL,线性回归方程为Y=0.722X+3.591(r=0.993,P<0.001)。见图5。

图5 自建CMIA检测HbsAg的剂量-反应曲线
2.3.2 最低检测限 将零浓度标准品的RLU代入剂量-反应方程,得到自建CMIA的最低检测限为9.9 IU/mL。
2.3.3 精密度 自建CMIA检测高、低值HBsAg样本的批内CV分别为8.2%、8.4%,批间CV分别为8.9%、8.7%,均符合要求(CV<10.0%)。
2.3.4 交叉反应 自建CMIA对其他病毒阳性样本均无明显交叉反应,HBsAg均<20 IU/mL,特异性为100%。
2.3.5 干扰实验 Hb<400 mg/L、胆红素<4 mg/L、类风湿因子<800 IU/mL、三酰甘油<2 mg/L、柠檬酸钠<22 mmol/L、乙二胺四乙酸(ethylenediamineteraacetic acid,EDTA)<8 mmol/L对自建CMIA检测HBsAg无干扰,相对偏差均<10%。见表1。

表1 自建CMIA干扰实验结果
2.3.6 稳定性实验 配制好的试剂在37 ℃可稳定6 d,开盖后上机(2~8 ℃)保存可稳定4周,2~8 ℃密封保存可稳定6个月。见表4。

表4 自建CMIA试剂的稳定性实验结果
2.3.7 方法学比较 自建CMIA与电化学发光法检测HBsAg的相关性良好,线性回归方程为Y=1.001X-0.018(r=0.978,P<0.001),见图6。Bland-Altman散点图显示266份样本中仅有3份(1.13%)样本在95%一致性界限外,低于临床可接受要求(2.5%),2种方法的一致性良好,见图7。

图6 自建CMIA与电化学发光法检测HBsAg的相关性

图7 自建CMIA与电化学发光法检测HBsAg的Bland-Altman散点图
3 讨论
HBV是一种嗜肝性DNA病毒,60%的肝硬化和80%的肝癌是由HBV感染所致[8]。HBsAg是慢性乙型肝炎患者诊断和治疗监测重要的血清学指标,HBsAg由阳性转为阴性是患者免疫清除的最终目标[9]。有研究结果显示,血清HBsAg基线水平和治疗后血清HBsAg水平的下降幅度都可较好地预测患者抗病毒治疗的疗效和预后[10-11]。根据电化学发光法试剂说明书的声明,611例HBV感染者中约有80%的患者血清HBsAg水平分布于100~100 000 IU/mL。ARCHITECT iR2000全自动免疫分析系统(美国雅培公司)的灵敏度较高,但线性范围很窄,仅为0.05~250 IU/mL,高于250 IU/mL的样本需设置500倍稀释重检或手工稀释后重检,这大大降低了检测效率。cobas e601全自动电化学发光免疫分析仪在首次检测HBsAg时需强制进行400倍稀释,线性范围为20~52 000 IU/mL,低于20 IU/mL的样本需原倍重检,高于52 000 IU/mL的样本需手工稀释后重检。有研究结果显示,与ARCHITECT i2000全自动免疫分析系统相比,cobas e601全自动电化学发光免疫分析仪对HBsAg突变株的检测能力具有明显优势[12-13]。
综上所述,本研究建立的检测血清HBsAg的CMIA在精密度、特异性、稳定性等方面均符合临床检测要求,与电化学发光法有较好的相关性和一致性。自建CMIA的优势是具有更宽的线性范围(20~100 000IU/mL),可覆盖临床上绝大部分乙型肝炎患者血清HBsAg水平的范围,既降低了因稀释样本造成的实验误差,又降低了检测成本,提高了检测效率。该法的不足之处在于检测<20 IU/mL的低值样本时有一定的局限性,但这是在提高检测上限时无法避免的问题。临床上血清HBsAg<20 IU/mL的HBV感染患者很少,针对这部分样本本研究建立了针对低值样本的检测方法。在指导慢性乙型肝炎患者抗病毒治疗的用药选择上,临床对高值样本的检测需求远高于低值样本,因此该局限性并不影响自建CMIA的临床应用价值。另外,自建CMIA的试剂原料大部分为国产,成本较低,获取方便。因此,自建CMIA具有较好的临床应用前景。
