基于HPLC的菖远胶囊指纹图谱分析与6个成分定量方法的建立
2020-11-06黄永锋乔晶晶霍艳虹高亚亚
封 婷,赵 瑞,黄永锋,朱 江,赵 斌,乔晶晶,刘 霞,霍艳虹,高亚亚
(1榆林市第一医院神经内科,榆林 719000;2陕西省人民医院神经内一科;3西安市第五医院神经内科;*通讯作者,E-mail:sxgaoyaya@163.com)
菖远胶囊由石菖蒲、远志、丹参、人参、熟地、郁金和茯苓等组成,具有滋阴补气、开窍通经、破瘀行血、醒神益智和的功能。方中石菖蒲具有开窍豁痰、醒神益智、化湿开胃等功效[1-5];人参有治疗神经退行性疾病、改善记忆功能和保护脑组织等作用[1,6-8];远志具有安神益智、交通心肾、祛痰、消肿等功效[1,9-12];丹参具有养血安神、活血祛瘀和改善微循环等作用[1,13,14];川芎有行气活血、祛风止痛等功效[1,15,16];郁金有抗炎镇痛、抗血栓凝血、增强机体免疫等药理作用[1,17];茯苓有增强机体免疫力、抗炎和护肝等作用[1,18]。该药作为院内制剂应用多年,其制备工艺为原料药材粉碎、水提、喷雾干燥、制粒等。笔者前期药理研究证实菖远胶囊具有明显的健脑益智、增强记忆、改善脑缺血症状、抗疲劳、耐缺氧和增强免疫功能的作用[19]。本课题通过对菖远胶囊的HPLC指纹与6个成分(即梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1)定量控制的方法进行研究,旨在建立菖远胶囊的HPLC质量控制新方法与过程控制新方法,同时亦为扩大临床应用范围、服务更多的患者提供科学依据,为进一步开发中药新药奠定基础。
1 材料与方法
1.1 仪器与试药
岛津高效液相色谱仪(Prominence-i LC-2030C 3D,带自动进样器,LC/Labsoluion色谱工作站,日本岛津公司);ME235S型电子分析天平(德国塞多利斯公司);KQ-5200DE型数控超声波发生器(昆山超声仪器有限公司)。乙腈(色谱纯,美国Honeywell公司,批号:AH015-2),甲醇(色谱纯,美国Honeywell公司,批号:AH230-3);娃哈哈纯净水(杭州娃哈哈集团有限公司,批号:190818);磷酸(分析纯,西安三浦化学试剂有限公司,批号:180913);其余试剂均为分析纯。人参皂苷Rg1(批号:HGO27162),人参皂苷Re(批号:HGO27169),人参皂苷Rb1(批号:HGO27159),纯度均为≥98.0%,均购自宝鸡市晨光生物科技有限公司;细叶远志皂苷(批号:JOT10162),梓醇(批号:JOT-10011),丹酚酸B(批号:115939-25-8),纯度均为≥98.0%,均购自成都普菲德生物技术有限公司;菖远胶囊(批号:20190612,20190613,20190614,20190615,20190709,20190710,20190711,20190806,20190807,20190808),由榆林市第一医院药剂科制备。
1.2 指纹图谱测定
1.2.1 色谱条件 色谱柱为Kromasil C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱见表1。记录时间为110 min。流速:0.8 ml/min;柱温:30 ℃;检测波长:203 nm;进样量10 μl。
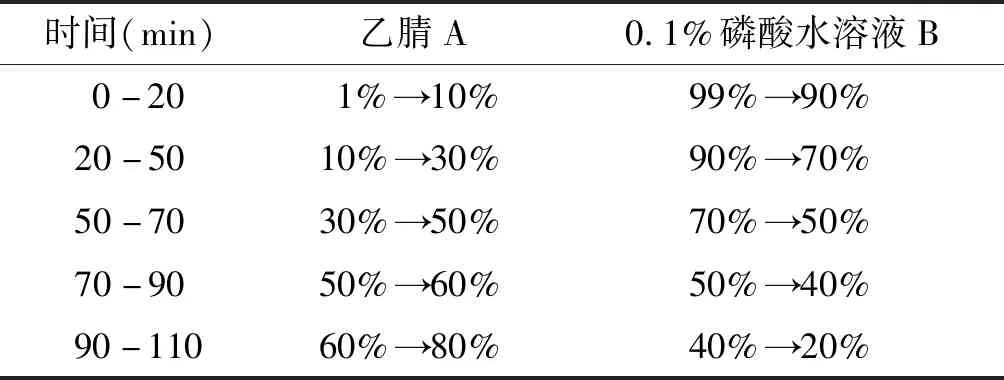
表1 梯度洗脱
1.2.2 参比物及供试品溶液的制备 参比物溶液的制备:称取丹酚酸B对照品5.10 mg置于50 ml量瓶中,加50%甲醇至刻度,摇匀,即得质量浓度为0.1 mg/ml的参比物溶液。
供试品溶液的制备:取20粒本品,倾出内容物,研细,混匀,称取粉末2 g,精密称定,置于25 ml量瓶中,加50%甲醇适量,超声处理(功率250 kW,频率40 kHz)30 min,放凉,加50%甲醇至刻度,摇匀,静置,0.45 μm微孔滤膜滤过,取续滤液,即得。
1.2.3 方法学考察 精密度试验:取供试品溶液(批号201906012),连续进样6次测定,计算共有峰的相对保留时间的RSD(%)和相对峰面积的RSD(%)。
稳定性试验:取供试品溶液(批号201906012),分别于0,3,6,9,12,24 h进样测定,计算共有峰的相对保留时间的RSD(%)和相对峰面积的RSD(%)。
重复性试验:取6份供试品(批号201906012),按1.2.2项制备供试品溶液与1.2.1项色谱条件进样测定,计算共有峰的相对保留时间的RSD(%)和相对峰面积的RSD(%)。
菖远胶囊指纹图谱建立及相似度分析:采用国家药典委员会《中药色谱指纹图谱相似度评价系统》(2012版本),依据文献[20]对10批菖远胶囊的指纹图谱进行相似度分析,将色谱工作站数据导入中药指纹图谱相似度计算软件,对选定共有色谱峰进行谱峰匹配,得出指纹图谱的共有模式,同时进行整体相似度评价及计算10批产品共有峰的相对保留时间的RSD(%)和相对峰面积的RSD(%)。
1.3 含量测定
1.3.1 色谱条件 同1.2.1项。
1.3.2 各种溶液的制备 对照品溶液的配制:分别称取梓醇5.00 mg、丹酚酸B 15.00 mg、人参皂苷Rg1 4.50 mg、人参皂苷Re 3.30 mg、人参皂苷Rb1 4.80 mg和细叶远志皂苷15.20 mg,置于50 ml量瓶中,加50%甲醇至刻度,摇匀,即得混合对照品溶液,作为储备液。
混合对照品溶液:分别称取梓醇0.032 62 g、丹酚酸B 0.153 18 g、人参皂苷Rg1 0.031 51 g、人参皂苷Re 0.016 33 g、人参皂苷Rb1 0.336 81 g和细叶远志皂苷0.159 21 g置于100 ml量瓶中,加50%甲醇至刻度,摇匀,即得混合对照品溶液,浓度分别为梓醇0.32 mg/ml、丹酚酸B 1.50 mg/ml、人参皂苷Rg1 0.31 mg/ml、人参皂苷Re 0.16 mg/ml、人参皂苷Rb1 3.30 mg/ml和细叶远志皂苷1.56 mg/ml。
供试品溶液的制备:制备方法同1.2.2项。
阴性对照溶液的制备:依据处方,分别制备缺地黄、丹参、人参和远志药材的制剂,依据1.2.2项分别制备相应的阴性对照溶液。
1.3.3 方法学考察 线性关系:分别精密量取储备液0.01,0.05,0.20,0.40,080,1.00 ml置于各个1 ml量瓶中并加50%甲醇稀释至刻度,用0.45 μm微孔滤膜滤过,进样。以各对照品的质量浓度(x,μg/ml为横坐标,峰面积值(y)为纵坐标,通过计算,得线性方程。
专属性试验:按上述1.2.1项条件分别进样缺熟地黄、丹参、人参、远志阴性对照溶液、供试品溶液、混合对照溶液。
精密度试验:精密吸取供试品溶液(批号201906012),重复进样5次测定峰面积,计算梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和细叶远志皂苷的RSD(%)。
稳定性试验:精密吸取供试品溶液(批号201906012),分别在第0,2,4,8,12,24小时进样测定,计算梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和细叶远志皂苷的峰面积的RSD(%)。
重复性试验:精密称取6份样品(批号201906012),分别按1.2.2项下方法制备供试品溶液,按1.2.1项下色谱条件进样测定,计算梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和细叶远志皂苷的平均含量(mg/g)与RSD(%)值。
加样回收率试验:取20粒本品(批号201906012),倾出内容物,研细,混匀,称取粉末2 g,精密称定,置于25 ml量瓶中,分别添加混合对照品溶液8.00 ml或10.00 ml或12.00 ml,再加50%甲醇至刻度,按照1.2.2项下方法制备供试品溶液,共制备9份样品,按照1.2.1项下色谱条件进样测定,计算平均回收率(%)与RSD(%)。
含量测定:精密称取10批样品,分别按照1.2.2项下方法制备供试品,按照1.2.1项下色谱条件进样测定。计算10批样品中梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和细叶远志皂苷的平均含量(mg/g)、RSD(%)。
2 结果
2.1 指纹图谱测定
2.1.1 精密度试验 各共有峰的相对保留时间与相对峰面积RSD值分别小于2.0%和3.0%(见表2,3),表明该方法精密度良好。
2.1.2 稳定性试验 各共有峰相对保留时间与相对峰面积RSD值分别小于2.0%、3.0%(见表4,5),表明供试品溶液在24 h内具有良好的稳定性。
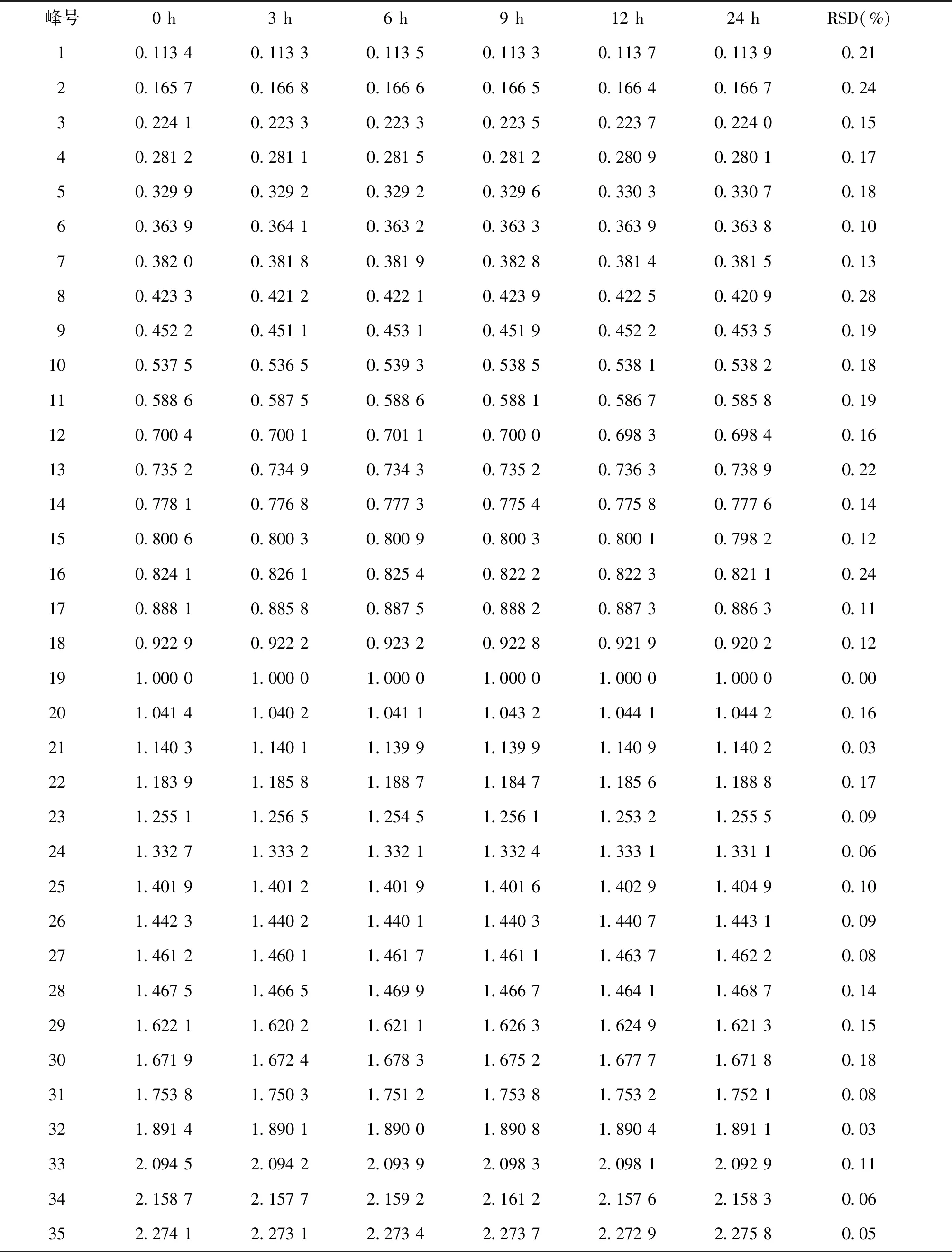
表4 菖远胶囊指纹图谱稳定性的相对保留时间结果

表5 菖远胶囊指纹图谱稳定性的相对峰面积的结果
2.1.3 重复性试验 各共有峰相对保留时间与相对峰面积RSD值分别小于1.5%和3.0%(见表6、表7),表明该方法重复性良好。
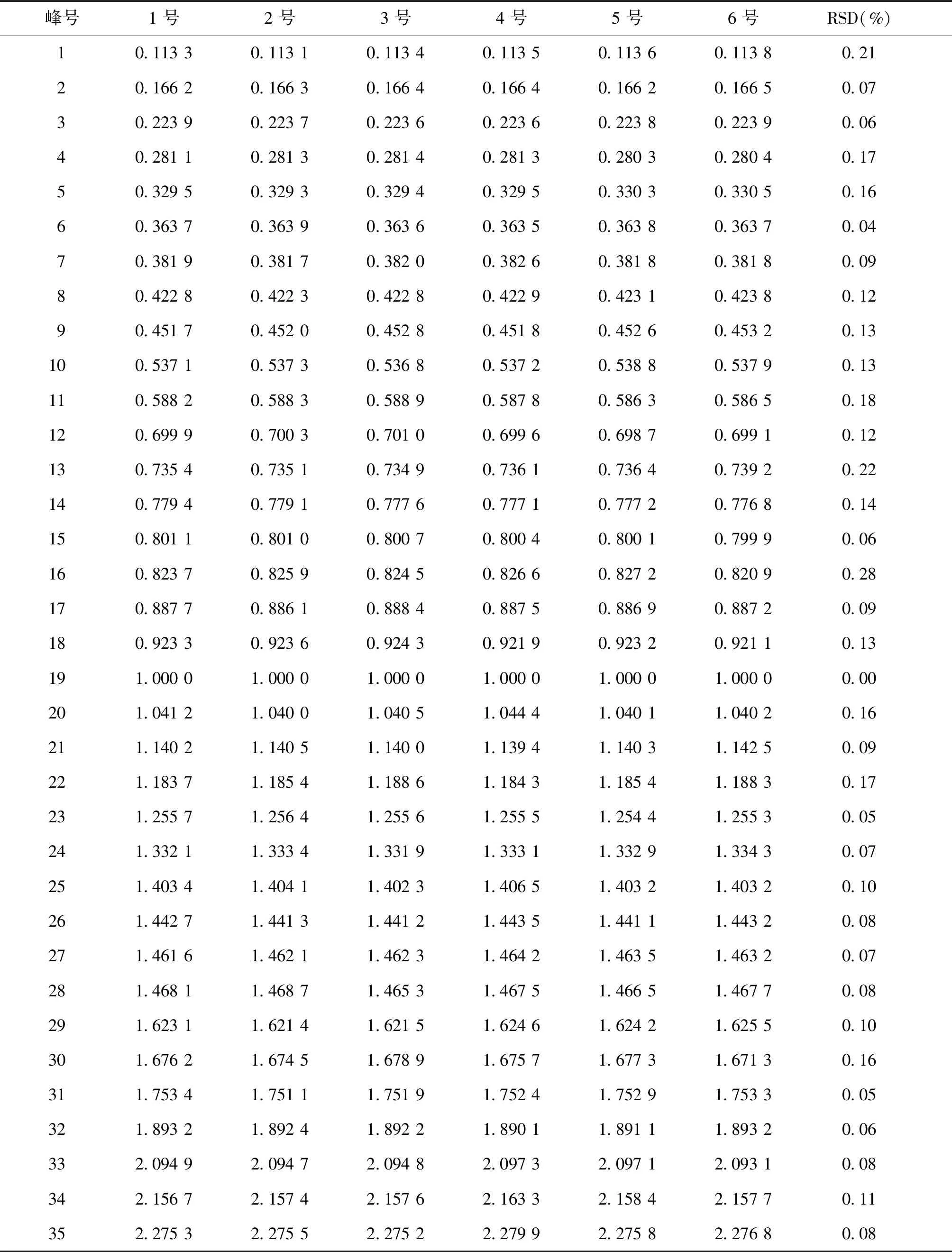
表6 菖远胶囊指纹图谱重复性的相对保留时间结果
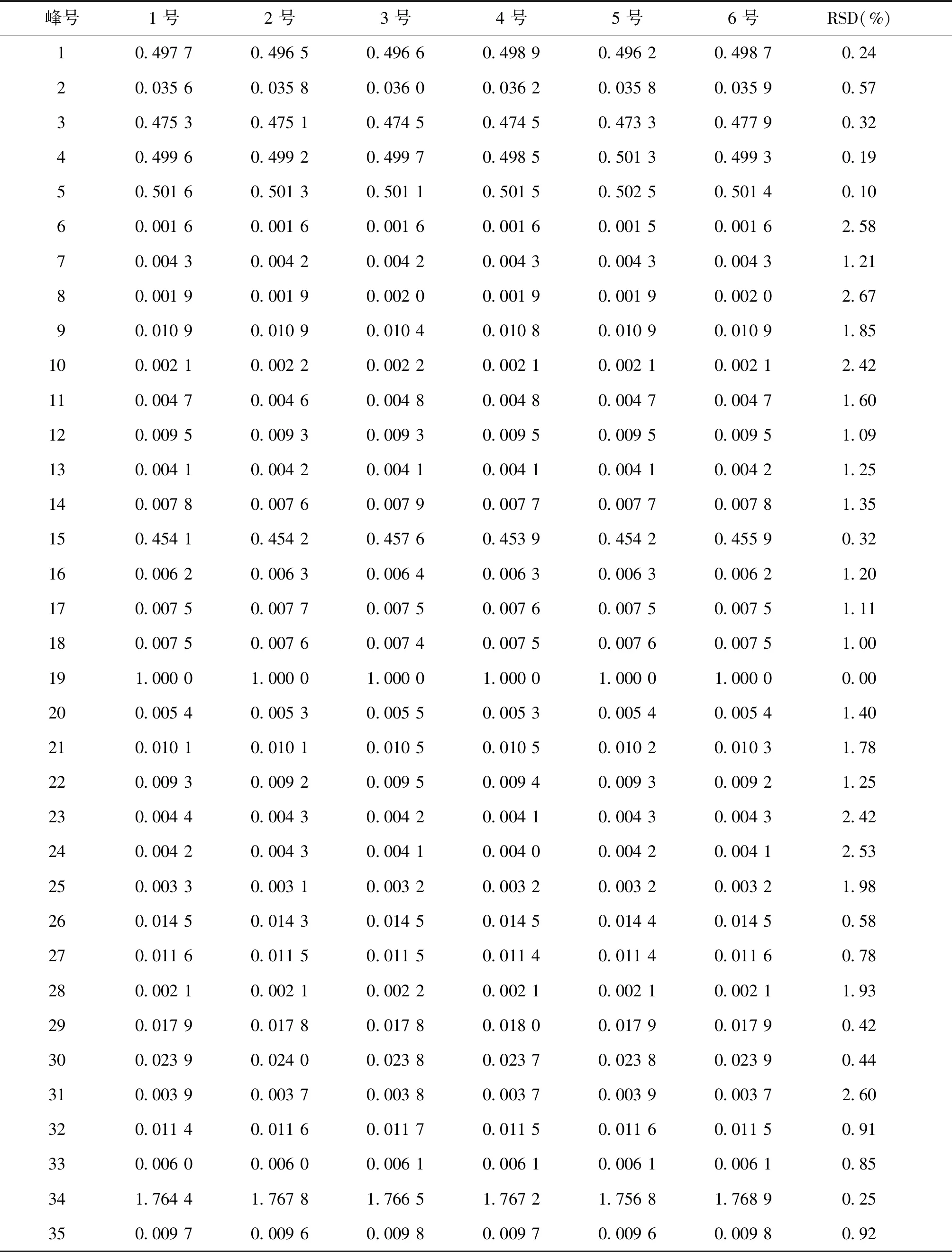
表7 菖远胶囊指纹图谱重复性的相对峰面积的结果
2.1.4 指纹图谱的建立及相似度分析 建立了指纹图谱,结果见图1,以峰19(丹酚酸B)为参比峰,标定了35个特征峰。10批样品共有色谱峰的相对保留时间与相对峰面积的RSD值均分别小于2.0%、3.0%(见表8,9)。10批菖远胶囊的指纹图谱进行相似度分析结果见表10,相似度在0.956-0.995之间。

表8 10批菖远胶囊的相对保留时间结果
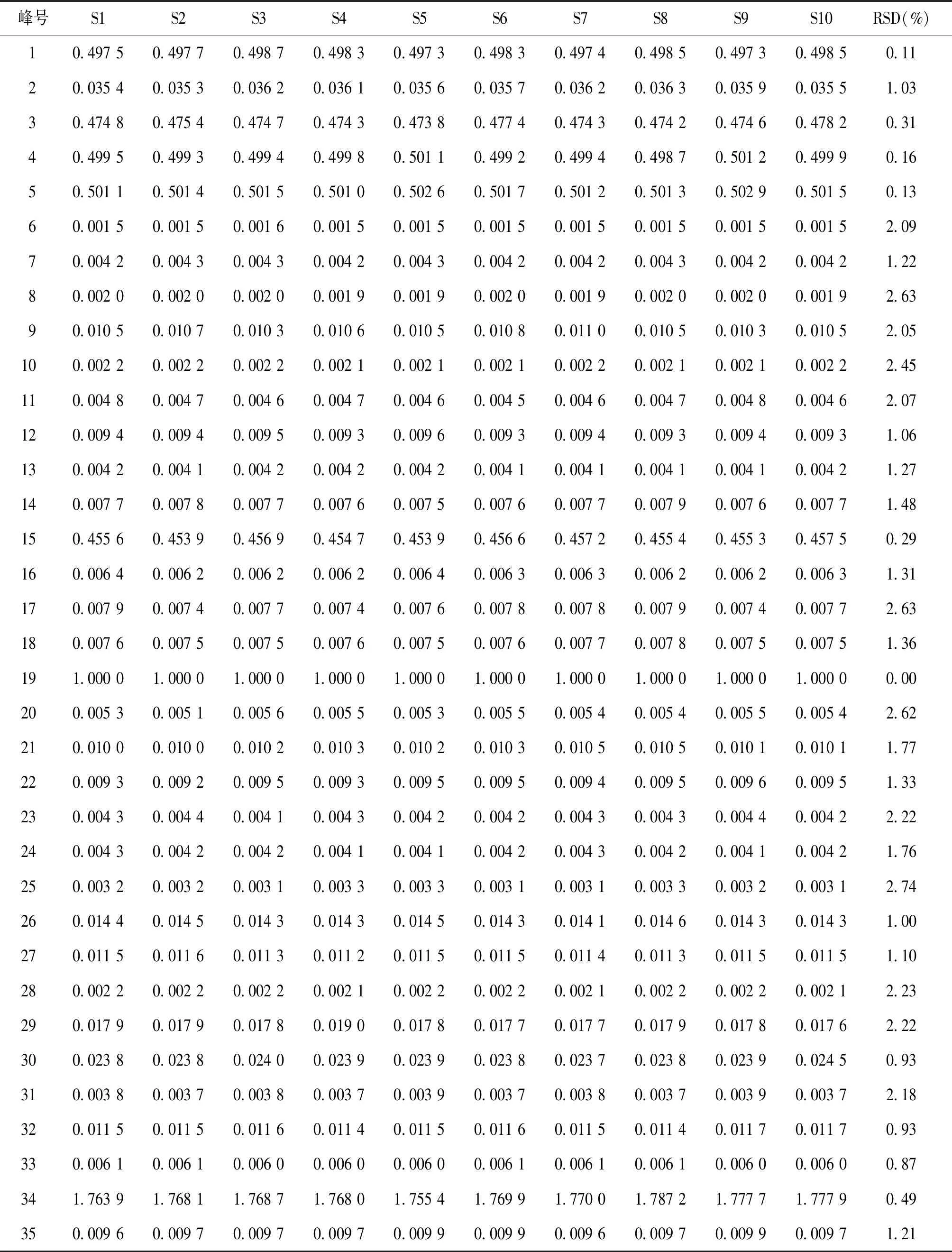
表9 10批菖远胶囊的相对峰面积

表10 10批相似度结果
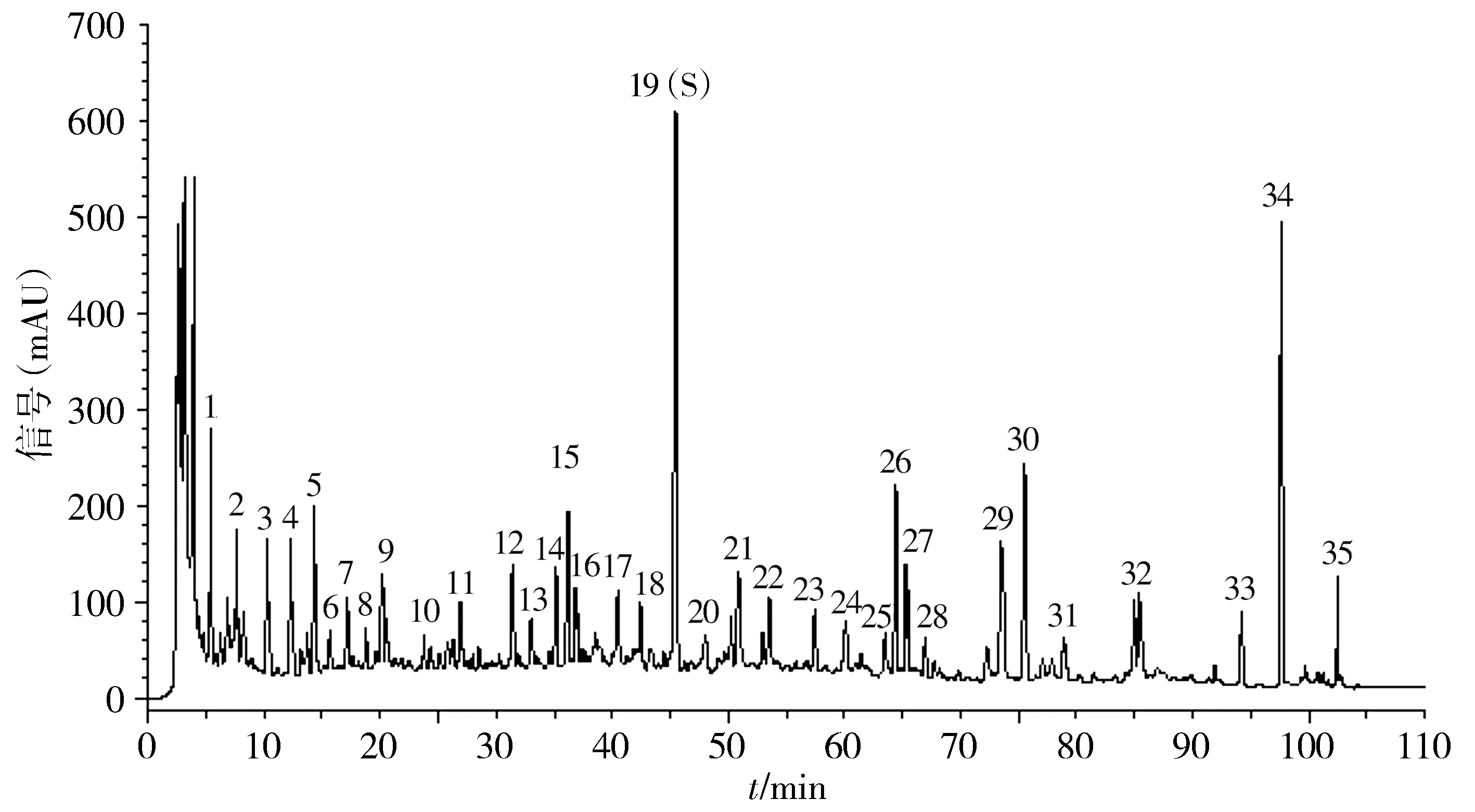
1-35.特征指纹峰;4.梓醇;19.丹酚酸B(作为参照物的色谱峰);26.人参皂苷Rg1;27.人参皂苷Re;30.人参皂苷Rb1;34.细叶远志皂苷图1 菖远胶囊HPLC指纹图谱Figure 1 HPLC fingerprint of Changyuan capsules
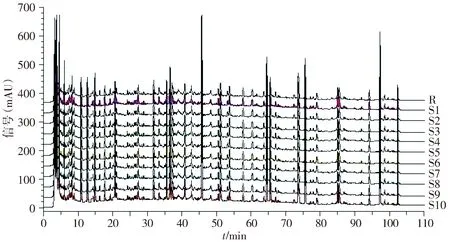
R.10批拟合指纹图谱;S1.生产批号20190612;S2.生产批号20190613;S3.生产批号20190614;S4.生产批号20190615;S5.生产批号20190709;S6.生产批号20190710;S7.生产批号20190711;S8.生产批号:20190806;S9.生产批号:20190807;S10.生产批号20190808图2 10批菖远胶囊的HPLC指纹图谱Figure 2 HPLC fingerprint of 10 batches of Changyuan capsules
2.2 含量测定
2.2.1 线性关系 对照品的线性方程结果见表11,表明各对照品在相应浓度范围内线性关系良好。
2.2.2 专属性试验 阴性对照均无干扰,专属性强(见图3)。

表11 对照品的线性方程及其浓度范围

1.梓醇;2.丹酚酸B;3.人参皂苷;4.人参皂苷;5.人参皂苷;6.细叶远志皂苷图3 混合对照品、供试品与阴性对照HPLC图谱Figure 3 HPLC chromatograms of mixed reference, test sample of Changyuan capsule and negative control sample
2.2.3 精密度试验 测得梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和细叶远志皂苷的相对标准差(RSD)分别为0.93%,0.98%,1.03%,0.92%,0.97%,1.01%,表明该方法精密度良好。
2.2.4 稳定性试验 测得梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和细叶远志皂苷的峰面积的RSD值分别为0.69%,0.72%,0.99%,0.86%,0.92%,0.98%,表明该溶液在24 h内稳定性良好。
2.2.5 重复性试验 测得梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和细叶远志皂苷平均含量与RSD值分别见表12,表明该方法具有良好重复性。

表12 重复性测定结果
2.2.6 加样回收率试验 测得梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和细叶远志皂苷的平均回收率与RSD值分别见表13,表明该方法回收率良好。

表13 加样回收率测定结果

续表13 加样回收率测定结果
2.2.7 含量测定 各批样品中梓醇、丹酚酸B、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和细叶远志皂苷的平均含量(mg/g)、RSD见表14。
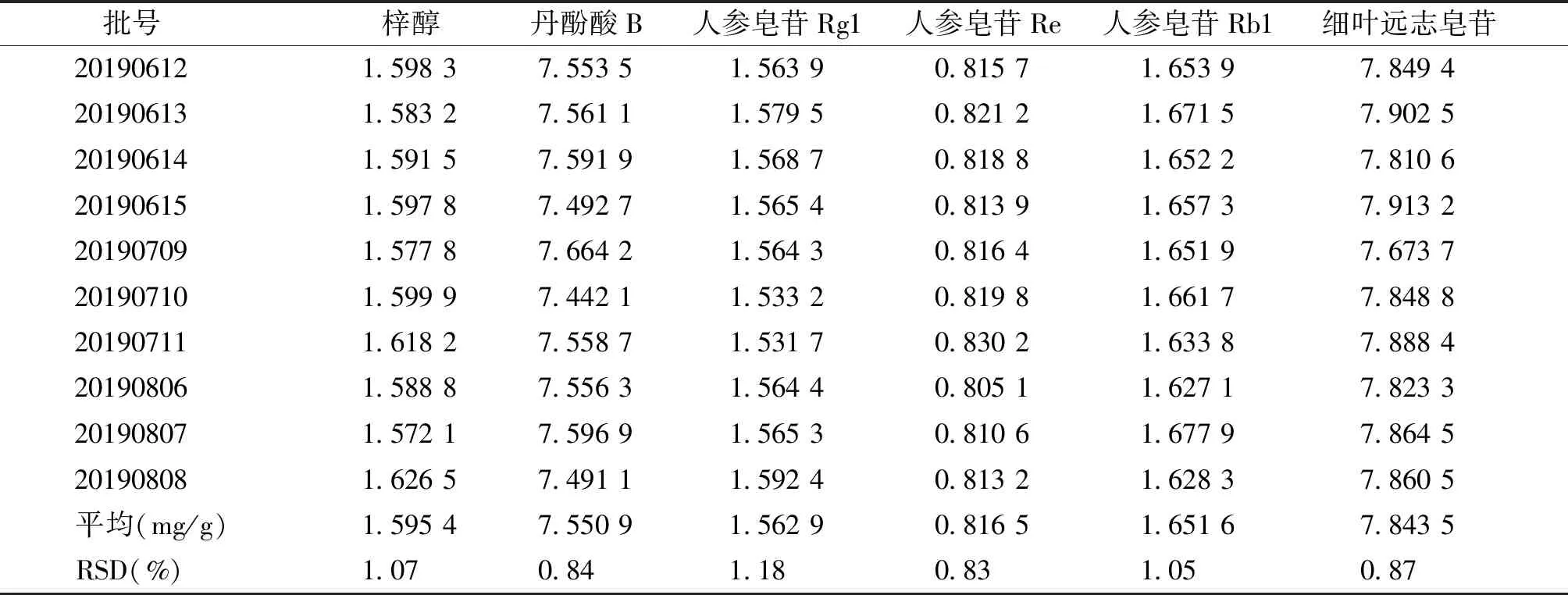
表14 菖远胶囊6个成分含量测定结果 (n=3,mg/g)
3 讨论
采用二极管阵列检测器全波长对菖远胶囊样品进行测定,结果203 nm时信息量较多。检测示6个各成分的最大吸收梓醇为210 nm,丹酚酸B为286 nm,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1均为203 nm,细叶远志皂苷为210 nm,结果在203 nm情况下,6个成分分离度符合要求,阴性对照均无干扰;在286 nm情况下,丹酚酸B分离度符合要求,阴性对照也无干扰,但考虑到所用检测设备HPLC必须配备二极管阵列检测器或多波长检测器,这对企业增加了成本或不必要的检测障碍,因此,选用简单、方便、易于实现的检测条件即选用203 nm作为指纹与定量的检测波长。
由于中药复方中成分复杂,等度洗脱难以充分分离各种成分,所以采用梯度洗脱的方法。对不同流动相系统乙腈-磷酸水溶液、乙腈-水、甲醇-水、乙腈-醋酸水溶液等进行比较,结果显示,乙腈-0.1%磷酸水溶液流动相理想。本制剂为胶囊剂,主要分析水溶性成分,所以比较使用0、30%、50%、70%、100%甲醇作为溶剂,采用不同时间超声处理方法(5,10,20,25,40,50,60 min)或加热回流,结果发现,加50%甲醇超声30 min较理想。对不同柱温与流速进行比较,柱温超过或低于30 ℃,大部分色谱峰分离度小或不能分开;流速高于或低于0.8 ml/min,大部分色谱峰分离度差;色谱记录时间,在110 min之后,无色谱峰出现。因此,选择柱温为30 ℃,记录时间为110 min,流速为0.8 ml/min。
综上所述,通过对10批次的菖远胶囊样品进行相似度计算,结果数值介于0.956-0.995。同时6种成分定量结果含量均一稳定,表明笔者建立的菖远胶囊的HPLC指纹图谱方法及定量方法具有简便、稳定可靠、重复性好等优势。因此,该方法可作为本制剂质量有效评价的方法,同时亦为临床疗效提供了理论依据。
