基于数据驱动和机制模型的丹参提取动力学研究
2022-01-13陈泽麒谢欣媛陈思铭瞿海斌
陈泽麒,谢欣媛,陈思铭,傅 豪,瞿海斌*
基于数据驱动和机制模型的丹参提取动力学研究
陈泽麒1, 2,谢欣媛1, 2,陈思铭1, 2,傅 豪1, 2,瞿海斌1, 2*
1. 浙江大学药学院,药物信息学研究所,浙江 杭州 310058 2. 组分中药国家重点实验室 浙江大学交叉创新中心,浙江 杭州 310058
获取丹参提取过程知识,提高丹参提取工艺质量控制水平。基于数据驱动和机制模型考察丹参提取过程中丹酚酸的转移、转化规律。首先基于机制模型,获得不同工艺条件下丹酚酸的提取动力学参数,再通过响应曲面法建立工艺参数与提取动力学参数间关系。建立了丹酚酸B(salvianolic acid B,SAB)、丹酚酸E(salvianolic acid E,SAE)、紫草酸(lithospermic acid,LA)、丹酚酸A(salvianolic acid A,SAA)和丹参素(salvianic acid,DSS)5个成分的提取动力学模型。模型验证结果丹酚酸B、丹酚酸E、紫草酸、丹酚酸A和丹参素峰面积的预测平均绝对偏差分别为151.85、27.76、19.46、214.61、105.68,表明模型预测性能较好。揭示了丹参提取过程原料属性、工艺参数、产品质量属性间关系,为丹参提取过程质量控制提供了理论知识。
数据驱动;机理模型;丹参;提取;动力学模型;丹酚酸;紫草酸;丹参素
通过过程建模明确原料属性、工艺参数、产品质量属性之间关系,构建出反映工艺过程变化特征及其对质量影响的数学模型,从而获取中药生产过程知识,是实现中药生产过程控制的基础[1-2]。
工业过程建模主要包括机制建模、统计建模和混合建模3种。机制建模是通过分析工业过程中相关物理化学现象的机制来建立数学模型的方法,该方法可精确反映系统内部的运行机制以及输入输出关系,但是需要对工业过程相关物理化学现象具有深刻认识[3-4]。统计建模是通过统计方法或者机器学习算法,分析工业过程采集到的数据从而建立模型的方法,又可称为“黑箱模型”,该方法不需要对过程有深入理解,但是建立的模型反映的过程信息较少[1]。混合建模[5]通过结合机制建模和统计建模,可较好地提高模型有效性,避免模型过于复杂。
丹参已被制成各种中药剂型,广泛用于冠心病、心绞痛、心肌梗塞、脑血栓等疾病的治疗及辅助治疗[6-8]。但是,现阶段丹参制剂产品质量波动大,如何保证丹参制剂产品质量一致性,从而确保丹参制剂产品疗效是目前亟需解决的问题。丹参提取工艺是丹参制剂产品生产的重要操作单元,通过对丹参提取工艺模型化研究可提高丹参提取液质量,从而提高丹参制剂产品的质量和临床效果[9]。现阶段,丹参提取过程中丹酚酸的传质[10-12]和降解规律[13-14]已经有了较多的研究基础,但是提取过程工艺参数对丹酚酸传质和降解的影响机制仍不明确。因此,本研究采用混合建模方法,以已有的丹参提取过程动力学研究为基础,推导出丹参提取机制模型,用于解释丹酚酸在丹参提取过程的转移、转化规律,并基于实验数据拟合不同工艺参数下的丹酚酸提取动力学参数,再通过响应曲面法[15]考察丹参提取工艺参数同丹酚酸提取动力学参数间的定量关系,最终建立包含原料属性和工艺参数信息的丹参提取动力学模型。
1 提取动力学模型推导
1.1 传质过程
根据作者之前的研究结论[10],丹酚酸B的传质模型如公式(1)所示,而经丹酚酸B降解得到的系列产物在较高温度下的传质速率要远大于降解速率,因此可忽略传质阻力的影响,得降解产物的传质模型如公式(2)所示。
dL/d=aS/[L(1/S+/L)]+(L+S)L/[L(1/S+/L)] (1)
L=S/(S+L) (2)
L为提取溶剂中目标成分含量(含量用液相峰面积表示),S为提取体系中时刻目标成分的总量(无量纲),为药材比表面积,L为提取过程提取溶剂体积(液相体积),S为药材吸水膨胀后体积(固相体积),为平衡常数(无量纲),S为药材内传质系数,L为药材外传质系数
1.2 降解过程
丹参药材中主要的酚酸类成分为丹酚酸B。在提取过程中,丹酚酸B会发生复杂降解反应生成系列产物[14]。丹酚酸B主要的降解产物为丹酚酸E、紫草酸、丹酚酸A和丹参素[14],其主要降解路径如图1所示。
已知,酚酸类成分降解属于一级降解动力学过程[16],体系中丹酚酸B、丹酚酸E、紫草酸、丹酚酸A和丹参素5个成分的含量随时间的变化规律如下。
dS丹酚酸B/d=−S丹酚酸B丹酚酸B(3)
dS丹酚酸E/d=S丹酚酸B1-S丹酚酸E丹酚酸E(4)
dS紫草酸/d=S丹酚酸B2-S紫草酸紫草酸(5)
dS丹酚酸A/d=S紫草酸3(6)

图1 提取过程丹酚酸B主要降解路径[14]
dS丹参素/d=S丹酚酸B4+S丹酚酸E5(7)
丹酚酸B、丹酚酸E、紫草酸依次为丹酚酸B、丹酚酸E和紫草酸的降解速率常数,1为单位丹酚酸B降解生成单位丹酚酸E速率常数,2为单位丹酚酸B降解生成单位紫草酸速率常数,3为单位紫草酸降解生成单位丹酚酸A速率常数,4为单位丹酚酸B降解生成单位丹参素速率常数,5为单位丹酚酸E降解生成单位丹参素速率常数
整理积分公式(3)~(7)得提取体系中丹酚酸B、丹酚酸E、紫草酸、丹酚酸A和丹参素5个成分含量的计算公式。由于,药材中主要酚酸成分为丹酚酸B[17],因此忽略初始时刻药材中丹酚酸E、紫草酸、丹酚酸A和丹参素含量。
S丹酚酸B=0丹酚酸Bexp(−丹酚酸B) (8)
S丹酚酸E=0丹酚酸B1/(丹酚酸B-丹酚酸E)[exp(−丹酚酸E)-exp(−丹酚酸B)] (9)
S紫草酸=0丹酚酸B2/(丹酚酸B-紫草酸)[exp(−紫草酸)-exp(−丹酚酸B)] (10)
S丹酚酸A=0丹酚酸B23/[紫草酸(丹酚酸B-紫草酸)][1-exp(−紫草酸)]-0丹酚酸B23/[丹酚酸B(丹酚酸B-紫草酸)][1-exp(−丹酚酸B)](11)
S丹参素={0丹酚酸B4/丹酚酸B-0丹酚酸B15/[丹酚酸B(丹酚酸B-丹酚酸E)]}[1-exp(−丹酚酸B)]+0丹酚酸B15/[丹酚酸E(丹酚酸B-丹酚酸E)]}[1-exp(−丹酚酸E)] (12)
0丹酚酸B为初始时刻药材中丹酚酸B含量,下标中丹酚酸B、丹酚酸E、紫草酸、丹酚酸A和丹参素代表该物理量分别属于丹酚酸B、丹酚酸E、紫草酸、丹酚酸A和丹参素
1.3 提取动力学模型
将公式(8)代入公式(1),公式(9)~(12)代入公式(2),得丹酚酸B、丹酚酸E、紫草酸、丹酚酸A和丹参素的提取动力学模型,依次为公式(13)~(17)。
S丹酚酸B=/(-丹酚酸B)[ exp(−)+exp(−丹酚酸B)](13)
S丹酚酸E=[0丹酚酸Bexp(−丹酚酸E)-exp(−丹酚酸B)]/[V(丹酚酸B-丹酚酸E)] (14)
S紫草酸=[0丹酚酸Bexp(−紫草酸)-exp(−丹酚酸B)]/[V(丹酚酸B-紫草酸)] (15)
S丹酚酸A=0丹酚酸B{[exp(−紫草酸)-1]/紫草酸-[exp(−丹酚酸B)-1]/丹酚酸B}/[V(紫草酸-丹酚酸B)] (16)
S丹参素=0丹酚酸B[1-exp(−丹酚酸E)]/(V丹酚酸B)+0丹酚酸B{[1-exp(−丹酚酸E)]/丹酚酸E-[1-exp(−丹酚酸B)]/丹酚酸B}/ [V(丹酚酸B-丹酚酸E)] (17)
其中,~为丹酚酸动力学模型参数,与温度、pH和氮气流量相关。
=0丹酚酸B/(丹酚酸BV)
=(V+V丹酚酸B)/(丹酚酸BV)
=1V/(V丹酚酸E+V)
=2V/(V紫草酸+V)
=23V/(V丹酚酸A+V)
=4V/(V丹参素+V)
=15V/(V丹参素+V)
此外,本研究进一步通过响应曲面法[15]建立工艺参数与丹酚酸动力学模型参数间的定量关系,模型形式如公式(18)所示。
lg=0+aX+aX2+aXX(18)
为各丹酚酸动力学模型参数,1为温度倒数,2为pH值,3为氮气流量,0为常数项,为回归系数
2 仪器与试剂
2.1 仪器
XS105、AB204-N型电子分析天平,梅特勒-托利多上海有限公司;SE6001型电子天平,奥豪斯仪器有限公司;Milli-Q型超纯水机,美国Millipore公司;DF-101S型集热式恒温加热磁力搅拌器,河南予华仪器有限公司;Centrifuge 5424型高速离心机,德国Eppendorf公司;SHA-B型恒温振荡器,上海力辰仪器科技有限公司;Agilent 1260型高效液相色谱仪,配四元梯度泵、自动进样器、柱温箱、紫外检测器、ChemStation工作站,美国Agilent科技有限公司。
2.2 试剂
丹参药材由正大青春宝药业有限公司提供,经浙江大学药物信息学研究所潘坚扬高级实验师鉴定,为唇形科鼠尾草属植物丹参Bge.的干燥根和根茎;一水合柠檬酸(批号20200721)、无水磷酸氢二钠(批号20181025),分析纯,均购自国药集团化学试剂有限公司;乙腈、甲醇,色谱纯,质量分数≥99%,均购自德国Merck公司;甲酸,色谱纯,质量分数≥99%,购自Roe Scientific公司;超纯水由Milli-Q型超纯水机制备得到;氮气,质量分数≥99%,购自杭州今工物资有限公司。
3 方法
3.1 色谱条件[18]
液相分离采用Waters Cortecs C18色谱柱(100 mm×4.6 mm,2.7 μm);流动相为0.4%甲酸水溶液(A)-0.4%甲酸乙腈溶液(B),线性洗脱程序:0~14 min,2%~11% B;14~29 min,11%~15% B;29~52 min,15%~20% B;52~60 min,20%~21% B;60~67 min,21%~40% B;67~68 min,40%~88% B;紫外检测波长280 nm;体积流量0.8 mL/min;进样量3 μL;柱温25 ℃。
3.2 丹参药材中丹酚酸B含量测定
参考《中国药典》2020年版方法[19],精密称取150.0 mg丹参粉末(过60目筛)于100 mL具塞锥形瓶中,精密加入80%甲醇水溶液50 mL,密塞,超声处理(功率140 W、频率42 kHz)30 min,放冷,用80%甲醇水溶液补足损失的质量,摇匀,滤过,取续滤液,用80%甲醇水溶液稀释1倍后按“3.1”项下色谱条件测定样品中丹酚酸B含量。
3.3 提取体系两相体积测定
准确称取15 g丹参药材于250 mL锥形瓶中,分别加入200 mL纯净水,恒温静置,充分浸泡吸水(浸泡时间大于12 h)后滤过,用滤纸吸干药材表面水分后称量得湿药材质量,并用体积法测量湿药材体积[20]。根据吸水后药材体积、质量和干药材质量比值(依次为和)计算固相体积(S)和液相体积(L)。
S=(19)
L=-(-)(20)
为单次提取所需水的体积;为水的密度,近似为1 g/mL
3.4 丹参提取工艺
基于作者之前的研究结果[8],温度和搅拌对丹参提取过程存在显著影响。此外已有研究表明[21-23],pH值对丹酚酸降解影响非常显著,因此本研究重点考察温度、pH值、搅拌对丹参提取动力学模型参数的影响。根据之前实验发现,提取过程长时间搅拌会对药材造成破坏,从而影响药材比表面积,因此以通氮气方式替代搅拌桨搅拌。采用D-最优实验设计进行丹参提取工艺研究,具体实验条件见表1。丹参提取工艺操作流程:量取600 mL一定pH值的磷酸氢二钠-柠檬酸缓冲液于1000 mL三颈烧瓶中,将缓冲液预热至设定的提取温度后加入50 g预先切成小段的丹参药材进行回流提取并打开氮气阀门,往三颈烧瓶底部通氮气,通过流量计控制氮气流量。每隔一定时间取样,取样量约为1 mL,取出后用冰箱迅速冷却后按“3.1”项下色谱条件测定样品中丹酚酸含量。
3.5 数据处理
本研究采用平均绝对偏差[11](average absolute deviation,AAD)评估模型性能,其计算公式如下所示。
表1 丹参提取工艺参数D-最优实验设计和拟合结果
Table 1 D-optimal experimental design and fitting results of SMRR extraction process
序号温度/KpH值氮气流量/(L∙min−1)lgk丹酚酸BlgAlgBlgk丹酚酸ElgClgk紫草酸lgDlgElgFlgG 1363.153.60.5−3.7952.021−2.030−2.726−4.524−2.204−3.553−5.762−4.096− 2353.156.00.5−3.4931.911−2.216−3.914−3.799−2.782−3.785−6.713−4.360−8.124 3353.156.61.5−3.1121.910−2.223−5.000−3.418−2.809−3.723−6.642−4.358−7.139 4353.156.60.5−3.2111.926−2.147−5.000−3.367−2.721−3.727−6.593−4.288−7.343 5363.154.81.5−3.5572.054−2.051−2.914−4.137−2.332−3.554−5.794−4.042− 6373.153.61.5−3.2812.152−1.927−2.473−4.139−2.029−3.436−5.222−3.779− 7353.153.61.0−−−−−−−−−− 8353.153.61.5−4.4381.883−2.234−3.124−5.199−2.648−3.817−6.877−4.487− 9363.156.61.0−2.6282.136−1.849−2.820−2.813−2.324−3.449−5.670−3.976−6.160 10353.154.20.5−4.0631.860−2.257−3.149−4.893−2.674−3.801−6.780−4.474− 11373.153.60.5−3.1422.160−1.921−2.474−4.165−2.017−3.410−5.228−3.816− 12373.156.60.5−2.3332.209−1.615−2.443−2.545−1.942−3.320−4.966−3.775−5.493 13363.155.41.0−3.3542.084−2.049−3.169−3.810−2.379−3.534−5.837−4.040−8.125 14373.156.61.5−2.3422.293−1.654−2.498−2.511−2.000−3.259−5.027−3.772−5.520 15373.154.81.0−3.1012.160−1.922−2.577−3.795−2.065−3.411−5.219−3.805−7.154 16363.155.41.0−3.2982.123−2.016−3.019−3.754−2.344−3.498−5.783−4.021−7.804 17363.155.41.0−3.270−2.044−2.059−3.048−3.742−2.344−3.539−5.705−4.006−7.634
AAD=(∑|pre-exp|)/(21)
pre和exp分别代表提取液中各丹酚酸峰面积的预测值和测量值,为目标成分建模样本数
实验设计以及响应曲面法分析使用MODDE Pro 11.0.1(MKS Umetrics,Sweden)软件完成,其余所有计算程序使用Matlab R2019b(美国Math Works公司)编写。
4 结果
4.1 模型参数
4.1.1 丹参药材中丹酚酸B含量 根据3次重复测量结果,单位质量丹参药材中丹酚酸B峰面积(0丹酚酸B)为(74 116 277±519 642)/g。
4.1.2 两相体积 根据3次重复测量结果,得吸水后药材体积对干药材质量比值()为2.61±0.04,吸水后药材质量对干药材质量比值()为2.78±0.02。根据公式(19)和公式(20)计算得V=130.5 mL,V=511.0 mL。
4.2 丹酚酸动力学模型参数拟合
根据实验数据,拟合得到各组丹酚酸动力学模型参数结果见表1。组1~3、组10~12提取缓冲液pH值和温度均较低,丹酚酸E含量非常小,模型参数拟合误差大,因此除去。组7因实验过程异常断电导致数据异常而舍去。
4.3 响应曲面法分析
根据表1中拟合结果,采用MODDE软件建立模型参数与工艺参数间的回归模型。经模型显著性分析,各回归系数、值及2见表2。各酚酸动力学参数的预测模型2均大于0.904,说明模型可以很好的解释工艺参数和动力学模型参数间的定量关系。氮气流量回归系数的值均大于0.05,表明氮气流量对各动力学模型参数影响均不显著。
各丹酚酸动力学模型参数等高线图见图2,丹酚酸B、丹酚酸E和紫草酸化学结构式见图3。在实验条件范围内,丹酚酸动力学参数与1/呈负相关,表明酚酸动力学模型参数均随温度升高而升高,这与实际动力学情况相符;lg丹酚酸B、lg、lg与pH值呈正相关,表明pH值升高可以加快丹酚酸B降解生成丹酚酸E和紫草酸,这与丹酚酸B的酯键与呋喃环水解受碱催化有关,其中pH值对lg的影响较lg显著,表明丹酚酸B的呋喃环水解更易受pH值影响;lg、lg、lg与pH值呈正相关,表明随pH值升高丹酚酸A和丹参素生成速率均会升高;lg丹酚酸E和lg紫草酸在较低温度下与pH值呈负相关,推测其主要发生受酸催化的脱羧反应,但是丹酚酸E的降解速率要远小于紫草酸的降解速率,表明丹酚酸A主要由紫草酸降解生成;lg丹酚酸E和lg紫草酸在较高温度下与pH值呈正相关,推测可能为1号位酯键(图3)空间位阻小,所以结构较为稳定,在较高温度下才易发生水解有关,这也表明丹酚酸B主要降解路径为呋喃环和2号位酯键的水解生成紫草酸和丹酚酸E。此外,随着pH值增加,lg和lg也有明显增加,即传质速率会增加,推测可能为pH缓冲液对丹参药材表面存在一定程度破坏作用。
表2 酚酸动力学模型参数方差分析结果
Table 2 ANOVA results of phenolic acid kinetic model parameters
模型参数常数项1/TpH1/T2pH2pH/TR2 lgk丹酚酸B14.243 (0.000)−6 320.120 (0.000)−0.445 (0.000)−0.077 (0.008)−0.976 lgA7.492 (0.000)−2 025.370 (0.000)0.028 (0.001)−−−0.949 lgB−2.036 (0.000)206.608 (0.000)1.294 (0.000)−0.034 (0.001)−574.747 (0.000)0.980 lgk丹酚酸E−36.440 (0.000)12 580.100 (0.000)11.440 (0.001)−−−4 245.130 (0.001)0.904 lgC9.751 (0.000)−5 998.230 (0.000)0.573 (0.000)−−−0.977 lgk紫草酸4.183 (0.000)−2 335.260 (0.000)1.216 (0.092)−−−447.987 (0.012)0.980 lgD3.835 (0.000)−2 749.920 (0.000)0.036 (0.000)−−−0.965 lgE−173.562 (0.000)132 139.000 (0.000)0.067 (0.000)−25 902 300 (0.000)−−0.994 lgF6.694 (0.000)−4 075.500 (0.000)0.156 (0.011)−−0.012 (0.008)−0.962 lgG89.346 (0.000)−37 551.500 (0.000)−9.325 (0.000)−−3 809.580 (0.013)0.959
括号内为各回归系数相应的值,“−”处代表该因子对模型的影响不显著
the parentheses are the correspondingvalues of each regression coefficient, “−” indicates the corresponding item with no significance
根据响应曲面法所得的模型预测曲线与实测值关系图见图4,从图中可以发现组6、9、14的丹酚酸B、丹酚酸E和丹参素(负值)拟合结果极差,主要原因为此3组温度和pH值均较大,体系中丹酚酸降解极快,酯键或呋喃环水解会产生明显逆反应。由于所推导的动力学模型未包含逆反应过程,因此剔除上述3组数据后进一步优化动力学参数回归模型。
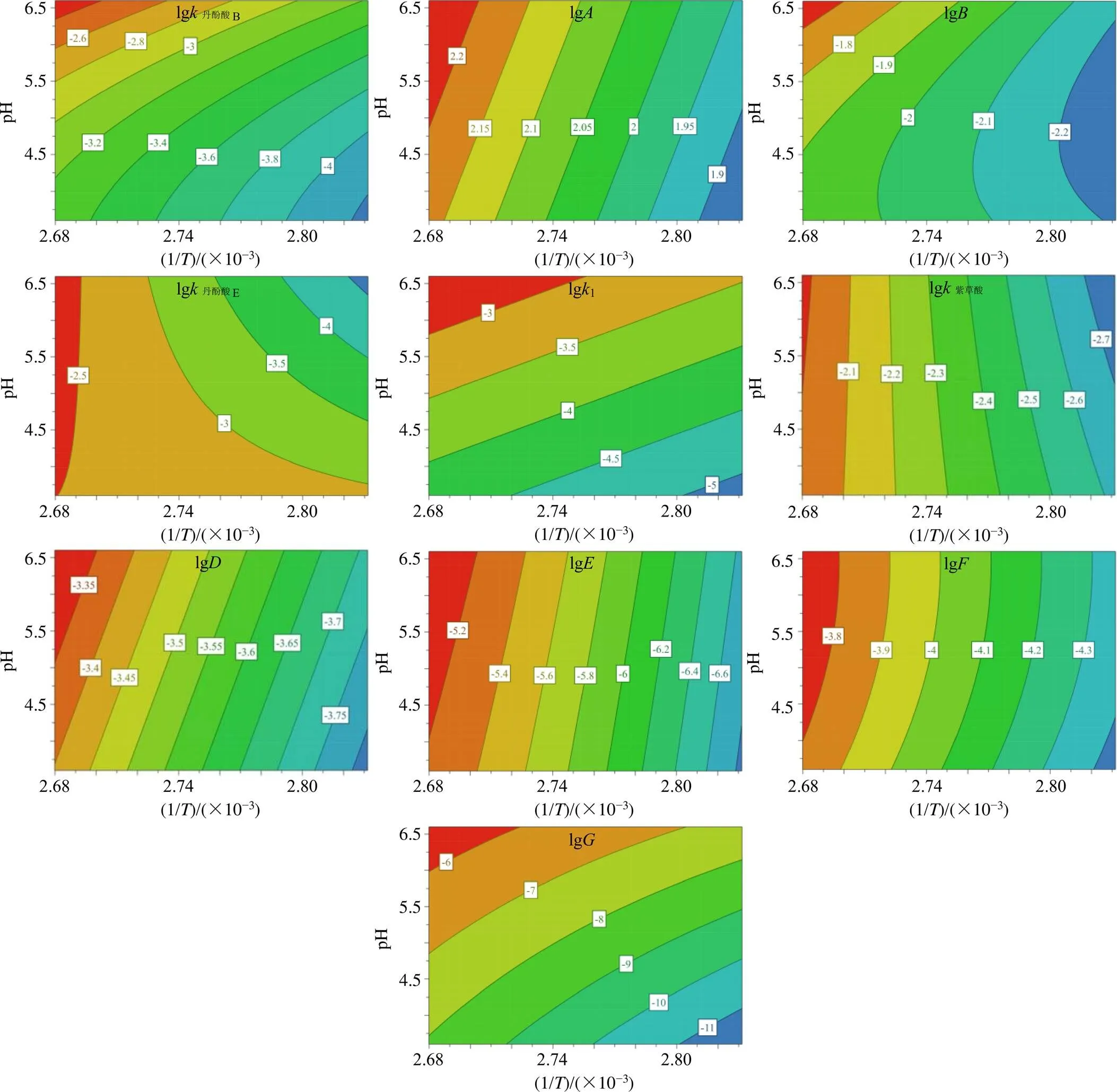
图2 丹酚酸动力学模型参数等高线图

①-1号位酯键 ②-2号位酯键 ③-呋喃环

图4 酚酸动力学模型预测值与实测值
4.4 回归系数优化
剔除3组(组6、9、14)数据后,选择组1~5、8、10、11、13、15~17为建模组,以“4.3”项下回归系数拟合结果作为初始值,基于建模组数据,利用Matlab R2019b中lsqcurvefit函数优化回归系数,并以组12数据对优化后结果进行验证,优化后的回归系数如表3所示。经优化后的模型预测曲线与实测值关系见图5,与响应曲面法获得的结果相比,丹酚酸B、丹酚酸E、丹酚酸A和丹参素预测效果有了明显改善。利用公式(21)计算丹酚酸B、丹酚酸E、紫草酸、丹酚酸A、丹参素峰面积的平均绝对偏差,结果分别为299.00、120.24、33.06、164.72、42.97。平均绝对偏差值较小,表明实测值和预测值非常接近,动力学模型预测性能良好。
4.5 模型验证
利用验证组(组12)对建立好的丹参提取动力学模型进行验证,结果如图6所示。表4中列出了验证组丹酚酸的平均峰面积和模型预测的平均绝对偏差。根据预测结果可知,模型预测值的平均绝对偏差较小,实测值和预测值基本符合,表明本研究建立的丹参提取动力学模型具有较好的预测能力。
5 讨论
本研究基于数据驱动和机理模型方法考察丹参提取过程中丹酚酸的转移、转化规律。通过响应曲面法分析发现,温度和pH值对丹酚酸传质和降解均存在显著影响,而氮气流量对丹酚酸提取过程并无显著影响。温度和pH值同酚酸降解动力学参数间的关系表明,在本实验工艺范围内,丹酚酸B主要的降解位点为1号位酯键和呋喃环,丹酚酸E和紫草酸主要发生脱羧反应,丹酚酸A主要由紫草酸降解生成,间接证明本研究所用丹酚酸B降解网络的合理性。最后,对优化后的丹酚酸动力学模型进行验证,结果表明模型具有较好的预测精度,能够反映丹酚酸B、丹酚酸E、紫草酸、丹酚酸A和丹参素含量的变化规律。
表3 回归系数优化结果
Table 3 Optimized results of regression coefficients
模型参数常数项1/TpH1/T2pH2pH/T lgk丹酚酸B17.242−7 014.186−1.018−0.146− lgA7.607−2 043.8050.015−−− lgB8.148−3 785.927−0.863−−0.014355.184 lgk丹酚酸E−84.19028 628.94623.242−−8 283.846− lgC10.570−6 730.1720.780−−− lgk紫草酸11.161−4 833.202−0.279−−86.446 lgD4.008−2 816.8200.040−−− lgE−150.027114 827.2200.021−22 692 084−− lgF8.571−4 172.028−0.587−0.069− lgG96.846−41 016.786−11.207−−4 571.111

图5 优化后的酚酸动力学模型预测值与实测值
本研究通过建立丹酚酸提取过程动力学模型,揭示了丹参药材属性、提取工艺参数和丹酚酸含量之间的关系,加深了对丹参提取过程的理解,为丹参提取过程质量控制奠定了基础。此外,基于数据驱动的动力学参数拟合方法无需提供初始值便可快速获得较优的结果,适合于动力学模型复杂,参数繁多且缺乏深入理解的过程建模。

图6 验证组预测结果
表4 验证组丹酚酸类成分的平均峰面积和模型预测平均绝对偏差
Table 4 Average peak area and average absolute deviation of salvianolic acid in validation group
成分平均峰面积平均绝对偏差丹酚酸B9 109.97151.85丹酚酸E465.6027.76紫草酸785.9419.46丹酚酸A1 631.51214.61丹参素647.29105.68
利益冲突 所有作者均声明不存在利益冲突
[1] 熊皓舒, 田埂, 刘朋, 等. 中药生产过程质量控制关键技术研究进展 [J]. 中草药, 2020, 51(16): 4331-4337.
[2] 程翼宇, 钱忠直, 张伯礼. 创建以过程管控为核心的中药质量控制技术体系 [J]. 中国中药杂志, 2017, 42(1): 1-5.
[3] Chen J Y, Gui W H, Dai J Y,. A hybrid model combining mechanism with semi-supervised learning and its application for temperature prediction in roller hearth kiln [J]., 2021, 98: 18-29.
[4] 严斌俊. 数据驱动的中药制药过程质量控制方法及应用研究 [D]. 杭州: 浙江大学, 2015.
[5] Setford P C, Jeffery D W, Grbin P R,. Mathematical modelling of anthocyanin mass transfer to predict extraction in simulated red wine fermentation scenarios [J]., 2019, 121: 705-713.
[6] Wang K H, Zhang D, Wu J R, et a. A comparative study of Danhong injection andinjection in the treatment of cerebral infarction: A systematic review and meta-analysis [J]., 2017, 96(22): 7079-7087.
[7] 姜言红, 田颖, 练佳颖, 等. 丹参川芎嗪注射液辅助治疗72 h内急性缺血性卒中的系统评价 [J]. 中草药, 2021, 52(18): 5663-5675.
[8] 郝晨伟, 李正翔, 张铭慧, 等. 丹参及其配伍制剂治疗冠心病的研究进展 [J]. 中草药, 2021, 52(13): 4096-4106.
[9] 王赛君, 伍振峰, 杨明, 等. 中药提取新技术及其在国内的转化应用研究 [J]. 中国中药杂志, 2014, 39(8): 1360-1367.
[10] 陈泽麒, 瞿海斌. 丹参提取过程动力学研究: 模型建立及关键工艺参数考察 [J]. 中国中药杂志, 2021, 46(3): 605-613.
[11] Lau Y T, Ng K M, Chen N,. Quality assurance of Chinese herbal medicines: Procedure for multiple-herb extraction [J]., 2014, 60(12): 4014-4026.
[12] 陈勇, 蔡铭, 瞿海斌, 等. 基于圆柱型结构的中药材提取动力学模型 [J]. 浙江大学学报: 工学版, 2006, 40(9): 1600-1603.
[13] 潘坚扬. 丹酚酸类物质降解规律研究 [D].杭州: 浙江大学, 2019.
[14] 黄世超. 若干丹参酚酸的降解和解离性质研究 [D].杭州: 浙江大学, 2016.
[15] Bezerra M A, Santelli R E, Oliveira E P,. Response surface methodology (RSM) as a tool for optimization in analytical chemistry [J]., 2008, 76(5): 965-977.
[16] Gong X C, Huang S C, Pan J Y,. Modeling of degradation kinetics of Salvianolic acid B at different temperatures and pH values [J]., 2017, 25(1): 68-73.
[17] 李伟, 李淑明, 李挺洋, 等. 复方丹参滴丸中君药丹参的质量标志物研究 [J]. 中草药, 2018, 49(9): 2000-2006.
[18] [18] 陈丽冰, 何容, 李辉, 等. 恤彤注射液中间体丹参提取液的指纹图谱分析及多指标含量测定 [J]. 中国现代应用药学, 2020, 37(9): 1085-1089.
[19] 中国药典[S]. 一部. 2020: 77.
[20] 陈杨, 张晋, 倪健, 等. 提取动力学模型的简化及黄芩总黄酮模型适应性研究 [J]. 中国中药杂志, 2014, 39(2): 230-234.
[21] 朱静, 陈慧清, 白鹏, 等. 丹酚酸B水溶液分解反应的动力学研究 [J]. 中成药, 2009, 31(4): 541-544.
[22] 卢召战, 朱靖博, 刘天赐. pH及添加剂对丹酚酸B水溶液稳定性的影响 [J]. 大连工业大学学报, 2008, 27(3): 209-211.
[23] Guo Y X, Zhang D J, Wang H,. Hydrolytic kinetics of lithospermic acid B extracted from roots of[J]., 2007, 43(2): 435-439.
Study on extraction kinetics ofetbased on data-driven and mechanism model
CHEN Ze-qi1, 2, XIE Xin-yuan1, 2, CHEN Si-ming1, 2, FU Hao1, 2, QU Hai-bin1, 2
1. Pharmaceutical Informatics Institute, College of Pharmaceutical Sciences, Zhejiang University, Hangzhou 310058, China 2. Innovation Center in Zhejiang University, State Key Laboratory of Component-Based Chinese Medicine, Hangzhou 310058, China
In order to obtain the process knowledge of Danshen (et, SMRR) extraction and improve the level of quality control in extraction process.The transfer and transformation rules of salvianolic acid in the extraction process of SMRR were studied based on data-driven and mechanism modeling methods. First, the extraction kinetic parameters of salvianolic acid under different process conditions were obtained by mechanism model, and then the relationship between the extraction kinetic parameters and process parameters was established by response surface methodology.The extraction kinetics models of salvianolic acid B, salvianolic acid E, lithospermic acid, salvianolic acid A, and salvianic acid were established. The results of model validation showed that the average absolute deviations of salvianolic acid B, salvianolic acid E, lithospermic acid, salvianolic acid A, and salvianic acid were 151.85, 27.76, 19.46, 214.61, 105.68, respectively, indicating that the models performed well.This study revealed the relationship among raw material attributes, process parameters and product quality attributes in the extraction process of SMRR, and provided theoretical knowledge for the quality control of its extraction process.
data-driven; mechanism model;et; extraction; kinetic model;salvianolic acid; lithospermic acid; danshensu
R283.6
A
0253 - 2670(2022)01 - 0051 - 09
10.7501/j.issn.0253-2670.2022.01.008
2021-07-18
国家“重大新药创制”科技重大专项(2018ZX09201011-002)
陈泽麒,男,硕士研究生,研究方向为中药科学与工程学。E-mail: chenzq@zju.edu.cn
瞿海斌,博士生导师,教授,从事中药制药过程质量控制研究。Tel: (0571)88208428 E-mail: quhb@zju.edu.cn
[责任编辑 郑礼胜]
