万古霉素血清浓度检测UPLC法的建立与评价
2020-11-05李发双李惠英张力麟黎林波
李发双,宗 静,李惠英,张力麟,李 强,黎林波
(昆明医科大学附属儿童医院药剂科,昆明 650228)
万古霉素是一种主要经肾脏排泄的糖肽类抗生素,在临床上用于治疗需氧G+菌感染,可用于治疗由耐甲氧西林金黄色葡萄球菌、表皮葡萄球菌和肠球菌引起的严重的新生儿感染[1]。在临床用药中,万古霉素剂量不足可能导致耐药菌株的产生[2],过量给药又会造成严重的毒副作用,如肾毒性和耳毒性[3]。此外,万古霉素的治疗窗窄[4]且个体差异大,因此,其血药浓度监测对于确保足够的治疗浓度同时避免药品不良反应(adverse drug reactions,ADRs)是必要的。
治疗药物监测(therapeutic drug monitoring,TDM)在药物治疗中起着重要作用,特别是对于治疗窗窄的药物。监测儿童血液中的万古霉素浓度可以避免副作用,并可根据监测结果及时调整剂量。目前临床常用于检测血清中万古霉素浓度的免疫学方法包括化学发光免疫分析法(chemiluminescent immunoassays,CMIA)和酶倍增免疫分析法(enzyme-multiplied immunoassays,EMIT)[5]等。而超高效液相色谱(UPLC)法与上述方法相比,在速度、稳定性、灵敏度、准确性和时效上更具优势。本研究建立了一种UPLC法来快速、准确地检测儿童血清中万古霉素的浓度,为临床合理使用万古霉素提供参考。
1 材 料
1.1 仪器 UPLC仪(沃特世科技上海有限公司);MGS氮气吹扫浓缩装置(倍捷科技有限公司);XH-B型旋涡混合器(江苏康健医疗用品有限公司);SC-3616低速离心机(安徽中科中佳科学仪器有限公司)。
1.2 试药 万古霉素对照品(含量100%,批号130338-201704)和内标去甲万古霉素对照品(含量87.7%,批号130360-201302)均由中国食品药品检定研究院提供;乙腈(色谱纯,德国Merck公司);高氯酸为优级纯;甲酸为分析纯;水为纯化水;空白血清由昆明医科大学附属儿童医院提供。
2 方法和结果
2.1 色谱条件 ACQUITY UPLC BEH C18色谱柱(50 mm×2.1 mm,1.7 μm);以0.3%甲酸溶液为流动相A,乙腈为流动相B进行梯度洗脱(0~2 min,90%A;2~5 min,60%A;5~6 min,0%A;6~6.1 min,60%A;6.1~7 min,90%A),检测波长236 nm,流速0.25 ml/min,柱温40 ℃,进样量5 μl。
2.2 对照品溶液的制备 分别称取内标去甲万古霉素和万古霉素对照品10 mg,置于10 ml容量瓶中,分别加入纯化水溶解并稀释至刻度,得质量浓度分别为0.877 mg/ml和1 mg/ml的去甲万古霉素对照品溶液和万古霉素对照品溶液,于2~8 ℃冰箱保存备用。
2.3 样品预处理 精密吸取血清180 μl,加入浓度为0.877 mg/ml的去甲万古霉素和1 mg/ml的万古霉素对照品溶液各20 μl,涡旋混合后加入乙腈-4%高氯酸混合液(1∶3.5)200 μl,涡旋1 min后,室温下以1.4×104×g离心10 min后,取上清液200 μl进样。
2.4 专属性考察 专属性实验样本为空白血清、空白血清加入20 μl 100 μg/ml万古霉素对照品溶液、空白血清加入20 μl 87.7 μg/ml去甲万古霉素对照品溶液(内标溶液)、空白血清同时加入20 μl 100 μg/ml万古霉素对照品溶液和20 μl 87.7 μg/ml内标溶液,以及患者服用药物后的血清样品。按2.3项下方法对样本进行处理,按2.1项色谱条件进样分析,得色谱图(见图1)。由图1可见,万古霉素保留时间为3.862 min,内标去甲万古霉素保留时间为3.734 min,各峰完全分离,峰形较好,空白血清的内源性物质不干扰万古霉素和去甲万古霉素的测定。
2.5 线性和定量下限 取万古霉素对照品溶液制备成万古霉素理论浓度为5、10、25、50、75、100 μg/ml的系列对照品溶液。吸取空白血清180 μl至离心管中,分别精密加入20 μl不同浓度的万古霉素对照品溶液及20 μl浓度为87.7 μg/ml的内标溶液,涡旋混匀,按2.3项下方法处理,再按2.1项下色谱条件进样。以测得的万古霉素峰面积与内标峰面积比值(y)对万古霉素浓度(x)进行直线回归,得万古霉素的回归方程为y=1.012 3x-0.152 2(r=0.999 9),万古霉素在5~100 μg/ml范围内线性关系良好,定量下限为5 μg/ml。
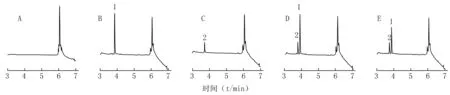
图1 人血清中万古霉素的UPLC谱图A:空白血清;B:空白血清+20 μl 100 μg/ml万古霉素对照品溶液;C:空白血清+20 μl 87.7 μg/ml去甲万古霉素 对照品溶液(内标溶液);D:空白血清+20 μl 87.7 μg/ml内标溶液+20 μl 100 μg/ml万古霉素对照品溶液; E:万古霉素血清样品+87.7 μg/ml内标溶液;1:万古霉素;2:内标去甲万古霉素
2.6 回收率和精密度实验 制备低、中、高浓度为10、50、75 μg/ml的万古霉素血清样品,按2.1项下色谱条件进样,每个浓度取5个样本检测;同时配制低、中、高浓度为10、50、75 μg/ml的万古霉素对照品溶液,按2.1项下色谱条件进样测定,每个浓度取5个样本检测。以样品实测浓度与对照品溶液峰面积代入标准曲线算得的浓度的比值为提取回收率,样品实测浓度与理论浓度的比值为方法回收率,结果显示该方法符合样品分析要求。配制低、中、高浓度为10、50、75 μg/ml的万古霉素血清样品,按2.1项下色谱条件进样测定,每个浓度取5个样本检测,每天测定5次,连续测定5 d,计算该方法的日内、日间精密度和准确度,结果见表1。

表1 回收率及精密度实验结果 (n=5,%)
2.7 稳定性实验 取空白血清加入万古霉素对照品溶液,分别配制低、中、高浓度分别为10、50、75 μg/ml的万古霉素血清样品,分别于室温放置24 h、4 ℃冰箱放置24 h、-20 ℃冰箱放置3 d、反复冻融两次考察其稳定性,结果显示万古霉素在上述条件下稳定性良好。
2.8 临床应用 选取本院100例使用了万古霉素的严重感染新生儿(万古霉素用法用量1 g,q6 h,ivgtt),于用药第3天第4剂万古霉素给药前30 min取外周静脉血2 ml,采用本研究建立的方法测定万古霉素血药浓度(即谷浓度)[6],结果见表2。根据中国药理学学会治疗药物监测分会制订的《万古霉素治疗药物监测指南》中的参考值,在所测样品中仅有33%的血样中万古霉素血药浓度在10~20 μg/ml的有效谷浓度[7]范围内,表明万古霉素血药浓度在新生儿不同个体间存在较大差异,经验性给药达到有效血药浓度的比例不高。

表2 100例新生儿万古霉素血药浓度的分布情况
3 讨 论
万古霉素在临床主要用于治疗G+菌引起的严重感染,其药理作用与血药浓度之间有一定的相关性[4],且万古霉素血药浓度在不同个体间存在较大差异,经验性给药达到有效血药浓度的比例不高,为了确保患者用药的疗效及安全,建议使用万古霉素时监测血药浓度。本研究建立了一种UPLC法测定儿童血清中的万古霉素。对流动相的选择,在预实验中考察了甲醇-水、乙腈-水、乙腈-0.1%甲酸溶液、乙腈-0.5 mol/L KH2PO4溶液和甲醇-0.5 mol/L KH2PO4溶液等系统,并调整了流动相比例,但仍会出现拖尾或者双重肩峰,经过优化最终确定了乙腈-0.3%甲酸溶液为流动相梯度洗脱,在本研究设定的洗脱条件下万古霉素和去甲万古霉素可以很好地分离,峰形对称,无拖尾,且稳定性较好。
作者尝试了多种有机溶剂如甲醇,5%、7%、10%高氯酸溶液,乙酸乙酯,10%三氯乙酸等处理血样,结果表明采用乙腈-4%高氯酸溶液(1∶3.5)进行蛋白质沉淀的效果优于其他有机溶剂,沉淀后离心,可直接取上清进样。此方法简便,样品回收率高,可有效避免空白血清内源性物质对待测物的干扰,色谱基线稳定,响应值高,结果准确可靠,重复性也较好。
有文献报道[8]选用替硝唑或维生素B12作为内标物,但这些药物在临床上常与万古霉素联合用药,会影响测定结果,最终没有选择。去甲万古霉素的化学结构与万古霉素相似,在本研究条件下能与万古霉素完全分离,且出峰间隔时间短,因此选择其作为内标。
万古霉素TDM被推荐用于药物疗效和安全性评估。本研究建立的UPLC法具有较高的选择性、灵敏度和准确度,通过对100例新生儿血清中万古霉素浓度的测定,确定了本法的可行性与实用性。
