卡马西平药品不良反应与HLA-B*1502基因多态性及血药浓度相关性研究
2020-11-05许倍铭
许倍铭,陈 冰
(上海交通大学医学院附属瑞金医院药剂科,上海 200025)
CBZ常见的药品不良反应(adverse drug reactions,ADRs)主要涉及皮肤及附件、神经和精神系统、血液系统损害等。美国食品药品监督管理局(FDA)于2007年警告CBZ会增加HLA-B*1502等位基因阳性亚裔患者出现Stevens-Johnson综合征(Stevens-Johnson Syndrome,SJS)和中毒性表皮坏死松解症(toxic epidermal necrolysis,TEN)的风险,建议亚裔患者在使用CBZ前进行HLA-B*1502等位基因筛查[3]。除了遗传因素以外,CBZ的治疗药物窗较窄,推荐的安全血药浓度范围在4~12 μg/ml,一旦超出血药浓度范围容易出现相应的ADRs。本研究回顾性收集在上海交通大学医学院附属瑞金医院住院并进行过HLA-B*1502基因检测或CBZ血药浓度检测的患者资料,结合其CBZ使用情况、血药浓度、实验室检测指标以及ADRs发生情况进行综合分析,以了解癫治疗中CBZ基因多态性、血药浓度与ADRs的相关性,为CBZ的安全、合理使用提供参考依据。
1 资料和方法
1.1 患者资料 回顾性收集2017-01-01至2019-12-31在本院进行过HLA-B*1502基因检测或使用CBZ后进行了血药浓度检测的住院患者资料,共148例,其中101例检测过HLA-B*1502基因rs3909184以及rs2844682位点基因型[4]。60例患者服用过CBZ并监测血清谷浓度。采集患者HLA-B*1502基因型检测结果、CBZ用药情况、血药浓度和患者实验室检查结果,包括血常规(白细胞、红细胞、血小板)、肝肾功能指标(天冬氨酸转氨酶、丙氨酸转氨酶、碱性磷酸酶、总胆红素、直接胆红素、尿素氮、血肌酐、尿酸)、电解质指标(血钠、血钾、血钙),以及患者ADRs信息。
1.2HLA-B*1502基因检测 采集患者用药前全血2.0 ml,乙二胺四乙酸(EDTA)抗凝,取200 μl全血加入1 mol/L氯化铵溶液1 ml,3×103×g离心5 min,弃去上清液,加入50 μl核酸纯化试剂纯化DNA。加入相应基因位点的探针试剂。置于TL998A荧光检测仪(天隆科技公司)中,根据荧光检测结果判断HLA-B*1502基因型。
1.3 CBZ血药浓度检测 服用CBZ待血药浓度达稳态后,采集患者服药前的全血3.0 ml,1×103×g离心20 min分离血清,采用酶联免疫法检测血清中CBZ的稳态谷浓度。
1.4 ADRs关联性评价 CBZ引起的ADRs通过主动监测实验室信息系统(laboratory information system,LIS)中的异常指标进行采集。依据国家药品不良反应监测中心的ADRs关联性评价标准,即发生的时间顺序、是否为已知ADRs类型、去激发反应、再激发反应以及其他因素能否解释来进行肯定、很可能、可能、可疑、不相关5级关联性评价。
1.5 统计学处理 应用SPSS 21.0软件,采用χ2检验分析HLA-B*1502基因型与ADRs的相关性。采用Pearson相关性分析CBZ血药浓度与实验室异常指标之间的相关性。
2 结 果
2.1 患者基本情况 148例患者分别来自13个科室,神经内科患者最多(占65.54%)。其中男性77例,女性71例,无明显性别倾向。患者平均年龄(52±20)岁,平均体质量(63.38±15.90) kg。与卡马西平相关的临床诊断主要为癫(95例,占64.19%)、神经痛(53例,占35.81%)等,见表1。
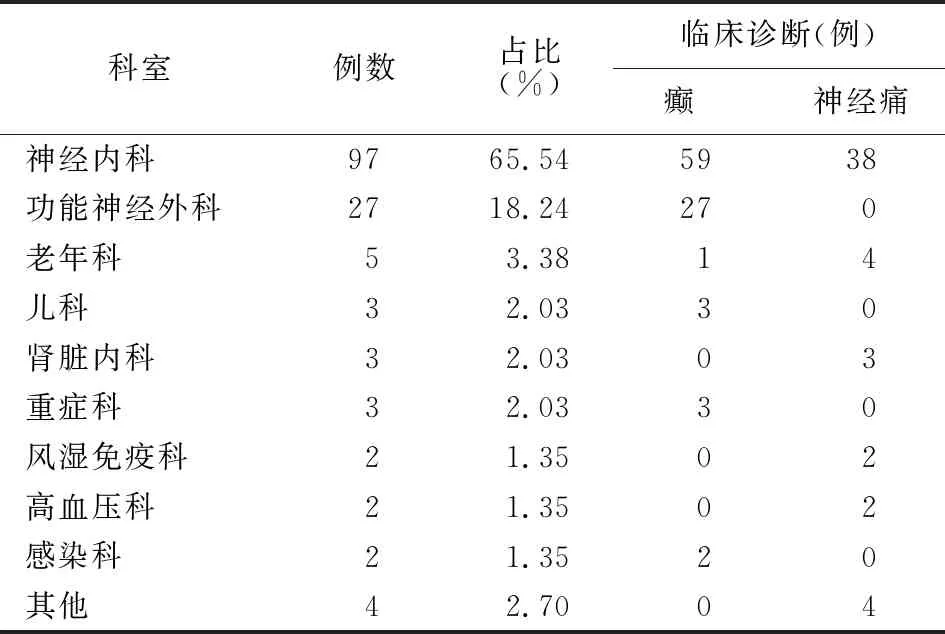
表1 患者科室分布和临床诊断Table 1 Department distribution and clinical diagnosis of the patients
2.2 患者HLA-B*1502基因型检测结果 148例患者中有101例进行过HLA-B*1502基因型检测,其中34例为阳性[阳性定义参照2017年临床药物基因组学实施联盟(Clinical Pharmacogenetics Implementation Consortium,CPIC)的指导意见,即HLA-B*1502等位基因杂合或纯合突变为阳性][5],阳性率33.66%,其中1例为纯合突变型,33例为杂合突变型,杂合突变型患者中有1例患者出现两个位点同时杂合突变,见表2。
2.3 卡马西平使用情况 148例患者中有78例使用了CBZ治疗,其中HLA-B*1502基因型检测结果为阳性的患者中有3例未遵循基因检测推荐的意见,回到当地医院使用了CBZ治疗,占阳性患者的8.82%。HLA-B*1502基因型阴性(野生型)患者中有28例使用了CBZ治疗,占阴性患者的41.79%。

表2 HLA-B*1502基因型分布Table 2 Distribution of HLA-B*1502 genotypes
2.4 CBZ血药浓度检测结果 78例使用了CBZ的患者中有60例(86例次)进行了CBZ血药浓度检测,检测率为76.92%。86例次检测结果均值为(4.99±2.44) μg/ml,其中53例次在推荐的4~12 μg/ml浓度范围[6]内(占61.63%), 32例次(37.21%)低于推荐的浓度范围,1例次高于推荐的浓度范围,为15 μg/ml。
2.5 ADRs发生情况 收集78例使用了CBZ患者的相关实验室检测结果,以及病程记录中有关其他临床表现的描述,根据国家药品不良反应监测中心的判断标准,其中12例患者的ADRs很可能与CBZ相关,包括白细胞下降5例、肝功能异常2例、血钠下降2例、尿素氮升高2例、皮疹1例,其余异常实验室检测结果或头晕、头痛、恶心等症状,不能排除由患者自身疾病或其他药物引起的可能,见表3。

表3 患者出现的不良反应与卡马西平的相关性分析Table 3 Correlation analysis of adverse reactions and carbamazepine
12例出现了CBZ相关ADRs的病例中,男性4例,女性8例,年龄最小12岁,最大95岁。其中3例HLA-B*1502基因为阳性,2例未检测,其余为阴性。CBZ使用剂量最低为100 mg,bid,最高为200 mg,tid。ADRs发生在用药1周或1个月后。其中7例进行过CBZ血药浓度检测, 5例检测结果在参考浓度范围内(4~12 μg/ml),1例低于参考浓度范围,1例高于参考浓度范围,血药浓度均值在(6.85±3.89) μg/ml。
使用Pearson相关性分析对86例次CBZ血药浓度数据与患者同期的白细胞、丙氨酸转氨酶、血钠数据进行相关性分析,未发现明显的相关性,P均>0.05。
3 讨 论
本研究探讨了CBZ相关ADRs与HLA-B*1502基因多态性及血药浓度的相关性。78例使用了CBZ的患者中,12例出现CBZ相关ADRs,占15.38%,低于其他文献报道的比例[7],其中WBC下降与皮疹发生率低于药品说明书中记载的相应ADRs的发生频率,这可能与本研究患者有不少来自功能神经外科、老年科、重症科有关,这类患者WBC下降或出现皮疹不能完全排除自身疾病、手术操作或其他合并用药引起的可能性。ADRs出现的时间基本集中在使用卡马西平1周或1个月后,与其他文献报道的发生时间吻合[8]。
148例患者中,101例进行了HLA-B*1502基因rs3909184及rs2844682位点的检测,另外47例患者由于长期服用CBZ未发生ADRs,未进行基因检测。本研究中rs3909184位点的基因突变率为15.84%,略高于美国国家生物技术信息中心(NCBI)基因数据库中的10%;rs2844682位点的基因突变率为18.81%,与NCBI基因数据库中的数据相近。本研究中HLA-B*1502基因阳性率为33.66%,高于Chen等[9]对中国台湾人群的研究结果(约8%)。有研究显示,我国南方人群的HLA-B*1502基因阳性率接近30%,远高于我国北方人群[10]。本研究中的患者主要来自南方,结果与这项研究接近。值得注意的是,本研究发现3例基因型阳性的外地患者,回到当地医院后仍然使用了CBZ治疗。其中1例HLA-B*1502基因纯合突变患者,使用了CBZ 100 mg,bid的方案,一周后出现双下肢大面积斑丘疹。临床药师通过随访联系患者后建议立即停用CBZ,改用其他抗癫药物,并予以对症处理,随后症状好转。该例患者的情况证明,HLA-B*1502基因突变极易导致严重的皮疹ADRs,与之前研究结果一致[11]。本研究还发现另2例HLA-B*1502基因阳性患者分别出现白细胞下降、低血钠以及尿素氮升高,也在停用卡马西平、对症处理后好转。可见HLA-B*1502基因突变型与CBZ诱导的相关皮疹有密切相关性,应严格遵照相关推荐意见[3],在使用CBZ前进行基因筛查,尤其对于我国南方人群,有利于安全用药。
78例使用CBZ的患者中,60例进行了CBZ血药浓度检测。其中61.63%在推荐的浓度范围内,37.21%低于推荐的浓度范围。低于推荐浓度范围的原因可能有:(1)CBZ血药浓度检测时间过早,部分患者在首次服用CBZ仅3 d后就进行浓度检测。CBZ单次给药时半衰期为25~65 h,长期服用由于其自诱导作用,半衰期降为10~20 h。因此一般在首次服用CBZ一周左右的时间进行血药浓度检测较为合适。(2)抗癫药物疗效因人而异,部分患者在药物浓度尚未达到血药浓度参考范围下限时已出现癫发作次数的明显下降,医师不再增加CBZ的给药剂量。(3)患者病情复杂,合并多种癫发作形式,因此在使用CBZ的同时联用其他抗癫药物,病情通过多种抗癫药物得以控制。
本研究发现,5例白细胞计数下降的患者中有2例CBZ血药浓度检测结果在参考范围内,其中4例患者在减少CBZ用量并逐渐改用其他抗癫药物过程中,白细胞计数未出现好转,另1例好转。2例肝功能异常患者中1例进行过CBZ血药浓度检测,结果低于参考范围。2例患者在逐渐停用CBZ并予以相应的保肝药对症处理后均好转。2例出现低钠血症的患者中,1例血药浓度在正常范围,未停用CBZ,1例高于正常范围,达15 μg/ml,减少CBZ用量后,均予以10%氯化钠30 ml分次稀释后口服补钠,后复查血钠均有所好转。2例出现尿素氮升高的患者CBZ血药浓度均在正常范围,未进一步复查。本研究结果提示,CBZ引起的低钠血症和肝功能异常,在通过相应的补钠、保肝对症处理后,可在较短时间内恢复,与文献[12]结果一致,而CBZ引起的白细胞计数下降,即使停用CBZ后,仍难以在短时间内恢复,与之前的报道不同[13]。本研究中CBZ引起的尿素氮升高发生率高于药品说明书所提示的发生率,在临床上也未受到重视,未进一步复查患者的尿素氮,在今后应予以重点监测。出现CBZ相关ADRs患者的CBZ血药浓度均值为(6.85±3.89) μg/ml,高于总体均值(4.99±2.44) μg/ml,由于受病例数量所限,其是否具有临床意义仍需大样本研究来验证。
