超高浓度甲氨蝶呤中毒抢救成功1例并文献复习
2020-11-04袁宇婷刘丽丽叶中绿
袁宇婷,田 川,刘丽丽,叶中绿
(1.广东医科大学,广东 湛江 524000 2.广东医科大学附属医院 儿童医学中心,广东 湛江 524000)
甲氨蝶呤(MTX)是急性淋巴细胞白血病(ALL)和许多其他恶性肿瘤治疗药物的重要组成部分。 患有白血病的儿童经常使用大剂量或超大剂量甲氨蝶呤(MTX)化学疗法使血液中的血药浓度显着升高,从而可以穿透血脑屏障,除有利于外周及骨髓中肿瘤细胞的杀灭,更重要的是还可以起到防治中枢系统白血病的作用,以改善预后。但使用大剂量 MTX时须严格监测血液浓度,在正常的细胞遭到致命损害前,及时给予甲酰四氢叶酸(CF)解救。否则可能会引起致死性化疗毒性。我中心曾诊治超高MTX血药浓度中毒并经连续肾脏替代治疗(CRRT)、血浆置换等抢救成功的患者1例,现报道如下。
1 病例资料
患儿4岁,男性,因确诊急性淋巴细胞白血病(B系 高危)5月余,按照华南地区儿童急性淋巴细胞白血病治疗协作组方案(SCCLG- ALL-2016),为进行巩固阶段化疗于2019-05-14再次住院。经完善相关检查,确认患儿符合继续化疗的临床条件,化疗前按要求予足量水化、碱化,总液体超过到3000 ml/m2;5%碳酸氢钠达115 ml/m2,并按照治疗方案给予HR-block1: 地塞米松(DXM )20 mg/(m2·d) ,d1-5;长春新碱(VCR)1.5 mg/m2(≤2 mg/次) d1,d 6;大剂量甲氨蝶呤(HDMTX) 5 g/m2d1;环磷酰胺(CTX) 200 mg/m2q12 h×5, d2-4,阿糖胞苷(Ara-C)2 g/m2q12 h×2 d5;培门冬(PEG- Asp)2 500 U/m2(≤3 750 U) d 6。化疗期间同时涉及的其余药物包括:头孢哌酮他唑巴坦、威凡、洛赛克;化疗开始后,患儿诉腹痛,呈阵发性,家属抚摸肚子可缓解,但仍间断诉有腹痛,考虑化疗引起的胃肠黏膜损伤,故予洛赛克护胃。其中HDMTX 5 g/m2,起30、48、72小时常规测MTX血药浓度;亚叶酸钙剂量按照首剂MTX起第43小时(即满42小时)进行解救,亚叶酸钙每次用量为15 mg/m2。患儿MTX治疗48小时后开始腹痛呈进行性加重,不能缓解;不伴呕吐,有大便,查体全腹压痛,无反跳痛及包块,肠鸣音弱。腹部胃肠道彩色超声未见明显异常;血、尿淀粉酶正常。 48小时MTX血药浓度:32 μmol/L。考虑MTX中毒,暂停所有化疗,按照MTX中毒方案予大剂量亚叶酸钙解救,并加强补液、碱化,强迫利尿等处理, 但患儿腹痛症状改善不明显;72小时MTX血药浓度16.9 μmol/L。继续予大剂量亚叶酸钙、水化、碱化。患儿腹痛无改善,提示单独使用亚叶酸钙无法快速解除MTX中毒。故于第82小时起行CRRT,并继续监测病情变化。96小时MTX血药浓度仍达到7.2 μmol/L ,考虑CRRT效果不佳,为加快MTX的清除,故于MTX后124小时开始行血浆置换,血浆置换后继续行CRRT。第120小时,MTX血药浓度下降到3.8 μmol/L。MTX后144小时查B型尿钠肽(BNP )为10 224 pg/ml, 予米力农强心,继续行CRRT,过程顺利。中毒第7天即148小时,为加快解毒再次行血浆置换。第168小时MTX血药浓度下降到1.11 μmol/L,第192小时MTX血药浓度下降到0.52 μmol/L,患儿生命体征稳定后撤机,停止CRRT,患儿病情持续保持稳定。因MTX血药浓度尚未下降到正常值,继续静脉予水化、碱化、亚叶酸钙,最终于3天后血药浓度水平下降到0.18 μmol/L,解救成功。
2 讨 论
患儿MTX前予足量水化、碱化,MTX后继续足量水化、碱化、亚叶酸钙解救,治疗规范,整过程严格监测尿量,医嘱执行过程亦无差错。但48小时MTX血药浓度为32 μmol/L, 提示超高浓度MTX中毒(HDMTX化疗后正常的血药浓度:C24<10 μmol/L;C48<1 μmol/L;C72<0.1 μmol/L),经加大水化、碱化,加大亚叶酸钙用量后,96小时 MTX浓度为7.2 μmol/L, 经持续CRRT、血浆置换后患儿MTX浓度逐渐将至正常,未出现新的MTX相关中毒症状。目前单独使用高剂量亚叶酸钙治疗严重MTX中毒的资料较少,有资料指出,单独使用大剂量亚叶酸钙结合水化和碱化虽然最终也可治愈MTX中毒,但近期发病率高(骨髓抑制,粘膜炎等)[1]。研究表明单独使用亚叶酸并不是最佳选择。
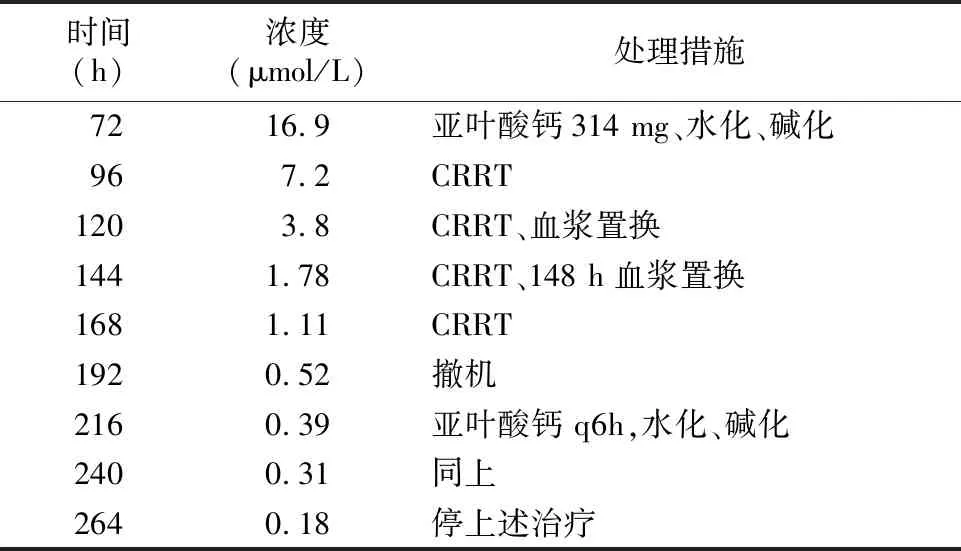
表1 HDMTX浓度变化及处理措施
本例患儿化疗前生化未提示肾功能不全,各项检查也提示重要器官功能良好,骨髓处于缓解状态,化疗前及化疗期间水化碱化充足、无腹水或胸腔积液等第三空间液体、亚叶酸钙用量足够。患儿出现中毒原因不是很明确,患儿本次化疗期间涉及的药物:威凡(伏立康唑)、头孢哌酮他唑巴坦(β-内酰胺类)、洛赛克(质子泵抑制剂)。通过查找相关文献,高达90%的MTX在尿液中排出,不到10%通过胆汁排泄,β-内酰胺类抗生素与 MTX 在肾脏有相同的转运途径,都可以通过肾基底外侧膜有机阴离子转运蛋白OAT(包括OAT1和OAT3)排泄,理论上β-内酰胺类抗生素可竞争性的结合转运蛋白,从而阻碍MTX的分泌,但MTX主要通过OAT3进行转运,β-内酰胺类抗生素对MTX转运的影响取决于其与OAT3的亲和力程度,需要进一步研究来确定这种相互作用的程度[2]。郭继红等[3]通过收集医院的33例使用HDMTX化疗的病历资料,对数据进行多元线性回归分析,发现MTX的血药浓度与同时使用的糖皮质激素之间存在明显正相关性(P<0.05),与β内酰胺类抗生素存在正相关性(P=0.0956)。对于伏立康唑,是否会对MTX的排泄造成干扰,有文献指出,伏立康唑与MTX二者之间的药代动力学相互作用被认为是不可能的,因为伏立康唑被肝细胞色素P450代谢,随后被清除进入胆汁,而MTX主要经肾脏消除[4]。此外,关于在HDMTX治疗中使用质子泵抑制剂引起MTX浓度升高甚至MTX中毒已见报道,邹羽真等[5]报道1例36岁女患者,第一次化疗中MTX用药过程顺利,第二次化疗使用MTX时出现上腹疼痛,查大便潜血(+),考虑胃黏膜受损,给予奥美拉唑,次日患者出现血肌酐水平上升, 第3天发现MTX血药浓度为17.64 μmol/L,经亚叶酸钙解救治疗后,MTX浓度迅速下降。相关资料指出,质子泵抑制剂可能通过抑制H+/K+-ATP酶泵,从而导致MTX清除障碍(H+/K+-ATP酶泵通过将氢离子分泌到肾小管中并吸收钾离子,而MTX与氢离子同时排出,奥美拉唑可以抑制肾脏清除氢离子从而阻断MTX的肾小管分泌)[6-7]。综合以上资料,本患儿出现MTX中毒不除外是所使用的头孢哌酮他唑巴坦、地塞米松、洛赛克综合作用的结果。患儿解救成功后,再完善了与MTX代谢相关的基因检查:结果未见相关基因有异常表达,提示患儿中毒可能与体质无关。
目前药物方面有效治疗MTX中毒的药物主要是羧肽酶G2(CPDG2),CPDG2可使MTX转换化为无毒性的代谢产物4-脱氧-4-氨基N10-甲基蝶酸( DAMPA) 和谷氨酸[8],现在被美国食品和药物管理局批准为治疗急性肾损伤导致MTX清除延迟的MTX中毒的拯救剂[9],但由于价格昂贵、处于实验阶段,属于特殊用药。
血液净化是把患者的血液引至体外,并通过净化器去除其中一些致病物质,净化血液以达到治疗疾病的目的。其主要原理是:弥散、对流、吸附。弥散是指溶质以浓度差为驱动力通过半透膜;对流是指溶质在跨膜压力差的作用下,溶质及溶剂一起通过半透膜;吸附是通过提供特定的吸附剂(如活性炭或树脂等),当有害物质经过吸附膜时被吸附,从而达到清除有害物质的目的。血液净化的方式有多种,根据原理不同,为血液滤过(HF)、血液灌流(HP)、血液透析(HD)、透析滤过(HDF)、血浆置换(PE)、免疫吸附(IA)等; 根据治疗时间,可分为间隙性、持续性和延长性的血液净化。
普通血液透析适用于清除低蛋白结合率、水溶性、分布容积小的小分子物质和部分中分子物质(相对分子质量约500~1 200)。血液滤过、高流量透析、透析滤过适用于清除相对分子质量0~5 000的小、中分子物质。血液灌流适用于相对分子质量在100~40 000的水溶性及脂溶性物质,许多情况显示,采用血液灌流进行有害物质清除在清除率方面优于血液透析、腹膜透析等,但对于水溶性低、小分子物质还是倾向于选择血液透析,且随着高流量透析膜的出现,高流量透析膜的清除作用与血液灌流相当,因此血液灌流的优势也随之减弱。血浆置换、免疫吸附适用于清除相对分子质量大于10 000的大分子物质。CRRT是指所有每天24小时或接近24小时的缓慢、连续、清除水分和溶质的治疗方法的总称,包括:缓慢连续超滤(SCUF)、连续静脉血液滤过(CVVH)、连续静脉血液透析(CVVHD)、连续高通量透析(CHFD)、连续静脉血液透析滤过(CVVHDF)、血浆滤过吸附(CPFA)等。
通过查阅相关文献,目前采取血液净化方式降低MTX血药浓度的相关报道大多为个案,最有效的治疗手段尚未达成一致。腹膜透析降低血浆MTX浓度作用最小,Ahmad等[10]记录了使用HDMTX治疗骨肉瘤的47岁患者1例,治疗期间出现了急性肾功能衰竭,给予连续7天的腹膜透析,但MTX血液浓度并未发生明显改变,原因包括在生理pH下MTX的高度电离和低脂质溶解性,以及MTX与血浆蛋白结合的百分比为50%。Widemann等[11]使用MEDLINE和CancerLit数据库(1980-2002年)对文献进行了回顾,该研究统计了49例MTX中毒引起肾功能障碍的患者基于透析的MTX清除方法的效果,其中最多见被使用的方法是血液透析(49例中有10例)、高通量血液透析(49例中有9例)和活性炭血液滤过(49例中有7例),16例患者采用多种联合方式治疗。高通量血液透析在最短的时间(中位时间4小时)内使血浆MTX浓度下降最多(中位下降百分比为76%)。然而,仅有3例患者在1次透析治疗中使用单一方法实现MTX血药浓度下降大于90%。MTX是一个分子量为454 d的小分子物质,与蛋白质结合的比例约为50%,具有非常大的体积分布(0.4~0.8 l/kg的溶质分布体积),与组织结合率高,血清浓度容易反弹,故连续的血液净化技术通常更容易实现,并可能阻止反弹重新分配。亦有文章指出,分子量较小,溶质分布体积≤0.7 l/kg和蛋白质结合率<80%更适合采取HD和CRRT的方式[12-13]。在一次MTX中毒治疗中,Vilay 等[14]比较了连续静脉血液透析(CVVHD),单次通过白蛋白透析(SPAD),连续静脉血液透析滤过(CVVHDF)对血内MTX的清除效率,指出采用CVVHDF模式实现了体外疗法中最高的清除率,病人的临床状况稳步改善。另外再有一个案例,报道了1例79岁的男性因中枢神经系统淋巴瘤接受了静脉内MTX治疗,34小时后MTX浓度为59.05 μmol/L,并且在34小时内血清肌酐从1.09 mg/dl增加到2.24 mg/dl,给予大量利尿、碱化、亚叶酸钙和CPDG2治疗后,MTX浓度下降,但出现反弹,考虑到大量MTX在细胞内储存,决定采取CRRT的血液净化方式,他们采取了CVVH模式,后因持续的肾衰竭改用CVVHD模式,MTX浓度逐渐下降至正常没出现反弹[15]。对于血浆置换,有相关外国文献指出,血浆交换并无法有效治疗MTX中毒,因为MTX的血清分布体积很大[16];余莉华等[17]在1例报道亦指出血浆置换适用于与血浆蛋白结合率高的药物,而 MTX蛋白结合率较低,不宜选用。但Cecyn等[18]的一个治疗MTX中毒的案例中,观察到在每天血浆置换过程中,血清MTX水平逐渐降低,且在最初MTX血药浓度最高时,其清除效率最大,但随着药物血清水平的降低,其效率逐渐降低,并且停止血浆置换后未观察到血药浓度的反弹,与顾敏等[19]的观察结果一致。
以上研究结果表明,解救MTX中毒的最佳治疗措施尚无定论,但根据MTX的分子特点,CRRT值得借鉴,具体哪一种模式才是最佳,目前相关文献尚未给出一个统一的答案。是否应该联合其他血液净化方式,也许应该根据临床实际情况综合考虑。
本次案例处理措施为:①持续性肾脏替代治疗;② 血浆置换;③大剂量亚叶酸钙;④大量水化;⑤碱化;⑥预防其他器官功能损害。积极心态及持之以恒的努力是也是成功的关健。本文案例的成功经验,为CRRT联合血浆置换等方式抢救严重MTX中毒提供了借鉴经验。
