显微镜下应用超声骨刀行钩椎关节切除在颈椎病前路手术中的疗效分析
2020-11-04陈跃秦刘忠国林建春
陈跃秦 刘忠国 林建春
福建中医药大学附属厦门市第三医院骨科,福建厦门 361100
颈椎病在临床领域中十分常见,是指颈椎椎间盘组织退行性改变、继发病理改变累及其周围组织结构(脊髓、神经根、交感神经、椎动脉等),出现相应的临床症状、体征[1]。根据受累结构及组织不同,颈椎病可分为脊髓型颈椎病、神经根型颈椎病、交感型颈椎病、椎动脉型颈椎病、食管型颈椎病、颈型颈椎病等,如同时存在两种以上类型,称为混合型颈椎病[2];在颈椎病各种类型中,神经根型颈椎病的发病率最高,达60%~70%。临床上绝大部分神经根型颈椎病可通过颈部制动、休息、牵引、止痛及神经营养药物等保守治疗获得良好效果,部分患者经过正规保守治疗3个月以上无效,或临床症状严重、出现肌力下降,严重影响患者日常生活和工作,应尽早手术治疗[3]。对于致压因素来源于椎管前方的颈椎病患者,经前路减压固定融合手术治疗通过切除退变椎间盘、增生骨赘,增加椎间隙高度,间接增大椎间孔面积,可实现神经根管间接减压。有学者指出通过钩椎关节切除直接减压可以获得较好的临床效果[4]。本研究选取我院2016年8月~2018年8月确诊为神经根型颈椎病和伴有神经根症状的混合型颈椎病患者55例,根据治疗方式的不同分为两组,对两组患者的临床疗效进行评估分析,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2016年8月~2018年8月我院收治确诊为神经根型颈椎病和伴有神经根症状的混合型颈椎病患者55例。根据治疗方式的不同分为两组,术中应用超声骨刀切除钩椎关节为A组,术中应用传统工具行神经根管减压为B组。A组30例患者,其中年龄35~69岁,病程5~29个月,行颈椎体次全切除植骨融合术(ACCF)10例,行颈椎间盘切除植骨融合术(ACDF)20例。B组25例患者,其中年龄34~68岁,病程6~33个月,行ACCF手术12例,ACDF手术13例。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。见表1。
1.2 纳入及排除标准
纳入标准:所有患者均有严重的神经根型症状,表现为严重的颈项部疼痛、受压神经根支配区域感觉异常或肌力下降,经正规保守治疗3个月以上无效或临床症状严重影响日常生活和工作[5];臂丛牵拉试验或(和)椎间孔挤压试验阳性;影像学检查提示相应神经根受压,相应节段钩椎关节退变、骨质增生。排除标准:颈椎外伤;3节段及以上椎间盘组织退变并引起相应临床症状患者;影像学检查提示多节段脊髓前后受压患者。
1.3 手术方式
(1)所有患者术前常规行颈椎正侧位片、颈椎动力位片、颈椎三维CT、颈椎MRI检查,术前一周开始推拉训练,吸烟患者至少于术前一周戒烟;术前一晚予西乐葆400mg口服[6]。
(2)麻醉方式选用气管插管全麻,患者仰卧位,肩部垫枕,于右侧颈椎责任间隙水平作横切口,切开皮肤、皮下及颈阔肌。止血后分别向上、下游离颈阔肌皮瓣,分离组织[7]。在胸锁乳突肌内侧缘纵行切开颈前筋膜,找到血管鞘并予以保护,锐性分离结合钝性分离至椎前筋膜,牵拉气管到对侧,在椎间隙插定位针,透视确定手术椎间隙[8]。安置手术显微镜(Leica M525 OH4 手术显微镜),切除退变责任椎间盘,切除范围为两侧颈长肌之间,再以刮匙切除残余间盘及软骨组织,超声骨刀(水木天蓬XD860A)切除椎体后骨刺,行ACCF手术者应用超声骨刀切除椎体开窗减压,后方充分减压、暴露出后纵韧带,两侧达钩椎关节,切除后纵韧带,硬脊膜膨起。
(3)A组患者手术措施如下:将一神经剥离子垂直放置于钩椎关节外侧、紧贴骨面,以保护椎动脉,超声骨刀切除增生的钩椎关节,彻底减压至神经根硬脊膜膨起,适度撑开椎间隙,撑开器撑开椎间隙,置入颈椎椎间融合装置,手术切口常规留置引流管。以超声骨刀切除增生的钩椎关节,彻底减压至神经根硬脊膜膨起。适度撑开椎间隙,置入颈椎椎间融合装置,手术切口常规留置负压引流装置[9]。
表1 两组患者一般情况比较()
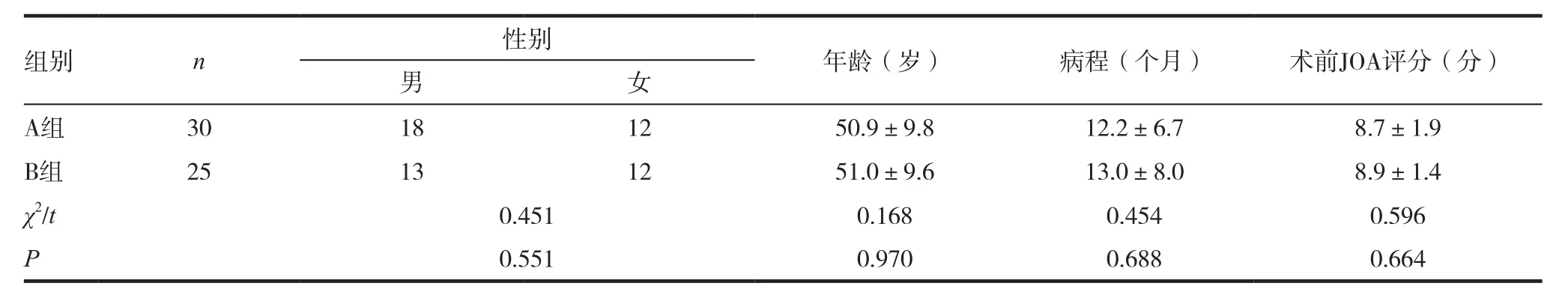
表1 两组患者一般情况比较()
组别 n 性别 年龄(岁) 病程(个月) 术前JOA评分(分)男女A组 30 18 12 50.9±9.8 12.2±6.7 8.7±1.9 B组 25 13 12 51.0±9.6 13.0±8.0 8.9±1.4 χ2/t 0.451 0.168 0.454 0.596 P 0.551 0.970 0.688 0.664
(4)B组患者手术措施如下:使用枪式椎板咬骨钳、刮匙去除钩椎关节后内侧骨赘、行神经根管潜行减压。用带钩的神经剥离子探查两侧神经根管的狭窄程度,如带钩的剥离子不能通过神经根管,则用磨钻及咬骨钳切除一侧或两侧部分钩突,扩大神经根管。用神经剥离子分离后纵韧带与硬脊膜,切除后纵韧带。在切除钩突的过程中,尽量减少切除范围,只需切除部分钩突,解除神经根压迫即可,避免向外盲目切除钩突导致椎动脉损伤[10]。适度撑开椎间隙,置入颈椎椎间融合装置,手术切口常规留置负压引流装置。
两组患者术后均予以常规颈托保护、预防感染、止痛、神经营养药物等对症处理,术后48h内拔除切口引流管,术后3d行颈椎正侧位片检查、术后3个月复查颈椎动力位片、颈椎MRI及CT[11]。
1.4 观察指标及评价标准
采用日本骨科协会评估治疗(Japanese orthopedic association,JOA)分数[12],对患者术前、术后3d、术后3个月、术后6个月及术后12个月的神经功能进行评估,JOA总评分最高为17分,最低0分。分数越低表明功能障碍越明显;计算JOA评分改善率:JOA改善率=(术后JOA评分-术前JOA评分)/(17-术前JOA评分)×100%。记录两组患者手术时间、术中出血量、手术并发症。
1.5 统计学方法
应用SPSS17.0统计学软件对数据进行分析。两组患者计量资料比较采用t检验,多组间比较采用F检验,两组计数资料比较采用χ2检验。P<0.05表示差异有统计学意义。
2 结果
2.1 两组患者手术情况比较
A组手术时间及术中出血量均小于B组,但组间比较差异无统计学意义(P>0.05),见表2。
表2 两组患者手术情况比较()
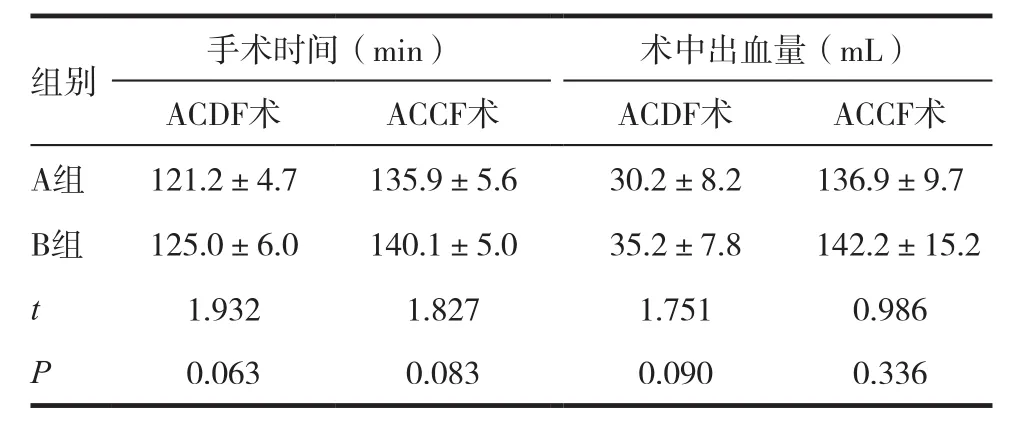
表2 两组患者手术情况比较()
组别 手术时间(min) 术中出血量(mL)ACDF术 ACCF术 ACDF术 ACCF术A组 121.2±4.7 135.9±5.6 30.2±8.2 136.9±9.7 B组 125.0±6.0 140.1±5.0 35.2±7.8 142.2±15.2 t 1.932 1.827 1.751 0.986 P 0.063 0.083 0.090 0.336
表3 两组患者术前、术后JOA评分比较(,分)
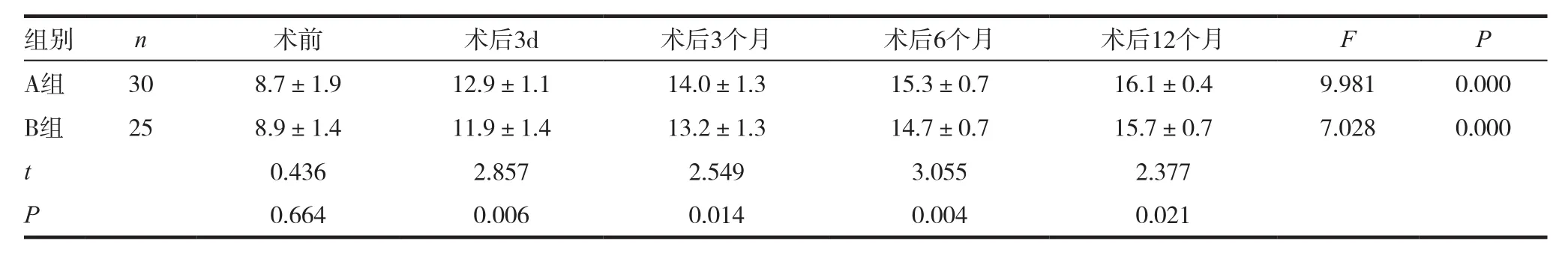
表3 两组患者术前、术后JOA评分比较(,分)
组别 n 术前 术后3d 术后3个月 术后6个月 术后12个月 F P A组 30 8.7±1.9 12.9±1.1 14.0±1.3 15.3±0.7 16.1±0.4 9.981 0.000 B组 25 8.9±1.4 11.9±1.4 13.2±1.3 14.7±0.7 15.7±0.7 7.028 0.000 t 0.436 2.857 2.549 3.055 2.377 P 0.664 0.006 0.014 0.004 0.021
表4 两组患者JOA改善率比较(,%)
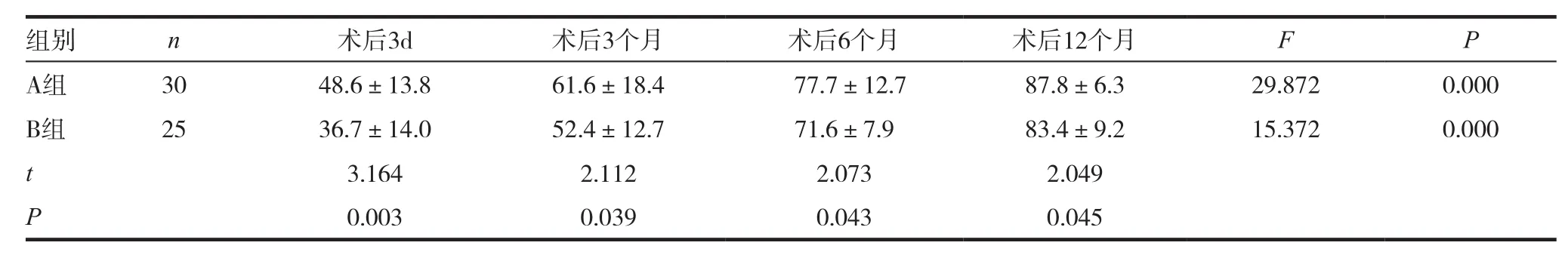
表4 两组患者JOA改善率比较(,%)
组别 n 术后3d 术后3个月 术后6个月 术后12个月 F P A组 30 48.6±13.8 61.6±18.4 77.7±12.7 87.8±6.3 29.872 0.000 B组 25 36.7±14.0 52.4±12.7 71.6±7.9 83.4±9.2 15.372 0.000 t 3.164 2.112 2.073 2.049 P 0.003 0.039 0.043 0.045
2.2 两组患者术前、术后JOA评分比较
两组患者术后3d、3个月、6个月、12个月的JOA评分均高于术前,且A组术后JOA评分均高于B组同期,差异有统计学意义(P<0.05),见表3。
2.3 两组患者JOA改善率比较
A组患者术后 3d、3个月、6个月、12个月的JOA评分改善率均高于B组同期,差异有统计学意义(P< 0.05),见表 4。
2.4 两组患者术后并发症情况
两组手术患者均未出现椎动脉损伤、神经根及硬脊膜损伤、术后脑脊液漏情况。A组患者术后出现吞咽困难1例,术后3个月症状自行缓解。
3 讨论
3.1 手术显微镜在颈前路手术中应用
传统颈前入路椎间盘减压固定融合手术治疗,手术空间狭小,为获得良好的手术视野,术者需佩戴头戴式手术放大镜、低头并根据手术部位调整颈部姿势,长时间手术易造成术者颈部疲劳,同时手术助手由于受到手术视野限制往往无法获得良好的手术视野,增加了手术风险[13]。我院使用的手术显微镜(Leica M525 OH4手术显微镜)具有三个手术目镜,且自带光源,能同时为术者及两位手术助手提供同样清晰、放大的三维手术视野,有利于提高术者与手术助手的配合度,提高手术的精细程度,更彻底的去除微小致压物,更好地进行微小出血点的止血,避免了对神经组织误损伤,提高了手术安全性。对于减少术后硬脊膜外血肿发生也有着积极意义。术中通过手术显微镜调整手术视野及方向,手术中术者无需为获得良好的手术视野改变颈部姿势、术者及助手可始终保持颈椎中立位进行手术操作、减少术者疲劳。
3.2 颈椎手术中使用超声骨刀的安全性
在传统手术中,使用枪式椎板咬骨钳或刮匙进行潜行减压,需将枪式椎板咬骨钳或刮匙置入脊髓或神经根与致压物间,存在一定脊髓及神经根损伤的风险。应用高速磨钻切骨时一旦损伤神经根、硬脊膜时,因高速磨钻的卷刮易造成硬脊膜撕裂及神经根严重损伤。且应用传统工具行颈椎前路手术的学习曲线较长,对术者手术技巧要求较高[14]。超声骨刀作为一种新型切骨工具,其工作原理为将电能转换为机械能,其工作频率为22.5~40kHz。在超声刀声强作用下,骨组织产生机械振动并超过其弹性极限,从而达到切割效果。因超声刀作用于软组织产生的机械振动低于其弹性极限,软组织可通过弹性振动来吸收碰触超声刀头时产生的振动能量,从而避免损伤[15]。超声骨刀配备有不同类型的刀头,我院在临床实践中所采用的方法是使用超声骨刀切除颈椎后缘骨赘时以片状刀头直接沿椎体长轴自终板斜形并逐层切割至椎体后缘,进一步切除椎体后缘骨赘;或用匙状刀头由浅入深刮除骨赘。在治疗过程中不必追求一次性全切骨赘,而是尽量避免突破骨性组织后刀头对软组织的惯性物理作用,降低术中脊髓及硬脊膜损伤风险[16]。
3.3 钩椎关节切除的安全性
钩椎关节退变其形成的骨赘可以影响到椎间孔孔径、颈椎管管径及椎动脉横突孔孔径,造成临床上各种类型颈椎病症状。临床上通过手术切除退变的钩椎关节,可以扩大椎间孔前后径、去除神经根及脊髓前方的致压物,从而达到直接减压的效果。手术的难点在于切除钩椎关节时前外方有椎动脉,后外方有颈脊神经根,后内侧为脊髓,稍许失手即可造成严重后果。在本组30例切除钩椎关节患者手术过程中,未出现椎动脉损伤、脊神经根、脊髓损伤等并发症。结合以往临床经验,本研究提示在切除钩椎关节时将一神经剥离子垂直放置于钩椎关节外侧、紧贴骨面,可以更好地保护椎动脉,再以超声骨刀片状刀水平方向由前向后切除钩椎关节,如遇减压不充分时可改用超声骨刀勺状刀头由后向前、由浅入深刮除增生钩椎关节直至彻底减压、神经根硬脊膜膨起(图1)。实施此类手术时我院一般于杂交手术室进行,手术室配备的西门子造影机具有快速三维CT成像功能,该检查具有扫描时间短、成像清晰、多平面重建等优点,术中可实时确认神经根管扩大及减压情况(图2),保证手术效果。
综上所述,显微镜辅助下应用超声骨刀行钩椎关节切除减压钩椎关节切除减压在神经根型颈椎病及伴有神经根症状的混合型颈椎病手术治疗中是有效、安全的方法。但本研究仅纳入55例患者,样本数量较少,末次随访时间较短,仅为12个月,结果验证有待于更大量样本、多中心、更长随访时间及前瞻性的研究。
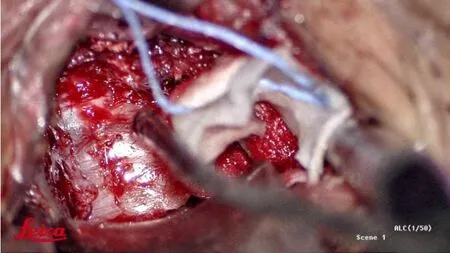
图1 术中神经根彻底减压、硬脊膜膨起
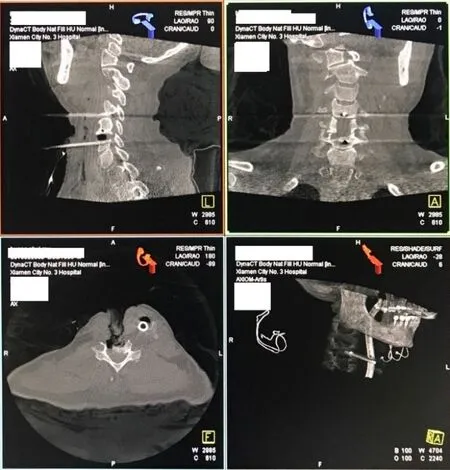
图2 术中影像学检查确认神经根及脊髓减压范围充分
