一测多评法测定多枝雾水葛软膏中3种黄酮类成分含量*
2020-10-29梁素仪莫楚铭李志慧郭丽冰陶曙红尹永芹
梁素仪,莫楚铭,李志慧,郭丽冰,陶曙红,尹永芹
(广东药科大学中药学院,广州 510006)
多枝雾水葛[Pouzolziazeylanica(L.) Benn.Var.Microphylla (Wedd.)W.T.Wang]为荨麻科雾水葛属植物。研究表明,多枝雾水葛提取物具有消肿排脓、促进伤口愈合、抗炎、镇痛、抑菌等作用[1-3],通过大孔吸附树脂纯化的多枝雾水葛总黄酮具有显著的体外抗炎作用[4]。本课题组以多枝雾水葛总黄酮提取物为药效成分,自主研制了多枝雾水葛软膏(专利公开号:CN107233368A),该软膏具有抗感染、消肿排脓、加速皮肤创面愈合等功效[5-7]。目前,对多枝雾水葛软膏质量标准已有研究,确定了多枝雾水葛总黄酮中的7种黄酮苷类成分,其中芹菜素-6-C-α-L-阿拉伯糖8-C-β-D-葡萄糖苷(简称:芹菜素苷),槲皮素-3,7-2-O-α-L-吡喃鼠李糖苷(简称:槲皮素苷)以及山奈酚-3,7-2-O-α-L-吡喃鼠李糖苷(简称:山奈酚苷)3种成分总含量>50%[6],由于对照品难以获得,需要自制,限制了对本制剂质量控制的应用。王智民等[8]提出一测多评方法,通过中药有效成分间存在的内在函数关系和比例关系,仅测定 1种成分 (对照品较容易得到者),来实现多种成分 (对照品没有或难以供应 ) 的同步监控。该方法操作简易、精确,广泛应用于中药材以及中药制剂的质量控制[9-14]。笔者在本实验将一测多评法用于多枝雾水葛软膏的质量控制,以含量最高的槲皮素苷为内参物,建立其他两个成分的相对校正因子,以期为多枝雾水葛软膏质量控制和评价提供技术检测依据。
1 仪器与试药
1.1仪器 LC-20AT高效液相色谱仪(日本岛津企业管理有限公司),SPD-20A检测器(日本岛津企业管理有限公司),KQ-30E型超声波清洗器(昆山市超声仪器有限公司),Sartorius BP211D电子天平(南京创睿仪器仪表有限公司,感量:0.01 mg)。
1.2试药 芹菜素苷对照品(自制,含量≥98%),槲皮素苷对照品(自制,含量≥98%),山奈酚苷对照品(自制,含量≥98%)。TLC验证:不同展开剂下均为单一斑点;HPLC检测:用面积归一化法检测不同波长不同流动相下的对照品峰面积百分比,结果峰面积百分比≥98%。多枝雾水葛软膏(自制,批号:2018112401,2018112402,2018112403,2018112404,2018112405,2018112406,2018112407,2018112408,2018112409),乙腈(广州飞恩新材料有限公司,色谱纯),甲酸(广州飞恩新材料有限公司,色谱纯),纯化水(广州屈臣氏食品饮料有限公司)。
2 方法与结果
2.1多枝雾水葛总黄酮提取物及软膏的制备
2.1.1多枝雾水葛总黄酮提取物的制备[6]取多枝雾水葛药材,[2016年1月购自广西壮族自治区玉林市,经广东药科大学中药标本馆刘基柱副教授鉴定为荨麻科雾水葛属植物多枝雾水葛Pouzolzia zeylanica (L.) Benn. Var. Microphylla (Wedd.)W.T.Wang带根全草]粉碎,称量药材粗粉500 g,置圆底烧瓶,分别加入8倍量石油醚80 ℃回流提取2 次,每次1 h。滤渣挥去石油醚,加入8倍量70%乙醇回流提取3 次,每次1 h,滤过,合并滤液,减压浓缩至无醇味,加水使充分溶解,3000 r·min-1离心10 min(r=16 cm),取上清液加水调整至相当于生药0.3 g·mL-1并调节 pH 值至5。将上述样品溶液加入AB-8大孔树脂柱(直径:5.0×30 cm),上样流速2倍柱体积(BV)·h-1,加水2 BV 除杂,加 60%乙醇2 BV以2 BV·h-1洗脱,收集洗脱液,减压浓缩至流浸膏状,冷冻干燥,粉碎,即得。
2.1.2软膏的制备 分别称取硬脂酸2.4 g、液体石蜡1 g、白凡士林1 g和单硬脂酸甘油酯1.1 g,85 ℃水浴加热溶化作为油相。称取十二烷基硫酸钠0.14 g、三乙醇胺0.6 g、甘油1.2 g、纯化水12 mL、月桂氮酮0.7 g、尼泊金乙酯0.01 g及多枝雾水葛总黄酮提取物1.00 g,85 ℃水浴加热至无细小颗粒作为水相。将水相缓慢加入油相,磁力搅拌器200 r·min-1搅拌5 min至乳化完全,制得多枝雾水葛软膏。
2.2色谱条件及系统适应性 XBridge Shield RP18色谱柱(4.6 mm×250 mm,5 μm),流动相为0.2%甲酸-乙腈溶液,梯度洗脱乙腈10%~60%,50 min,流速0.8 mL·min-1,检测波长330 nm,柱温30 ℃,进样量5 μL。此条件下各待测成分分离度良好,色谱图见图1。

A.软膏基质阴性对照品;B.混合对照品;C.软膏供试品(批号:2018112401);1.芹菜素-6-C-α-L-阿拉伯糖8-C-β-D-葡萄糖苷;2.槲皮素-3,7-2-O-α-L-吡喃鼠李糖苷;3.山奈酚-3,7-2-O-α-L-吡喃鼠李糖苷。
Fig.1HPLCchromatogramofPouzolziaZeylanicaointmentandthreereferencestandards
2.3对照品溶液的制备 精密称取芹菜素苷10.40 mg、槲皮素苷20.54 mg,山奈酚苷30.45 mg,置10 mL量瓶,70%乙醇溶解定容,制成每毫升含芹菜素苷1.04 mg、槲皮素苷2.054 mg、山奈酚苷3.045 mg的混合对照品储备液。分别取储备溶液0.2,0.5,1.0,1.5,2.0,2.5 mL置5 mL量瓶,加70%乙醇溶解定容,得3个对照品混合溶液,将其编号为Ⅰ,Ⅱ,Ⅲ,Ⅳ,Ⅴ,Ⅵ。
2.4供试品溶液的制备 精密称取多枝雾水葛软膏1.00 g于50 mL具塞锥形瓶,精密移取70%乙醇30 mL于锥形瓶中,称质量,经45 min超声处理(300 W,5 Hz),放凉,缓慢滴加70%乙醇补足减失质量,混合均匀,转移至冰箱4 ℃静置1 h,滤过,取滤液至50 mL量瓶,以70%乙醇定容至50 mL,得0.02 g·mL-1供试品溶液。
2.5方法学考察
2.5.1线性关系考察 取“2.3”项对照品溶液Ⅰ,Ⅱ,Ⅲ,Ⅳ,Ⅴ,Ⅵ分别进样5 μL,平行各进样3针,按“2.2”项HPLC色谱条件测定峰面积,计算峰面积平均值。结果以浓度(μg·μL-1)为横坐标(X),峰面积为纵坐标(Y),线性回归,绘制标准曲线,得回归方程为:芹菜素苷Y=238 709X-1 268.7(R2=0.9991),线性范围为41.6~520.0 μg·mL-1,槲皮素苷Y=169 202X+ 1 124.9(R2=0.999 3),线性范围为82.2~1027.0 μg·mL-1,山奈酚苷Y=51 507X-184.36(R2=0.999 3),线性范围121.8~1 522.5 μg·mL-1。
2.5.2精密度实验 取多枝雾水葛软膏适量,按照“2.4”项方法制备供试品溶液,在“2.2”项色谱条件下操作,连续进样供试品溶液6次,测定芹菜素苷、槲皮素苷、山奈酚苷峰面积,计算RSD。结果显示芹菜素苷、槲皮素苷及山奈酚苷的峰面积RSD分别为1.46%,1.42%,1.78%,RSD均<2%,表明实验仪器精密度良好。
2.5.3重复性实验 取多枝雾水葛软膏适量,各6份,按“2.4”项方法制备供试品溶液,在“2.2”项色谱条件操作,测定供试品溶液中芹菜素苷、槲皮素苷、山奈酚苷的峰面积,计算RSD。结果显示芹菜素苷、槲皮素苷及山奈酚苷的峰面积RSD分别为2.82%,0.99%,1.47%,RSD均<3%,表明该方法有良好的重复性。
2.5.4稳定性实验 取供试品溶液,按“2.2”项色谱条件,分别在 0,4,8,12,20,24 h 不同时间点测定芹菜素苷、槲皮素苷、山奈酚苷的峰面积,计算RSD。结果芹菜素苷、槲皮素苷及山奈酚苷的峰面积RSD分别为3.38%,3.25%,4.19%,RSD均<5%,表明供试品溶液在24 h内测定结果基本稳定。
2.5.5加样回收率实验 称取6份已知含量多枝雾水葛软膏,精密称重,精密加入芹菜素苷3.10 mg;取已知含量多枝雾水葛软膏样品6份,精密加入槲皮素苷9.00 mg;取已知含量多枝雾水葛软膏样品6份,精密加入山奈酚苷3.66 mg。按“2.4”项方法制备供试品溶液,依法测定,计算加样回收率,结果见表1。多枝雾水葛软膏中芹菜素苷的平均加样回收率为98.16%,RSD为0.84%(n=6),槲皮素苷的平均加样回收率为97.83%,RSD为1.17%(n=6)。山奈酚苷平均加样回收率97.77%,RSD为1.24%(n=6),表明软膏中3种成分加样回收实验良好,符合定量分析要求。
2.6相对校正因子的建立
2.6.1相对校正因子的测定 精密吸取“2.3”项编号为Ⅰ,Ⅱ,Ⅲ,Ⅳ,Ⅴ,Ⅵ 的混合对照品溶液各5 μL,在“2.2”项色谱条件下进样测定,记录色谱峰峰面积。相对校正因子计算公式fz/x=fz/fx=(Ax×Cz)/(Cx×Az),其中C代表浓度,A代表峰面积,z为对照品内参物;x为对照品中待测成分,以多枝雾水葛软膏提取物中特征成分槲皮素苷为内参物,分别建立其与芹菜素苷和山奈酚苷之间的校正因子(relative correlatoin factor,RCF)值,结果见表2。
2.6.2不同柱温对RCF的影响 取“2.3”项混合对照品溶液,进样 5 μL,考察其在不同柱温(25,30,35 ℃)下对 RCF 值的影响,按“2.2”项色谱条件,记录多枝雾水葛软膏3种成分在不同柱温下的峰面积值,计算RCF值。结果显示,不同柱温(25,30,35 ℃)条件下测得的f槲皮素苷/芹菜素苷和f槲皮素苷/山奈酚苷的RSD分别为0.71%,1.27%,RSD 均<5%,说明柱温在此范围内波动时对RCF值并无大的影响,校正因子在25~35 ℃均适用。
2.6.3不同流速对RCF值的影响 取“2.3”项混合对照品溶液,进样5 μL,考察其在不同流速(0.7,0.8,0.9 mL·min-1)条件下对RCF值得影响,按“2.2”项色谱条件,记录多枝雾水葛软膏3个成分峰面积值,计算RCF值。结果显示,不同流速(0.7,0.8,0.9 mL·min-1)条件下测得f槲皮素苷/芹菜素苷和f槲皮素苷/山奈酚苷的RSD分别为1.19%,1.08%, RSD 均<5%,说明流速在此范围内波动时对 RCF 值影响不大。
2.6.4不同色谱柱对RCF值的影响 取“2.3”项混合对照品溶液,进样5 μL,考察其在不同色谱柱:XBridge Shield RP18色谱柱(4.6 mm×250 mm,5 μm),Waters symmetryshild RP18(4.6 mm×250 mm,5 μm) ,Dikma Platisil ODS(4.6 mm×250 mm,5 μm)对RCF值的影响,按“2.2”项色谱条件,记录多枝雾水葛软膏中3种黄酮苷类成分的峰面积值,计算RCF值。结果显示,不同色谱柱测得的f槲皮素苷/芹菜素苷和f槲皮素苷/山奈酚苷的RSD分别为4.53%,0.80%,RSD 均<5%,说明3个色谱柱测定对 RCF 值影响不大。见表3。
2.7待测组分色谱峰的定位 色谱峰定位以多枝雾水葛软膏中3种黄酮苷类成分色谱峰相对保留时间来确定,结果显示,两待测成分与内参物色谱峰相对保留时间的RSD分别为0.11%,0.10%,均<5%。
2.8相对误差评价一测多评法与外标法所得含量结果 分别精密称取9批自制软膏各1.00 g,按照“2.3”项方法制备供试品溶液,依法测定,记录各成分色谱峰峰面积,分别采用常规外标法和一测多评法计算各成分含量,比较两种方法所得结果(表4),外标法所测槲皮素苷平均含量38.482 8 mg·g-1,芹菜素苷平均含量3.262 2 mg·g-1,山奈酚苷平均含量6.346 5 mg·g-1,一测多评法中芹菜素苷平均含量3.240 0 mg·g-1,山奈酚苷6.320 0 mg·g-1,见表4。9批软膏含量测定结果,两种方法RSD均<5%,差异无统计学意义。

表3 不同因素对RCF值的影响
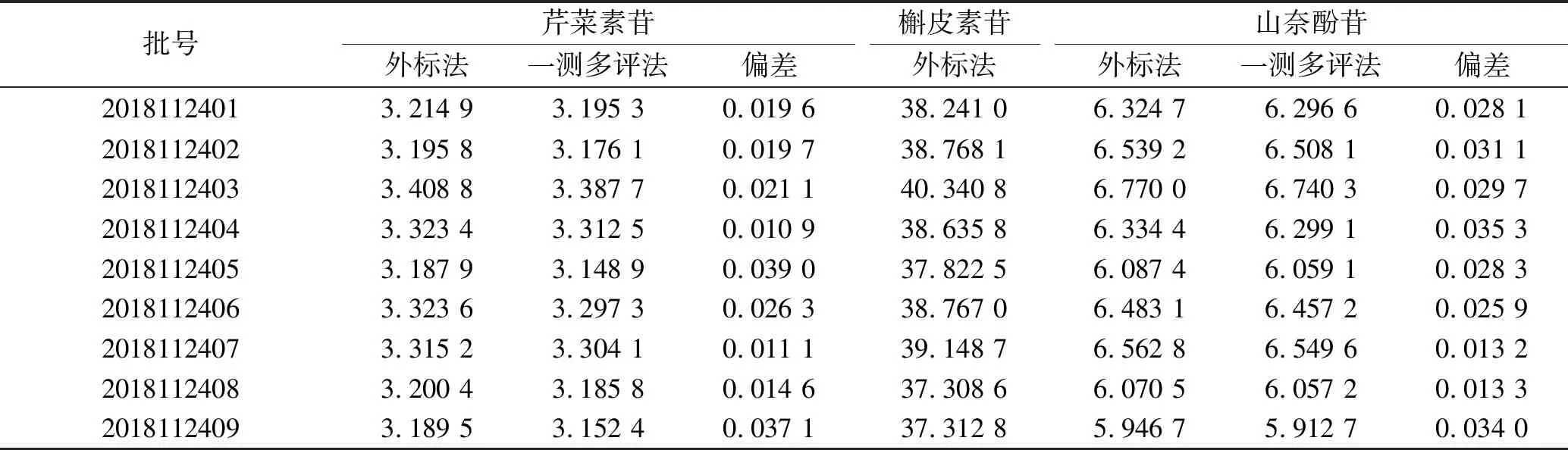
表4 一测多评法与外标法所得含量结果比较
3 讨论
笔者在本实验考察相对保留时间法及保留时间差法,结果显示,待测成分与内参物色谱峰相对保留时间与保留时间的差值的RSD分别均<5%。但保留时间差值的RSD较相对保留时间的RSD大,故采用相对保留时间法来定位色谱峰。对软膏的供试液处理,前期用简单的过滤方法,放置一段时间后滤液中有细小颗粒,滤过不完全,放入冰箱冷处理后,情况好转。
笔者在本实验选用槲皮素苷为内参物,因为其在多枝雾水葛药材及软膏中含量均最高,自制对照品相对容易些。研究结果表明,3种主要有效成分色谱分离效果良好,所建立的一测多评法,方法耐用性良好,与外标法结果比较差异无统计学意义,可用于多枝雾水葛软膏的含量测定,为多枝雾水葛软膏质量标准完善及质量评价提供了依据。
多枝雾水葛总黄酮有效部位中,其他4种黄酮苷类成分含量低,未能大量分离出来作为对照品,故暂未建立其与槲皮素苷之间的相对校正因子,此方面研究有待课题组后续进一步完善。
