高浓度EDTA-Co(Ⅲ)废水处理工艺探索研究
2020-10-26韩笑
韩 笑
(浙江华友钴业股份有限公司, 浙江 桐乡 314500)
0 前言
某特殊钴冶金生产过程中,需加入高浓度的EDTA(乙二胺四乙酸),导致其合成尾液中含有大量EDTA,废水中Co与CODCr都较高,需要经过后续处理才能达标排放(《铜、镍、钴工业污染物排放标准》排放标准Co≤1 mg/L、CODCr≤300 mg/L)。
氢氧化钴废水主要由硫酸钠、硫酸钴及钴络合物组成。由生产工艺所决定,废水中Co大部分以+3价存在,而Co(Ⅲ)与EDTA的络合物在所有EDTA金属络合物中稳定性最高(稳定常数Kf(Co(EDTA)-)=1.0×1036),造成此类废水使用常见方法处理困难。
EDTA-Co(Ⅲ)废水处理未见相关报道,而处理EDTA废水方法主要有化学法、物理法、生化法等,经过相关实验研究发现:物理吸附法[1]处理络合Co废水时吸附不够完全、吸附容量小,不能满足废水处理需求;纳滤法[2-4]由于废水中含有合成过滤后生成的大量纳米级氢氧化钴(Ⅲ)而导致膜容易堵塞,普通酸无法溶解,导致纳滤法无法正常使用;废水中硫酸钠含量高,会对微生物的生化活性产生抑制,导致该废水无法应用生化法[5]进行处理;微电解法[6]无法将EDTA分解完全,且微电解法中Fe与Co的活性相近,Fe2+与Co(Ⅲ)相互作用较弱,又由于EDTA-Co(Ⅲ)的稳定性影响,导致Co与CODCr处理效果均不够理想;同时通过探索,其它方法如:O3氧化法、电解法等也无法将EDTA-Co(Ⅲ)废水一次性处理达标。
芬顿氧化法是一种高级氧化法,产生的羟基自由基氧化电位高,本研究采用常规沉淀去除重金属Co、Fenton氧化法降解CODCr。
1 实验部分
1.1 实验仪器及试剂
六联异步搅拌水浴锅、四联电磁搅拌机、电感耦合等离子体光谱仪(ICP);EDTANa2、CaO、NaOH、Na2CO3、H2O2、FeSO4·7H2O、K2Cr2O6、H2O2等分析纯试剂。
1.2 实验过程
1.2.1 废水来源及水质情况
本次实验全过程使用中试生产氢氧化钴所产生废水,其Co浓度为397.4 mg/L、CODCr为2 194.3 mg/L、Na2SO4浓度约为184 g/L、pH为8.5~9.0、EDTA约0.01 mol/L。
1.2.2 EDTA标准CODCr曲线
由于准确测定EDTA较困难,本实验通过测定CODCr值来表征EDTA浓度情况,绘制CODCr与EDTA浓度标准曲线。
配置EDTA浓度分别为0.005 mol/L、0.01 mol/L、0.015 mol/L、0.02 mol/L标准溶液各100 mL,并进行CODCr的检测,绘制EDTA与CODCr标准曲线如图1所示。

图1 CODCr与EDTA标准曲线
1.2.3 实验条件
为避免Co对CODCr影响,本次实验先进行沉钴实验,后以沉钴后液进行Fenton氧化降解CODCr实验,最后进行沉钴与氧化顺序实验。
1.2.4 主要测试项目及方法
CODCr:重铬酸钾法(HJ 828—2017);Co:ICP。
2 结果与讨论
2.1 沉钴实验
2.1.1 沉淀剂的选择
分别加入8倍理论量的CaO、Ca(OH)2、NaOH、Na2CO3于70 ℃反应4 h沉淀Co。

表1 沉淀剂选择实验
由于Ca2+可以与EDTA发生络合,高含量的Ca可以与Co进行置换,故含Ca沉淀剂沉淀效果明显较好,同时,由于CaO和Ca(OH)2溶解度小,故仍存在大量固体,对络合Co具有一定的吸附作用,但从CODCr方面进行分析,沉Co的主要反应是置换。而CaO较Ca(OH)2虽然效果稍差,但CaO用量更小、价格更低,故沉钴所用沉淀剂选用CaO。
2.1.2 温度对沉钴效果的影响
CaO加入量为10 g/L、反应6 h时,由图2可知,温度越高对沉钴越有利,但在70 ℃时已趋于平衡,继续升高温度效果不够明显,在70 ℃时沉钴后液Co浓度为2.13 mg/L,Co去除率>99%,故实验确定沉钴温度为70 ℃。

图2 温度对沉钴效果的影响
2.1.3 反应时间对沉钴效果的影响
CaO加入量为10 g/L、温度为70 ℃时,由图3可以看出,时间越长沉钴效果越好,在4 h后沉钴效果基本趋于稳定,沉钴后液中Co浓度降低到2.24 mg/L左右,Co去除率>99%,故实验确定沉钴时间为4 h。

图3 反应时间对沉钴效果的影响
2.1.4 CaO加入量对沉钴效果的影响
反应温度为70 ℃、时间为4 h时,CaO加入量越大沉钴效果越好,但在加入量达到10 g/L后沉钴效果已基本稳定,其原因可能为硫酸体系中CaSO4为微溶物质,而络合Co可被高浓度Ca进行置换,但Ca达到饱和后,继续加大CaO加入量已无明显作用,故实验确定沉钴CaO加入量选择为10 g/L。

图4 CaO加入量对沉钴效果的影响
2.2 CODCr氧化降解实验
CODCr降解实验所用废水为CaO加入量10 g/L时、进行4 h温度为70 ℃的沉钴后液,由于过滤后液温度仍有约65 ℃,故Fenton反应不另行加温,温度定为65 ℃。
2.2.1 pH值对CODCr的影响
由图5可知,不同pH值对CODCr去除率随pH值的升高先增大后降低,在pH为2.5~3.5时CODCr去除率达到最高。其原因可能为[7~8]:Fenton反应在pH值<3时,Fe2+会形成[Fe(Ⅱ)H2O)5]2+水合物,使Fe2+与H2O2反应速度缓慢,而当pH值>3时,Fe离子会产生沉淀,溶解态的铁离子减少,Fenton反应受抑制。

图5 pH值对CODCr的影响
2.2.2 H2O2投加量对CODCr影响
由图6可知,CODCr的去除效率随H2O2投加量的增加而升高,但当H2O2投加量达到980 mmol/L时继续投加H2O2反而会引起CODCr下降。其原因可能为,过量的H2O2会消耗体系中的·OH,体系的Fenton与类Fenton氧化作用受到限制,使EDTA的分解率下降[9]。实验确定H2O2的最佳投加量为980 mmol/L。

图6 H2O2对CODCr影响
2.2.3 Fe2+投加量对CODCr的影响
随着Fe2+投加量的增加,CODCr去除率升高,当Fe2+投加量为11 mmol/L,CODCr去除率达到最大值,继续增加Fe2+投加量,CODCr去除率趋于稳定。实验确定Fe2+的最佳投加量为11 mmol/L。

图7 Fe2+对CODCr的影响
2.3 处理顺序对沉钴效果影响
通过对先沉淀钴后Fenton氧化实验与先Fenton氧化后沉淀钴实验进行对比,确定不同方案对Co与CODCr的影响,而反应过程中实验条件根据2.2、2.3节确定,实验结果如表2所示。
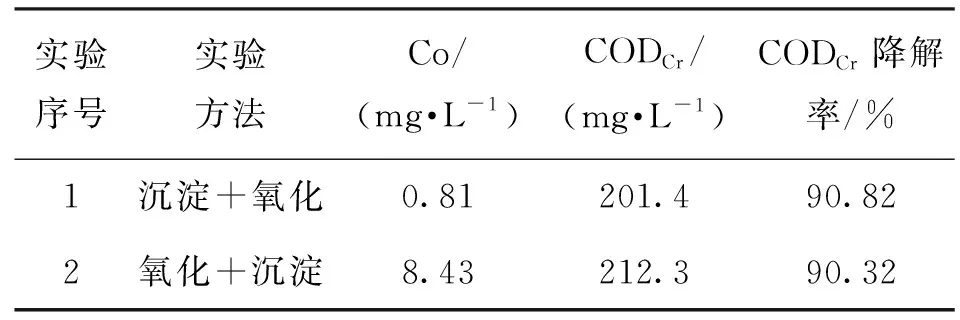
表2 处理顺序实验
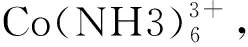
3 结论和展望
络合废水先经CaO沉淀除Co,后经Fenton氧化降解CODCr,可以将Co降低到1 mg/L以下、CODCr降低到300 mg/L以下,达到废水国家二级排放标准。
工艺条件为:沉淀段:CaO加入量为10 g/L、温度为70 ℃以上、反应时间为4 h、沉钴完成后过滤;Fenton氧化絮凝段:过滤后液调节pH 2.5~3.5、H2O2加入量为980 mmol/L、Fe2+加入量为11 mmol/L、反应时间为30 min、反应后调节pH为7~9、絮凝沉淀除Fe3+、Co。
通过该方法,废水可以处理达到国家二级排放标准,但该方法存在过程复杂,成本偏高的问题,有进一步改进的空间,如何提高Fenton试剂的利用率、简化操作步骤将是后续探索的主要方向,可以考虑通过与微波、活性炭等处理方法联用,降低Fenton试剂的加入量。
