基于免疫磁珠的胶体金免疫层析法快速检测水产品中地西泮残留
2020-10-23桑丽雅陈笑笑陈青舟李诗言
桑丽雅,陈笑笑,王 扬,陈青舟,周 钦,李诗言,叶 茂,*
(1.杭州南开日新生物技术有限公司,浙江杭州 311215;2.浙江省水产质量检测中心,浙江杭州 310023)
地西泮(Diazepam,DZP)又名安定,是一种苯二氮卓类中枢神经系统镇静剂,临床上主要用于治疗焦虑、镇静催眠、抗癫痫等[1-2]。近年来,随着畜牧养殖业的迅速发展,在提高饲料转化率和高额利润的驱动下,地西泮被大量非法用作动物生长促进剂[3]。当人体长期摄入含地西泮残留的动物源性食品后,会引起记忆受损、头脑昏沉,甚至白细胞和运动神经受损等严重不良反应,给人类健康带来严重的潜在威胁[4-5]。2002年,我国农业部发布的《食品动物禁用的兽药及其它化合物清单》(第193号公告)和《动物性食品中兽药最高残留限量》(第235号公告)中明确规定,地西泮只能用于治疗,禁止用于食品动物抗应激、提高饲料报酬和促生长,不得在动物性食品中检出[6-7]。
目前,地西泮残留检测方法主要有高效液相色谱法(high performance liquid chromatography,HPLC)[8-9]、气相色谱串联质谱法(gas chromatography-mass spectrometer,GC-MS)[10]、液相色谱串联质谱法(liquid chromatography-tandem mass spectrometry,LC-MS/MS)[11-13]以及酶联免疫吸附法(enzyme linked immunosorbent assay,ELISA)[14-15]等。这些方法虽然灵敏度高、准确性好,但样本前处理复杂、耗时长、费用高,难以满足现场大批量快速检测要求。因此,如何快速、准确检测动物源性食品中地西泮残留,具有重要的意义。
胶体金免疫层析法(colloidal gold immunochromatographic assay,CGICA)是以胶体金作为示踪标志物应用于抗原抗体的一种新型检测方法,因其简便快速、结果直观,无需复杂操作和特殊设备等特点,成为了食品安全快速检测的有效方法。柳爱春等[16]采用CGICA检测水产品中的喹诺酮类药物,灵敏度高于HPLC法,检测结果与LC-MS/MS法较一致,单个样品检测耗时25 min。霍如林等[17]制备了猪肝中喹乙醇残留的胶体金免疫层析试纸条,可在15 min内完成定性和定量检测;Han等[18]利用CGICA建立的多条带免疫层析法,能在10 min左右完成羊体液中磺胺类药物的快速检测。但CGICA在实际应用中仍存在灵敏度低、不能满足低检测限检测要求等不足[19]。本研究建立了一种快速检测水产品中地西泮残留的免疫磁珠-胶体金免疫层析法,利用免疫磁珠实现地西泮的高倍数富集和快速分离[20-21],从而提高检测方法的灵敏度,可用于实际水产品中地西泮残留的现场快速检测。
1 材料与方法
1.1 材料与仪器
鱼、虾、鳖等样本 均来自杭州市某农贸市场,取可食用部分约100 g,用组织捣碎机充分绞碎混匀,装入干净容器,标明标识,-18 ℃避光保存;地西泮、氟西泮、替马西泮、奥沙西泮、氟硝西泮标准品 中国医药(集团)上海化学试剂公司;链霉亲和素磁珠 赛默飞世尔科技公司(挪威);地西泮单克隆抗体、包被抗原 课题组自制;牛血清白蛋白(BSA)、羊抗鼠二抗 美国Sigma公司;活泼酯化的长链生物素(Sulfo-NHS-LC-Biotin) 美国Pierce公司;C18固相萃取柱(3 mL,500 mg) 美国Supelco公司;其余试剂 均为国产分析纯。
Agilent 6890N-5973I气相色谱质谱联用仪 美国Agilent公司;紫外-可见分光光度计、磁力架 赛默飞世尔科技(中国)有限公司;BioJet XYZ3000型点膜机、CM4000型试纸条切割机 美国BioDot公司;硝酸纤维素膜(NC膜) 美国Millipore公司;MYP11-2恒温磁力搅拌器 上海梅颖浦仪仪表制造有限公司;Avanti J-26XP高速冷冻离心机 美国Beckman公司;DHG-9023A型恒温鼓风干燥箱 上海精宏实业设备有限公司;胶体金读数仪 杭州南开日新生物技术有限公司。
1.2 实验方法
1.2.1 地西泮胶体金免疫层析试剂卡制备
1.2.1.1 胶体金制备及其标记抗体优化 将100 mL 0.01%氯金酸溶液置于仪器上加热至沸腾后,加入1 mL 0.1%柠檬酸三钠水溶液,保持煮沸15 min,冷却至室温后,用0.1 mol/L K2CO3和0.1 mol/L HCl调节pH至9,4 ℃保存备用,并用可见光-紫外分光光度计(400~800 nm)测定溶液的吸收峰波长和吸收值。
将地西泮单克隆抗体用0.01 mol/L的PB缓冲液(pH7.4)配制成0.5 mg/mL溶液,15000 r/min 4 ℃离心30 min,去除蛋白聚合物。取5支小试管中分别加入1 mL胶体金溶液和10、15、20、25、30 μg/mL的抗体用量进行预标记,10 min后每管分别加入10 μg BSA结合未标记完全的胶体金。标记结束后,每个浓度的金标抗体溶液均取2 μL滴加到空白胶体金垫上,分别滴加PBS(0.01 mol/L)和地西泮标准品(1 μg/L),筛选抗体最佳标记量。余下的胶体金溶液,以抗体最佳标记量进行标记,15000 r/min离心30 min,弃上清,沉淀用10 mL金标抗体保存液使其复溶,4 ℃保存备用。
1.2.1.2 NC膜抗原、羊抗鼠二抗包被量优化 T线抗原浓度分别设置0.3、0.6和1.2 mg/mL三个浓度;C线羊抗鼠二抗浓度分别设置0.75、1.50和3.00 mg/mL三个浓度,抗体以最佳标记量进行标记,分别滴加PBS(0.01 mol/L)和地西泮标准品(1 μg/L),使用胶体金读数仪进行读数。判定原则:T/C比值1.0(T线比C线淡或几乎看不见)为阳性;T/C比值≥1.0(T线比C线深或一样深)为阴性;若未出现任何色带或C线未出现,则此试剂卡已失效、过期或操作不当,需另做一次测试。
1.2.1.3 金标抗体喷量优化 分别选择2.0、3.0和4.0 μL/cm三个喷量,按照已经筛选出的最佳T线抗原浓度、C线羊抗鼠二抗浓度和抗体标量,制备胶体金试纸条,分别滴加PBS(0.01 mol/L)和地西泮标准品(1 μg/L),使用胶体金读数仪进行读数。
1.2.1.4 试剂卡的制备及组装 将金标抗体喷在胶体金垫上,然后用点膜仪将地西泮人工抗原(T线)、羊抗鼠二抗(C线)喷于NC膜上,37 ℃烘干后,按图1方法组装成胶体金试纸条。将试纸条切成宽度为3.84 mm,加塑料卡后制成试剂卡。
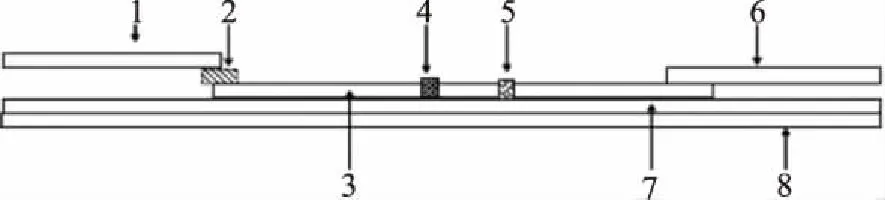
图1 免疫胶体金试纸条结构示意图
1.2.2 免疫磁珠-胶体金免疫层析法构建及评价
1.2.2.1 免疫磁珠的制备 参照周松等[22]制备免疫磁珠的方法并略加改进。取一定量的地西泮单克隆抗体溶于PBS(0.01 mol/L,pH7.4)中调整浓度至2~3 mg/mL,按摩尔比1∶3加入Sulfo-NHS-LC-Biotin,25 ℃下孵育2 h,用0.01 mol/L PBS透析3 d,获得生物素化抗体按体积比1∶1加入甘油-20 ℃保存。
取1 mg链霉亲和素磁珠,用800 μL PBS(0.01 mol/L)洗涤2次并重悬,磁力架磁吸分离移除上清,加入50 μg生物素化抗体,放置摇床上,70 r/min室温下偶联1 h,期间保持磁珠悬浮状态。磁分离去上清,用1 mL封闭缓冲液(0.01 mol/L PBS,0.01% BSA)重悬,4 ℃封闭过夜。磁分离去上清,用800 μL PBST(0.01 mol/L PBS,0.05% Tween-20,pH7.4)洗涤洗涤3次,最后用1 mL 0.01 mol/L PBS重悬,4 ℃下保存。
1.2.2.2 样品前处理 免疫磁珠法:准确称取(4±0.05) g均质样本,加入10 mL含20%甲醇-PBS(0.01 mol/L,pH7.4)溶液后于涡旋振荡器上振荡5 min,5000 r/min离心3 min。取0.5 mL上清液加入300 μL免疫磁珠,室温下涡旋富集5 min。磁吸回收磁珠,并用PBS(0.01 mol/L,pH7.4)洗涤3次,200 μL纯甲醇洗脱5 min,收集洗脱液用PBS(0.01 mol/L,pH7.4)稀释至1 mL,供胶体金免疫层析试剂卡检测。
常规处理法:参考Bugey等[23]和Ming等[24]的方法并优化,具体步骤为:准确称取(4±0.05) g均质样本,加入1 mL 1 mol/L盐酸和4 mL乙腈,涡旋振荡5 min,之后加1 g氯化钙,涡旋振荡5 min,5000 r/min离心5 min,取2 mL上清液于75 ℃氮气吹干,加1 mL PBS(0.01 mol/L,pH7.4)复溶,供胶体金免疫层析试剂卡检测。
样品净化:当按免疫磁珠法进行前处理时,收集的洗脱液用水稀释至1 mL,作为备用液;当按常规处理法进行样品前处理时,经氮气吹干的残余物中加入1 mL水复溶,作为备用液。依次用3 mL甲醇,3 mL水活化C18固相萃取柱,取备用液过柱,3 mL甲醇-水(50∶50,v/v)洗涤,3 mL甲醇-水(70∶30,v/v)洗脱。洗脱液于50 ℃水浴下氮气吹干,用200 μL乙腈溶解后供气相色谱-质谱测定。
1.2.2.3 气相色谱-质谱(GC-MS)条件 GC条件:色谱柱为DB-5MS柱(30 mm×0.25 mm,0.25 μm);载气为氦气;载气流速0.9 mL/min;进样口温度290 ℃;程序升温步骤为初始温度150 ℃,保持1 min后以10 ℃/min程序升温至290 ℃,保持4 min;进样量1 μL,恒流模式,不分流。
MS条件:电子轰击离子源(EI),电子轰击能70 eV,离子源温度230 ℃;四级杆温度150 ℃;溶剂延迟9 min;选择离子检测模式(SIM),检测离子(m/z)为283、256、241、221,定量离子(m/z)为256。
1.2.2.4 免疫磁珠-胶体金免疫层析法的评价 添加回收率测定:取经GC-MS法检测确定的阴性水产样品,分别添加1、5、10、15 μg/kg 4个不同浓度的西泮标准溶液,各浓度进行5个平行试验,按上述免疫磁珠法进行样品前处理,用GC-MS法测定样品中地西泮浓度。计算回收率和相对标准偏差(RSD)。
回收率(%)=(实际检测浓度/添标浓度)×100
相对标准偏差(RSD,%)=(实际检测浓度的标准差/实际检测浓度平均值)×100
检出限评价:取经GC-MS检测确定的阴性样本分别添标至地西泮浓度为0、0.25、0.50、1.00 μg/kg,分别经免疫磁珠法和常规方法处理后,使用制备的地西泮胶体金检测试剂卡进行检测,每个浓度重复3次。
特异性评价:在经GC-MS检测确定的阴性样本中分别添加地西泮、氟西泮、替马西泮、奥沙西泮以及氟硝西泮标准品0、0.5、1.0、2.0、10.0 μg/kg,每个浓度重复3次,评价方法的特异性。
稳定性评价:取3种不同批次试剂卡在37 ℃条件下放置20 d,分别于第1、5、10、15、20 d随机抽取试剂卡检测阴性样本和0.5 μg/kg阳性添标样本,评价方法的稳定性。
方法学分析:用本方法与国家标准《动物源性地西泮和安眠酮多残留的测定 气相色谱-质谱法》(GB 29697-2013)规定的GC-MS法分别检测40份水产品样本,包括添标检测试验和盲样检测试验,进行方法学分析。
1.3 数据处理
采用Microsoft Excel对数据进行处理。
2 结果与分析
2.1 胶体金的紫外扫描图谱
制备的胶体金溶液,可经肉眼观察到均一的酒红色。将胶体金溶液在400~800 nm波长范围内进行紫外扫描,结果见图2所示。由图2可知,胶体金溶液在波长524 nm左右有单一的最大吸收峰,峰宽较小,说明胶体金颗粒整体上比较均一。根据胶体金颗粒直径与最大吸收峰之间的关系λ=0.4271φ+514.56[25]计算,胶体金的颗粒大小约为22 nm,符合胶体金层析法要求。
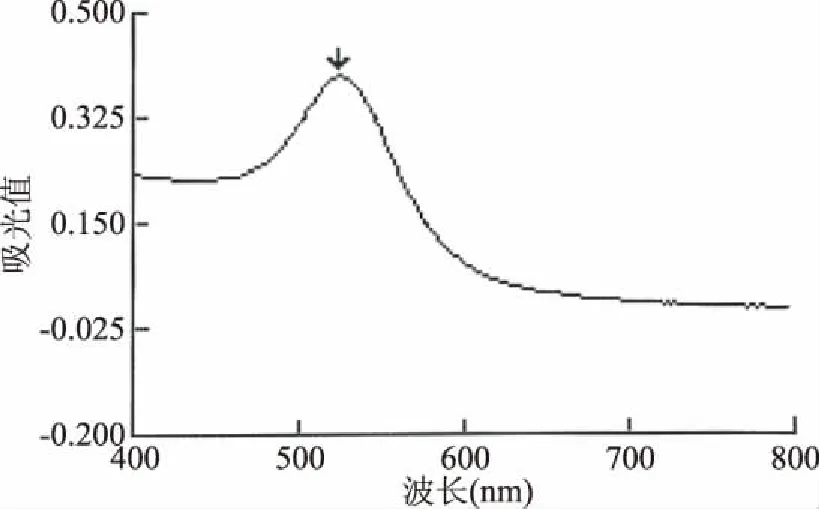
图2 胶体金紫外可见分光扫描图谱
2.2 地西泮胶体金免疫层析试纸条参数优化
2.2.1 标记抗体预试验结果 T/C比值法在一定程度上可以消除时空、环境温度以及样本基质对试纸条显色差异的影响,是一种较合理的胶体金定量检测法[26]。本研究利用胶体金读数仪分别读取检测卡T、C的显色深度,以T/C值作为产品质控指标,要求控制阴性T/C值范围为1.5~2.9、阳性T/C值范围为0.5~0.9,并以阴性T/C值和阳性T/C值的差值判断最佳。实验以添加1 μg/L地西泮标准品的PBS溶液为阳性组,以等体积PBS溶液的空白对照为阴性组进行胶体金标记抗体预试验,结果见表1。由表1可知,抗体标记量为20~30 μg/mL时,阴性T/C值符合质控要求;抗体标记量为15~30 μg/mL时,阳性T/C值符合质控要求。其中,当抗体标记量为25 μg/mL时,阴阳性梯度较好,即最佳抗体标记量为25 μg/mL。
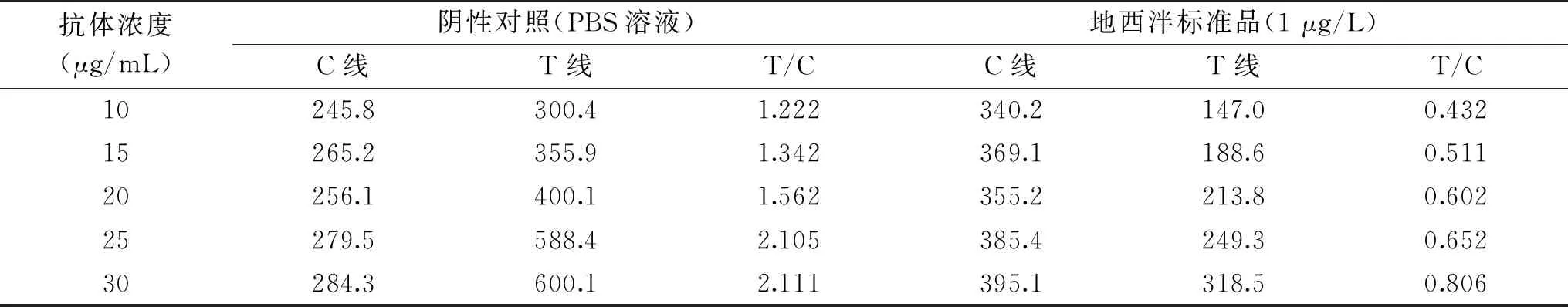
表1 胶体金标记抗体预试验结果
2.2.2 NC膜抗原、羊抗鼠二抗包被量优化试验结果 NC膜抗原、羊抗鼠二抗包被量优化试验结果见表2。由表2可知,满足质控要求的T线的抗原包被量和C线的羊抗鼠二抗包被量为0.3和1.50 mg/mL、0.6和1.5 mg/mL、1.2和3.00 mg/mL。其中,0.6和1.50 mg/mL组阴性T/C值和阳性T/C值的差值最大,阴阳性梯度较好,故T线的抗原包被量最适浓度为0.6 mg/mL,C线的羊抗鼠二抗包被量最适浓度为1.50 mg/mL。
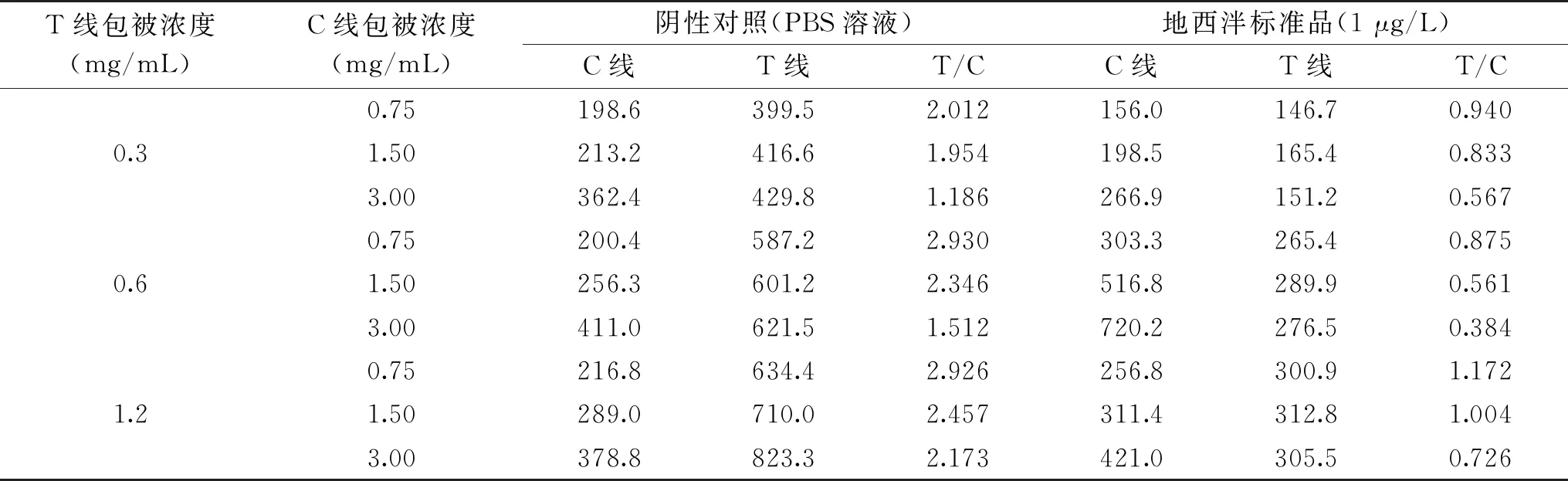
表2 NC膜抗原、羊抗鼠二抗包被量优化结果
2.2.3 金标喷量优化试验结果 金标喷量优化试验结果见表3。由表3可知,最优金标喷量为3.0 μL/cm,T线、C线显色和阴阳性梯度都较好。
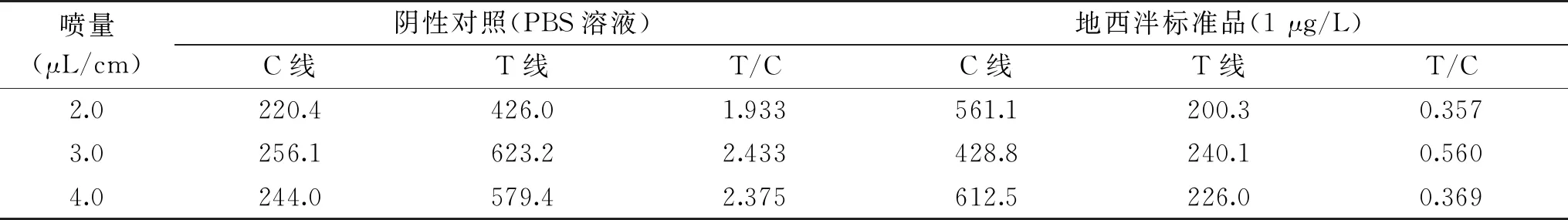
表3 金标喷量优化结果
2.3 免疫磁珠-胶体金免疫层析法性能评价
2.3.1 添加回收率的测定 对地西泮进行1、5、10、15 μg/kg 4个水平的空白添加回收试验,各浓度设5个平行试验,计算回收率和相对标准偏差。由表4可知,地西泮的平均回收率为78.34%~90.40%,RSD为5.03%~8.96%,说明本方法回收率较高,稳定性、重复性好,可满足地西泮残留检测的要求。
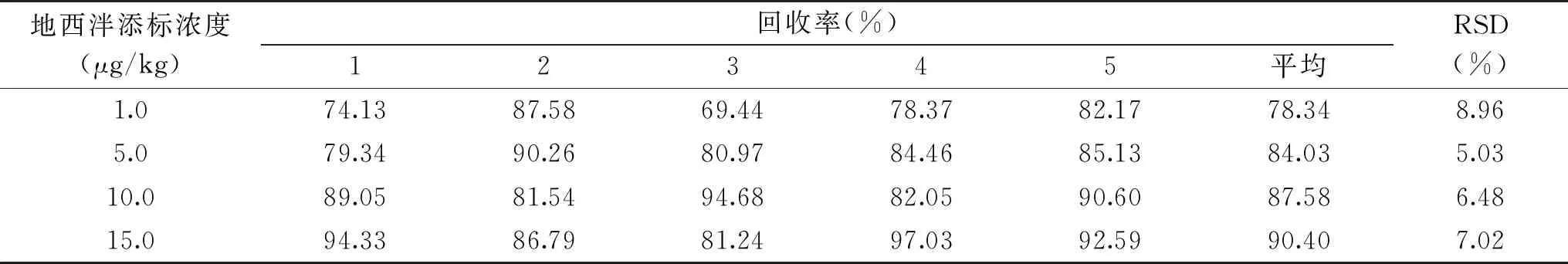
表4 地西泮的添加回收率和相对标准偏差(n=5)
2.3.2 检出限试验结果 不同浓度地西泮添加到阴性样本中,分别经免疫磁珠法和常规方法处理后,使用地西泮胶体金检测试剂卡检测,5 min后用胶体金读数仪进行读数,结果如表5所示。经常规方法处理,0~0.50 μg/kg地西泮添标浓度检测结果为阴性,1.00 μg/kg时检测结果为阳性。而经免疫磁珠法处理,地西泮添标浓度在0.25 μg/kg以下检测结果为阴性,0.50 μg/kg以上检测结果为阳性。由此可知,地西泮胶体金检测试剂卡以免疫磁珠法处理时,检出限为0.50 μg/kg,明显优于常规前处理方法。
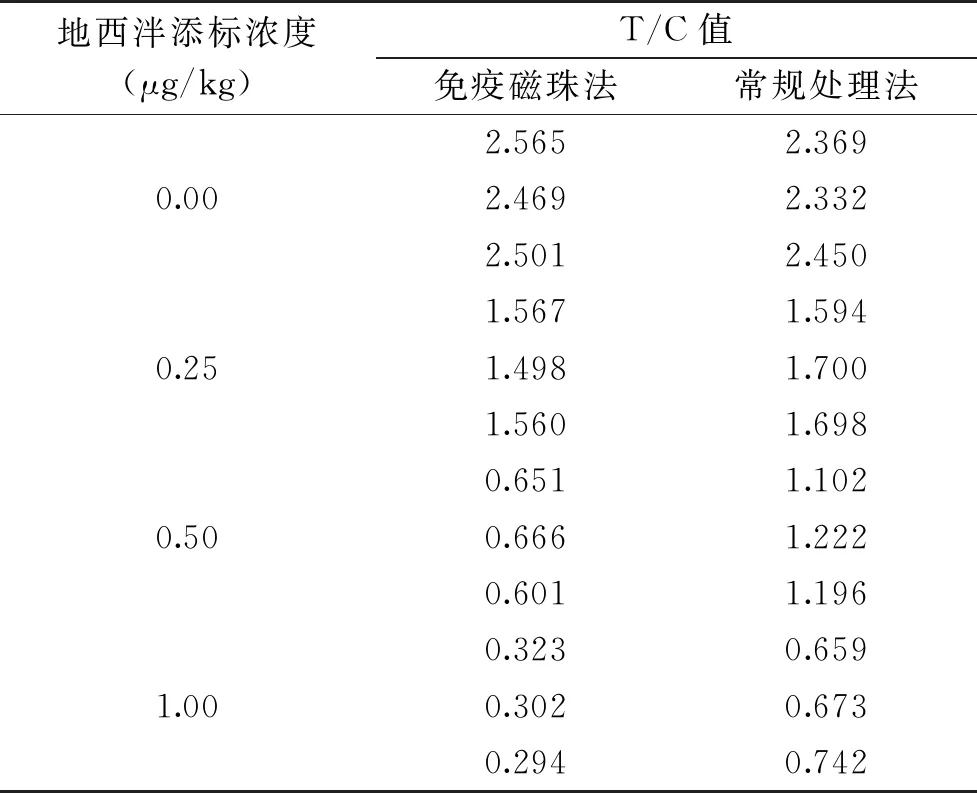
表5 不同前处理方法的检测结果
2.3.3 特异性试验结果 通过检测地西泮和四种地西泮结构类似物,来判定地西泮胶体金检测试剂卡是否具有特异性。结果显示,试剂卡检测不同浓度的氟西泮、替马西泮、奥沙西泮和氟硝西泮,结果均为阴性(见表6)。说明该试剂卡特异性良好,能保证检测时避免其他药物的干扰。
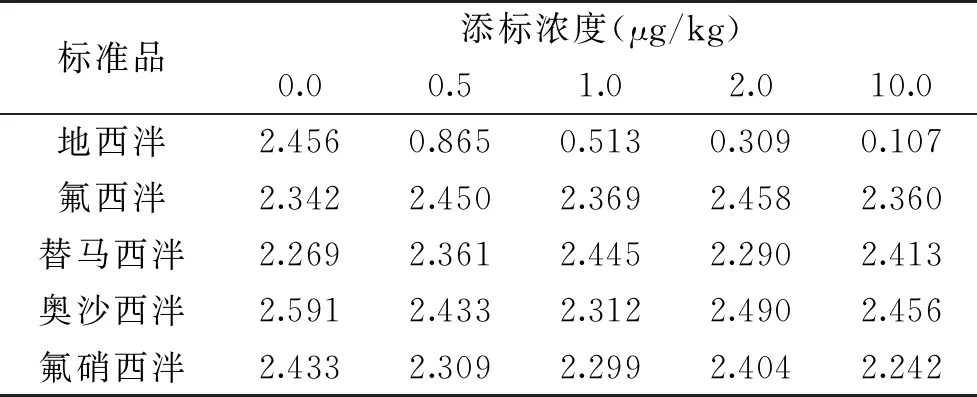
表6 特异性试验的T/C平均值
2.3.4 稳定性试验结果 试剂卡在37 ℃条件下放置20 d,于不同时期随机抽取进行稳定性试验。研究发现,试剂卡检测读数结果未发生明显变化(见表7),说明在保存期内稳定性很好。
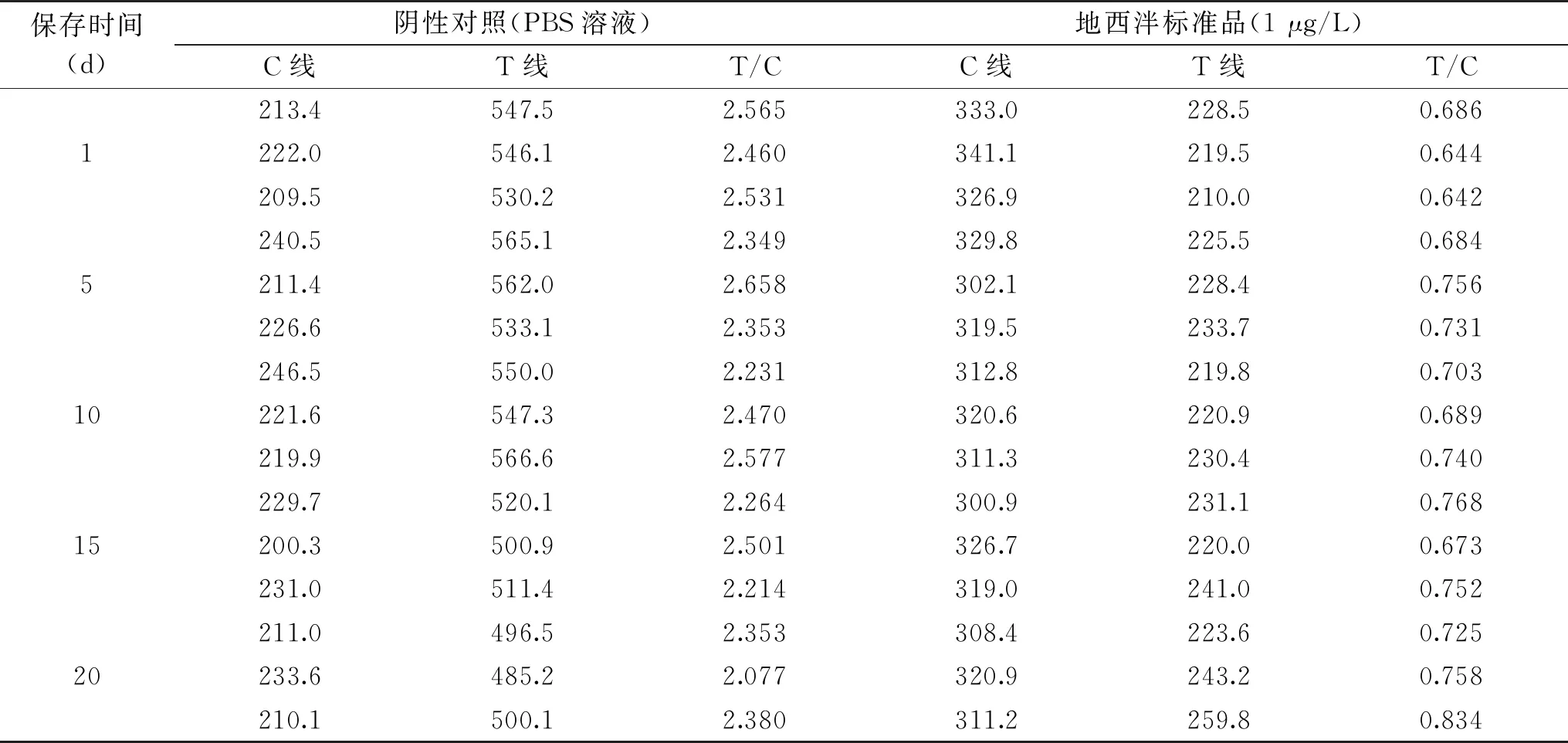
表7 稳定性试验结果
2.3.5 与气相色谱-质谱法(GC-MS)比较试验结果 由国家标准《动物源性地西泮和安眠酮多残留的测定 气相色谱-质谱法》(GB 29697-2013)可知,GC-MS法的检出限为0.5 μg/kg,定量限为1.0 μg/kg。用免疫磁珠-胶体金免疫层析法和GC-MS法对40份水产样本(其中鱼肉样本20份、虾肉样本10份、鳖肉样本10份)进行检测,其中10份阴性样本、10份添加0.5 μg/kg的阳性添标样本和20份随机盲样,结果见表8和表9。结果表明,在添标检测试验和盲样检测试验中,免疫磁珠-胶体金免疫层析法与GC-MS法的检测结果一致,适用于实际样品中地西泮的检测。
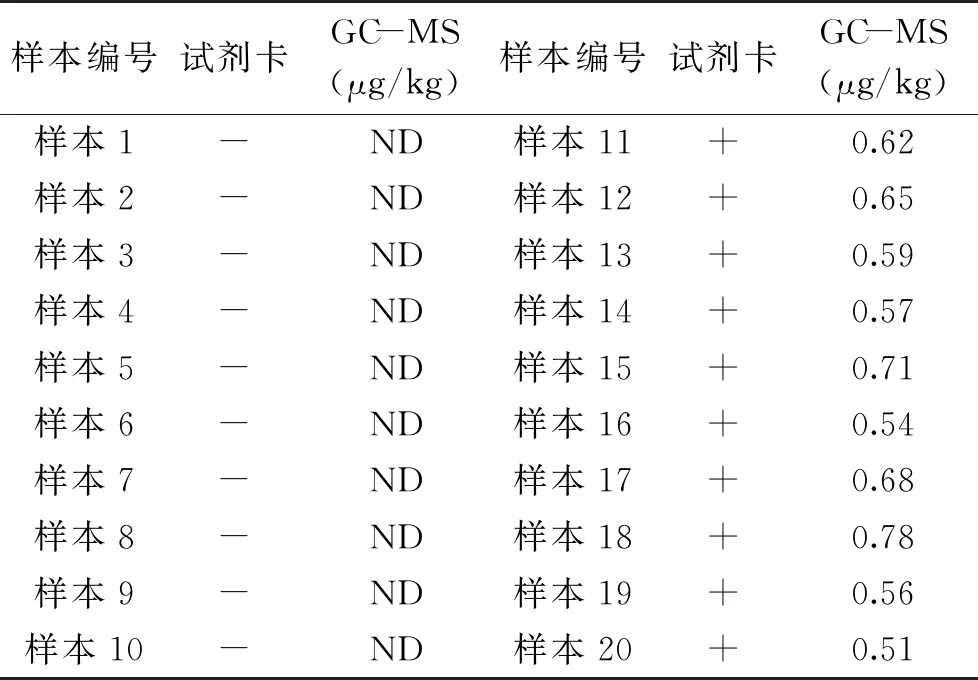
表8 不同检测方法的添标检测试验结果对比
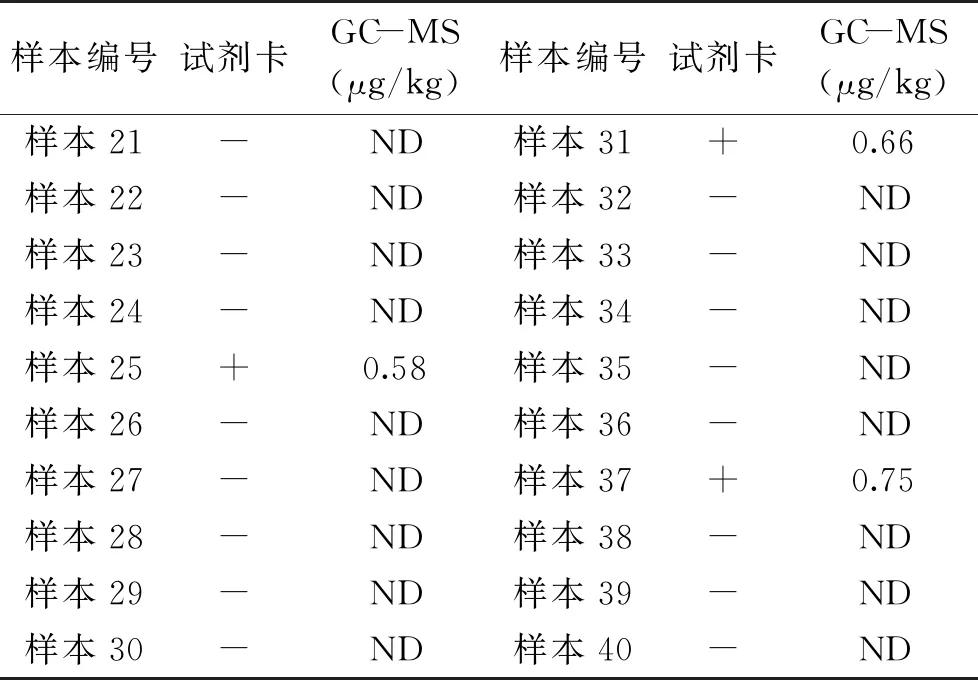
表9 不同检测方法的盲样检测试验结果对比
3 结论
免疫磁珠可通过磁场作用特异性分离、富集目的物,具有简便快速、灵敏度高、特异性强等特点,已广泛应用于食品微生物检测、细菌毒素检测、生化及分子遗传学等领域[20]。
本研究建立了一种快速检测水产品中地西泮残留的免疫磁珠-胶体金免疫层析法。该方法利用免疫磁珠选择性吸附、分离水产品中地西泮残留,操作简便、灵敏度高,平均回收率为78.34%~90.40%,RSD为5.03%~8.96%,单个样本可在25 min内完成检测,地西泮检出限为0.5 μg/kg,优于常规前处理法。同时优化了地西泮胶体金检测试剂卡,最佳工艺为金标抗体标记量25 μg/mL、T线抗原包被量0.6 mg/mL、C线羊抗鼠二抗包被量1.50 mg/mL、金标喷量3.0 μL/cm。经验证,该方法特异性强、稳定性好,检测结果与GC-MS法结果一致,可用于水产品中地西泮残留的现场快速检测,为食品安全提供保障。
