Dawson结构磷钨钼酸催化氧化苯甲醛绿色合成苯甲酸
2020-10-23曹小华徐常龙占昌朝叶志刚李佳艺黄华南
曹小华 ,徐常龙 ,占昌朝 ,叶志刚 ,李佳艺 ,黄华南
(1. 九江学院 化学与环境工程学院,江西 九江 332005;2.江西省生态化工工程技术研究中心,江西 九江 332005)
苯甲酸又称安息香酸,是一种重要的化工原料,广泛用作药物、防腐剂、染料中间体、改性剂和媒染剂等[1]。工业上主要采用重金属盐(如钴、锰、铬等)催化剂催化氧化甲苯制备苯甲酸,虽然工艺成熟,但污染严重,亟需开发绿色清洁的制备工艺[1-3]。
近年来,以苯甲醛为原料、30%(w) H2O2为氧化剂绿色合成苯甲酸工艺引起了广泛关注[4-10]。杂多酸(盐)以独特的酸性、“准液相”行为及多功能(酸、氧化、光电催化)等优点,在催化30%(w)H2O2氧化反应中显示出了优越的催化性能,从而备受关注[6-13]。Dawson结构磷钨钼酸在诸多反应中表现出优异的氧化催化性能,目前尚无Dawson结构磷钨钼酸催化H2O2氧化苯甲醛合成苯甲酸的相关报道。
本工作采用水热法制备了Dawson结构磷钨钼酸催化剂,利用FTIR,XRD,SEM,EDS等分析方法对磷钨钼酸进行表征,考查了Dawson结构磷钨钼酸催化30%(w) H2O2氧化苯甲醛合成苯甲酸的性能。
1 实验部分
1.1 原料与仪器
Na2WO4·2H2O、Na2MOO4·2H2O、85%(w)磷酸、37%(w)盐酸、苯甲醛、30%(w)H2O2:分析纯,中国医药集团上海化学试剂公司。Dawson结构磷钨钼酸依照文献[12]制备,分子式为H6P2W9Mo9O62·24H2O。
DF-101S型恒温油浴磁力搅拌器:巩义市予华仪器有限公司;KH-100型水热反应釜:巩义英峪高科技仪器厂;TENSOR 27型傅里叶变换红外光谱仪:Bruker公司,KBr压片,分辨率4 cm-1,扫描速率0.2 cm/s,波数范围500~4 000 cm-1;TESCAN-VEGAIIRSU型扫描电子显微镜:Tescan公司;X-ACT型能谱仪:Oxford Instruments公司;D8 Advance型X射线粉末衍射仪:Bruker公司,CuKα射线(λ= 0.150 64 nm),管电压40 kV,管电流100 mA,扫描范围10°~80°,扫描速率3(°)/min。
1.2 苯甲酸的合成
在100 mL圆底烧瓶中加入0.4 g自制磷钨钼酸、50 mL30%(w) H2O2(500 mmol),室温下磁力搅拌至充分溶解,然后加入10.20 mL苯甲醛(100 mmol)。控制温度为90 ℃左右,回流搅拌反应3.5 h。稍冷后将待反应液转移至烧杯中,0 ℃冷藏12 h,抽滤,少量冷水洗涤,得白色产品。将滤液浓缩至约10 mL, 0 ℃冷藏12 h,再次抽滤得白色产品,浓缩后的滤液用于后续催化剂的重复实验。合并2次产品,干燥至恒重,称重,计算产品收率。
2 结果与讨论
2.1 催化剂表征结果
2.1.1 FTIR表征结果
图1为催化剂的FTIR谱图。由图1可知,自制磷钨钼酸在1 090.7,957.6,911.3,785.9 cm-1处出现Dawson结构特征吸收峰[12],未出现Keggin结构特征吸收峰(1 072.4,972.5,877.8,790.9 cm-1)[8-9],说明自制磷钨钼酸具备Dawson结构。
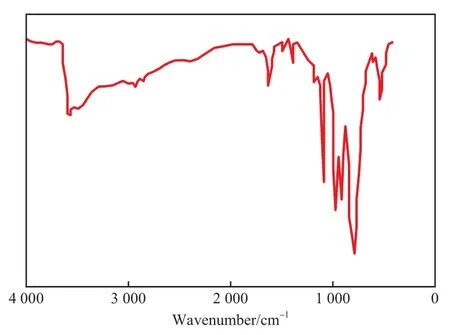
图1 H6P2W9Mo9O62·24H2O的FTIR谱图Fig.1 FTIR spectrum of H6P2W9Mo9O62·24H2O.
2.1.2 XRD表征结果
图2为催化剂的XRD谱图。由图2可知,自制磷钨钼酸在2θ=7°~ 9°,17°~20°,25°~ 30°,31°~38°处出现Dawson结构杂多酸晶体的4组特征衍射峰[12]。而Kgggin的特征衍射峰出现在2θ=10°,21°,25°,30°,35°处[9],但图 2 中并未出现。因此,进一步表明自制磷钨钼酸催化剂具有Dawson结构。

图2 H6P2W9Mo9O62·24H2O的XRD谱图Fig.2 XRD pattern of H6P2W9Mo9O62·24H2O.
2.1.3 SEM表征结果
图3是为自制磷钨钼酸催化剂的SEM照片。从图3可看出,自制磷钨钼酸表面光滑,呈类似长方体的块状物,分布不均匀,局部块状物聚集在一起。

图3 H6P2W9Mo9O62·24H2O的SEM照片Fig.3 SEM image of H6P2W9Mo9O62·24H2O.
2.1.4 EDS表征结果
图4为自制磷钨钼酸催化剂的EDS谱图。由图4可知,磷钨钼酸催化剂中主要含O,W,Mo,P四种元素。进一步计算分析结果显示,P,W,Mo的原子个数比分别为1.56%,10.14%,7.89%,原子质量分数分别为1.22%,47.13%,19.14%,均与磷钨钼酸分子式相接近。说明自制磷钨钼酸催化剂具备Dawson结构。而H元素未在谱图中显示出来,是因为它的相对原子质量过小。

图4 H6P2W9Mo9O62·24H2O的EDS谱图Fig.4 EDS spectrum of the H6P2W9Mo9O62·24H2O.
2.2 苯甲酸合成条件优化
2.2.1 磷钨钼酸催化剂用量对苯甲酸收率的影响
磷钨钼酸催化剂用量对苯甲酸收率的影响见图5。由图5可知,无催化剂时,苯甲酸收率仅为24.5%;随催化剂用量的增加产物收率增加,当催化剂用量为0.3 g时,产物收率最高;再进一步增加催化剂用量,收率反而下降。这是因为适量的磷钨钼酸可与H2O2生成活性配合物{PO4[WO(O2)2]4}3-,{PO4[MoO(O2)2]4}3-,{PO4[Mo4-xWxO20]4}3-, 催化30%(w)H2O2氧化苯甲醛生成苯甲酸[13]。催化剂用量偏少时,活性中心过少,部分反应物停留在中间产物,产率较低。磷钨钼酸催化剂用量过多时,造成H2O2无效分解[13]。因此,磷钨钼酸催化剂适宜的用量为0.3 g(即基于苯甲醛质量的2.9%)。
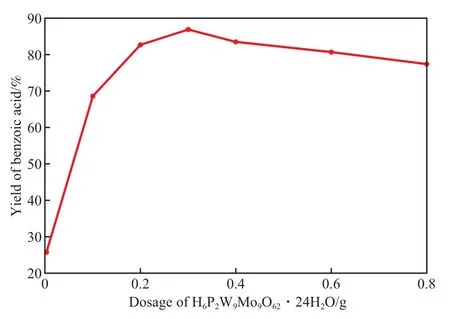
图5 H6P2W9Mo9O62·24H2O用量对苯甲酸收率的影响Fig.5 The effect of H6P2W9Mo9O62·24H2O dosage on benzoic acid yield.Reaction conditions:n(benzaldehyde)∶n(30%(w) H2O2)=1∶5,80 ℃,3.0 h.
2.2.2 H2O2用量对苯甲酸收率的影响
30%(w)H2O2用量对苯甲酸收率影响见图6。由图6可知,随H2O2用量的增加,产物收率先增加后减少。H2O2用量为50 mL时,产物收率最高。这是因为H2O2用量不足时,产物停留在中间体,而H2O2用量过量时则反应过于剧烈,加速了产物深度氧化导致副反应的发生[6]。因此,30%(w)H2O2适宜用量为50 mL(即n(苯甲醛)∶n(30%(w) H2O2)=1∶5)。

图6 30%(w)H2O2用量对苯甲酸收率的影响Fig.6 The effect of 30%(w) H2O2 amount on benzoic acid yield.Reaction conditions:0.3 g H6P2W9Mo9O62·24H2O,80 ℃,3.0 h.
2.2.3 反应温度对苯甲酸收率的影响
图7为反应温度对苯甲酸收率的影响。由图7可知,适宜反应温度为80 ℃。由于反应是放热反应,需要合适的吸氧速度,温度过低H2O2有效分解成活性氧自由基过慢,催化活性降低,产物停留在中间体阶段[9];温度过高则加剧了H2O2的无效分解,同时降低了活性氧在体系中的溶解度,抑制正反应的进行,促使副反应的发生,降低了反应的选择性[10]。

图7 反应温度对苯甲酸收率的影响Fig.7 Effect of reaction temperature on benzoic acid yield.Reaction conditions:n(benzaldehyde)∶n(30% (w) H2O2)=1∶5,0.3 g H6P2W9Mo9O62·24H2O,3.0 h.
2.2.4 反应时间对苯甲酸收率的影响
图8为反应时间对苯甲酸收率的影响。由图8可知,随反应时间的延长,苯甲酸收率逐渐增加。当反应时间为3.0 h时,可观察到有大量白色物质,此时苯甲酸收率最高;再延长反应时间,苯甲酸发生深度氧化或分解,生成过氧苯甲酸或酚类等副产物,收率下降[7]。因此,适宜的反应时间为3.0 h。
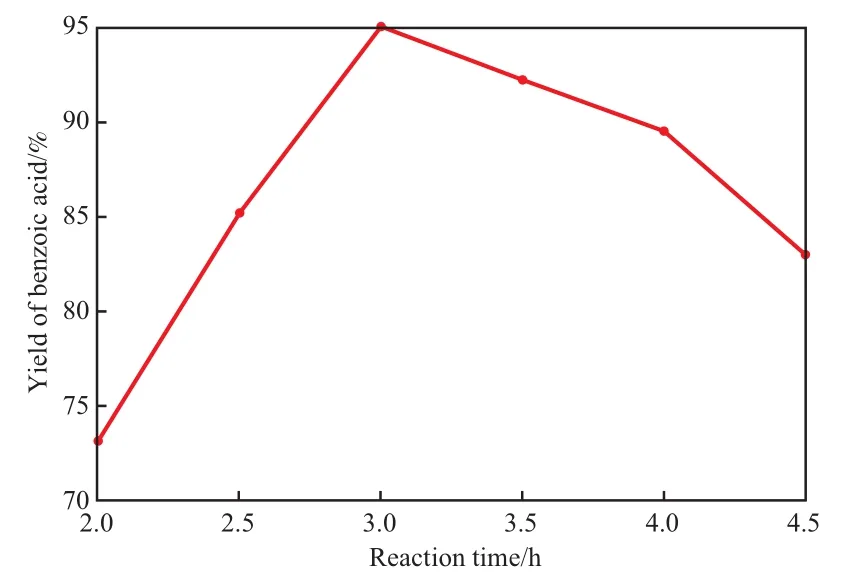
图8 反应时间对苯甲酸收率的影响Fig.8 Effect of reaction time on benzoic acid yield.Reaction conditions:n(benzaldehyde)∶n(30%(w) H2O2)=1∶5,0.3 g H6P2W9Mo9O62·24H2O,80 ℃ .
2.3 催化剂的稳定性和重复使用性能
在优化条件下,即2.9%(w) 磷钨钼酸(基于苯甲醛质量)、n(苯甲醛)∶n(30%(w) H2O2)=1∶5、80 ℃、3.0 h,进行5次平行实验。苯甲酸的收率分别为95.7%,94.8%,95.0%,95.2%,94.6%,平均收率为95.1%,高于文献[3-10]报道工艺收率。说明磷钨钼酸催化剂的催化活性较好,催化工艺稳定。
向浓缩后的滤液中加入补加10.2 mL新鲜苯甲醛和n(苯甲醛)∶n(30%(w) H2O2)=1∶5(不加催化剂),于80 ℃下反应3.0 h,进行催化体系重复套用实验。5次套用实验苯甲酸的收率依次为95.2%,91.9%,85.7%,79.4%,74.5%,由此可见,随着重复使用次数的增加,苯甲酸收率逐渐下降。这是因为随使用次数的增加,体系中的副产物增多,破坏了催化剂活性络合物的结构,且催化剂溶脱损失,导致催化剂的催化氧化活性下降[12-13]。催化体系使用至第5次,苯甲酸的收率仍可达74.5%,说明Dawson结构磷钨钼酸具有较好的重复使用性能。
2.4 产品纯度的测定
产物苯甲酸及其标样的FTIR谱图见图9。由图9可知,实验产物与苯甲酸标样谱峰高度吻合,其中,3 058 cm-1处为芳烃C—H的伸缩振动峰,1 780 cm-1处为—COOH的伸缩振动峰,1 769 cm-1处为C=O的伸缩振动峰,表明产物为高纯度苯甲酸[5]。
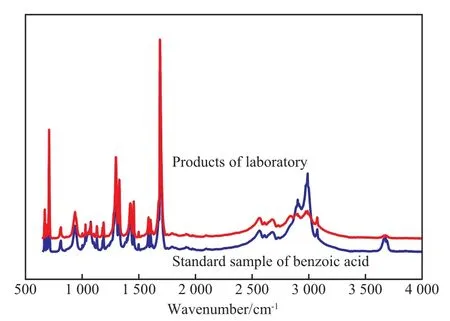
图9 苯甲酸的FTIR谱图Fig.9 FTIR spectra of the benzoic acid.
3 结论
1)以钼酸钠、钨酸钠和浓磷酸为原料,采用水热法制备了Dawson结构磷钨钼酸,表征结果显示,自制磷钨钼酸为Dawson结构。
2)自制Dawson结构磷钨钼酸在催化30%(w)H2O2氧化苯甲醛合成苯甲酸反应中表现出良好的催化性能。优化条件为:磷钨钼酸用量为2.9%(w)(基于苯甲醛质量)、n(苯甲醛)∶n(30%(w)H2O2)=1∶5、反应温度为80 ℃、反应时间为3.0 h,此条件下的产物收率达95.1%,催化剂重复使用5次后,产物收率仍可达74.5%。
