恩诺沙星残留酶联免疫分析法的建立
2020-10-10穆洪涛李嘉慧刘凤银黄玉琦
穆洪涛, 李嘉慧, 刘凤银, 黄玉琦
(广东第二师范学院 生物与食品工程学院, 广东 广州510303)
0 引言
喹诺酮类抗生素具有抗菌谱范围广、杀菌活性高及毒副作用较小的特点,对水生、陆生动物的疾病预防与治疗有良好的效果,因此被广泛应用于兽医临床中[1]. 市场调研显示,畜禽类产品中存在检出喹诺酮类药物超标的现象[2-5],残留的药物被人体摄入后会产生不良作用[6-9],因此开发快速简便的喹诺酮类药物检测方法势在必行. 目前检测喹诺酮类药物的方法主要有高效液相色谱法、高效毛细管电泳法、酶联免疫分析法、胶体金免疫层析法等[10-16]. 色谱法虽然灵敏度高,重复性强,准确性强,但对检测样品的处理要求较高,对仪器依赖强,不适于大批样品的快速筛查;免疫法具有操作简单、特异性强、快速灵敏等特点,且样品前处理方法简单,适用于大批量样品的快速检测. 因此本研究选择恩诺沙星、达氟沙星、沙拉沙星3 种药物为研究对象,通过制备高效的免疫原免疫动物获得抗恩诺沙星抗体,开发检测恩诺沙星的酶联免疫分析法.
1 材料与方法
1.1 试剂和材料
1.1.1 主要试剂与材料
盐酸恩诺沙星(≥98.0%)、甲磺酸达氟沙星(≥98.0%)、盐酸沙拉沙星(≥98.0%)、氧氟沙星(≥98.0%)、环丙沙星(≥98.0%)、诺氟沙星(≥98.0%)、氟甲喹(≥98.0%)、噁喹酸(≥98.0%)、牛血清白蛋白(BSA,99%)、卵清白蛋白(OVA,99%)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC,99%)、3,3′,5,5′-四甲基联苯胺(TMB,99%)、过氧化脲等,广州齐云生物技术有限公司提供; BALB/c 雌性小鼠(3 周)和新西兰雌性白兔(2 kg),广东省医学实验动物中心提供; 其他试剂均为分析纯.
1.1.2 主要仪器
SP-Max2300A 光吸收型全波长酶标仪(上海闪谱生物科技有限公司)、RT-3100 全自动洗板机(深圳雷杜生命科学股份有限公司)、DK-8AD 电热恒温水热槽(上海一恒科学仪器有限公司)、XP.5002 电子天平(上海越平科学仪器有限公司)、MX-F 震荡仪(SCILOGEX)、PHSI-5 实验室pH 计(上海仪电科学仪器股份有限公司).
1.2 人工抗原的合成与鉴定
用紫外分光光度法测0.5 mg·mL-1ENR-BSA、ENR-OVA 在200 ~800 nm 进行全波长扫描,根据其峰值判断人工抗原的偶联情况.
1.3 动物免疫及血清评价
1.3.1 BALB/c 雌性小鼠免疫
本研究先选用BALB/c 雌性小鼠(3 周)进行腹部皮下和腿部肌肉注射免疫,初次免疫时使用弗氏完全佐剂与1 mg·mL-1的1.2 合成的ENR-BSA、DAN-BSA、SARA-BSA 等量混合乳化,后续改用弗氏不完全佐剂作为乳化剂,隔1 周免疫1 次,共进行6 次免疫,最后1 次不使用乳化剂乳化,按100 μL/只的剂量给药.
1.3.2 新西兰大白兔免疫
选用新西兰大白兔(2 kg)进行背部皮下注射免疫,免疫次数和乳化方法同1.3.1 所述,所用免疫原为ENR-BSA、DAN-BSA,按1 mL/只的剂量给药.
1.3.3 血清评价
将所得鼠抗血清进行icELISA 实验,测定其效价,以确定是否有抗体产生; 将所得的兔抗血清进行icELISA 实验,筛选出高效的特异性强的抗体及检测抗原,用于后续建立icELISA 方法.
1.4 最佳工作条件的优化
1.4.1 最佳包被液稀释度和抗体稀释度
1)农机装备水平高。主要表现为装备标准高,配套农具数量多;科技含量高,自动化、智能化、机电液一体化程度高。
使用棋盘滴定法,对酶标板横列进行划分,因素为抗体稀释浓度,同一倍数设2 列,使用PBST 溶液按1、2、4、8、16、32 k 倍对一抗进行稀释; 再对竖列进行划分,因素为包被原稀释度,每个稀释度设1 横,使用包被缓冲液按1、2、4、8、16、32、64、128 k 倍对1 mg·mL-1的包被原进行稀释,进行icELISA 实验,结合ODmax值和IC50值对比,确定最佳包被稀释度及一抗稀释度.
1.4.2 一抗抗原最佳竞争时间
在37℃条件下分别竞争30、40、50 和60 min,进行icELISA 实验,结合ODmax值和IC50值对比,确定一抗抗原最佳竞争时间.
1.4.3 酶标抗体最佳稀释度
使用PBST 溶液对酶标抗体进行3、4、5、6 k 倍稀释,进行icELISA 实验,结合ODmax值和IC50值对比,确定酶标抗体最佳稀释度.
1.5 标准曲线的绘制
设置恩诺沙星标准溶液的质量浓度梯度为0.05、0.25、1、4、20、100、500 μg·mL-1,以恩诺沙星标准品溶液质量浓度的常用对数值为x,实验所得的OD 值为y,在Origin 8.5 软件内绘制标准曲线,然后对所得的曲线使用4 参数对数方程进行拟合[17],得到50%抑制值(IC50)和线性范围(IC20~IC80).
1.6 特异性测试
分析7 种恩诺沙星结构类似物:达氟沙星(DAN)、沙拉沙星(SARA)、氧氟沙星(OFL)、环丙沙星(CIP)、诺氟沙星(NOR)、噁喹酸(OXO)、氟甲喹(FLU)与一抗的交叉反应,计算交叉反应率[18]. 计算公式如下:

2 结果
2.1 人工抗原的鉴定
使用碳化二亚胺法将恩诺沙星与BSA 偶联作为免疫抗原,与OVA 偶联作为包被抗原,紫外吸收光谱图如图1 所示. 由图1 可以看出,经过偶联的人工抗原的峰值所在的位置较BSA、OVA 相比往左偏移,且2 种人工抗原所在的吸收光谱各自都在半抗原ENR 和偶联蛋白BSA、OVA 之间,由此可以判断,半抗原ENR 成功偶联到载体蛋白BSA、OVA 上.

图1 ENR、BSA、OVA、ENR-BSA 和ENR-OVA紫外扫描图谱
2.2 血清评价
2.2.1 鼠抗血清
6 组鼠抗血清的效价结果如表1 所示,达氟沙星的效价最高(1∶125 000),恩诺沙星(1 ∶27 000)其次,均可用于新西兰大白兔的免疫. 效价亦称滴度,指某种抗血清与相应的抗原发生沉淀反应或凝集反应的能力,一般以显现反应的最高稀释度来表示.
2.2.2 兔抗血清
2 组兔抗血清的效价结果如表1 所示,恩诺沙星效价较达氟沙星高,因此使用兔抗恩诺沙星血清来开发用于检测恩诺沙星的icELISA. 其中,抑制率表示标本在竞争结合中标本对阴性反应显色的抑制程度,按下式计算:

2.3 icELISA 条件的优化
棋盘滴定法优化包被抗原稀释倍数和一抗稀释倍数,单因素实验优化一抗抗原竞争反应时间、二抗稀释倍数,通过ODmax和IC502 个指标参考,从而得出最优的条件参数. 其中, ODmax值为标本最大吸光值,IC50为半数抑制浓度.

表1 血清效价结果
2.3.1 最佳包被稀释度及抗体稀释度的确定
根据棋盘滴定法设计对包被原和一抗进行一系列的梯度稀释,从中选择OD 值在1.0 ~1.5 的3 组进行icELISA 实验,即A 组(64 000/16 000)、B 组(128 000/8 000)和C 组(32 000/32 000)(包被原稀释倍数/一抗稀释倍数),最终获得的ODmax和IC50如表2 所示. 由表2 可知,当包被原稀释1∶64 000,一抗稀释1∶16 000时所得的标准曲线ODmax值相对稳定在1.0~1.5 之间,且IC50值相对较小,因此确定本设计使用的icELISA 方法的包被原稀释1∶64 000,抗体稀释1∶16 000.
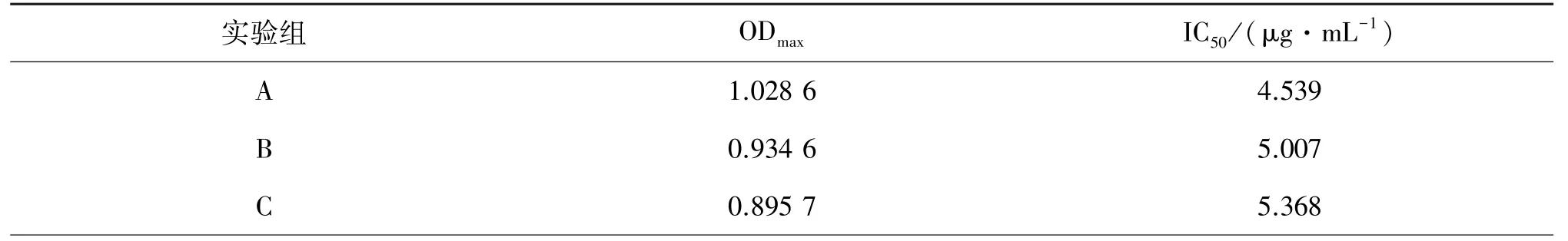
表2 包被原稀释度及一抗稀释度的选择
2.3.2 一抗抗原最佳反应时间的确定
设置一抗抗原反应时间(30、40、50 和60 min),进行icELISA 实验,实验所得的ODmax和IC50如表3 所示.由表3 可知,一抗抗原反应时间为60 min 时的IC50相对较低,且ODmax又相对稳定在1.0~1.5 之间,因此选择60 min 作为一抗抗原抗的反应时间.
2.3.3 酶标抗体最佳稀释度的确定
设计的酶标抗体使用PBST 缓冲液稀释1∶3 000、1∶4 000、1∶5 000 和1∶6 000,进行icELISA 实验,实验所得的ODmax和IC50如表3 所示. 由表3 可知,酶标抗体稀释倍数为5 000 倍时的IC50相对较低,且ODmax相对稳定在1.0~1.5 之间,因此选择酶标抗体稀释1∶5 000 作为酶标抗体最佳稀释倍数.

表3 竞争时间和酶标抗体稀释度的选择
2.4 icELISA 的标准曲线
结合2.3 优化的结果,最终得到本设计建立的icELISA 方法的最佳工作条件:使用包被缓冲液将人工抗原ENR-OVA 稀释1 ∶64 000,在37 ℃恒温水浴条件下孵育12 h,使用PBST 溶液将一抗稀释1∶16 000;用PBS 溶液将药物按0.05、0.25、1、4、20、100、500 μg·mL-1浓度进行梯度稀释,一抗与抗原竞争反应时间为60 min,使用PBST 溶液将酶标抗体稀释1∶5 000,进行icELISA 实验,按1.5 方法绘制抑制曲线,如图2 所示,IC50为4.539 μg·mL-1,线性范围(IC20~IC80)为0.595~34.632 μg·mL-1.

图2 抗恩诺沙星抗体标准曲线
2.5 交叉反应的鉴定
一抗与7 种恩诺沙星结构类似物的交叉反应率如下表4 所示. 由表4 可知,兔抗恩诺沙星血清与CIP、NOR、OFL 都有较高的交叉反应率,均超过100%,与DAN、FLU、OXO 无明显的交叉反应,说明所建立的icELISA 方法除对恩诺沙星之外,对CIP、NOR、OFL、SARA 也有较好的识别作用,可以实现这几种药物的同时检测.

表4 抗ENR 抗体与7 种Qus 的CR
不同的国家和卫生组织根据自身情况对检测食品中恩诺沙星的残留情况制定了不同的限量标准[19-20],具体如表5 所示. 美国对恩诺沙星的检测要求最高,不允许检出; 中国对恩诺沙星的最大残留限量要求低于一些国外标准,为100 μg·kg-1. 依据中国标准,本测试方法的灵敏度还可以通过制备相应的单克隆抗体建立检测方法来提高.

表5 恩诺沙星的最大限量标准
3 结论
合成并鉴定了人工免疫原和包被原,通过免疫BALB/c 小鼠初步筛选了可用的免疫原,进一步免疫新西兰大白兔制备多克隆抗体. 人工抗原ENR-OVA 稀释1∶64 000,在37 ℃恒温水浴条件下孵育12 h,一抗稀释1 ∶16 000,一抗与抗原竞争反应60 min,酶标抗体稀释1∶5 000 时最佳. 本方法的IC50为4.539 μg·mL-1,线性范围(IC20~IC80)为0.595~34.632 μg·mL-1; 与DAN、FLU、OXO 无明显的交叉反应,说明所建立的icELISA 方法除对恩诺沙星之外,对CIP、NOR、OFL、SARA 有较好的识别作用,可以实现这几种药物的同时检测.
